MODELO ANIMAL PARA LA SELECCIÓN Y VALIDACIÓN DE AGENTES ACTIVOS CONTRA EL ENFISEMA PULMONAR Y EL CÁNCER COLORRECTAL.
Un modelo animal de roedor que no expresa una o más sestrinas funcionales o que expresa niveles de traducción reducidos al menos el 50% de una o más sestrinas,
y que no expresa proteína de unión al factor de crecimiento transformante ß latente 4 (ltbp4) o que expresa niveles de traducción reducidos al menos el 50% de ltbp4
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/059227.
Solicitante: FRANKGEN BIOTECHNOLOGIE AG.
Nacionalidad solicitante: Alemania.
Dirección: WILHELM-BONN-STRASSE 8F 61476 KRONBERG/TAUNUS ALEMANIA.
Inventor/es: MELCHNER,Harald von, WEMPE,Frank, DE-ZOLT,Silke.
Fecha de Publicación: .
Fecha Solicitud PCT: 4 de Septiembre de 2007.
Clasificación Internacional de Patentes:
- A01K67/027M2
- C12N15/85A3
Clasificación PCT:
- C12N15/85 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para células animales.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2359826_T3.pdf


Fragmento de la descripción:
La presente invención se refiere a un modelo animal de roedor, a cultivos celulares y tisulares obtenidos del mismo, que no producen o que producen sólo niveles subóptimos de una o más sestrinas funcionales y que, además, no producen o producen sólo niveles subóptimos de proteína de unión al factor de crecimiento transformante β latente 4 (ltbp4). Además, la presente invención se refiere a un procedimiento para seleccionar agentes para tratar el enfisema pulmonar y/o el cáncer colorrectal mostrado utilizando el modelo animal, cultivo celular o tisular de la invención. El modelo animal de roedor, cultivo celular o tisular es adecuado para el ensayo preclínico de la eficacia, toxicidad y biodisponibilidad de agentes potenciales.
Antecedentes de la invención
La enfermedad pulmonar obstructiva crónica con enfisema pulmonar (EPOC) es una enfermedad altamente prevalente que tiene un gran impacto sobre la calidad de vida de los pacientes y sus familias y que mata a millones de personas en todo el mundo. Aunque el factor de riesgo principal para la EPOC es la inhalación de partículas y gases tóxicos que se generan principalmente, pero no exclusivamente, en el humo del tabaco, también están implicadas anomalías primarias (genéticas) de las vías respiratorias, ya que sólo una fracción de los fumadores desarrollan EPOC. La EPOC está asociada con costes muy importantes de atención sanitaria, en gran parte debido a tratamientos costosos tales como la terapia con oxígeno a largo plazo y las admisiones hospitalarias, así como costes indirectos incluyendo la pérdida de capacidad laboral. Además, el tratamiento de la EPOC se limita a los síntomas, ya que no se ha demostrado hasta ahora que ninguna intervención farmacológica modifique la historia natural de la enfermedad (Vestbo J. y Hogg, J. C. Thorax. 61: 86-8, 2006; Fabbri L. M., y col. Am J Respir Crit Care Med. 173: 1056-65, 2006).
El cáncer colorrectal es una de las neoplasias más comunes en el hemisferio Occidental y representa un desafío de salud pública muy importante a pesar de los progresos en la detección y la terapia. La mortalidad total a los 5 años es de aproximadamente el 40%. Aunque la enfermedad en fase temprana puede curarse mediante cirugía, sólo está disponible un tratamiento paliativo para pacientes con cáncer metastásico no resecable cuya tasa de supervivencia está entre 7-24 meses (Shaheen N. J., y col. Am J Gastroenterol. 2006).
De lo anterior se hace evidente que son altamente deseables nuevos compuestos farmacéuticos para el tratamiento de ambas afecciones y que podrían identificarse con el modelo animal de la invención, que muestra tanto enfisema pulmonar como cáncer colorrectal como resultado de mutaciones de pérdida de función en los genes de sestrina 2 y proteína de unión a factor de crecimiento transformante beta latente 4.
Los factores de crecimiento transformante β (TGF-β) pertenecen a una superfamilia de proteínas cuyos miembros controlan el crecimiento y la diferenciación celular en una diversidad de tejidos adultos y están implicados en una amplia variedad de respuestas inflamatorias e inmunes (Shi Y. y Massague, J. Cell. 113: 685-700, 2003; Sheppard
D. Proc Am Thorac Soc. 3: 413-7, 2006). La mayoría de las células secretan TGF-β como una citocina latente funcionalmente inactiva, que forma un complejo con su propéptido asociado a latencia (LAP), que interacciona con sus receptores sólo después de su activación por escisión proteolítica. Hay dos complejos latentes estructuralmente diferentes conocidos de TGF-β. El complejo latente pequeño consiste en un dímero de TGF-β maduro unido a la parte N-terminal del propéptido TGF-β-LAP. El complejo latente grande contiene, además de TGF-β-LAP, una de las tres proteínas de unión a TGF-β latentes (ltbp 1, 3 y 4). A menos que se desplace de las ltbp después de la secreción, el TGF-β se deposita habitualmente en la matriz extracelular (MEC) como un complejo de alto peso molecular con ltbp y LAP (Annes J. P., y col. J Cell Sci. 116: 217-24, 2003). Las 4 isoformas existentes de ltbp (ltbp 1-4) se han inactivado por mutación en el ratón (Dabovic B., y col. J Cell Biol. 56: 227-232, 2002; Sterner-Kock A., y col. Genes Dev. 16: 2264-2273, 2002; Shipley J. M., y col. Mol Cell Biol. 20: 4879-87, 2000). Aunque los fenotipos de los ratones knock out variaban entre isoformas, tanto los mutantes ltbp3 como ltbp4 desarrollan enfisema pulmonar debido a defectos en la señalización de TGF-β. Sin embargo, al contrario que los ratones ltbp3 mutantes que desarrollan enfisema, que es relativamente leve y estrictamente evolutivo (Dabovic B., y col. J Cell Biol. 56: 227-232, 2002), los enfisemas en los ratones ltbp4 (ltbp4-/-) mutantes empeoran con la edad y progresivamente adquieren las características de los enfisemas de inicio tardío que se desarrollan en el contexto de la EPOC en seres humanos (Sterner-Kock A., y col. Genes Dev. 16: 2264-2273, 2002; WO 03/015505). La relevancia potencial de ltbp4 en la patogénesis de la EPOC se ha subrayado recientemente por un estudio clínico que describe una correlación altamente significativa entre síntomas de EPOC específicos y un polimorfismo de un solo nucleótido (SNP) en ltbp4 (Hersh C. P., y col. Am J Respir Crit Care Med. 173: 977-84, 2006). Además del enfisema, los ratones ltbp4 mutantes desarrollan cáncer colorrectal invasivo (Sterner-Kock A., y col. Genes Dev. 16: 2264-2273, 2002; documento WO 03/015505). También se ha descrito recientemente una relación entre la expresión de ltbp4 y la progresión del cáncer en un estudio clínico de pacientes con cáncer colorrectal (Bertucci F., y col. Oncogene. 23: 1377-91, 2004).
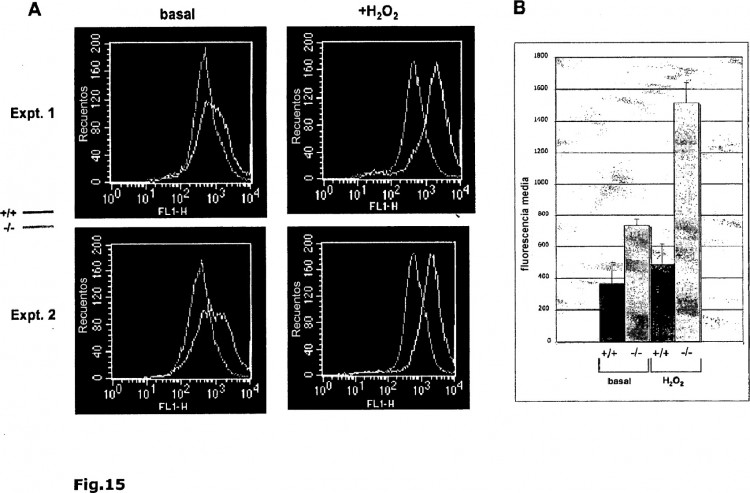
La sestrina 2 pertenece a una familia de proteínas altamente conservadas descubiertas inicialmente como proteínas inducibles por p53 (Velasco-Miguel S., y col. Oncogene. 18: 127-37, 1999; Peeters H., y col. Hum Genet. 112: 57380, 2003; Budanov A. V., y col. Oncogene. 21: 6017-31, 2002; documentos WO 00/12525; US 2002/0103353). Las células de mamífero expresan tres isoformas denominadas sestrina 1 (sestrina 1; también conocida como PA26), sestrina 2 (sestrina 2; también conocida como Hi95) y sestrina 3 (Figura 1). Se ha demostrado recientemente que dos de las sestrinas (sestrina 1 y sestrina 2) regulan los niveles de peróxido intracelular (ROS) (Budanov A. V., y col. Science. 304: 596-600, 2004; Sablina A. A., y col. Nat Med. 11: 1306-13, 2005). Más específicamente, se cree que las sestrinas regeneran (reducen) las peroxirredoxinas (Prx), que son proteínas antioxidantes altamente conservadas y expresadas ubicuamente (revisado en Georgiou G. y Masip, L. Science. 300: 592-4, 2003; Wood Z. A., y col. Trends Biochem Sci. 28: 32-40, 2003). Al reducir el H2O2 a H2O, las Prx se oxidan en su denominada cisteína peroxidática (Cys-SH), que se convierte en ácido sulfénico (Cys-SOH) (Figura 2). En bacterias, cuando la Prx AhpC es la secuestrante primaria de H2O2, la AhpC oxidada se reduce posteriormente por la reductasa especializada AhpF. Sin embargo, a diferencia de AhpC, las Prx de mamífero son altamente susceptibles a la sobreoxidación produciendo ácido sulfínico (Cys-SO2H) en presencia de altas concentraciones de peróxido (Figura 2). Los ácidos sulfínicos de proteínas no pueden reducirse por reductores celulares típicos tales como glutatión y tiorredoxina y, por lo tanto, su formación se ha considerado un proceso irreversible. Una vez que la Prx se ha convertido en ácido sulfínico ya no es enzimáticamente activa, y la enzima inactiva se acumula en las células expuestas a estrés oxidativo (Wood Z. A., y col. Trends Biochem Sci. 28: 32-40, 2003). Sin embargo, más recientemente se ha observado una recuperación gradual de las Prx después de la inactivación oxidativa inicial en células eucariotas (Mitsumoto A., y col. Free Radic Biol Med. 30: 625-35, 2001; Woo H. A., y col. Science. 300: 6536, 2003) y se ha propuesto a las sestrinas como las enzimas catalizantes debido a su homología con el homólogo de sestrina bacteriano —AhpD—, que regenera la AhpC Prx, y debido a su capacidad para reducir los niveles de ROS intracelulares (Budanov A. V., y col. Science. 304:596-600, 2004).
Se cree que en células eucariotas las Prx son tanto antioxidantes que protegen frente al estrés como reguladores de la señalización mediada por ROS (Wood Z. A., y col. Science. 300: 650-3, 2003). Se ha sabido durante algún tiempo que las interacciones de ligando/receptor generan explosiones de ROS, que actúan como segundos mensajeros en las rutas de transducción de señales, incluyendo la ruta de TGF-β (Bae Y. S., y col. J Biol Chem. 272: 217-21, 1997; Lo... [Seguir leyendo]
Reivindicaciones:
1. Un modelo animal de roedor que no expresa una o más sestrinas funcionales o que expresa niveles de traducción reducidos al menos el 50% de una o más sestrinas, y que no expresa proteína de unión al factor de crecimiento transformante β latente 4 (ltbp4) o que expresa niveles de traducción reducidos al menos el 50% de ltbp4.
2. El modelo animal de roedor de la reivindicación 1, en el que
(i) el genoma del roedor comprende una interrupción homocigota o heterocigota de un gen de sestrina, seleccionándose preferentemente el gen de sestrina interrumpido de sestrina 1, sestrina 2 y sestrina 3, y siendo más preferentemente sestrina 2; y/o
(ii) el genoma del roedor comprende una interrupción homocigota o heterocigota del gen de ltbp4.
3. El modelo animal de roedor de la reivindicación 2, en el que la interrupción se genera por una mutación, y preferentemente dicha mutación
(i) es una mutación por inserción, deleción o sustitución; y/o
(ii) se genera por direccionamiento génico, atrapamiento génico o mutagénesis química; y/o
(iii) se ha producido en un exón, intrón, región reguladora o sitio de corte y empalme de los genes de sestrina y ltbp4; y/o
(iv) da origen a la expresión de un gen indicador; y/o
(v) se ha producido en el 9º intrón del gen de sestrina 2; y/o
(vi) se ha producido en el 5º intrón del gen de ltpb4.
4. El modelo de animal roedor de la reivindicación 2 ó 3, en el que
(i) el gen de sestrina 2 se interrumpe en el 9º intrón por inserción de un vector de trampa de genes, preferentemente pT1bgeo (SEC ID Nº: 10); y/o
(ii) el gen de ltbp4 se interrumpe en el 5º intrón por inserción de un vector de trampa de genes, preferentemente U3Cre (SEC ID Nº: 16).
5. El modelo animal de roedor de una cualquiera de las reivindicaciones 1 a 4, en el que
(i) dicho roedor es un ratón o rata; y/o
(ii) dicho roedor muestra enfisema pulmonar y cáncer, preferentemente el cáncer es un cáncer de colon.
6. Un modelo animal de roedor que no expresa una o más sestrinas funcionales o que expresa niveles de traducción reducidos al menos el 50% de una o más sestrinas, siendo preferentemente dicho modelo animal de roedor como se define en las reivindicaciones 1 a 5.
7. Un cultivo celular o tisular aislado de los modelos animales de roedor de las reivindicaciones 1 a 6, en el que los niveles de expresión en la célula o en las células del tejido, de las proteínas sestrina y ltbp4 son como se define en las reivindicaciones 1 a 6.
8. El cultivo celular o tisular de la reivindicación 7, en el que el cultivo celular o tisular es de pulmón o colon.
9. Un procedimiento para preparar el modelo animal de roedor de las reivindicaciones 1 a 6, que comprende interrumpir el gen de sestrina y/o ltbp4 en una célula germinal de un roedor de partida.
10. El procedimiento de la reivindicación 9, en el que la célula germinal es una célula ES.
11. Un procedimiento para seleccionar un agente para tratar un síntoma que aparece en el modelo animal de roedor de la reivindicación 1, que comprende:
(i) aplicar uno o más agentes a ensayar a dicho modelo animal de roedor,
(ii) determinar si uno o más síntomas que aparecen en dicho modelo animal de roedor han cambiado como resultado de la aplicación de dicho agente o agentes.
12. El procedimiento de la reivindicación 11, en el que el síntoma se selecciona de un grupo que consiste en cáncer y enfisema pulmonar.
13. Un procedimiento de selección de un agente que interfiere con la producción de ROS y la señalización de TGFβ, que comprende:
(i) aplicar uno o más agentes a ensayar al cultivo celular o tisular de la reivindicación 7,
(ii) determinar si los niveles de ROS celulares y la señalización de TGF-β han cambiado como resultado de la aplicación de dicho agente o agentes.
14. El procedimiento de la reivindicación 13, en el que el cultivo celular o tisular es de pulmón o colon.
15. Un procedimiento para analizar si el cáncer y/o enfisema pulmonar está causado por una expresión proteica o génica de ltbp4 y sestrina o un nivel de expresión diferencial o por un defecto en el gen de ltbp4 y sestrina, que comprende:
(i) caracterizar la expresión proteica o génica de ltbp4 y sestrina o el nivel de expresión o el estado alélico del 5 gen de ltbp4 y sestrina de un individuo que tiene cáncer o enfisema pulmonar,
(ii) caracterizar la expresión proteica o génica de ltbp4 y sestrina o el nivel de expresión o el estado alélico del gen de ltbp4 y sestrina de un individuo de control, indicando una diferencia en la expresión proteica o génica de ltbp4 y sestrina o el nivel de expresión o el estado alélico del gen de ltbp4 y sestrina que el cáncer y/o el enfisema pulmonar y/o la cardiomiopatía está relacionada con una expresión proteica o génica de ltbp4 y
10 sestrina o un nivel de expresión diferencial o por un defecto en los genes de ltbp4 y sestrina.
16. El procedimiento de la reivindicación 15, en el que
(i) la expresión de ltbp4 y sestrina o el nivel de expresión se detecta por RT-PCR, análisis de Northern, análisis de micromatrices o anticuerpos dirigidos contra las proteínas ltbp4 y sestrina; y/o
(ii) la expresión génica de ltbp4 y sestrina o el nivel de expresión se detecta por RT-PCR, análisis de Northern, 15 análisis de micromatrices o anticuerpos dirigidos contra las proteínas ltbp4 y sestrina; y/o
(iii) el estado alélico del gen de ltbp4 y sestrina se detecta por exploración de mutaciones.
Patentes similares o relacionadas:
BLOQUEO DE LA MIGRACIÓN DE LEUCOCITOS Y DE LA INFLAMACIÓN POR INTERFERENCIA CON CD99/HEC2, del 17 de Noviembre de 2011, de CORNELL RESEARCH FOUNDATION, INC.: Un anticuerpo anti-CD99 que inhibe la migración transendotelial (MTE) de leucocitos mediada por CD99, para uso en un procedimiento para el tratamiento de una estado […]
MODELO ANIMAL QUIMERICO SUSCEPTIBLE A LA INFECCION POR VIRUS DE LA HEPATITIS C HUMANO, del 19 de Octubre de 2010, de KNETEMAN, NORMAN M. TYRRELL, LORNE D. MERCER, DAVID F: Ratón transgénico quimérico huésped infectado con el virus de la hepatitis C humano (VHC) que comprende: un ratón transgénico inmunodeficiente, deficiente […]
 UTILIZACION DE UN AGONISTA DE GALANINA EN LA PREPARACION DE UN MEDICAMENTO PARA MEJORAR LA MEMORIA Y OTRAS FUNCIONES COGNITIVAS, del 14 de Junio de 2010, de NEUROTARGETS LIMITED: Utilización de un agonista de galanina en la preparación de un medicamento para mejorar la memoria y otras funciones cognitivas
UTILIZACION DE UN AGONISTA DE GALANINA EN LA PREPARACION DE UN MEDICAMENTO PARA MEJORAR LA MEMORIA Y OTRAS FUNCIONES COGNITIVAS, del 14 de Junio de 2010, de NEUROTARGETS LIMITED: Utilización de un agonista de galanina en la preparación de un medicamento para mejorar la memoria y otras funciones cognitivas
USO DE SECUENCIAS REGULATORIAS PARA LA EXPRESION TRANSITORIA ESPECIFICA EN CELULAS DETERMINADAS DE MANERA NEURONAL, del 8 de Marzo de 2010, de F. HOFFMANN-LA ROCHE AG: Uso de una secuencia reguladora seleccionada del grupo que consiste en (a) secuencias reguladoras que comprenden la secuencia de nucleótidos mostrada […]
 UN METODO PARA TRATAMIENTO Y PROFILAXIS, del 24 de Febrero de 2010, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Un agente que inhibe la actividad del factor que estimula la colonia de granulocito (G-CSF), o el receptor del factor que estimula la colonia de granulocito […]
UN METODO PARA TRATAMIENTO Y PROFILAXIS, del 24 de Febrero de 2010, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Un agente que inhibe la actividad del factor que estimula la colonia de granulocito (G-CSF), o el receptor del factor que estimula la colonia de granulocito […]
MAMIFERO NO HUMANO MUTANTE PARA LA EXPRESION DE LA SUBUNIDAD ALFA6 DEL RECEPTOR NICOTINICO DE LA ACETICOLINA Y USO PARA SELECCIONAR SUSTANCIAS SUSCEPTIBLES DE INTERACCIONAR CON DICHO RECEPTOR, del 20 de Noviembre de 2009, de INSTITUT PASTEUR CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS): Uso de un mamífero no humano, portador de una mutación en el gen que codifica la subunidad alfa6 del receptor nicotínico de la acetilcolina (nAChR), […]
 MODELO EXPERIMENTAL DE NEUROINFLAMACION, PROCEDIMIENTO DE OBTENCION Y SUS APLICACIONES, del 1 de Diciembre de 2008, de CONSEJO SUPERIOR INVESTIGACIONES CIENTIFICAS: Modelo experimental de neuroinflamación, procedimiento de obtención y sus aplicaciones.#El modelo experimental de neuroinflamación consiste en un […]
MODELO EXPERIMENTAL DE NEUROINFLAMACION, PROCEDIMIENTO DE OBTENCION Y SUS APLICACIONES, del 1 de Diciembre de 2008, de CONSEJO SUPERIOR INVESTIGACIONES CIENTIFICAS: Modelo experimental de neuroinflamación, procedimiento de obtención y sus aplicaciones.#El modelo experimental de neuroinflamación consiste en un […]
MODELO ANIMAL PARA ADHD, del 13 de Diciembre de 2011, de UCL BUSINESS PLC: El uso de un roedor NK1-/- o un roedor que tiene un receptor funcional de la sustancia P al cual se ha administrado un antagonista del receptor […]