FACTOR INTERMEDIARIO TRANSCRIPCIONAL 2.
Un polipéptido que tiene una actividad de proteína TIF2 que comprende una secuencia de aminoácidos seleccionada entre el grupo que consiste en:
(a) aminoácidos 1 a 1464 de la SEC ID Nº: 2; (b) la secuencia de aminoácidos completa tal como ha codificado el ADNc contenido en el Nº de Depósito ATCC 97612; (c) aminoácidos 624 a 869 de la SEC ID Nº: 2; (d) aminoácidos 624 a 1131 de la SEC ID Nº: 2; (e) aminoácidos 1410 a 1131 de la SEC ID Nº: 2; (f) aminoácidos 1288 a 1464 de la SEC ID Nº: 2; (g) aminoácidos 624 a 1287 de la SEC ID Nº: 2; (h) aminoácidos 624 a 1179 de la SEC ID Nº: 2; (i) aminoácidos 624 a 1010 de la SEC ID Nº: 2; (j) aminoácidos 870 a 1179 de la SEC ID Nº: 2; (k) aminoácidos 1010 a 1179 de la SEC ID Nº: 2; (l) aminoácidos 940 a 1179 de la SEC ID Nº: 2; (m) aminoácidos 940 a 1131 de la SEC ID Nº: 2 y (n) una secuencia de aminoácidos al menos el 90 % idéntica a una cualquiera de (a) (m); en el que dicha actividad de TIF2 se selecciona del grupo que consiste en: unión a un receptor nuclear y potenciamiento de la transcripción
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E07101726.
Solicitante: INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM)
CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS)
UNIVERSITÉ DE STRASBOURG
BRISTOL-MYERS SQUIBB COMPANY.
Nacionalidad solicitante: Francia.
Dirección: 101, RUE DE TOLBIAC 75654 PARIS CEDEX 13 FRANCIA.
Inventor/es: VOEGEL, JOHANNES, CHAMBON, PIERRE, GRONEMEYER, HINRICH, LUTZ,YVES.
Fecha de Publicación: .
Fecha Solicitud PCT: 11 de Julio de 1997.
Clasificación Internacional de Patentes:
- C07K14/47A1
Clasificación PCT:
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
- C07K16/18 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C12N15/12 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas animales.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/566 G01N 33/00 […] › utilizando un soporte específico o proteínas receptoras como reactivos para la formación de uniones por ligando.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia.
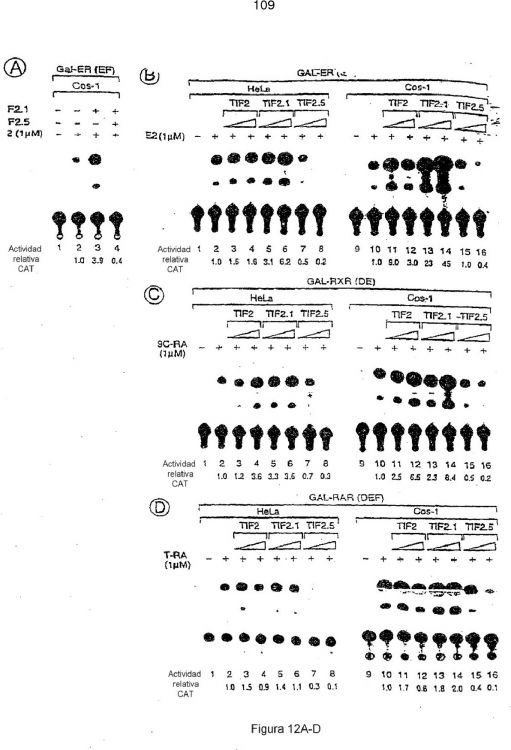
Fragmento de la descripción:
Campo de la Invención
La presente invención se refiere a un mediador transcripcional de receptor nuclear (RN). Más específicamente, se dan a conocer moléculas de ácidos nucleicos aisladas que codifican factor intermediario transcripcional 2 (TIF2). Los procedimientos recombinantes para producir polipéptidos TIF2 también se dan a conocer ya que son procedimientos de exploración para identificar agonistas y antagonistas de la función de activación AF-2 de receptores nucleares, así como anticuerpos TIF2. También se dan a conocer procedimientos de exploración para identificar agonistas y antagonistas de la actividad del dominio de activación AD1 de TIF2, así como se dan a conocer procedimientos de exploración para identificar agonistas y antagonistas de la actividad del dominio de activación AD2 de TIF2. Antecedentes de la Invención
Los activadores que potencian la iniciación de la transcripción por ARN polimerasa B (II) están compuestos de al menos dos dominios funcionales: un dominio de unión a ADN y un dominio de activación (M. Ptashne, Nature 335: 683-689 (1988); P. J. Mitchell y col., Science
245: 371-378 (1989)). Estos dos dominios son generalmente unidades funcionales separables y cada una puede de hecho intercambiarse con la región complementaria de un activador no relacionado, produciendo por lo tanto activadores quiméricos funcionales (S. Green y col., Nature 325: 75-78 (1987)).
Se han realizado varios análisis de función-estructura de la transcripción de eucariotas, centrándose principalmente en las proteínas de levadura GAL4 y GUN4 y en miembros de la familia de receptores nucleares. Las proteínas GAL4 y GCN4 activan la transcripción uniéndose a secuencias de activación cadena arriba específicas, que tienen muchas de las características de elementos potenciadores de eucariotas superiores (K. Struhl, Cell 49: 295297 (1987)). El activador de herpes simplex VP16 representa otro tipo de activador, que activa la transcripción uniéndose al factor de transcripción del octámero unido a ADN en lugar de unirse al ADN directamente (T. Gerster y col., Proc. Natl. Acad Sci. USA 85: 6347-6351 (1988)).
La familia de los receptores nucleares que incluye receptores de hormonas esteroideas, hormonas tiroideas, vitamina D y el derivado de vitamina A ácido retinoico, son también factores que potencian la transcripción que se unen a ADN directamente en presencia de su ligando afín por reconocimiento de elementos potenciadores específicos, es decir, elementos sensibles a hormona o ligando (R. M. Evans, Cell 240: 889-895 (1988)). Estos ligandos afines tienden a ser moléculas pequeñas hidrófobas, que incluyen hormonas esteroideas tales como estrógeno y progesterona, hormona tiroidea, vitamina D y varios retinoides (S. Halachmi y col.,
Science 264: 1455-1458 (1994); Gronemeyer, H. y Laudet, V., Protein Profile 2: 1173-1308 (1995)).
A pesar de su pequeño tamaño y aparentemente simple estructura, sin embargo, se sabe que los ligandos afines asociados con RN inducen un amplio intervalo de respuestas fisiológicas. Los esteroides adrenales por ejemplo, tales como cortisol y aldosterona, influyen ampliamente en la homeostasis corporal, controlando el glucógeno y metabolismo mineral, tienen efectos generalizados en los sistemas inmune y nervioso e influyen sobre el crecimiento y diferenciación de células en cultivo. Las hormonas sexuales (progesterona, estrógenos y testosterona) provocan el desarrollo y determinación del sistema reproductor embrionario, feminizan/masculinizan el cerebro al nacimiento, controlan la reproducción y comportamiento relacionado en adultos y son responsables del desarrollo de los caracteres sexuales secundarios. La vitamina D es necesaria para el desarrollo óseo adecuado y desempeña un papel crítico en el metabolismo del calcio y la diferenciación del hueso. Significativamente, la producción aberrante de estas hormonas se ha asociado con un amplio espectro de enfermedades clínicas, incluyendo cáncer y afecciones patológicas similares.
Todos los RN presentan una estructura modular, con de cinco a seis regiones distintas, denominadas A-F. La región N terminal A/B contiene la función de activación AF-1, que puede activar la transcripción constitutivamente. La región C abarca el domino de unión a ADN (DBD), que reconoce elementos que actúan en cis afines. La región E contiene el dominio de unión a ligando (LBD), una superficie de dimerización y la función de activación transcripcional dependiente de ligando AF-2 (revisada en Mangelsdorft, D. J. y col., Cell 83:835-839 (1995a); Mangelsdorft & Evans, Cell 83: 841-850 (1995b); Beato, M. y col., Cell 83: 851-857 (1995); Gronemeyer & Laudet, "Transcription Factors 3: Nuclear Receptors", in Protein Profile, vol. 2, Academic Press (1995); Kastner, P. y col., EMBD J. 11: 629-642 (1992); Chambon, P., FASEB J 10: 940-954 (1996)).
Varias clases de dominios en activadores son capaces de mediar la activación transcripcional. Los activadores de levadura GAL4 y GCN4 y VP16 de herpes simplex contienen todos dominios de activación que están compuestos de secuencias de aminoácidos ácidas, que pueden actuar formando hélices α anfipáticas (I. A. Hope y col., Cell 46: 885-894 (1986); J. Ma y col., Cell 48: 847-853 (1987); E. Giniger y col., Nature 330: 670-672 (1987); S.
J. Triezenberg y col., Genes Dev. 2: 718-729 (1988)). Las funciones de activación de proteínas humanas Sp1 y CTF/NPI contienen áreas ricas en glutamina y prolina, respectivamente (A. J. Courey y col., Cell 55: 887-898 (1988); N. Mermod y col., Cell 58: 741-753 (1989)). Los estudios con receptores de hormonas esteroideas han mostrado que tanto el dominio N terminal A/B como el dominio de unión a hormona (HBD) C terminal contienen funciones de activación de la transcripción (AF) (M. T. Bocquel y col., Nucl. Acids Res., 17: 2581-2595 (1989); L. Tora y col., Cell 59: 477-487 (1989)). Las AF del receptor de estrógenos humano (hER) no contienen secuencias de aminoácidos ácidos (S. Halachmi y col., Science 264: 14551458 (1994)). Por el contrario, sin embargo, el receptor de glucocorticoides humano (hGR) contiene dos funciones de activación τ-1(localizado en el domino A/B) y τ-2 (localizado en la región N terminal del HBD), ambos de los cuales son ácidos (S. M. Hollenberg y col., Cell 55: 899-906 (1988)).
A partir de los resultados de estudio sobre interferencia/silenciamiento transcripcional entre receptores nucleares y sobre estimulación homo y heterosinérgica de iniciación de la transcripción a partir de promotores mínimos por las funciones de activación presentes en hER (AF-1 y AF-2) y el activador ácido VP16, se ha propuesto que las AF pueden activar la transcripción interaccionando con diferentes componentes del complejo de iniciación básico (Bocquel y col., Nucl. Acids. Res. 17: 2581-2595 (1989); Meyer y col., Cell 57: 433-442 (1989),
L. Tora y col., Cell 59: 477-487 (1989)). Los estudios de las propiedades de interferencia/silenciamiento transcripcional de AAD, hER AF-1 y hER AF-2, sin embargo, mostraron que tanto hER AF-1 como AF-2 pueden silenciar activadores ácidos, tales como VP16, pero que lo contrario no era cierto, es decir, AAD no silencia hER AF-1 o AF-2. Sin embargo, hER AF-1 y AF-2, que se distinguen claramente por sus propiedades sinérgicas, sin embargo se silenciaban entre ellos (D. Tasset y col., Cell 62: 1177-1187 (1990)).
Basándose en estos resultados, se propuso que existe una serie de factores intermediarios transcripcionales (TIF), interpuesta entre factores potenciadores y los factores transcripcionales básicos. Por ejemplo, se ha sugerido que AF-1 y AF-2 se ponen en contacto con la serie de TIF a puntos funcionalmente equivalentes, mientras que se cree que AAD interaccionan en un punto más temprano en la serie (D. Tasset y col., Cell 62: 11771187(1990)).
Se han caracterizado varios TIF coactivadores potenciales para RN AF-2 (véase Chambon, P., FASEB J 10: 940-954 (1996); Glass, C. K. y col., Current Opin. Cell Biol. 9: 222232 (1997); Horwitz, K. B. y col., Mol. Endocrinol. 10: 1167-1177 (1996) para revisiones recientes). Voegel. J. y col., EMBO J. 15: 3667-3675(1996) han clonado un TIF2 de longitud completa que exhibe las propiedades esperadas para un mediador de AF-2. LeDouarin, B. y col., EMBO J. 15: 6701-6715 (1996) han demostrado que un fragmento de 10 aminoácidos de TIF1α es necesario y suficiente para mediar la interacción con RXR en un ligando de un modo dependiente de integridad de AF-2 y ligando. Notablemente, dentro de este fragmento...
Reivindicaciones:
1. Un polipéptido que tiene una actividad de proteína TIF2 que comprende una secuencia de aminoácidos seleccionada entre el grupo que consiste en:
(a) aminoácidos 1 a 1464 de la SEC ID Nº: 2;
(b) la secuencia de aminoácidos completa tal como ha codificado el ADNc contenido en el Nº de Depósito ATCC 97612;
(c) aminoácidos 624 a 869 de la SEC ID Nº: 2;
(d) aminoácidos 624 a 1131 de la SEC ID Nº: 2;
(e) aminoácidos 1410 a 1131 de la SEC ID Nº: 2;
(f) aminoácidos 1288 a 1464 de la SEC ID Nº: 2;
(g) aminoácidos 624 a 1287 de la SEC ID Nº: 2;
(h) aminoácidos 624 a 1179 de la SEC ID Nº: 2;
(i) aminoácidos 624 a 1010 de la SEC ID Nº: 2;
(j) aminoácidos 870 a 1179 de la SEC ID Nº: 2;
(k) aminoácidos 1010 a 1179 de la SEC ID Nº: 2;
(l) aminoácidos 940 a 1179 de la SEC ID Nº: 2;
(m) aminoácidos 940 a 1131 de la SEC ID Nº: 2 y
(n) una secuencia de aminoácidos al menos el 90 % idéntica a una cualquiera de (a)
(m); en el que dicha actividad de TIF2 se selecciona del grupo que consiste en: unión a un receptor nuclear y potenciamiento de la transcripción.
2. El polipéptido de la reivindicación 1, en el que la secuencia de aminoácidos de (n) es al menos el 95 % idéntica a una cualquiera de (a)-(m).
3. El polipéptido de la reivindicación 1 ó 2, que es producida por una célula huésped recombinante.
Patentes similares o relacionadas:
MÉTODOS Y MATERIALES PARA GENERAR DOMINIOS SH3 CON PROPIEDADES DE UNIÓN SELECCIONADAS, del 3 de Enero de 2012, de NEXT BIOMED TECHNOLOGIES NBT OY: Método para generar dominios SH3 con propiedades de unión seleccionadas, que consta de a) Producir una colección de dominios SH3 que contengan […]
FACTOR DE REPROGRAMACIÓN CELULAR, del 4 de Noviembre de 2011, de KYOTO UNIVERSITY: Un factor de reprogramación celular para una célula somática que comprende: a) un gen de la familia Oct o producto génico; b) un gen de la familia Klf o producto génico; y […]
SECUENCIA DE MECP2 SINTÉTICA PARA LA TERAPIA DE SUSTITUCIÓN DE PROTEÍNAS, del 29 de Junio de 2011, de GEORG-AUGUST-UNIVERSITÄT GÖTTINGEN STIFTUNG ÖFFENTLICHEN RECHTS: Un polipéptido que comprende (i) una proteína MeCP2 o fragmento biológicamente activo o un derivado de dicha proteína o fragmento, y (ii) un dominio […]
COMPOSICIONES Y METODOS PARA INHIBIR LA ACTIVIDAD DE P300, del 17 de Febrero de 2011, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: La invención se relaciona con variantes del dominio N-terminal de activación de transcripción de p300 que presentan mutaciones en los sitios de fosforilación […]
 MODELOS DE RATONES CON ENVEJECIMIENTO PREMATURO DESTINADOS A LA DEFINICION DEL PAPEL DEL DAÑO DEL ADN DERIVADO DEL ENVEJECIMIENTO E INTERVENCION EN UNA PATOLOGIA RELACIONADA CON EL ENVEJECIMIENTO, del 10 de Septiembre de 2010, de ERASMUS MC: Un método para la selección de un compuesto, o una mezcla de compuestos, comprendiendo dicho método los pasos de:
- proporcionar un ratón alterado […]
MODELOS DE RATONES CON ENVEJECIMIENTO PREMATURO DESTINADOS A LA DEFINICION DEL PAPEL DEL DAÑO DEL ADN DERIVADO DEL ENVEJECIMIENTO E INTERVENCION EN UNA PATOLOGIA RELACIONADA CON EL ENVEJECIMIENTO, del 10 de Septiembre de 2010, de ERASMUS MC: Un método para la selección de un compuesto, o una mezcla de compuestos, comprendiendo dicho método los pasos de:
- proporcionar un ratón alterado […]
SECUENCIAS DE ADN CON ACTIVIDAD ANTI-REPRESORA, del 17 de Agosto de 2010, de CHROMAGENICS B.V.: Una secuencia de ADN aislada y/o recombinante que tiene actividad anti-represora, seleccionada dicha secuencia del grupo que consiste en: (a) […]
SECUENCIAS DE ADN CON ACTIVIDAD ANTI-REPRESORA, del 17 de Agosto de 2010, de CHROMAGENICS B.V.: Una secuencia de ADN aislada y/o recombinante que tiene actividad anti-represora, seleccionada dicha secuencia del grupo que consiste en: (a) el SEQ ID: 27 […]
 CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]