COMPOSICIONES POLIMÉRICAS LÍQUIDAS PARA LA LIBERACIÓN CONTROLADA DE SUSTANCIAS BIOACTIVAS.
Una composición polimérica líquida para la liberación controlada de eprinomectina que consiste esencialmente en:
(a) de 1 a 10% en p/v de eprinomectina; (b) de 1 a 10% en p/v de copolímero poli(lactida-co-glicólido); en la que la proporción en peso entre el copolímero poli(lactida-co-glicólido) y la eprinomectina es 1:1 o inferior y la proporción lactida:glicólido del copolímero poli(lactida-co-glicólido) es de 75:25 a 65:35; y (c) una mezcla de disolventes hidrófilos y lipófilos, en la que la proporción en volumen de los disolventes hidrófilos y lipófilos es de 80:20 a 5:95
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E04076699.
Solicitante: MERCK SHARP & DOHME CORP.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 126 EAST LINCOLN AVENUE RAHWAY, NJ 07065 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHERN, REY, T., ZINGERMAN, JOEL, R.
Fecha de Publicación: .
Fecha Solicitud PCT: 18 de Marzo de 1999.
Clasificación PCT:
- A61F2/02 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › Prótesis implantables en el cuerpo.
- A61K9/50 A61 […] › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Microcápsulas (A61K 9/52 tiene prioridad).
- B01J13/02 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 13/00 Química de los coloides, p. ej. producción de sustancias coloidales o de sus soluciones, no prevista en otro lugar; Fabricación de microcápsulas o de microbolas. › Fabricación de microcápsulas o de microbolas.
- B32B5/16 B […] › B32 PRODUCTOS ESTRATIFICADOS. › B32B PRODUCTOS ESTRATIFICADOS, es decir, HECHOS DE VARIAS CAPAS DE FORMA PLANA O NO PLANA, p. ej. CELULAR O EN NIDO DE ABEJA. › B32B 5/00 Productos estratificados caracterizados por la heterogeneidad o estructura física de una de las capas (B32B 9/00 - B32B 29/00 tienen prioridad). › caracterizados por el hecho de que una de las capas está formada por partículas, p. ej. virutas, fibras cortadas, polvo.
Clasificación antigua:
- A61F2/02 A61F 2/00 […] › Prótesis implantables en el cuerpo.
- A61K9/50 A61K 9/00 […] › Microcápsulas (A61K 9/52 tiene prioridad).
- B01J13/02 B01J 13/00 […] › Fabricación de microcápsulas o de microbolas.
- B32B5/16 B32B 5/00 […] › caracterizados por el hecho de que una de las capas está formada por partículas, p. ej. virutas, fibras cortadas, polvo.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2359973_T3.pdf
Fragmento de la descripción:
Campo de la invención
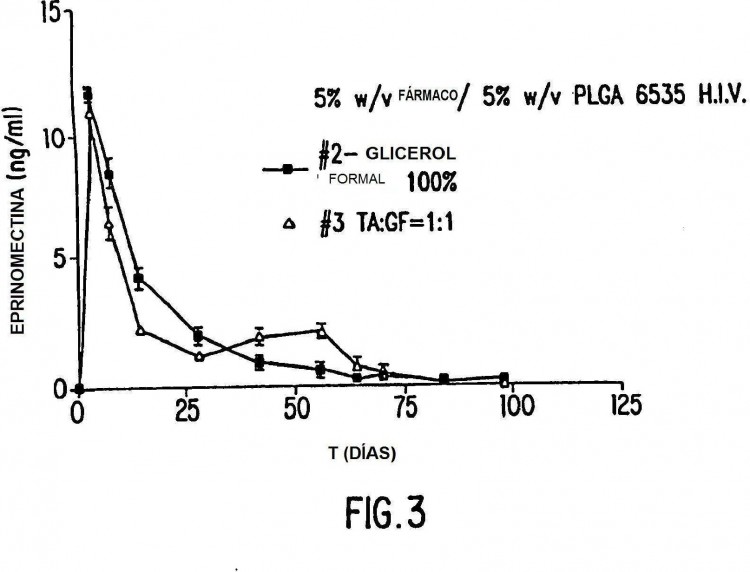
La presente invención se refiere a composiciones poliméricas líquidas para la liberación controlada de una sustancia bioactiva, es decir una sustancia bioactiva hidrófoba, tal como una composición polimérica líquida que puede formar un líquido encapsulado en película, por ejemplo in situ, y/o que puede conseguir una liberación sostenida a largo plazo en un paciente o huésped (p. ej., animal o ser humano) tal como perfiles plasmáticos que muestran una eficacia elevada (superior al 70%, tal como al menos 80%, preferentemente al menos 90%, por ejemplo una eficacia de aproximadamente 100% durante más de 12 meses y/o niveles en plasma sostenidos durante al menos 50 o aproximadamente 60 días o al menos aproximadamente dos meses o al menos aproximadamente ocho semanas, por ejemplo al menos 90 días o aproximadamente tres meses o aproximadamente 12 semanas o al menos 120 días o aproximadamente cuatro meses o aproximadamente 16 semanas, o al menos 150 días o aproximadamente cinco meses o aproximadamente 20 semanas o incluso más prolongado, por ejemplo hasta un año o más; por ejemplo de 1 a 12 meses.
La presente invención además se refiere a una composición polimérica líquida que consiste esencialmente en (1) 110% en p/v de sustancia bioactiva (es decir, sustancia bioactiva hidrófoba que es eprinomectina); (2) 1-10% en p/v de un “polímero” biológicamente aceptable (es decir, “copolímero”, un polímero polimerizado mediante al menos dos comonómeros) (es decir, copolímero poli(lactida-glicólido), en el que la proporción en peso entre el polímero y la sustancia bioactiva puede ser 1:1 o menor, por ejemplo de 0,3:1 a 1:1; y (3) una mezcla de disolventes hidrófilos y lipófilos en la que la proporción en volumen entre los disolventes hidrófilos y lipófilos es de 80:20 a 5:45, por ejemplo de
80:20 a 10:90 o 5:95, disolventes hidrófilos y lipófilos, por ejemplo de 65:35 a 35:65, y/o en la que el disolvente lipófilo o inmiscible en agua está presente en una cantidad de al menos 16,5% en peso (p. ej., incluido aproximadamente 16,465% en peso), tal como al menos de 16,5% a 45% en peso, por ejemplo al menos de 16,5% a 30% en peso (p. ej., al menos 29% en peso) o al menos más de 40% en peso (por ejemplo y al menos aproximadamente 42-45% en peso); por ejemplo composiciones tales en las que haya menos del 10% del polímero y de 1 a 10% de la sustancia activa bioactiva o aproximadamente menos de 7% (p. ej., 6,7%) o 5% o menos polímero, con el contenido en sustancia bioactiva inferior o igual a aproximadamente 10% o 5%.
La presente invención además también se refiere a una composición polimérica líquida que consiste esencialmente en lo anterior, en la que la composición polimérica líquida es capaz de formar un líquido encapsulado en película por ejemplo in situ, y/o que tiene liberación sostenida a largo plazo, en la que el término “que consiste esencialmente en” se usa en el sentido que se le ha atribuido en documentos de patentes y el término es excluyente en cuanto a los ingredientes que pueden obstaculizar la capacidad de la composición para formar así un líquido encapsulado en película.
La presente invención además también se refiere a procedimientos para fabricar, y describe el uso, dichas composiciones. Por ejemplo, un procedimiento para fabricar dichas composiciones que comprende mezclar los ingredientes mencionados con anterioridad; por ejemplo, disolver, preferentemente, tanto el polímero como la sustancia bioactiva (en oposición a suspender, encapsular o tener presente como un sólido, la sustancia bioactiva, que, aunque no necesariamente excluida por la invención, puede ser menos preferible a disolver). O, un procedimiento para el uso de dichas composiciones, que comprende administrar a un paciente o huésped (animal, por ejemplo un mamífero tal como un animal doméstico, por ejemplo un animal de compañía o animal de alimentación o un ser humano) una composición de la invención.
Éstos y otros aspectos a los que se refiere la invención serán evidentes a partir del texto siguiente. En el texto siguiente se citan varios documentos, sin ninguna admisión de que ninguno de estos documentos sea la técnica anterior en lo que respecta a la invención.
Antecedentes de la invención
Se han usado polímeros biodegradables en formulaciones parenterales de liberación controlada de compuestos bioactivos. En un enfoque, el polímero se fabrica dentro de microesferas que se pueden inyectar a través de una jeringuilla y el compuesto bioactivo queda atrapado dentro de las microesferas. No se ha probado que este enfoque sea práctico, en parte debido a la dificultad en el procedimiento de fabricación para producir productos estériles y reproducibles y al elevado coste de la fabricación. En otro enfoque, el polímero biodegradable y el material bioactivo se disuelven en un disolvente biocompatible miscible en agua para proporcionar una composición líquida. Cuando la composición líquida se inyecta en el cuerpo, el disolvente se disipa al entorno acuoso que lo rodea y el polímero forma un depósito sólido del que se libera el material bioactivo.
La solicitud de patente europea 0537559 se refiere a composiciones poliméricas que tienen un polímero termoplástico, agente modificador de la velocidad, material bioactivo hidrosoluble y disolvente orgánico miscible en agua. Tras la exposición a un entorno acuoso (p. ej., fluidos corporales), la composición líquida es capaz de formar una matriz polimérica sólida microporosa biodegradable para la liberación controlada de materiales bioactivos hidrosolubles o dispersables en agua durante aproximadamente cuatro semanas. El polímero termoplástico puede ser, entre muchos citados, polilactida, poliglicólido, policaprolactona o copolímeros de los mismos, y se usa a una concentración elevada (de 45 a 50%). El agente modificador de la velocidad puede ser, entre otros muchos citados, triacetato de glicerol (triacetina); no obstante, sólo se pone de ejemplo heptanoato de etilo; y la cantidad del agente modificador de la velocidad no es superior a 15%.
De hecho, con respecto a la literatura de patentes, se hace referencia a: Estos documentos tienden a proporcionar composiciones que forman una masa sólida, en gel o coagulada; por ejemplo, en estos documentos se contempla una cantidad significativa de polímero, similar a la solicitud de patente europea 0537559.
Nº DE PATENTE INVENTOR 4.150.108 Graham 4.329.332 Couvreur y col. 4.331.652 Ludwig y col. 4.333.919 Kleber y col. 4.389.330 Tice y col. 4.489.055 Couvreur y col. 4.526.938 Churchill y col. 4.530.840 Tice y col. 4.542.025 Tice y col. 4.563.489 Urist 4.675.189 Kent y col. 4.677.191 Tanaka y col. 4.683.288 Tanaka y col. 4.758.435 Schaaf 4.857.335 Bohm 4.931.287 Bae y col. 5.178.872 Ohtsubo y col. 5.252.701 Jarrett y col. 5.275.820 Chang 5.478.564 Wantier y col. 5.540.912 Roorda y col. 5.447.725 Damani y col. 5.599.852 Scopelianos y col. 5.607.686 Totakura y col. 5.609.886 Wantier y col. 5.631.015 Bezwada y col. 5.654.010 Herbert y col. 5.700.485 Johnson y col. 5.702.717 Berde y col. 5.711.968 Tracy y col. 5.733.566 Lewis 4.938.763 Dunn y col. 5.077.049 Dunn y col. 5.278.201 Dunn y col. 5.278.202 Dunn y col. 5.288.496 Lewis 5.324.519 Dunn y col. 5.324.520 Dunn y col. 5.340.849 Dunn y col. 5.368.859 Dunn y col. 5.401.507 Lewis 5.419.910 Lewis 5.427.796 Lewis 5.487.897 Polson y col. 5.599.552 Dunn y col. 5.632.727 Tipton y col. 5.643.595 Lexis 5.660.849 Polson y col. 5.686.092 Lewis y col. 5.702.716 Dunn y col. 5.707.647 Dunn y col. 5.717.030 Dunn y col. 5.725.491 Tipton y col. 5.733.950 Dunn y col. 5.736.152 Dunn y col. 5.744.153 Yewey y col. 5.759.563 Yewey y col. 5.780.044 Yewey y col.También se menciona: Shah y col. (J. Controlled Release. 1993, 27:139-147), en relación a formulaciones para liberación sostenida de compuestos bioactivos que contienen varias concentraciones de copolímero de ácido poli(láctico-coglicólico) (PLGA) disuelto en vehículos tales como triacetina; Lambert y Peck (J. Controlled Release, 1995, 33:189 195), como estudio de la liberación de proteína de una solución de PLGA al 20% en N-metilpirrolidona expuesta a fluido acuoso; y Shivley y col. (J. Controlled Release, 1995, 33:237-243), como estudio del parámetro de solubilidad del copolímero poli(lactida-co-glicólido) en diversos disolventes y la liberación in vivo de naltrexona a partir de dos implantes inyectables (5% de naltrexona en 57% de PLGA y 38% de N-metilpirrolidona o 35% de PLGA y 60% de N-metilpirrolidona).
No obstante, existe la necesidad de composiciones de liberación... [Seguir leyendo]
Reivindicaciones:
1. Una composición polimérica líquida para la liberación controlada de eprinomectina que consiste esencialmente en:
(a) de 1 a 10% en p/v de eprinomectina;
(b) de 1 a 10% en p/v de copolímero poli(lactida-co-glicólido);
en la que la proporción en peso entre el copolímero poli(lactida-co-glicólido) y la eprinomectina es 1:1 o inferior y la proporción lactida:glicólido del copolímero poli(lactida-co-glicólido) es de 75:25 a 65:35; y
(c) una mezcla de disolventes hidrófilos y lipófilos, en la que la proporción en volumen de los disolventes hidrófilos y lipófilos es de 80:20 a 5:95. 2. La composición de acuerdo con la reivindicación 1, en la que el disolvente lipófilo es triacetina.
3. La composición de acuerdo con la reivindicación 1 ó 2, en la que el disolvente hidrófilo es N-metil-pirrolidona. 4. La composición de cualquiera de las reivindicaciones precedentes, en la que (a) consiste en aproximadamente 5% en p/v de eprinomectina.
5. La composición de cualquiera de las reivindicaciones precedentes, en la que la proporción lactida:glicólido del
copolímero poli(lactida-co-glicólido) es de aproximadamente 75:25. 6. La composición de cualquiera de las reivindicaciones precedentes, en la que (b) es 5% en p/v de copolímero poli(lactida-co-glicólido).
7. Uso de una composición como se ha definido en cualquiera de las reivindicaciones precedentes para la fabricación de un medicamento para tratar a un mamífero. 8. El uso de acuerdo con la reivindicación 7, en el que el mamífero es un bovino. 9. El uso de acuerdo con la reivindicación 7, en el que el mamífero es ovino.
10. El uso de acuerdo con la reivindicación 7, en el que el mamífero es canino. 11. Una composición como se ha definido en una cualquiera de las reivindicaciones 1 a 6 para usar en un procedimiento de tratamiento como se ha definido en la reivindicación 8, 9 ó 10.
Patentes similares o relacionadas:
Composición que comprende hidrocortisona, del 22 de Julio de 2020, de Diurnal Limited: Una composición farmacéutica adaptada para administración oral que comprende: i) un portador que consiste esencialmente en partículas de celulosa microcristalina […]
Microesferas o micropartículas biodegradables o bioerosionables de liberación con el tiempo en suspensión en una formulación de fármaco inyectable de formación de depósito solidificante, del 8 de Julio de 2020, de ALLERGAN, INC.: Material compuesto para la administración de fármacos, que comprende: una pluralidad de micropartículas dispersas en una composición de medios; en el que las micropartículas […]
MATERIAL QUE INCORPORA VITAMINA D PARA SU POSTERIOR LIBERACIÓN Y MÉTODO PARA OBTENER DICHO MATERIAL, del 2 de Julio de 2020, de UNIVERSIDAD DE SANTIAGO DE CHILE: La presente invención se relaciona al campo de los materiales, más en específico al tratamiento de materiales para la liberación de compuestos activos […]
Composiciones y métodos no hormonales para la anticoncepción masculina que comprenden (R)-Silodosina, del 1 de Julio de 2020, de Laboratoires Major: Composición para su uso en un método anticonceptivo no hormonal para un sujeto masculino, en la que dicha composición es una formulación de liberación prolongada […]
Sales de butirato para uso en enfermedades inflamatorias, del 17 de Junio de 2020, de Birrbeheer B.V: Una preparación que comprende una sal de butirato para uso en el tratamiento de un sujeto que padece una enfermedad que está asociada con inflamación sistémica, […]
Formulaciones de ganaxolona y procedimientos para la preparación y uso de las mismas, del 3 de Junio de 2020, de Marinus Pharmaceuticals, Inc: Una composición que comprende partículas que comprenden ganaxolona; un polímero hidrófilo; un agente humectante; y un agente complejante, en la que el diámetro medio ponderado […]
Sistema para dirigir agentes hacia dentro de un ojo, del 3 de Junio de 2020, de UNIVERSITY OF MARYLAND: Un sistema para dirigir un agente hacia el interior o a traves de un tejido, que comprende: (a) un agente que es magnetico o magnetizable o que responde magneticamente; […]
Composiciones de polifenol, del 3 de Junio de 2020, de Nugerontix Limited: Enoteína B para uso en terapia para tratar, prevenir o retrasar la aparición de disfunción endotelial donde el tratamiento, prevención o retraso comprende […]