SOLVATO DE ACETONA DE FTALOILAMLODIPINO.
Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6- metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3- etilo y 5-metilo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/053737.
Solicitante: ESTEVE QUIMICA, S.A..
Nacionalidad solicitante: España.
Inventor/es: BERENGUER MAIMO,RAMON, MEDRANO RUPEREZ,JORGE, MERODIO CABANILLAS,JUAN,FRANCISCO.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Junio de 2010.
Clasificación Internacional de Patentes:
- C07D401/12 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
Clasificación PCT:
- C07D401/12 C07D 401/00 […] › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
5 La presente invención está dirigida a un solvato de acetona de ftaloilamlodipino, un procedimiento para su preparación y su uso en la síntesis de amlodipino.
ANTECEDENTES DE LA INVENCIÓN
10 El besilato de amlodipino, también conocido como bencenosulfonato de 2-{(2-aminoetoxi)-metil-4-(2-clorofenil)-3etoxicarbonil-5-metoxicarbonil-6-metil-1,4-dihidropiridina} o bencenosulfonato de 2-((2-aminoetoxi)metil)-4-(2-clorofenil)1,4-dihidro-6-metilpiridin-3,5-dicarboxilato de 3-etilo y 5metilo o 2-[(2-aminoetoxi)metil)-4-(2-clorofenil)-1,4-dihidro-6metil-3,5-piridindicarboxilato de 3-etilo y 5-metilo o bencenosulfonato de 4-(2-clorofenil)-1,4-dihidro-6-metil-2-(2amino-etoximetil)-3,5-piridindicarboxilato de 3-etilo y 5metilo, es un fármaco antiisquémico y antihipertensivo.
**(Ver fórmula)**
Cl**(Ver fórmula)**
H3CO2C
CO2CH2CH3
**(Ver fórmula)**
**(Ver fórmula)**
SO3HO
N
**(Ver fórmula)**
NH2H
**(Ver fórmula)**
Cl H3CO2C CO2CH2CH3
O O
CH3
**(Ver fórmula)**
N**(Ver fórmula)**
NHO
Ftaloilamlodipino
Por tanto, proporcionar ftaloilamlodipino con un buen rendimiento y pureza alta es el tema central en la síntesis de 5 amlodipino, especialmente para la síntesis de besilato de
amlodipino.
En el documento US 4.572.909 se obtiene ftaloilamlodipino mediante condensación de anhídrido ftálico con la correspondiente amina libre o condensación de 2clorobenzaldehído, 4-[2-(ftalimido)etoxi]acetoacetato y 3aminocrotonato de metilo. La purificación de ftaloilamlodipino se lleva a cabo mediante precipitación en ácido acético, seguido por resuspensión en metanol.
En el documento WO00/24714 se obtiene ftaloilamlodipino mediante condensación entre 3-amino-4-(2ftalimidoetoxi)crotonato de etilo y 2-(2clorobenciliden)acetoacetato de metilo. La purificación se lleva a cabo mediante recristalización en metanol, etanol, isopropanol, tolueno o xileno.
20 En el documento JP20001002677 se purifica ftaloilamlodipino mediante recristalización en un disolvente orgánico en presencia de ácido acético. En el documento WO02053135 se purifica ftaloilamlodipino recristalizando en primer lugar en ácido acético, resuspendiendo en metanol y finalmente mediante recristalización en acetato de etilo.
El documento US 6.784.297 describe un procedimiento para la síntesis de besilato de amlodipino partiendo de anhídrido ftálico y que comprende ftaloilamlodipino como producto intermedio (etapa d)). El ftaloilamlodipino se purifica posteriormente en la etapa e) en una secuencia de dos etapas que
comprende (i) disolverlo en un disolvente orgánico en la razón 1:2-1:5 p/v seguido por (ii) precipitación mediante la adición de agua a 35-60ºC. Según una realización preferida, el disolvente en la etapa (i) es acetona. El ftaloilamlodipino libre obtenido se transforma entonces en su base y luego en besilato de amlodipino.
Los métodos de purificación de la técnica anterior requerían métodos de purificación complicados y no pueden eliminar todas las impurezas hasta los niveles requeridos por el regulador.
BREVE DESCRIPCIÓN DE LAS FIGURAS
La figura 1 muestra un difractograma de polvo de rayos X del solvato de acetona de la invención. El eje de abscisas 15 muestra los ángulos 2θ y el eje de ordenadas muestra la
intensidad.
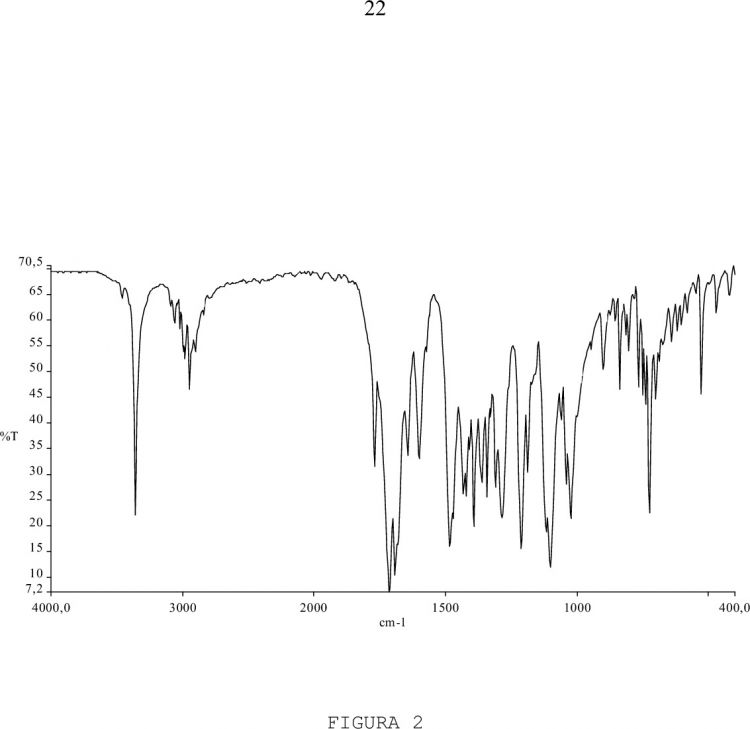
La figura 2 muestra un espectro infrarrojo del solvato de acetona de la invención. El eje de abscisas muestra la frecuencia (cm-1) y el eje de ordenadas muestra la transmitancia (%T).
SUMARIO DE LA INVENCIÓN
Los inventores han encontrado ahora sorprendentemente que el suministro de un solvato de acetona de ftaloilamlodipino 25 proporciona un método excelente para la purificación de
ftaloilamlodipino.
La recristalización de ftaloilamlodipino en acetona y enfriamiento adicional proporciona un solvato de acetona de ftaloilamlodipino con rendimiento y pureza altos, y sin la necesidad de usar métodos de tratamiento final complicados. Adicionalmente, dicho solvato de acetona de ftaloilamlodipino muestra un alto grado de cristalinidad, lo que lo hace fácil de manipular y almacenar. El solvato de acetona de ftaloilamlodipino de la invención tiene una solubilidad
excelente y puede usarse para obtener amlodipino con pureza alta.
Por tanto, según un primer aspecto, la presente invención
se refiere a un solvato de acetona de 4-(2-clorofenil)-1,4
dihidro-6-metil-2-[(2-ftalimidoetoxi)metil]-3,5
piridindicarboxilato de 3-etilo y 5-metilo.
Cl
H3CO2C CO2CH2CH3
O O
CH3
**(Ver fórmula)**
N**(Ver fórmula)**
NHOO
**(Ver fórmula)**
**(Ver fórmula)**
Solvato de acetona de ftaloilamlodipino
Según un segundo aspecto, la presente invención se refiere
10 a un procedimiento para la síntesis de dicho solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6-metil-2-[(2ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5metilo que comprende a) disolver 4-(2-clorofenil)-1,4-dihidro-6-metil-2-[(2
15 ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5-metilo en acetona a una temperatura comprendida entre por encima de 20ºC y el reflujo; y b) enfriar la mezcla hasta una temperatura comprendida entre -10º C y 20ºC con el fin de precipitar el solvato de
20 acetona de 4-(2-clorofenil)-1,4-dihidro-6-metil-2-[(2ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5-metilo. Según un tercer aspecto, la presente invención se refiere al uso de dicho solvato de acetona de 4-(2-clorofenil)-1,4dihidro-6-metil-2-[(2-ftalimidoetoxi)metil]-3,5piridindicarboxilato de 3-etilo y 5-metilo para la síntesis de 2-((2-aminoetoxi)metil)-4-(2-clorofenil)-1,4-dihidro-6metilpiridin-3,5-dicarboxilato de 3-etilo y 5-metilo, sus sales
o solvatos de los mismos, preferiblemente su sal de 30 bencenosulfonato (besilato de amlodipino).
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
Síntesis del solvato de acetona de ftaloilamlodipino
Contrariamente al método descrito en el documento US 6.784.297, el método de la invención no comprende la adición de 5 agua. En cambio, una vez que el ftaloilamlodipino se ha disuelto en acetona, se deja enfriar la mezcla hasta una temperatura comprendida entre -10º C y 20ºC. Los inventores han encontrado que en este intervalo de temperaturas, se obtiene fácilmente el solvato de acetona de ftaloilamlodipino deseado con buenos rendimientos y pureza alta. Según una realización preferida, se enfría la mezcla en la etapa b) a una temperatura comprendida entre -5ºC y 5ºC.
Se ha observado que se obtienen resultados excelentes cuando el enfriamiento en la etapa b) se realiza en dos etapas. Según una realización preferida, el enfriamiento en la etapa b) se realiza en dos etapas: un primer enfriamiento hasta una temperatura comprendida entre por encima de 5ºC y 20ºC y un segundo enfriamiento hasta una temperatura comprendida entre 10ºC y 5ºC.
20 Según una realización preferida, dicho primer enfriamiento comprende una temperatura entre 7ºC y 15ºC. Según una realización preferida, dicho primer enfriamiento comprende una temperatura entre 10ºC y 15ºC. Según una realización preferida, dicho primer enfriamiento 25 comprende una temperatura entre 8ºC y 12ºC. Según una realización preferida, dicho segundo enfriamiento comprende una temperatura entre 0ºC y 5ºC. La temperatura a la que el ftaloilamlodipino se calienta o la concentración de ftaloilamlodipino en la etapa a) del procedimiento no es crítica. El único requisito es que el ftaloilamlodipino se disuelva. Por tanto, cuanto mayor sea la temperatura y/o menor sea la concentración, más fácilmente se disuelve el ftaloilamlodipino.
Según una realización preferida, la temperatura en la 35 etapa a) está comprendida entre 30ºC y el reflujo. Según otra
realización preferida, la temperatura en la etapa a) está comprendida entre 40ºC y el reflujo. Según una realización preferida, la concentración de ftaloilamlodipino...
Reivindicaciones:
1. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo.
2. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo, caracterizado mediante un patrón de difractograma de polvo de rayos X que tiene picos expresados como ángulos 2θ a aproximadamente 10,2, 12,1, 13,0, 13,9, 15,3, 17,5, 19,7, 20,6, 22,7, 23,5 y 24,4º.
3. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo según la reivindicación 2, que muestra un difractograma de polvo de rayos X sustancialmente similar al mostrado en la figura 1.
4. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo según cualquiera de las reivindicaciones anteriores, en el que la pérdida de peso tras el análisis termogravimétrico está comprendida entre el 7 y el 12% p/p.
25 5. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo según cualquiera de las reivindicaciones anteriores, que tiene un pico endotérmico en un diagrama de calorimetría diferencial a una temperatura comprendida entre 75ºC y 85ºC.
6. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo según cualquiera de las reivindicaciones 35 anteriores, caracterizado por un espectro IR que tiene picos relevantes expresados en cm-1 a aproximadamente 3361, 2949, 1769,
1714, 1693, 1644, 1601, 1484, 1433, 1421, 1394, 1363, 1343, 1311, 1287, 1213, 1118, 1102, 1042, 1025, 727, 530.
7. Solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6metil-2-[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3etilo y 5-metilo según cualquiera de las reivindicaciones anteriores, que muestra un espectro IR sustancialmente similar al mostrado en la figura 2.
10 8. Procedimiento para la síntesis de un solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6-metil-2-[(2ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5metilo según cualquiera de las reivindicaciones 1 a 7 que comprende
15 a) disolver 4-(2-clorofenil)-1,4-dihidro-6-metil-2-[(2ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5metilo en acetona a una temperatura comprendida entre por encima de 20ºC y el reflujo; y b) enfriar la mezcla hasta una temperatura comprendida entre -10º C y 20ºC.
9. Procedimiento según la reivindicación 8, en el que la concentración de ftaloilamlodipino en la etapa a) está comprendida entre 0,02 y 0,3 g/ml.
25 10. Procedimiento según cualquiera de las reivindicaciones 8 a 9, en el que el enfriamiento en la etapa b) se realiza en dos etapas: un primer enfriamiento hasta una temperatura comprendida entre por encima de 5ºC y 20ºC y un segundo enfriamiento hasta una temperatura comprendida entre 10ºC y 5ºC.
11. Procedimiento según la reivindicación 10, en el que dicho primer enfriamiento comprende una temperatura entre 7ºC y 35 15ºC y/o dicho segundo enfriamiento comprende una temperatura
entre 0ºC y 5ºC.
12. Procedimiento según cualquiera de las reivindicaciones 8 a 9, que comprende la etapa adicional entre la etapa a) y la etapa b) de sembrar la mezcla con un cristal de un solvato de acetona de 4-(2-clorofenil)-1,4-dihidro-6-metil-2[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5-metilo.
13. Procedimiento según la reivindicación 12, en el que
10 a) se disuelve el 4-(2-clorofenil)-1,4-dihidro-6-metil-2[(2-ftalimidoetoxi)metil]-3,5-piridindicarboxilato de 3-etilo y 5-metilo en acetona a una temperatura comprendida entre 50ºC y el reflujo; b) se enfría la mezcla hasta una temperatura comprendida
15 entre 30ºC y 45ºC; c) se siembra con un cristal del solvato de acetona de 4(2-clorofenil)-1,4-dihidro-6-metil-2-[(2-ftalimidoetoxi)metil]3,5-piridindicarboxilato de 3-etilo y 5-metilo; y d) se enfría hasta una temperatura comprendida entre 10ºC y 20ºC.
14. Un uso de un solvato de acetona de 4-(2-clorofenil)1,4-dihidro-6-metil-2-[(2-ftalimidoetoxi)metil]-3,5piridindicarboxilato de 3-etilo y 5-metilo según cualquiera de las reivindicaciones 1 a 7 para la síntesis de [2-(2-aminoetoxi)metil]-4-(2-clorofenil)-1,4-dihidro-6-metilpiridin-3,5dicarboxilato de 3-etilo y 5-metilo, sus sales o solvatos de los mismos.
**(Ver fórmula)**
H
[2-(2-aminoetoxi)metil]-4-(2-clorofenil)-1,4-dihidro-6metilpiridin-3,5-dicarboxilato de 3-etilo y 5-metilo
15. Uso según la reivindicación 14, para la síntesis de bencenosulfonato de [2-(2-aminoetoxi)metil]-4-(2-clorofenil)1,4-dihidro-6-metilpiridin-3,5-dicarboxilato de 3-etilo y 5metilo.
**(Ver fórmula)**
Cl H3CO2CCO2CH2CH3
**(Ver fórmula)**
SO3H**(Ver fórmula)**
O
N
**(Ver fórmula)**
NH2H
bencenosulfonato de [2-(2-aminoetoxi)metil]-4-(2clorofenil)-1,4-dihidro-6-metilpiridin-3,5-dicarboxilato de 3etilo y 5-metilo.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Compuestos heterocíclicos que activan AMPK y métodos de uso de los mismos, del 29 de Julio de 2020, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que es N-((cis)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; N-((3S,4S)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Inhibidores de btk de tipo nicotinimida sustituida y su preparación y uso en el tratamiento del cáncer, la inflamación y las enfermedades autoinmunitarias, del 15 de Julio de 2020, de Guangzhou InnoCare Pharma Tech Co., Ltd: Un compuesto seleccionado del grupo que consiste en: 6-(1-acriloilpiperidin-4-il)-2-(4-fenoxifenil)nicotinamida; **(Ver fórmula)** 6-(4-acriloilpiperazin-1-il)-2-(4-fenoxifenil)nicotinamida; […]