METODOS PARA PRODUCIR ANTICUERPOS.
Un método para obtener un anticuerpo con una función deseada, método que comprende:
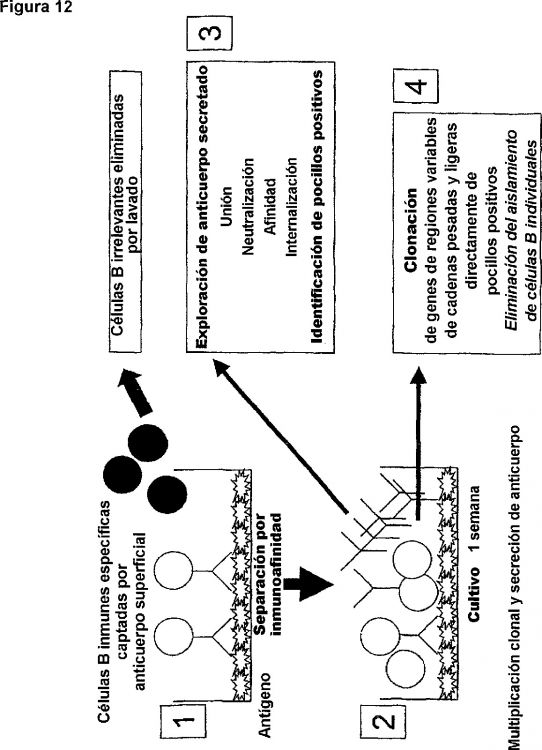
a) poner una población de células B en contacto con una serie de recipientes unitarios a los que se ha unido un antígeno;
b) separar de los recipientes unitarios aquellas células B que no se han unido al antígeno, mientras se conservan aquellas células B que se han unido al antígeno;
c) cultivar una pluralidad de las células B unidas en aquellos recipientes unitarios en que han quedado retenidas, preferiblemente bajo unas condiciones adecuadas para multiplicación clonal;
d) explorar el contenido de al menos un recipiente unitario para identificar por ello al menos un recipiente unitario positivo en cuanto a la presencia de células capaces de producir un anticuerpo con la función deseada; y
e) obtener el anticuerpo deseado directa o indirectamente de dicho recipiente unitario
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2004/002226.
Solicitante: UCB PHARMA, S.A..
Nacionalidad solicitante: Bélgica.
Dirección: ALLEE DE LA RECHERCHE 60,1070 BRUSSELS.
Inventor/es: LAWSON, ALASTAIR, DAVID, GRIFFITHS, LIGHTWOOD,DANIEL JOHN.
Fecha de Publicación: .
Fecha Concesión Europea: 3 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C07K16/24F
Clasificación PCT:
Clasificación antigua:
Fragmento de la descripción:
Métodos para producir anticuerpos.
Campo técnico
El presente invento se refiere, en general, a métodos mejorados para producir anticuerpos de alta afinidad con una función deseada.
Técnica fundamental
La tecnología de hibridomas para el aislamiento de anticuerpos monoclonales se limita, en general, a la generación de mAbs de roedores y da lugar a la inmortalización de sólo una pequeña fracción de las células formadoras de anticuerpos específicos, disponibles en un animal inmunizado. Por límites prácticos, los anticuerpos procedentes de bancos bacterianamente expresados están restringidos por el tamaño de los bancos y la necesidad de que el anticuerpo se pliegue y exprese apropiadamente en bacterias. Además, los anticuerpos generados por estos dos métodos requieren frecuentemente una potenciación de su afinidad para obtener anticuerpos con una afinidad suficientemente elevada para uso terapéutico. Se han diseñado diversos métodos alternativos para permitir que los anticuerpos de alta afinidad generados durante respuestas inmunes in vivo sean aislados de cualquier especie [Babcook et al. (1996), Proc. Natl. Acad. Sci. 93: 7843-7848; WO 92/02551; de Wildt et al. (1997), Journal of Immunological Methods 207: 61-67, y Catrin Simonsson Lagerkvist et al. (1995), BioTechniques 18 (5): 862-869].
El primer método alternativo que se diseñó fue el método del anticuerpo de linfocito seleccionado (SLAM; del inglés, selected lymphocyte antibody method), que permite que un único linfocito que está produciendo un anticuerpo con una especificidad deseada sea identificado dentro de una gran población de células linfoides y que la información genética que codifica la especificidad del anticuerpo sea rescatada de ese linfocito. Las células productoras de anticuerpo que producen anticuerpos que se unen a antígenos seleccionados son detectadas utilizando un método adaptado del ensayo de placas hemolíticas (Jerne y Nordin, 1963, Science 140: 405). En este ensayo, se revisten eritrocitos con el antígeno seleccionado y se incuban con la población de células productoras de anticuerpo y una fuente de complemento. Las células individuales que producen anticuerpo son identificadas por la formación de placas hemolíticas. Las placas de eritrocitos lisados son identificadas usando un microscopio invertido, y la célula individual productora de anticuerpo de interés situada en el centro de la placa es separada utilizando técnicas de micromanipulación. Los genes de anticuerpo de la célula son clonados mediante reacción en cadena de la polimerasa (PCR; del inglés, polymerase chain reaction) con transcripción inversa. El aislamiento físico de estas células limita el número de células B que pueden ser detectadas y aisladas. Como resultado, puede que muchos de los anticuerpos aislados aún requieran una potenciación de la afinidad ya que su afinidad puede estar solo en el intervalo nanomolar. Véase, por ejemplo, Babcook et al., supra, donde se describe una afinidad de sólo 1,76 nanomolar (1,76 x 109 M-1).
En el ensayo de placas hemolíticas anteriormente descrito, los glóbulos rojos son típicamente revestidos con antígeno por medio de un sistema de copulación de biotina/estreptavidina que requiere que el antígeno esté biotinilado. Por lo tanto, este método está restringido a antígenos que están disponibles en forma pura y a aquellos que pueden ser biotinilados sin que se afecte la presentación epitópica. Evidentemente, este método no permite el aislamiento de anticuerpos contra ciertos tipos de antígenos. Por ejemplo, muchas proteínas son difíciles de purificar, particularmente las proteínas que se expresan en la superficie celular, tales como las proteínas de tipo III. Tras la biotinilación, muchas proteínas tienen alteradas su conformación y la presentación de epítopos deseables, tales como, por ejemplo, las proteínas que contienen grupos lisina en su sitio activo.
Puede resultar también deseable producir anticuerpos contra antígenos desconocidos, tales como proteínas expresadas en la superficie de células tales como células tumorales y células T activadas. Dado el requisito de que en el ensayo de placas se produzca lisis celular para que se puedan identificar las placas que contienen células productoras de anticuerpos, es difícil conseguir el uso directo de células tumorales en lugar de eritrocitos antigénicamente revestidos. La lisis celular depende del tipo celular, el antígeno y la concentración de anticuerpo. Los glóbulos rojos revestidos con el antígeno deseado se unirán a grandes cantidades del anticuerpo disponible y se lisarán fácilmente en presencia de complemento. Otros tipos celulares, tales como las células tumorales, no se lisarán tan fácilmente, especialmente cuando la disponibilidad de antígeno en la superficie puede ser muy baja y, por lo tanto, la unión del anticuerpo es baja.
En el método de de Wildt et al., células B de pacientes aquejados de lupus eritematoso sistémico, una enfermedad autoinmune en que los pacientes producen a menudo autoanticuerpos contra la proteína U1A, fueron sometidas a separación por inmunoafinidad utilizando placas de cultivo revestidas con U1A. Las células que no se unían a la proteína U1A eran eliminadas por lavado. Las células adherentes fueron luego recogidas de las placas utilizando un tratamiento con tripsina y fueron sometidas a separación celular individual utilizando un citómetro de flujo para seleccionar las células B individuales específicas para U1A. Las células B individuales fueron luego cultivadas en placas de 96 pocillos y clonalmente multiplicadas. Se ensayaron luego los sobrenadantes de los cultivos en cuanto a la producción de anticuerpos y se identificaron los clones de células B específicas para U1A. Luego se extrajo el RNA total de los pocillos positivos y se clonaron las regiones VH/VL de las células B.
En Catrin Simonsson Lagerkvist et al. (1995), se aislaron PBMCs que se unían al toxoide tetánico (TT), procedentes de pacientes inmunizados contra el tétanos, usando glóbulos magnéticos revestidos con TT. Se aislaron células B individuales específicas para TT utilizando una pipeta automática. Luego se sembraron 0,3 células B por pocillo en microplacas de 96 pocillos y se multiplicaron clonalmente. Luego se ensayaron los pocillos en cuanto a la presencia de anticuerpos específicos para TT. Luego se clonaron los genes de la región V de los anticuerpos de los pocillos positivos.
Tanto el método de de Wildt et al. como el de Catrin Simonsson Lagerkvist et al. requieren, antes de la multiplicación clonal, el aislamiento de células B individuales que reconocen el antígeno de interés, aislamiento que puede ser pesado y llevar mucho tiempo. Además, puesto que sólo se siembra una célula B o pocas células B en cada pocillo para microtitulación, se requiere un gran número de placas de microtitulación que deben ser exploradas para identificar las células B que reconocen específicamente el antígeno de interés.
En consecuencia, existe la necesidad de métodos menos laboriosos para el aislamiento de anticuerpos con una función deseada. Además, existe la necesidad de anticuerpos de mayor afinidad que no requieran una subsiguiente potenciación de la afinidad.
El presente invento proporciona un método para el aislamiento de anticuerpos de alta afinidad con una función deseada.
Sumario del invento
De acuerdo con el presente invento, se proporciona un método para obtener un anticuerpo con una función deseada, método que comprende:
Reivindicaciones:
1. Un método para obtener un anticuerpo con una función deseada, método que comprende:
2. Un método de acuerdo con la Reivindicación 1, en que la operación c) comprende cultivar las células bajo unas condiciones adecuadas para multiplicación clonal.
3. Un método de acuerdo con cualquiera de las reivindicaciones precedentes, en que la operación d) comprende ensayar al menos un recipiente unitario en cuanto a la presencia de células que producen anticuerpos con la función deseada, explorando el sobrenadante de cultivo presente en el(los) recipiente(s) unitario(s).
4. Un método de acuerdo con la Reivindicación 3, en que se lleva a cabo un ensayo para identificar un recipiente unitario que es positivo en cuanto a la presencia de células que producen anticuerpos de alta afinidad hacia un antígeno de interés.
5. Un método de acuerdo con cualquiera de las reivindicaciones precedentes, en que, en la operación e), el anticuerpo deseado se obtiene de un recipiente unitario cuyo contenido es clonal.
6. Un método de acuerdo con cualquiera de las reivindicaciones precedentes, en que, en la operación e), el anticuerpo se obtiene de un recipiente unitario identificado como positivo en cuanto a la presencia de células que producen anticuerpos con la función deseada, cultivando las células presentes en el recipiente unitario o sus descendientes.
7. Un método de acuerdo con cualquiera de las Reivindicaciones 1 a 5, en que, en la operación e), el anticuerpo se obtiene de un recipiente unitario identificado como positivo en cuanto a la presencia de células que producen anticuerpos con la función deseada, aislando los genes que codifican el anticuerpo o partes del mismo y haciendo que se expresen (o una versión modificada de los mismos) en una célula huésped.
8. Un método de acuerdo con la Reivindicación 7, en que el aislamiento de los genes que codifican el anticuerpo o partes del mismo comprende multiplicar los genes que codifican el anticuerpo o partes del mismo.
9. Un método de acuerdo con la Reivindicación 8, en que la multiplicación se lleva directamente a cabo sobre las células, o sus descendientes, que están presentes en un recipiente unitario identificado como positivo en cuanto a la presencia de células que producen anticuerpos con la función deseada.
10. Un método de acuerdo con la Reivindicación 9, en que hay una operación de recuperación de ácido nucleico antes de la multiplicación.
11. Un método de acuerdo con la Reivindicación 8, 9 ó 10, en que la multiplicación se lleva a cabo utilizando el sobrenadante de cultivo de un recipiente unitario identificado como positivo en cuanto a la presencia de células que producen anticuerpos con la función deseada.
12. Un método de acuerdo con la Reivindicación 11, en que los genes que codifican el anticuerpo o partes del mismo son aislados determinando la secuencia de aminoácidos del anticuerpo (o partes del mismo) y deduciendo a partir de ella una secuencia de ácido nucleico que codifica el anticuerpo o partes del mismo.
13. Un método de acuerdo con cualquiera de las Reivindicaciones 7 a 12, en que los genes que codifican el anticuerpo o partes del mismo son modificados antes de su expresión.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Formulación anti-IFNAR1 estable, del 24 de Junio de 2020, de ASTRAZENECA AB: Una formulacion de anticuerpo que comprende: a. De 100 mg/ml a 200 mg/ml de anifrolumab; b. Lisina HCl 40 mM a 60 mM; c. Trehalosa […]
Proteínas y péptidos modificados, del 24 de Junio de 2020, de GLAXO GROUP LIMITED: Un dominio variable de inmunoglobulina único, que se une a TNFR1 y que se selecciona de cualquiera de las siguientes secuencias de aminoácidos: (a) DOM1h-131-206 caracterizada […]
Métodos para purificar una proteína objetivo de una o más impurezas en una muestra, del 17 de Junio de 2020, de EMD Millipore Corporation: Un metodo para purificar una proteina objetivo que contiene una region Fc de una o mas impurezas en una muestra, el metodo comprende las etapas de: a) poner en contacto […]
Dominios variables de inmunoglobulina, del 10 de Junio de 2020, de Ablynx NV: Dominio variable individual de inmunoglobulina de cadena pesada (ISVD), en que el residuo aminoacídico en la posición 89 es L y el residuo […]
Criterio de valoración terapéutico equivalente para inmunoterapia de enfermedades basada en antiCTLA-4, del 10 de Junio de 2020, de E. R. Squibb & Sons, L.L.C: Un anticuerpo antiCTLA-4 para su uso en el tratamiento de cáncer en un sujeto, tratamiento que comprende inducir un acontecimiento liminar […]