MARCADOR TUMORAL Y DE SENESCENCIA.
Uso de un compuesto aislado o producido de manera sintética seleccionado entre el grupo constituido por
a) una secuencia de nucleótidos que codifica una proteína o péptido regulador celular que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4,
un homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4, el péptido 86 (SEC DE ID Nº 5), el péptido 87 (SEC DE ID Nº 6), o el péptido 88 (SEC DE ID Nº 7);
b) un ARNm de sentido directo que se traduce en una proteína o péptido regulador celular que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4, un homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4, el péptido 86 (SEC DE ID Nº 5, el péptido 87 (SEC DE ID Nº 6), o el péptido 88 (SEC DE ID Nº 7);
c) un ARN de sentido contrario que es reactivo con un ARN de sentido directo que se traduce en una proteína o péptido regulador celular que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4, un homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4, el péptido 86 (SEC DE ID Nº 5), el péptido 87 (SEC DE ID Nº 6), o el péptido 88 (SEC DE ID Nº 7), y cuyo ARN de sentido contrario inhibe o bloquea la traducción de dicho ARNm de sentido directo;
d) una proteína o péptido regulador celular que está codificado por la SEC la SEC DE ID Nº 1, por la SEC DE ID Nº 3, por un homólogo de la SEC DE ID Nº 1, por un homólogo de la SEC DE ID Nº 3, por una parte de la SEC DE ID Nº 1 que codifica una región funcional de una proteína que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4, o por una parte de la SEC DE ID Nº 3 que codifica una región funcional de una proteína que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4;
e) una proteína o péptido regulador funcional que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4, un homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4, el péptido 86 (SEC DE ID Nº 5), el péptido 87 (SEC DE ID Nº 6), o el péptido 88 (SEC DE ID Nº 7); y
f) un anticuerpo reactivo con una proteína o péptido regulador que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4, un homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4r el péptido 86 (SEC DE ID Nº 5), el péptido 87 (SEC DE ID Nº 6), o el péptido 88 (SEC DE ID Nº 7);
en el que dicho homólogo de la SEC DE ID Nº 4 es una proteína, subunidad de proteína, parte de una proteína o un péptido que contiene una parte, región o región funcional que es estructural y funcionalmente idéntica con la SEC DE ID Nº 4, y en el que dicho homólogo de la SEC DE ID Nº 1 es una secuencia de nucleótidos que codifica la misma secuencia de aminoácidos pero que varia en la composición de los nucleótidos debido a la degeneración del código genético, y en el que dicho homólogo de la SEC DE ID Nº 3 es una secuencia de nucleótidos que codifica la misma secuencia de aminoácidos pero que varia en la composición de los nucleótidos debido a la degeneración del código genético, para la fabricación de una composición para interferir y/o detectar la senescencia celular o el desarrollo tumorogénico de una célula o tejido eucariota
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP01/00675.
Solicitante: POLYMUN SCIENTIFIC IMMUNBIOLOGISCHE FORSCHUNG GMBH.
Nacionalidad solicitante: Austria.
Dirección: NUSSDORFER LANDE 11,1190 WIEN.
Inventor/es: KATINGER, HERMANN, GRABHERR,REINGARD, GRILLARI,JOHANNES.
Fecha de Publicación: .
Fecha Concesión Europea: 7 de Abril de 2010.
Clasificación Internacional de Patentes:
- C07K14/47A33
Clasificación PCT:
- C07K14/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C12N15/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Clasificación antigua:
- C12N15/00 C12N […] › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
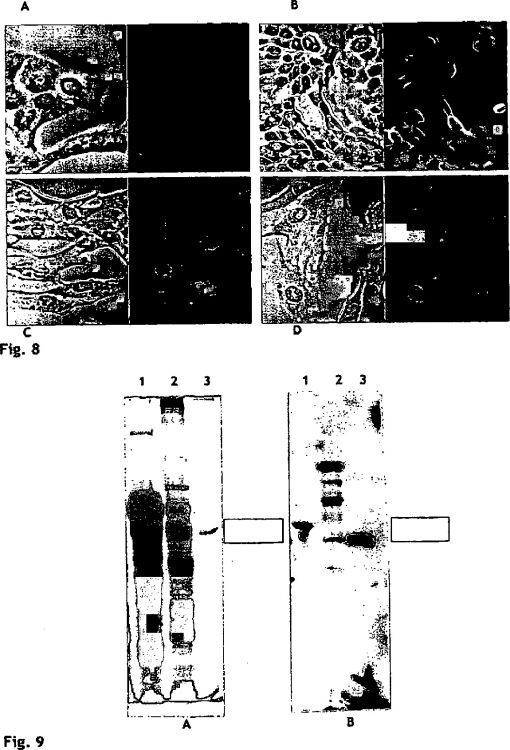
Fragmento de la descripción:
Marcador tumoral y de senescencia.
La presente invención pertenece a los campos de la biotecnología y la medicina y se refiere a una proteína que se ha encontrado que es un potencial marcador tumoral y/o de la senescencia útil para diagnósticos médicos y que adicionalmente tiene potencial terapéutico así como propiedades antiapoptóticas útiles para mejorar la viabilidad celular en la tecnología de cultivos celulares.
Introducción
El paso en serie de células humanas es un modelo ampliamente usado para estudiar los cambios que se producen durante el proceso de envejecimiento a nivel celular. Por tanto, se puede ganar una importante comprensión acerca de la regulación del ciclo celular y del fenotipo de la senescencia celular.
Los estudios de fusión celular de la técnica anterior fueron capaces de demostrar que el fenotipo senescente es dominante sobre el fenotipo inmortal transformado. Adicionalmente, la microinyección de ARNm derivada de células senescentes induce el fenotipo senescente en células jóvenes, y la inhibición de la síntesis de ADN está afectada por la preparación de la membrana plasmática de células senescentes y quiescentes. Esta detención del crecimiento se produce en la fase G1 tardía del ciclo celular y las células se bloquean al entrar en la fase S, incluso aunque se estimulen con cualquier combinación conocida de mitógenos, aun los receptores del factor de crecimiento están aún presentes en la superficie celular. Esta detención irreversible del crecimiento es dependiente de la pérdida de actividad de la telomerasa, debido a que los fibroblastos transfectados con la subunidad TERTh catalítica no entran en senescencia replicativa, ni muestran alteraciones tumorogénicas.
Los informes acerca de la expresión génica durante la senescencia localizan cambios en los diferentes grupos de genes: los genes reguladores del ciclo celular, los genes inducibles por los factores de transcripción y el factor de crecimiento, las proteínas de la matriz celular y las secretoras, y los genes mitocondriales.
Breve descripción de la invención
La presente invención se refiere al aislamiento y a la reproducción mediante técnicas de ingeniería genética recombinante de secuencias de ácido nucleico que codifican una proteína humana (denominada a partir de ahora en el presente documento proteína "SNEV") o sus homólogos, cuya proteína se encontró que interfería con los procesos reguladores celulares que determinan o afectan al menos un parámetro seleccionado entre el grupo constituido por crecimiento, viabilidad, alargamiento de la vida, y número de ciclos de replicación, de una célula eucariota, por ejemplo, una de mamífero o de ser humano.
La invención se refiere también al uso de las presentes proteínas SNEV, los péptidos, anticuerpos, secuencias de ácido nucleico, ARNm de sentido directo y ARN o APN de sentido contrario en al menos un campo de aplicación seleccionado entre el grupo constituido por diagnósticos, terapia médica y tecnología de cultivos celulares, particularmente para uso en diagnósticos de tumores, cáncer y senescencia, prevención o terapia. En una realización especifica, la invención se refiere al uso de las presentes proteínas SNEV o los ácidos nucleicos correspondientes para prolongar el alargamiento de la vida de una célula eucariota en un medio de cultivo adecuado in vitro. En otra realización especifica adicional, la invención se refiere a lo opuesto, es decir, a la inducción intencionada de la detención de la proliferación (senescencia) de las células eucariotas disminuyendo los niveles intracelulares de proteína SNEV usando ARN de sentido contrario o anticuerpos dirigidos contra SNEV.
Descripción detallada de la invención
Basándose en el conocimiento de los estudios anteriormente mencionados, se llevó a cabo un procedimiento de hibridación sustractiva con el fin de aislar nuevos genes reguladores de la senescencia y/o el crecimiento, que pueden estar también relacionados con enfermedades asociadas a la edad y la tumorogénesis. A este objeto, se produjo uno de los genes candidatos para ser tanto recombinantemente expresado en exceso como inhibido en HUVEC, con el fin de clarificar su significación biológica.
Mediante un procedimiento de hibridación sustractiva, se identificaron diversos genes expresados diferencialmente a partir de un paso temprano (5 P, es decir, 5 pasos) y de las células HUVEC endoteliales senescentes (35 P) de la vena umbilical humana, y se identificó un gen anteriormente desconocido, que se expreso a niveles mayores en células endoteliales jóvenes y quiescentes que en células endoteliales senescentes. A partir del análisis del marco de lectura abierto del ADNc de longitud completa, se dedujo una secuencia de aminoácidos, y la presunta proteína (denominada a partir de ahora en el presente documento como proteína "SNEV") que representa un nuevo miembro de la familia de las proteínas de repetición WD. La transcripción de este gen (denominado a partir de ahora en el presente documento como gen "SNEV") no se limita a las líneas de células endoteliales, sino que se observó en todos los tejidos humanos que se ensayaron, incluyendo riñón, pulmón, placenta, intestino delgado, hígado, leucocitos de la sangre periférica, bazo, timo, colon, músculo esquelético, corazón, y cerebro. Más aún; no se han identificado hasta el momento productos de corte y empalme alternativos. Adicionalmente, se han identificado transcripciones homologas de la misma longitud (2,3 kb) mediante transferencia Northern en células CHO, en tejido de la pituitaria de rata y en una línea de células tumorales de ratón, lo que indica que los roedores expresan una versión conservada de este ARNm.
Esta expresión ubicua de SNEV sugiere una importante función celular. Debido a que los inventores encontraron que este ARNm se expresaba más abundantemente en el paso temprano de las HUVEC que en sus contrapartes senescente, los inventores determinaron los niveles de expresión correspondientes en otras líneas celulares. Los resultados confirmaron que el fenómeno de disminución de los niveles de ARNm de SNEV en células senescentes no se limita a las HUVEC, sino que se puede observar también en fibroblastos diploides humanos y en células de riñón humano. Además, los inventores fueron capaces de demostrar que la disminución del ARNm de SNEV no es una consecuencia de la detención del crecimiento sino de la senescencia, debido a que no se podrían detectar diferentes niveles de SNEV entre HUVEC inhibidas por contacto y células en ciclación.
A diferencia de la disminución de los niveles de la transcripción en células senescentes de, por ejemplo, origen endotelial, fibroblastos, riñón o queratinocitos, se ha encontrado que los niveles de ARNm de SNEV están aumentados drásticamente en cuatro diferentes líneas de leucemia humana en comparación con sus controles normales, es decir, linfocitos activados, así como en una línea celular de queratinocitos transformados, y en células transformadas de SV40 y en células de carcinoma de riñón, en comparación con células primarias de riñón humano. Adicionalmente, dos de las líneas celulares de carcinoma de riñón ensayadas no muestran, sin embargo, niveles extremadamente elevados de expresión de SNEV.
Diversos experimentos han desvelado que la expresión en exceso de SNEV recombinante en HUVEC dio como resultado una expansión en el alargamiento de la vida, mientras que la infrarregulación mediante transfección del ARN de sentido contrario indujo la senescencia celular. Estos resultados destacan la importancia biológica del gen SNEV recientemente identificado para controlar la viabilidad celular, la senescencia y la inmortalización de las líneas celulares, y son una indicación adicional de la estrecha relación entre la detención irreversible de la proliferación (por ejemplo, senescencia) y la tumorogénesis. En 1986, O'Brien y col, Proc. Natl. Acad. Sci. USA 83, 8659-8663 contemplaban ya la idea de que la senescencia replicativa puede ser un mecanismo supresor tumoral, y debido a que incluso se confirmó consistentemente por diversos científicos la evidencia que indicaba que la senescencia y la tumorogénesis son estados celulares "opuestos".
En la práctica médica o biotecnológica, el gen SNEV, la proteína SNEV y sus homólogos permiten interferir de manera decidida con y modular el alargamiento de la vida celular, lo que incluye, por una parte, acelerar artificialmente la senescencia celular, y por la otra, prolongar la vida celular o incluso inmortalizar líneas celulares. Según esto, proporcionan...
Reivindicaciones:
1. Uso de un compuesto aislado o producido de manera sintética seleccionado entre el grupo constituido por
en el que dicho homólogo de la SEC DE ID Nº 4 es una proteína, subunidad de proteína, parte de una proteína o un péptido que contiene una parte, región o región funcional que es estructural y funcionalmente idéntica con la SEC DE ID Nº 4, y en el que dicho homólogo de la SEC DE ID Nº 1 es una secuencia de nucleótidos que codifica la misma secuencia de aminoácidos pero que varia en la composición de los nucleótidos debido a la degeneración del código genético, y en el que dicho homólogo de la SEC DE ID Nº 3 es una secuencia de nucleótidos que codifica la misma secuencia de aminoácidos pero que varia en la composición de los nucleótidos debido a la degeneración del código genético, para la fabricación de una composición para interferir y/o detectar la senescencia celular o el desarrollo tumorogénico de una célula o tejido eucariota.
2. Uso según la reivindicación 1, para la fabricación de una composición para tanto prolongar el alargamiento de la vida de dicha célula o tejido eucariota, como para acelerar la senescencia celular o detener la proliferación de dicha célula o tejido eucariota.
3. Uso de acuerdo con la reivindicación 1 ó 2, para la fabricación de una composición para el diagnóstico o el tratamiento terapéutico de un tumor o un cáncer.
4. Uso según la reivindicación 1, 2 ó 3, en el que el anticuerpo se puede obtener tras la inmunización de un mamífero con una proteína o péptido regulador celular seleccionado entre el grupo constituido por la SEC DE ID Nº 4, un dicho homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4, el péptido 86 (SEC DE ID Nº 5), el péptido 87 (SEC DE ID Nº 6), y el péptido 88 (SEC DE ID Nº 7).
5. Un procedimiento para detectar el desarrollo tumorigénico o la senescencia de una célula o tejido eucariota que comprende determinar y evaluar, in vitro,
en el que la proteína o péptido regulador celular tiene una secuencia de aminoácidos seleccionada entre el grupo constituido por la SEC DE ID Nº 4, un homólogo de la SEC DE ID Nº 4, una parte de la SEC DE ID Nº 4, el péptido 86 (SEC DE ID Nº 5), el péptido 87 (SEC DE ID Nº 6), y el péptido 88 (SEC DE ID Nº 7), siendo dicho homólogo de la SEC DE ID Nº 4 una proteína, subunidad de proteína, parte de una proteína o péptido que contiene una parte, región, región funcional que es estructural y funcionalmente idéntica con la SEC DE ID Nº 4.
6. El procedimiento según la reivindicación 5, en el que el nivel de expresión de dicha secuencia de nucleótidos afecta a al menos un parámetro seleccionado entre el grupo constituido por crecimiento, viabilidad, alargamiento de la vida, y número de ciclos de replicación, de dicha célula.
7. El procedimiento según la reivindicación 5 ó 6, en el que la expresión de dicha secuencia de nucleótidos está regulada en exceso en células tumorales en comparación con células normales del mismo tipo.
8. El procedimiento según la reivindicación 5 ó 6, en el que la expresión de la secuencia está infrarregulada en células senescentes en comparación con las células jóvenes del mismo tipo.
9. El procedimiento según una cualquiera de las reivindicaciones 5 a 8, en el que dicha secuencia de nucleótidos se selecciona entre el grupo constituido por la SEC DE ID Nº 1, la SEC DE ID Nº 3, un homólogo de la SEC DE ID Nº 1, un homólogo de la SEC DE ID Nº 3, una parte de la SEC DE ID Nº 1 que codifica una región funcional de una proteína que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4, y una parte de la SEC DE ID Nº 3 que codifica una región funcional de una proteína que tiene una secuencia de aminoácidos según la SEC DE ID Nº 4,
en el que dicho homólogo de la SEC DE ID Nº 1 es una secuencia de nucleótidos que codifica la misma secuencia de aminoácidos pero que varia en la composición de la secuencia de nucleótidos debido a la degeneración del código genético, y en el que dicho homólogo de la SEC DE ID Nº 3 es una secuencia de nucleótidos que codifica la misma secuencia de aminoácidos pero que varía en la composición de nucleótidos debido a la degeneración del código genético.
10. Un procedimiento de prolongar el alargamiento de la vida de una célula eucariota in vitro, que comprende
en el que dicho homólogo de la SEC DE ID Nº 4 es un proteína, subunidad de proteína, parte de una proteína o un péptido que contiene una parte, región o región funcional que es estructural y funcionalmente idéntica con la SEC DE ID Nº 4.
11. Un procedimiento de acelerar la senescencia celular o detener la proliferación de una célula eucariota in vitro, que comprende
en el que dicho homólogo de la SEC DE ID Nº 4 es una proteína, subunidad de proteína, parte de una proteína o un péptido que contiene una parte, región o región funcional que es estructural y funcionalmente idéntica con la SEC DE ID Nº 4.
12. El procedimiento de la reivindicación 11, que comprende introducir el ARN o APN de sentido contrario en la célula eucariota y dejar que el ARN o el APN de sentido contrario se híbride con el ARNm de sentido directo.
Patentes similares o relacionadas:
PÉPTIDOS CON ACTIVIDAD APOPTÓTICA, del 7 de Diciembre de 2011, de CYTOTOOLS AG: Medicamento para el tratamiento de la arteriosclerosis, que comprende al menos una sustancia de actividad apoptótica o una sal farmacéuticamente […]
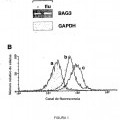 ANTICUERPOS BAG3 PARA SU USO EN INVESTIGACIÓN , DIAGNÓSTICO Y TRATAMIENTO DE ENFERMEDADES RELACIONADAS CON LA MUERTE CELULAR, del 23 de Mayo de 2011, de BIOUNIVERSA S.r.l: Un anticuerpo AC-1 secretado por el clon madre de hibridoma nº PD02009 depositado el 17/12/2002 en el Centro Biotecnologie Avanzate, Génova, […]
ANTICUERPOS BAG3 PARA SU USO EN INVESTIGACIÓN , DIAGNÓSTICO Y TRATAMIENTO DE ENFERMEDADES RELACIONADAS CON LA MUERTE CELULAR, del 23 de Mayo de 2011, de BIOUNIVERSA S.r.l: Un anticuerpo AC-1 secretado por el clon madre de hibridoma nº PD02009 depositado el 17/12/2002 en el Centro Biotecnologie Avanzate, Génova, […]
METODO PARA LA IDENTIFICACION DE COMPUESTOS QUE INDUCEN O INHIBEN ESTRES DE RETICULO ENDOPLASMATICO O ESTRES OXIDATIVO, del 24 de Enero de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: Método para la identificación de compuestos que inducen o inhiben estrés de retículo endoplasmático o estrés oxidativo.La presente invención […]
SUPRESION DE LA APOPTOSIS EN LINFOCITOS B EN ANIMALES TRANSGENICOS QUE EXPRESAN INMUNOGLOBULINA HUMANIZADA, del 26 de Noviembre de 2010, de THERAPEUTIC HUMAN POLYCLONALS, INC: Un animal transgénico no humano sometido a linfopoyesis a corto plazo que comprende al menos una construcción transgénica que comprende el inhibidor […]
PEPTIDOS QUE SE UNEN A LA PROTEINA FOSFATASA 2A Y POLINUCLEOTIDOS QUE CODIFICAN PARA LOS MISMOS, del 2 de Julio de 2010, de INSTITUT PASTEUR: Péptido caracterizado porque se une in vitro, de manera específica, a una holoenzima proteína fosfatasa de tipo 2A o una de sus subunidades y porque se elige […]
 CELULAS LOCALIZADAS EN TUMORES MODIFICADAS POR INGENIERIA GENETICA PARA PRODUCIR LIGANDO INDUCTOR DE APOPTOSIS RELACIONADO CON EL FACTOR DE NECROSIS TUMORAL (TRAIL), del 2 de Junio de 2010, de DOMPE S.P.A.: Células hematopoyéticas CD34+ procedentes de la sangre periférica de pacientes con cáncer tratados con factor de crecimiento y transducidas con el ligando inductor […]
CELULAS LOCALIZADAS EN TUMORES MODIFICADAS POR INGENIERIA GENETICA PARA PRODUCIR LIGANDO INDUCTOR DE APOPTOSIS RELACIONADO CON EL FACTOR DE NECROSIS TUMORAL (TRAIL), del 2 de Junio de 2010, de DOMPE S.P.A.: Células hematopoyéticas CD34+ procedentes de la sangre periférica de pacientes con cáncer tratados con factor de crecimiento y transducidas con el ligando inductor […]
NUEVAS PROTEINAS ASOCIADAS A LA MUERTE DE LA FAMILIA THAP Y RUTAS PAR4 RELACIONADAS IMPLICADAS EN EL CONTROL DE LA APOPTOSIS, del 3 de Mayo de 2010, de ENDOCUBE SAS CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS): Un método para identificar un compuesto de ensayo que modula las actividades mediadas por THAP ("THanatos-Associated Protein", proteína asociada […]
Polipéptidos de unión específica novedosos y usos de los mismos, del 15 de Julio de 2020, de Pieris Pharmaceuticals GmbH: Muteína de lipocalina lagrimal humana que tiene especificidad de unión para IL-17A, en la que la muteína se une a IL-17A con una KD de aproximadamente 1 nM o menos, en la que […]