COMPLEJOS METALICOS QUE UTILIZAN LA VITAMINA B12 COMO LIGANDO.
Complejo metálico de fórmula general M(L)n, en el que cada L se selecciona independientemente y representa un ligando,
y por lo menos un L es vitamina B12 (cianocobalamina) o un derivado de la misma que se encuentra unido mediante el átomo de nitrógeno del grupo cianuro de la misma a M, el cual es un elemento seleccionado de entre los metales de transición tecnecio, rodio, renio, paladio y platino, formando de esta manera un grupo M-NC-[Co], en el que [Co] representa la vitamina B12 sin cianuro y en el que n es 1, 2, 3, 4, 5 ó 6
Tipo: Resumen de patente/invención. Número de Solicitud: W05000168EP.
Solicitante: UNIVERSITAT ZURICH.
Nacionalidad solicitante: Suiza.
Dirección: RAMISTRASSE 71,8006 ZURICH.
Inventor/es: ALBERTO, ROGER, MUNDWILER,STEFAN, KNIGHT CASTRO,HECTOR,HUMBERTO, KUNZE,SUSANNE,BARBARA.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- A61K51/04G
Clasificación PCT:
- A61K49/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones para examen in vivo.
- C07D487/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › en los que el sistema condensado contiene cuatro o más heterociclos.
- C07F19/00 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › Compuestos metálicos cubiertos por más de uno de los grupos principales C07F 1/00 - C07F 17/00.
Clasificación antigua:
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- C07D487/22 C07D 487/00 […] › en los que el sistema condensado contiene cuatro o más heterociclos.
- C07F19/00 C07F […] › Compuestos metálicos cubiertos por más de uno de los grupos principales C07F 1/00 - C07F 17/00.
Fragmento de la descripción:
Complejos metálicos que utilizan la vitamina B12 como ligando.
La invención se refiere a complejos metálicos que contienen vitamina B12 como ligando. Asimismo, la invención se refiere a la utilización de dichos complejos en el radiodiagnóstico, la terapia con radionucleidos, la quimioterapia o como catalizadores.
Antecedentes de la técnica
Los fármacos anticáncer actuales, tales como el cisplatino, también resultan tóxicos para las células sanas normales. Las dosis relativamente elevadas que deben administrarse a un paciente provocan efectos secundarios severos. Una selectividad incrementada al dirigirse a las células de cáncer resultaría beneficiosa para el índice terapéutico y la calidad de vida del paciente.
En la terapia con radionucleidos se utiliza la acumulación metabólica de un radiofarmacéutico para administrar una dosis terapéutica de reacción en un tejido. El factor crítico para el éxito de la terapia de radionucleidos es la acumulación en el tejido diana comparado con el tejido normal, que se encuentra en el intervalo de entre 5 y 100 en todos los métodos conocidos hasta hoy. Una excepción a lo anterior es la muy exitosa terapia metabólica con yodo de la enfermedad tiroidea. Debido a la baja proporción de acumulación en diana respecto a tejido normal, la carga de radiación para los tejidos normales del paciente con frecuencia es relativamente elevada. De esta manera, existe una necesidad de un modo para administrar específicamente el radionucleido en el tejido diana.
Un compuesto candidato interesante que puede conducir a la incorporación específica de sitio es la vitamina B12. Las células de cáncer de proliferación rápida se denominan grandes consumidores de B12. Esta demanda muy elevada convierte a la vitamina B12 en un potencial "caballo de Troya" para la administración de agentes terapéuticos.
La cianocobalamina (vitamina B12) es bien conocida y su química ha sido revisada exhaustivamente. Existen muchas patentes y publicaciones sobre la derivatización de la vitamina B12 en el anillo tetrapirrólico con cobalto o en el grupo ribosa. Algunos de dichos derivados de la vitamina B12 han sido propuestos para la aplicación en la terapia o el diagnóstico del cáncer, aunque ninguno ha sido comercializado todavía.
La patente US No. 2004/224921, por ejemplo, se refiere a cobalaminas fluorescentes que comprenden un compuesto fluorescente, fosforescente, luminiscente o productor de luz que se encuentra covalentemente unido a la cobalamina. Estas cobalaminas fluorescentes pueden utilizarse como marcadores diagnósticos y prognósticos para distinguir las células y tejidos cancerosos de las células y tejidos sanos, y para determinar si un individuo responderá positivamente a la quimioterapia utilizando bioconjugados terapéuticos basados en la cobalamina. Los compuestos fluorescentes, fosforescentes o productores de luz pueden unirse covalentemente a la cobalamina. Estas cobalaminas fluorescentes pueden utilizarse como marcadores diagnósticos y prognósticos para distinguir las células y tejidos cancerosos de las células y tejidos sanos, y para determinar si un individuo responderá positivamente a la quimioterapia con bioconjugados terapéuticos basados en la cobalamina. Los compuestos fluorescentes, fosforescentes o productores de luz pueden unirse covalentemente al átomo de cobalto, al anillo tetrapirrólico o al grupo ribosa de la cobalamina. Este tipo de derivatización también se encuentra descrito para compuestos no fluorescentes.
La derivatización directamente en el cobalto conduce a que un compuesto conserve más del 90% de la actividad de la vitamina B12. La derivatización en esta posición es, de esta manera, una elección evidente. Sin embargo, dichos compuestos adolecen de desventajas. Por ejemplo, los compuestos alquilados del cobalto son sensibles a la luz.
Las derivatizaciones en la ribosa o en posiciones en la estructura tetrapirrólica presentan la desventaja de no poderse cortar, influyendo de esta manera sobre el comportamiento biológico de la vitamina B12 de manera significativa.
Existe, por lo tanto, la necesidad de un fármaco que pueda utilizarse para el diagnóstico y el tratamiento del cáncer, que no comporte efectos secundarios severos ni conduzca a una carga de radiación elevada.
Descripción resumida de la invención
Se ha encontrado según la invención que determinados complejos metálicos son capaces de coordinarse directamente con el grupo cianuro en la vitamina B12. Podría demostrarse que este tipo de unión se produce en particular para el complejo [Tc(NnO)(OH2)(CO)3] (NnO=ligando bidentado) en el que el átomo de nitrógeno del cianuro se une directamente al centro metálico Tc formando un grupo [Co]-CN-Tc. Lo anterior representa un ejemplo prototípico de un complejo en el que la vitamina B12 actúa como un ligando para un metal, en este caso para Tc. Sin embargo, otros complejos metálicos en los que la vitamina B12 es un ligando que se encuentra unido al metal a través de su cianuro también constituyen parte de la presente invención. En la totalidad de dichos complejos metálicos, la vitamina B12 actúa como ligando.
En la invención se propone por primera vez coordinar la vitamina B12 mediante el cianuro de la misma con un metal para formar un complejo [Co]-CN-M, en el que [Co] representa la vitamina B12 sin cianuro. Los inventores han encontrado que dichos derivados de la vitamina B12 son químicamente estables y pueden producirse fácilmente.
Con la excepción de la posición CN, todos los demás sitios en la vitamina B12 han sido propuestos en la literatura para el marcaje. El cianuro no ha sido utilizado con anterioridad debido a que no se esperaba que actuase como grupo ligando.
De esta manera, la invención se refiere a complejos metálicos de fórmula general M(L)n, en la que cada L se selecciona independientemente y es un ligando, y por lo menos una L se selecciona de entre la vitamina B12 (cianocobalamina) y los derivados de la misma unidos mediante el átomo de nitrógeno de su grupo cianuro a M, que es un elemento seleccionado de entre los metales de transición tecnecio, rodio, renio, paladio y platino, formando de esta manera un grupo M-NC-[Co], en el que [Co] representa la vitamina B12 o el derivado de la misma sin cianuro y en el que n es 1, 2, 3, 4, 5 ó 6.
No es necesario que los diferentes ligandos L presentes en un complejo metálico sean iguales, sino que cada L puede seleccionarse independientemente.
Para las aplicaciones en el diagnóstico y/o la terapia del cáncer, el metal ventajosamente es un isótopo radioactivo de Re o de Tc, tal como uno seleccionado de entre 99mTc, 188Re, 186Re o 105Rh.
En el caso de que M sea tecnecio o renio, los demás ligandos L convenientemente son tres grupos carbonilo (COs) y opcionalmente un ligando bidentado, opcionalmente acoplado a otro metal, una molécula biológicamente activa u otra molécula, tal como un agente fluorescente. También resulta posible disponer de dos ligandos monodentados, tales como H2O o Cl, en lugar de un ligando bidentado. Otros ligandos monodentados son los derivados monocarboxilato, los derivados monotiolato, las aminas alifáticas/aromáticas, etc., opcionalmente sustituidas con una molécula biológicamente activa.
El ligando bidentado se seleccionan convenientemente de entre dos partes amina alifáticas y/o aromáticas o una parte amina alifática o aromática y un grupo aniónico, tal como un carboxilato, un tiolato o un hidroxilato. Son ejemplos los a-aminoácidos o los derivados del ácido picolínico.
El ligando L también puede ser una molécula biológicamente activa.
Si M es platino, L puede seleccionarse de entre un ligando que contenga N, S, P, O o C como el átomo ligante de metal o cualquier otro donante con una pareja de electrones libres disponible para la coordinación con el metal, opcionalmente acoplados a una molécula biológicamente activa.
La molécula biológicamente activa u otra molécula se selecciona de entre agentes fluorescentes, farmacóforos con actividades citotóxicas, citostáticas u otras actividades farmacológicas, pigmentos ópticos, pigmentos NIR o pigmentos fosforescentes (tales como los dados a conocer en las patentes US 6.180.085 y US...
Reivindicaciones:
1. Complejo metálico de fórmula general M(L)n, en el que cada L se selecciona independientemente y representa un ligando, y por lo menos un L es vitamina B12 (cianocobalamina) o un derivado de la misma que se encuentra unido mediante el átomo de nitrógeno del grupo cianuro de la misma a M, el cual es un elemento seleccionado de entre los metales de transición tecnecio, rodio, renio, paladio y platino, formando de esta manera un grupo M-NC-[Co], en el que [Co] representa la vitamina B12 sin cianuro y en el que n es 1, 2, 3, 4, 5 ó 6.
2. Complejo metálico según la reivindicación 1, en el que el metal es un isótopo radioactivo de los elementos Re o Tc, tal como 99mTc, 188Re y 186Re.
3. Complejo metálico según la reivindicación 1 ó 2, en el que M es tecnecio o renio, comprendiendo los demás ligandos tres grupos carbonilo (COs) y opcionalmente un ligando bidentado, opcionalmente acoplados a otro complejo metálico o a otra molécula, tal como una molécula biológicamente activa o un agente fluorescente.
4. Complejo metálico según la reivindicación 3, en el que el ligando bidentado se selecciona de entre dos partes amina alifáticas y/o aromáticas o una parte amina alifática o aromática y un grupo aniónico tal como un carboxilato, un tiolato o un hidroxilato.
5. Complejo metálico según la reivindicación 4, en el que el ligando bidentado se selecciona de entre a-aminoácidos o derivados del ácido picolínico.
6. Complejo metálico según la reivindicación 1, en el que, en el caso de que M sea platino, L se selecciona independientemente de entre los ligandos que contienen N, S, P, O o C como átomo ligante de metal o cualquier otro donante con una pareja de electrones libres para la coordinación con el metal, opcionalmente acoplados a otro complejo metálico o a otra molécula, tal como una molécula biológicamente activa o una molécula fluorescente.
7. Complejo metálico según cualquiera de las reivindicaciones 3 a 6, en el que la otra molécula se selecciona de entre agentes fluorescentes, farmacóforos con actividades citotóxicas, citostáticas u otras actividades farmacológicas, pigmentos ópticos, pigmentos NIR o pigmentos fosforescentes.
8. Complejo metálico según la reivindicación 7, en el que el agente fluorescente se selecciona de entre fluoresceína, pireno, acridina y dansilo.
9. Complejo metálico según la reivindicación 7, en el que el agente citotóxico es tamoxifeno, metotrexato o ciclofosfamida.
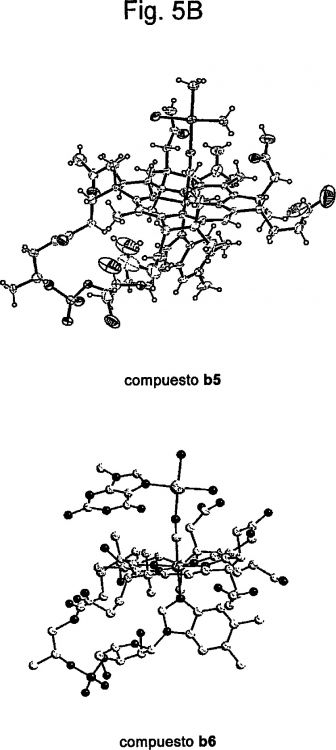
10. Complejo metálico según cualquiera de las reivindicaciones 1 a 9, que presenta una fórmula estructural seleccionada de entre las siguientes:

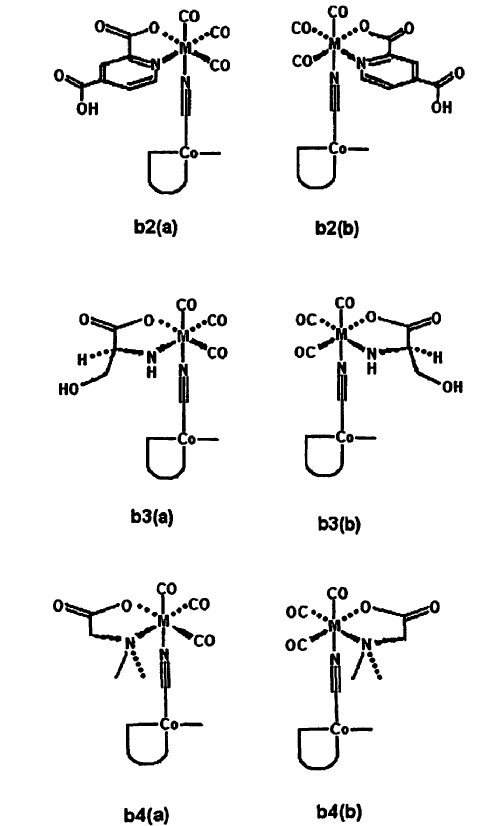
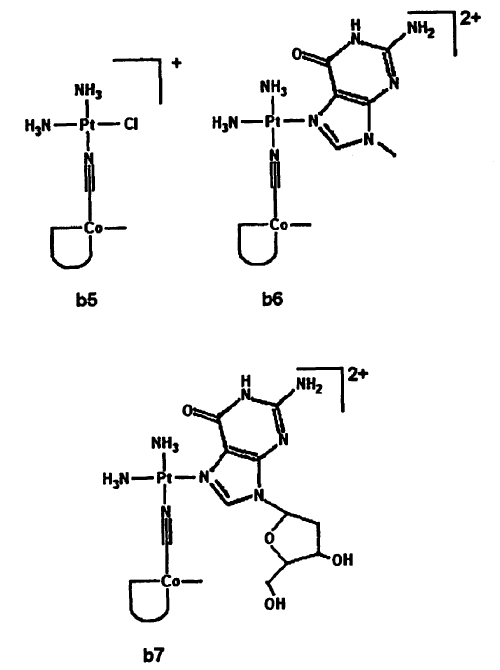
11. Procedimiento para la preparación de un complejo metálico según cualquiera de las reivindicaciones 1 a 10, que comprende mezclar la vitamina B12 con un complejo precursor de fórmula general M(L)n-1L', en la que M es un metal de transición seleccionado de entre tecnecio, rodio, renio, paladio y platino, n es 2, 3, 4, 5 ó 6, L' es un ligando que debe sustituirse por vitamina B12 o por un derivado de la misma, y cada L se selecciona independientemente y es un ligando, con el fin de obtener un complejo metálico con un puente [Co]-CN-M estable.
12. Complejo precursor que presenta una fórmula seleccionada de entre las siguientes:
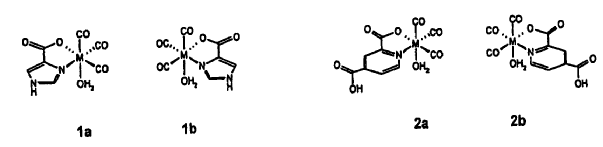
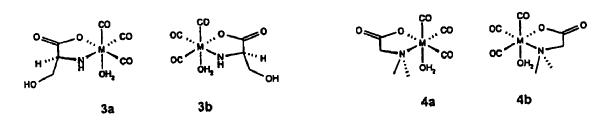
en las que M es un metal de transición seleccionado de entre tecnecio, rodio, renio, paladio y platino.
13. Complejo metálico según cualquiera de las reivindicaciones 1 a 10, para la utilización en radiodiagnóstico, quimioterapia o terapia de radionucleidos.
14. Complejo metálico según cualquiera de las reivindicaciones 1 a 10, en el que M es un metal catalíticamente activo para utilizar en catálisis.
Patentes similares o relacionadas:
NUEVO COMPUESTO QUE TIENE AFINIDAD POR AMILOIDE, del 9 de Enero de 2012, de NIHON MEDI-PHYSICS CO., LTD.: Un compuesto representado por la fórmula siguiente, o una sal del mismo: en la que todos de A1, A2, A3 y A4 representan un carbono, R 1 es un sustituyente de halógeno […]
NUEVO COMPUESTO ORGÁNICO, Y MÉTODO PARA PRODUCIR UN COMPUESTO ORGÁNICO MARCADO CON HALÓGENO RADIOACTIVO QUE USA EL MISMO, del 2 de Septiembre de 2011, de NIHON MEDI-PHYSICS CO., LTD.: Un compuesto orgánico representado mediante la siguiente fórmula : en la que R1 es un grupo alquilo de cadena lineal o cadena ramificada, con uno a 10 átomos […]
 NUEVO COMPUESTO QUE TIENE AFINIDAD POR AMILOIDE, del 22 de Marzo de 2011, de NIHON MEDI-PHYSICS CO., LTD.: Un compuesto representado mediante la siguiente fórmula , o una sal del mismo: en la que A1, A2, A3 y A4 representan independientemente un carbono o […]
NUEVO COMPUESTO QUE TIENE AFINIDAD POR AMILOIDE, del 22 de Marzo de 2011, de NIHON MEDI-PHYSICS CO., LTD.: Un compuesto representado mediante la siguiente fórmula , o una sal del mismo: en la que A1, A2, A3 y A4 representan independientemente un carbono o […]
PROCEDIMIENTO DE RADIOFLUORACIÓN DE VECTORES BIOLOGICAMENTE ACTIVOS, del 22 de Febrero de 2011, de GE HEALTHCARE AS HAMMERSMITH IMANET, LTD: Un procedimiento para radiofluoración que comprende hacer reaccionar un compuesto de fórmula (I) con un compuesto de fórmula (II): **(Ver fórmula)**18F-(Engarce)-R2 […]
LIGANDOS RADIOMARCADOS BASADOS EN QUINOLINA PARA LA FUNCIONALIDAD DEL RECEPTOR 5-HT6, del 2 de Diciembre de 2010, de GLAXO GROUP LIMITED: [11C-N-metil]-3-(3-Fluoro-bencenosulfonil)-8-(4-metil-piperazin-1-il)-quinolina
FLUORACION EN FASE SOLIDA DE URACILO, del 15 de Junio de 2010, de HAMMERSMITH IMANET LIMITED: Un procedimiento para la producción de [18F]fluorouracilo que comprende el tratamiento de un precursor unido a soporte sólido de fórmula (Ia):
 PREPARACION DE COMPUESTOS UTILES PARA LA DETECCION DE HIPOXIA, del 11 de Junio de 2010, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un procedimiento que comprende la etapa de poner en contacto un compuesto que tiene la fórmula:
PREPARACION DE COMPUESTOS UTILES PARA LA DETECCION DE HIPOXIA, del 11 de Junio de 2010, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un procedimiento que comprende la etapa de poner en contacto un compuesto que tiene la fórmula:
PIPERAZINIL Y DIAZEPANIL - BENZAMIDAS Y BENZOTIOAMIDAS, del 30 de Marzo de 2010, de JANSSEN PHARMACEUTICA NV: Un compuesto de fórmula (I):