ANTICUERPOS ANTI-CD22 CON AFINIDAD AUMENTADA POR LAS CELULAS LEUCEMICAS QUE EXPRESAN CD22.
Un anticuerpo anti-CD22 con una cadena ligera variable (VL) que tiene la secuencia de la cadena VL del anticuerpo RFB4 de la Figura 1 y una cadena pesada variable (VH) que tiene la secuencia de la cadena VH del anticuerpo RFB4 de la Figura 1,
siempre que los restos SSY de las posiciones 104, 105 y 106 de CDR3 de la cadena VH de dicho anticuerpo anti-CD22 sean remplazados por una secuencia de aminoácidos seleccionada del grupo que consiste en THW, YNW, TTW y STY
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US02/30316.
Solicitante: THE GOVERNMENT OF THE UNITED STATES OF AMERICA AS REPRESENTED BY THE SECRETARY OF HEALTH AND HUMAN.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: OFFICE OF TECHNOLOGY TRANSFER, 6011 EXECUTIVE BOULEVARD, SUITE NO. 325,ROCKVILLE, MD 20854.
Inventor/es: PASTAN, IRA, H., KREITMAN, ROBERT J., SALVATORE,GIULIANA, BEERS,RICHARD.
Fecha de Publicación: .
Fecha Concesión Europea: 19 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07K16/28A
Clasificación PCT:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C07K16/00 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C12N15/63 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C07H21/04 C07H 21/00 […] › con desoxirribosilo como radical sacárido.
- C07K16/00 C07K […] › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C12N15/63 C12N 15/00 […] › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Fragmento de la descripción:
Anticuerpos anti-CD22 con afinidad aumentada por las células leucémicas que expresan CD22.
Antecedentes de la invención
Las malignidades hematológicas son un grave problema de salud pública. Se ha estimado que en el año 2000, se produjeron más de 50.000 nuevos casos de linfoma no Hodgkin y más de 30.000 nuevos casos de leucemia en los Estados Unidos (Greenlee, R.T. et al., CA Cancer J. Clin., 50:7-33 (2000)) y se esperaban más de 45.000 muertes por estas enfermedades. Muchos más pacientes viven con una morbidez relacionada con enfermedades crónicas. Desafortunadamente, en un elevado porcentaje de pacientes, las terapias convencionales no son capaces de inducir remisiones completas a largo plazo.
En los últimos años se han desarrollado inmunotoxinas como enfoque terapéutico alternativo para tratar estas malignidades. Las inmunotoxinas estaban compuestas originalmente por un anticuerpo conjugado químicamente con una toxina vegetal o bacteriana. El anticuerpo se une al antígeno expresado en la célula diana y la toxina es internalizada ocasionando la muerte celular al detener la síntesis de proteínas e inducir la apoptosis (Brinkmann, U., Mol. Med. Today, 2:439-446 (1996)).
Las malignidades hematológicas son una diana atractiva para las terapias con inmunotoxinas ya que las células tumorales son fácilmente accesibles y tos antígenos diana son altamente expresados (Kreitman, R.J. y Pastan, I., Semin. Cancer. Biol., 6:297-306 (1995)). Uno de estos antígenos es CD25. Una prueba clínica con la inmunotoxina LMB-2 (anti-Tac(Fv)-PE38) que se dirige a CD25 demostró que el agente era bien tolerado y que tenía una actividad anti-tumoral sustancial (Kreitman, R.J. et al., Blood, 94:3340-3348 (1999); Kreitman, R.J. et al., J. Clin. Oncol. 18:16222- 1636 (2000)). Se observó una respuesta completa en un paciente con Leucemia de Células Pilosas y se observaron respuestas parciales en pacientes con Leucemia de Células Pilosas, leucemia linfocítica crónica, linfoma cutáneo de células T, enfermedad de Hodgkin y leucemia de células T adultas.
Otro antígeno que se ha utilizado como diana de inmunotoxinas es CD22, un antígeno de células B restringido por el linaje expresado en 60%-70% de los linfomas y leucemias de células B. CD22 no está presente sobre la superficie celular en las fases tempranas de desarrollo de las células B y no es expresado sobre las células pluripotenciales (Tedder, T.F. et al., Annu. Rev. Immunol, 5:481-504 (1997)). Se han llevado a cabo pruebas clínicas con una inmunotoxina que contiene un anticuerpo anti- CD22, RFB4, o su fragmento Fab, acoplado a ricina A desglicosilada. En estas pruebas se han observado respuestas clínicas sustanciales; no obstante, el síndrome de extravasación capilar, grave y en algunos casos fatal, resultó limitante de la dosis (Sausvilie, E.A. et al., Blood, 85:3457-3465 (1995); Amlot, P.L et al., Blood, 82:2624-2633 (1993); Vitetta, E.S, et al., Cancer Res., 51:4052-4058 (1991)).
Como enfoque alternativo, se utilizó el anticuerpo RFB4 para elaborar una inmunotoxina recombinante en la cual el fragmento Fv en forma de cadena sencilla se fusiona con una forma truncada de 38 kDa de la exotoxina A de Pseudomonas (PE38). PE38 contiene los dominios de translocación y de ribosilación del ADP de PE pero no la porción de unión a la célula (Hwuang, J. et al., Cell, 48:129-136 (1987)). RFB4 (Fv)-PE38 es citotóxico para las células CD22 positivas (Mansfield, E. et al., Biochem. Soc. Trans., 25:709-714 (1997)). Para estabilizar la inmunotoxina Fv de cadena sencilla y hacerla más adecuada para su desarrollo clínico, se diseñaron restos cisteína en regiones marco de VH y VL (Mansfield, E. et al., Blood, 90:2020-2026 (1997)) generando la molécula RFB4(dsFv)-PE38.
RFB4 (dsFv)-PE38 es capaz de eliminar las células leucémicas de pacientes e inducir remisiones completas en ratones que portan xenoinjertos de linfomas (Kretiman, R.J. et al., Clin. Cancer Res., 6:1476-1487 (2000); Kreitman, RJ. et al., Int. J. Cancer, 81:148-155 (1999)). RFB4 (dsFv)-PE38 (BL22) está siendo evaluado actualmente en un ensayo clínico en fase I en el Instituto Nacional del Cancer en pacientes con malignidades hematológicas. Se trataron dieciséis pacientes con leucemia de células pilosas resistente a análogos de purina con BL22 y 11 (86%) alcanzaron remisiones completas (Kreitman, R.J. et al., N. Engl. J. Med. (2001).
Debido a los beneficios clínicos obtenidos con BL22, y debido a que se ha demostrado que la mejora de la afinidad de unión mejora la liberación selectiva en el tumor de los scFv (Adams et al., Cancer Res. 58:485-490 (1998)), la mejora de la afinidad de unión de los scFv y otras fracciones localizadoras (tales como dsFv, Fab, y F(ab')2) de los productos inmunoconjugados pudo mejorar la eficacia de estos agentes al liberar moléculas efectoras para las células B malignas. El direccionamiento mejorado disminuye probablemente la dosis necesaria para lograr la remisión completa de estos cánceres.
Los factores que influyen en la afinidad de unión son afectados de manera múltiple y la obtención de scFv mutantes con una afinidad mejorada no es trivial. Aunque la estructura cristalina del anticuerpo-antígeno puede sugerir qué restos están implicados en la unión, los datos estructurales de la resolución atómica no se encuentran disponibles para la mayoría de los anticuerpos. Por otra parte, incluso cuando tales datos están disponibles generalmente no se puede predecir qué restos y qué mutaciones darán como resultado un anticuerpo con un incremento de la actividad de unión al antígeno.
Breve resumen de la invención
La presente invención proporciona anticuerpos mejorados para la unión a células que expresan CD22 (una "célula CD22+"), especialmente células cancerosas que expresan CD22 sobre su superficie exterior (una "célula cancerosa CD22+"). Con respecto a esto, la invención proporciona anticuerpos anti-CD22 con una cadena ligera variable (VL) que tiene la secuencia del anticuerpo RFB4 de la Figura 1 y una cadena pesada variable (VH) que tiene la secuencia de un anticuerpo RFB4 de ta Figura 1, pero en los que los restos 100, 100A y 100B de CDR3 de dicha cadena VH enumerada por el sistema de numeración de Kabat y Wu (restos 104, 105 y 106 como se numera de acuerdo con la Figura 1) tienen una secuencia de aminoácidos seleccionada del grupo que consiste en: THW, YNW, TTW, y STY. El anticuerpo puede ser una molécula de anticuerpo completa, pero es preferiblemente un Fv de cadena sencilla ("scFv"), un Fv estabilizado con disulfuro ("dsFv"), un Fab, o un F(ab'). En una forma particularmente preferida, el anticuerpo es dsFv. (Por conveniencia para la referencia, el término "anticuerpo" del texto de más abajo hace referencia a anticuerpos completos y, más preferiblemente, a scFv, dsFv, Fab, o F(ab')).
La invención proporciona adicionalmente composiciones que comprenden uno de estos anticuerpos conjugado o fusionado con un radical terapéutico o una marca detectable. El radical terapéutico puede ser una citotoxina, un fármaco, un radioisótopo, o un liposoma cargado con un fármaco o una citotoxina. En las realizaciones preferidas, el radical efector es una citotoxina. La citotoxina puede ser seleccionada del grupo que consiste en ricina A, abrina, ribotoxina, ribonucleasa, saporina, caliqueamicina, toxina de la difteria o una subunidad citotóxica o uno de sus mutantes, una exotoxina de Pseudomonas, o una de sus porciones citotóxicas, una exotoxina de Pseudomonas mutada, una de sus porciones citotóxicas, y toxinas A a F de botulinum. En las formas preferidas, la citotoxina es una exotoxina de Pseudomonas o uno de sus fragmentos citotóxicos, o una exotoxina de Pseudomonas mutada o uno de sus fragmentos citotóxicos. En formas particularmente preferidas, la exotoxina de Pseudomonas se selecciona del grupo que consiste en PE35, PE38, PE38KDEL, PE40, PE4E, y PE38QQR. En la realización más preferida, la exotoxina de Pseudomonas es PE38. Las composiciones pueden comprender adicionalmente un portador farmacéuticamente aceptable.
La invención proporciona adicionalmente el uso de un anticuerpo anti-CD22 de la invención como se ha descrito antes, para la fabricación de un medicamento para inhibir el crecimiento de una célula cancerosa CD22+. El anticuerpo puede ser, por ejemplo, un anticuerpo completo, un scFv, dsFv, Fab, o F(ab')2....
Reivindicaciones:
1. Un anticuerpo anti-CD22 con una cadena ligera variable (VL) que tiene la secuencia de la cadena VL del anticuerpo RFB4 de la Figura 1 y una cadena pesada variable (VH) que tiene la secuencia de la cadena VH del anticuerpo RFB4 de la Figura 1, siempre que los restos SSY de las posiciones 104, 105 y 106 de CDR3 de la cadena VH de dicho anticuerpo anti-CD22 sean remplazados por una secuencia de aminoácidos seleccionada del grupo que consiste en THW, YNW, TTW y STY.
2. Un anticuerpo de la reivindicación 1, donde dicho anticuerpo se selecciona del grupo que consiste en un scFv, un dsFv, un Fab y un F(ab')2.
3. Un anticuerpo de la reivindicación 1, donde dicho anticuerpo tiene una metionina añadida en el extremo N.
4. Un anticuerpo que es una forma humanizada del anticuerpo murino de la reivindicación 1.
5. Una composición que comprende un anticuerpo de una cualquiera de las reivindicaciones 1 a 4 conjugado o fusionado con un radical terapéutico o una marca detectable.
6. Una composición de la reivindicación 5, donde el radical terapéutico se selecciona del grupo que consiste en una citotoxina, un fármaco, un radioisótopo y un liposoma cargado con un fármaco o una citotoxina.
7. Una composición de la reivindicación 6, donde el radical terapéutico es una citotoxina.
8. Una composición de la reivindicación 7, donde la citotoxina se selecciona del grupo que consiste en ricina A, abrina, ribotoxina, ribonucleasa, saporina, caliqueamicina, toxina de la difteria o una de sus subunidades citotóxicas o mutantes, una exotoxina de Pseudomonas, una de sus porciones citotóxicas, una exotoxina de Pseudomonas mutada, una de sus porciones citotóxicas y las toxinas A a F de botulinum.
9. Una composición de la reivindicación 8, donde dicha citotoxina es una exotoxina de Pseudomonas o uno de sus fragmentos citotóxicos, o una exotoxina de Pseudomonas mutada o uno de sus fragmentos citotóxicos.
10. Una composición de la reivindicación 9, donde dicha exotoxina de Pseudomonas o uno de sus fragmentos se selecciona del grupo que consiste en PE35, PE38, PE38KDEL, PE40, PE4E y PE38QQR.
11. Una composición de la reivindicación 10, donde el fragmento de exotoxina de Pseudomonas es PE38.
12. Una composición de una cualquiera de las reivindicaciones 5 a 11, que comprende adicionalmente un portador farmacéuticamente aceptable.
13. El uso de un anticuerpo de acuerdo con una cualquiera de las reivindicaciones 1 a 4 o una composición de acuerdo con una cualquiera de las reivindicaciones 5 a 12 para la fabricación de un medicamento para inhibir el crecimiento de una célula cancerosa CD22+.
14. Un ácido nucleico que codifica un anticuerpo anti-CD22 de acuerdo con una cualquiera de las reivindicaciones 1 a 4.
15. Un ácido nucleico de la reivindicación 14, donde adicionalmente dicho ácido nucleico codifica un polipéptido que es un radical terapéutico o una marca detectable.
16. Un ácido nucleico de la reivindicación 15, donde adicionalmente dicho radical terapéutico es un fármaco o una citotoxina.
17. Un ácido nucleico de la reivindicación 16, donde dicha citotoxina es una exotoxina de Pseudomonas o uno de sus fragmentos citotóxicos, o una exotoxina de Pseudomonas mutada o uno de sus fragmentos citotóxicos.
18. Un ácido nucleico de la reivindicación 17, donde dicha exotoxina de Pseudomonas o uno de sus fragmentos se seleccionan del grupo que consiste en PE35, PE38, PE38KDEL, PE40, PE4E y PE38QQR.
19. Un ácido nucleico de la reivindicación 18, donde el fragmento de exotoxina de Pseudomonas es PE38.
20. Un vector de expresión que comprende un ácido nucleico de una cualquiera de las reivindicaciones 14 a 19 conectado operablemente a un promotor.
21. Un método para detectar la presencia de una célula cancerosa CD22+ en una muestra biológica, comprendiendo dicho método:
donde la detección de la presencia de dicha marca indica la presencia de una célula cancerosa CD22+ en dicha muestra.
22. Un método de la reivindicación 21, donde dicho anticuerpo se selecciona del grupo que consiste en un scFv, un dsFv, un Fab y un F(ab')2.
23. Un kit para detectar la presencia de una célula cancerosa CD22+ en una muestra biológica, comprendiendo dicho kit:
24. Un kit de la reivindicación 23, donde dicho anticuerpo se selecciona del grupo que consiste en un scFv, un dsFv, un Fab, y un F(ab')2.
25. Un método de inhibición del crecimiento de una célula cancerosa CD22+ poniendo en contacto dicha célula in vitro con un anticuerpo anti-CD22 de acuerdo con una cualquiera de las reivindicaciones 1 a 4, donde el anticuerpo está fusionado o conjugado con una citotoxina, cuya citotoxina inhibe el crecimiento de dicha célula.
26. Un anticuerpo de acuerdo con una cualquiera de las reivindicaciones 1 a 4 o una composición de acuerdo con una cualquiera de las reivindicaciones 5 a 12, para su uso en un método para inhibir el crecimiento de una célula cancerosa CD22+.
Patentes similares o relacionadas:
UTILIZACIÓN DE ANTÍGENOS A33 Y JAM-IT, del 10 de Febrero de 2012, de GENENTECH, INC.: Polipéptido para utilizar en el tratamiento de una enfermedad inflamatoria asociada con la sobreexpresión de STlgMA, en el que el polipéptido comprende […]
ANTICUERPOS CONTRA PD-1 Y SUS USOS, del 3 de Noviembre de 2011, de WYETH LLC MEDIMMUNE LIMITED: Un anticuerpo aislado o uno de sus fragmentos de unión al antígeno que comprende: Un dominio VH que comprende 3 CDRs; y un dominio VL que comprende 3 CDRs; […]
ANTICUERPOS ANTI-CD19 CON INMUNOGENICIDAD REDUCIDA, del 21 de Septiembre de 2011, de MERCK PATENT GMBH: Anticuerpo anti-CD19 diseñado y modificado derivado de anticuerpo B4 murino anti-CD19 caracterizado por la región variable de cadena pesada de […]
MOLÉCULAS DE ENLACE DE LINGO Y EL USO FARMACÉUTICO DE ESTAS, del 10 de Agosto de 2011, de NOVARTIS AG: Una molécula de enlace que es capaz de unirse a la proteína de acuerdo con la SEQ ID NO:1, SEQ ID NO: 2, o SEQ ID NO: 3, con una constante de disociación <1000nM, […]
ANTICUERPOS FRENTE A MAdCAM, del 11 de Julio de 2011, de PFIZER INC. AMGEN FREMONT INC: Una línea celular de hibridoma que produce un anticuerpo monoclonal humano que se une específicamente a la molécula de adhesión de Célula Mucosa […]
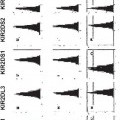 ANTICUERPOS QUE SE UNEN A RECEPTORES KIR2DL1, -2, -3 PERO NO A KIR2DS4 Y SU USO TERAPÉUTICO, del 6 de Junio de 2011, de NOVO NORDISK A/S Innate Pharma University of Genoa: Un anticuerpo humano o humanizado aislado, que se une a cada uno de receptores asesinos similares a Ig (KIR) 2DL1, KIR2DL2 y KIR2DL3, pero que no se une a KIR2DS4, […]
ANTICUERPOS QUE SE UNEN A RECEPTORES KIR2DL1, -2, -3 PERO NO A KIR2DS4 Y SU USO TERAPÉUTICO, del 6 de Junio de 2011, de NOVO NORDISK A/S Innate Pharma University of Genoa: Un anticuerpo humano o humanizado aislado, que se une a cada uno de receptores asesinos similares a Ig (KIR) 2DL1, KIR2DL2 y KIR2DL3, pero que no se une a KIR2DS4, […]
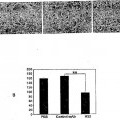 MOLÉCULAS INHIBIDORAS DE LA ANGIOGÉNESIS Y SU USO EN EL TRATAMIENTO Y DIAGNÓSTICO DEL CÁNCER, del 16 de Mayo de 2011, de MERCK SERONO SA: Una molécula que inhibe la angiogénesis, que se selecciona del grupo que consiste en el anticuerpo H33, producido por el hibridoma 13H33 según está depositado en el Deutsche […]
MOLÉCULAS INHIBIDORAS DE LA ANGIOGÉNESIS Y SU USO EN EL TRATAMIENTO Y DIAGNÓSTICO DEL CÁNCER, del 16 de Mayo de 2011, de MERCK SERONO SA: Una molécula que inhibe la angiogénesis, que se selecciona del grupo que consiste en el anticuerpo H33, producido por el hibridoma 13H33 según está depositado en el Deutsche […]
 ELEMENTOS DE UNIÓN A CD-3 DESINMUNIZADOS MULTIESPECÍFICOS, del 10 de Mayo de 2011, de MICROMET AG: Una construcción de unión específica a CD3 citotóxicamente activa que comprende un primer dominio que se une específicamente a CD3 humano […]
ELEMENTOS DE UNIÓN A CD-3 DESINMUNIZADOS MULTIESPECÍFICOS, del 10 de Mayo de 2011, de MICROMET AG: Una construcción de unión específica a CD3 citotóxicamente activa que comprende un primer dominio que se une específicamente a CD3 humano […]