Proteínas de unión y receptores solubles modificados con glicanos y su uso.
Un receptor de TNF soluble (sTNFR) modificado con glicanos que porta una Gal,
GlcNAc o GalNAc terminal,seleccionado de un asialo-TNFR soluble (as-sTNFR), asialo-agalacto-TNFR soluble (as-ag-sTNFR), TNFR solublelactosaminado (lac-sTNFR), y TNFR soluble N-acetilgalactosaminado (sTNFR-Gn).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IL2008/000574.
Solicitante: YEDA RESEARCH AND DEVELOPMENT CO. LTD..
Nacionalidad solicitante: Israel.
Dirección: WEIZMANN INSTITUTE OF SCIENCE P.O. BOX 95 76100 REHOVOT ISRAEL.
Inventor/es: RUBINSTEIN, MENACHEM, WERMAN,ARIEL, ALKAHE,BEN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/43 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Taumatina.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C07K14/715 C07K 14/00 […] › para citoquinas; para linfoquinas; para interferones.
PDF original: ES-2412892_T3.pdf
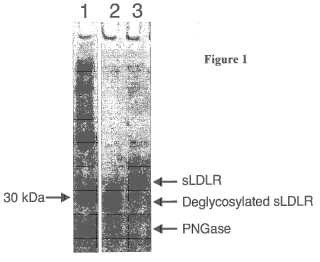
Fragmento de la descripción:
Proteínas de unión y receptores solubles modificados con glicanos y su uso Campo de la invención La presente invención se refiere a agentes capaces de retirar de la circulación componentes no deseados y al uso clínico de dichos agentes. Los ejemplos de dichos componentes no deseados son las citoquinas proinflamatorias, LDL, VLDL, LDL oxidada, lipoproteínas remanentes y factores del crecimiento.
Antecedentes de la invención Las proteínas de unión y los receptores solubles son proteínas en la circulación que se unen con alta afinidad y especificidad a diversas citoquinas, factores del crecimiento, hormonas polipeptídicas y otras proteínas efectoras en la circulación. En la mayoría de los casos, el receptor soluble se corresponde con el dominio de unión al ligando extracelular del correspondiente receptor de la superficie celular. Estos receptores solubles se generan mediante variantes de corte y empalme del ARNm que codifica el receptor soluble, o mediante el desprendimiento del dominio extracelular de unión al ligando del receptor de la superficie celular. Sin embargo, existen algunas proteínas de unión a citoquinas, tales como la proteína de unión a IL-18 (IL-18BP) y la osteoprotegerina, que no se corresponden con un receptor de la superficie celular.
La existencia de receptores solubles y la compleja regulación de su producción y función sugiere que desempeñan un papel importante en la fisiología normal y en respuesta a una enfermedad, aunque en algunos casos parecen contribuir al proceso patológico. Por ejemplo, un componente importante de la respuesta alérgica está mediado por eosinófilos cuya producción y actividad se ve significativamente estimulada por IL-5. En pacientes con asma alérgico, el nivel de ARNm que codifica el receptor de IL-5 unido a membrana en muestras de biopsia endobronquial aumenta con la gravedad del estrangulamiento bronquial. A medida que los pacientes tratados se recuperan de un episodio asmático agudo, la expresión del ARNm del receptor de IL-5 soluble aumenta, lo cual sugiere que el receptor de IL-5 soluble pueden contrarrestar los efectos de IL-5 en el pulmón y el aumento en su expresión puede producir la recuperación del asma (Heaney y Golde, 1998) .
Debido a su implicación fundamental en la patogénesis de muchas enfermedades, las citoquinas constituyen dianas clave para estrategias bioterapéuticas. El descubrimiento de que las formas solubles de los receptores de citoquinas están implicadas en la regulación endógena de la actividad de las citoquinas ha provocado un interés sustancial en su aplicación potencial como agentes inmunoterapéuticos. Como tales, los receptores de citoquinas solubles tienen muchas ventajas, incluyendo su especificidad, baja inmunogenicidad y alta afinidad. La capacidad de muchos receptores de citoquinas solubles para inhibir la unión y la actividad biológica de sus ligandos los hace ser antagonistas de citoquinas muy específicos. Varias empresas farmacéuticas han generado una serie de agentes terapéuticos basados en receptores de citoquinas solubles y muchos de ellos están sometiéndose a ensayos clínicos. El más avanzado con respecto al desarrollo clínico es el etanercept (Enbrel!, Amgen) , una proteína de fusión entre el receptor de TNF soluble de tipo II y la región Fc de la IgG1 humana. Este antagonista de TNF-∀ ha sido el primer receptor de citoquinas soluble que ha recibido aprobación para un uso en seres humanos. En general, la mayoría de los agentes basados en receptores de citoquinas solubles han resultado ser seguros, bien tolerados y sólo han mostrado unos pequeños efectos secundarios en la mayoría de los pacientes. Los receptores de citoquinas solubles constituyen una nueva generación de agentes terapéuticos con un tremendo potencial para aplicaciones en una amplia diversidad de enfermedades humanas (Idriss y Naismith, 2000) .
El TNF∀ se une a dos receptores cognados de peso molecular 55 y 75 kDa. El TNFR-1 humano consiste en 434 aminoácidos, mientras que el TNFR-2 comprende 439 restos. Estos receptores comparten una homología muy limitada en la región extracelular. La superfamilia de receptores de TNF se define por la presencia de unidades repetidas de agrupamientos de cisteínas. Los receptores de TNF están presentes en cada todos los tipos celulares conocidos con pocas excepciones, tales como eritrocitos y linfocitos T no estimulados. La densidad de los receptores varía de 200-10.000 por célula. No parece existir correlación entre el número de receptores presentes sobre una célula y la magnitud o dirección de la respuesta inducida por TNF. Se han identificado formas solubles de TNFR-1 y TNFR-2 en la orina humana y en el suero de pacientes con cáncer. Estas probablemente regulan la actividad del TNF atrayendo como señuelo al ligando, infrarregulando con ello las señales generadas.
Hasta la fecha se han identificado muchos receptores unidos a membranas (incluyendo TNFR-1 y -2) , que forman lo que se conoce como la superfamilia de receptores de TNF. Su peso molecular está en el intervalo de 50-120 kDa. Los miembros de la familia de receptores de TNF pertenecen a las glicoproteínas transmembrana de tipo I. También se ha identificado una serie de receptores relacionados denominados “receptores señuelo”, que actúan secuestrando a los ligandos segregados. Los receptores señuelo (DcR1, DcR2 y DcR3) secuestran a los ligandos Trail (DcR1 y DcR2) y Fas (DcR3) , evitando con ello la apoptosis. Además también se ha identificado un receptor señuelo no unido a membrana soluble denominado osteoprotegerina (OPG) . No se han indicado muchas modificaciones postraduccionales para la familia de TNFR-1. TNFR-1 y TNFR-2 están ambos N-glicosilados, pero sólo TNFR-2 está O-glicosilado. Todos los demás receptores de membrana también están glicosilados (Idriss y Naismith, 2000) .
La artritis reumatoide (AR) , una enfermedad sistémica, es la forma más común de artritis inflamatoria. El trastorno tiene una prevalencia muncial de aproximadamente 1% y una incidencia anual de 3 por cada 10.000 adultos. La AR viene acompañada de una significativa morbilidad y mortalidad. Dependiendo de la gravedad de la enfermedad en el momento de su aparición, el riesgo de discapacidad puede ser tan alto como 33%, y la mortalidad puede aumentar tanto como 52%, con frecuencia como resultado de una infección o una enfermedad circulatoria. Tal como puede esperarse, los pacientes con AR también presentan un deterioro significativo en su calidad de vida.
Los objetivos finales del tratamiento son la prevención o el control de los daños en las articulaciones, la prevención de la pérdida funcional, y el alivio del dolor. Con la introducción de los antagonistas del factor de necrosis tumoral (TNF) en 1999, la gestión de la AR ha cambiado considerablemente. El infliximab (Remicade#) , el etanercept (Enbrel#) y el adalimumab (Humira!) se han diseñado para modular la cascada inflamatoria de la AR mediante su unión a TNF, disminuyendo con ello su biodisponibilidad.
Se han detectado diversas citoquinas proinflamatorias en el fluido sinovial de pacientes con ARN, que incluyen TNF, interleuquina 1 (IL-1) , IL-17, IL-18 e IL-6. Estudios anteriores demostraron que en un sistema de cultivo de células sinoviales, la síntesis secundaria de IL-1 y otras citoquinas puede reducirse en gran medida dirigiéndose específicamente al TNF. El papel del TNF se basa en (1) su capacidad para degradar el cartílago y el hueso in vitro,
(2) sus propiedades artritogénicas en modelos animales, (3) la colocalización de sus receptores en el sinovio AR y la unión entre el pannus y el cartílago, y (4) su papel fundamental para regular la síntesis de IL-1 en células sinoviales derivadas de AR cultivadas.
El etanercept es una proteína de fusión que consiste en la porción de unión al ligando del receptor de TNF p75 humano más el fragmento Fc de IgG1 humana. El etanercept tiene una semivida terminal de 102 ∃ 30 horas. La dosis inicial recomendada es de 25 mg por vía subcutánea dos veces semanales, con o sin metotrexato. El tratamiento con etanercept produce unas reducciones significativas relacionadas con la dosis en la actividad de la enfermedad y no aparecen problemas de seguridad significativos. Los antagonistas de TNF representan un avance significativo en la terapia de la AR activa. Han demostrado eficacia en la inhibición de la destrucción de las articulaciones a lo largo de diversas longitudes de tiempo, reduciendo los síntomas y mejorando la función física en pacientes con AR (Schwartzman, Fleischmann et al., 2004) .
El etanercept está aprobado para su uso en EEUU como monoterapia subcutánea en adultos con psoriasis de moderada a grave que son candidatos para la terapia sistémica... [Seguir leyendo]
Reivindicaciones:
1. Un receptor de TNF soluble (sTNFR) modificado con glicanos que porta una Gal, GlcNAc o GalNAc terminal, seleccionado de un asialo-TNFR soluble (as-sTNFR) , asialo-agalacto-TNFR soluble (as-ag-sTNFR) , TNFR soluble lactosaminado (lac-sTNFR) , y TNFR soluble N-acetilgalactosaminado (sTNFR-Gn) .
2. El uso de un receptor de TNF soluble (sTNFR) modificado con glicanos que porta una Gal, GlcNAc o GalNAc terminal, para la fabricación de un medicamento para tratar o prevenir una enfermedad autoinmunológica o una enfermedad inflamatoria cuya patogénesis o desarrollo está asociado con los niveles o la actividad del TNF.
3. El uso según la reivindicación 2, en el que la enfermedad, el trastorno o la afección está asociado con un exceso de TNF y/o en el que el receptor soluble se selecciona de as-sTNFR, as-ag-sTNFR, lac-sTNFR y sTNFR-Gn.
4. El uso según la reivindicación 2 o 3, en el que la enfermedad autoinmunológica se selecciona de la artritis reumatoide, la enfermedad de Crohn, y la psoriasis.
5. Una composición farmacéutica que comprende un receptor soluble modificado con glicanos de la reivindicación 1, y un vehículo farmacéuticamente aceptable.
6. Un receptor de TNF soluble (sTNFR) modificado con glicanos que porta una Gal, GlcNAc o GalNAc terminal, para su uso en el tratamiento o la prevención de una enfermedad autoinmunológica o una enfermedad inflamatoria cuya patogénesis o desarrollo está asociado con los niveles y/o la actividad del TNF.
7. El receptor de TNF soluble (sTNFR) modificado con glicanos según la reivindicación 6, para su uso según se define en la reivindicación 6, en el que la enfermedad autoinmunológica se selecciona de la artritis reumatoide, la enfermedad de Crohn, y la psoriasis.
Patentes similares o relacionadas:
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Procedimientos de tratamiento del cáncer usando antagonistas de unión al eje de PD-1 e inhibidores de TIGIT, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo antagonista anti-PD-L1 o fragmento de unión a antígeno del mismo y un anticuerpo antagonista anti-TIGIT o fragmento de unión a antígeno del mismo para su uso […]
Uso de CAR basados en ICOS para mejorar la actividad antitumoral y la persistencia del CAR, del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una secuencia de ácido nucleico aislada que codifica un receptor de antígeno quimérico (CAR), en donde el CAR comprende un dominio de unión a antígeno, un dominio transmembrana […]
Péptido derivado de GPC3, composición farmacéutica para el tratamiento o la prevención de cáncer usando el mismo, inductor de inmunidad y método para producir células presentadoras de antígeno, del 17 de Junio de 2020, de CYTLIMIC INC: Composición farmacéutica para su uso en el tratamiento o la prevención de cáncer, que comprende un péptido que consiste en una secuencia de aminoácidos […]
Péptidos inhibidores derivados del transcrito de tipo TREM-1 (TLT-1) y sus usos, del 10 de Junio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un polipéptido de 6 a 16 aminoácidos que comprende al menos 6 aminoácidos consecutivos de la secuencia de aminoácidos sec. con núm. de ident.: 4 para su uso en el tratamiento […]
Fijación eficaz como objetivo de la leucemia humana primaria utilizando células T modificadas con receptor de antígeno quimérico anti-CD123, del 3 de Junio de 2020, de NOVARTIS AG: Una molécula de ácido nucleico aislada que codifica un receptor de antígeno quimérico (CAR), en donde dicho CAR comprende un dominio de unión anti-CD123 humanizado, […]
Dominios coestimuladores para su uso en células genéticamente modificadas, del 3 de Junio de 2020, de Precision Biosciences, Inc: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica un dominio coestimulador que comprende una secuencia de aminoácidos establecida […]
Método para proporcionar linfocitos T específicos de tumor, del 27 de Mayo de 2020, de HS Diagnomics GmbH: Un método para fabricar un receptor artificial de linfocitos T específicos de tumor, que comprende las etapas de: - proporcionar una preparación de linfocitos […]