Usos de inmunoconjugados dirigidos a CD138.
Un inmunoconjugado para su uso en el tratamiento de una enfermedad asociada a células diana que expresan CD138 en un sujeto humano,
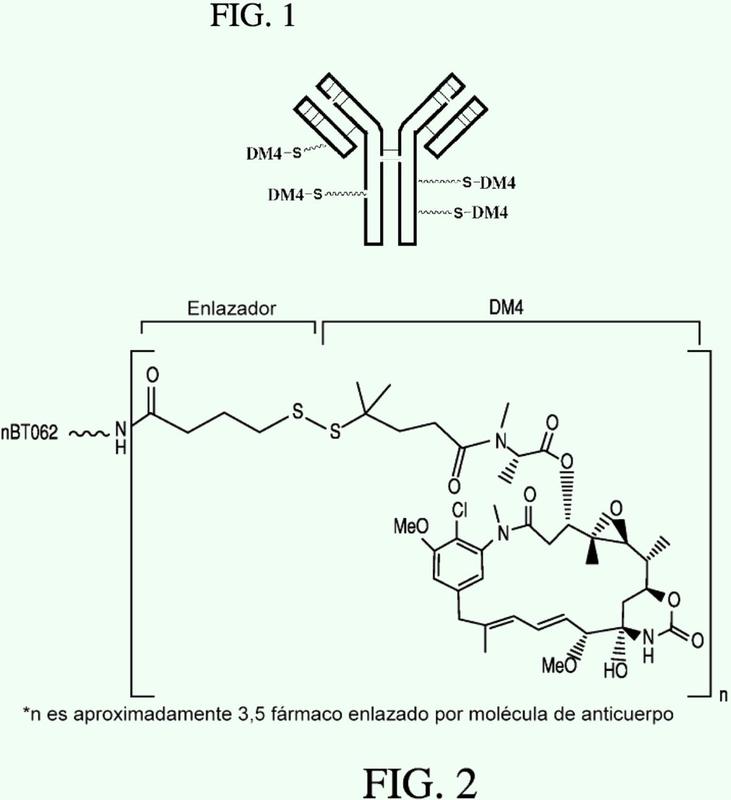
donde el inmunoconjugado comprende al menos un anticuerpo dirigido a diana de ingeniería que marca como diana células que expresan CD138 y
al menos una molécula efectora, donde dicho anticuerpo dirigido a diana de ingeniería se fija funcionalmente a dicha molécula efectora para formar dicho inmunoconjugado,
donde preferentemente al menos parte del anticuerpo dirigido a diana de ingeniería confiere propiedades de isotipo IgG4,
donde la molécula efectora es al menos un maitansinoide,
donde el anticuerpo dirigido a diana de ingeniería comprende:
(i) una región variable de cadena pesada CDR1 que comprende los restos de aminoácidos 31 a 35 de SEQ ID NO: 1, una región variable de cadena pesada CDR2 que comprende los restos de aminoácidos 51 a 68 de SEQ ID NO: 1 y una región variable de cadena pesada CDR3 que comprende los restos de aminoácidos 99 a 111 de SEQ ID NO: 1; y
(ii) una región variable de cadena ligera CDR1 que comprende los restos de aminoácidos 24 a 34 de SEQ ID NO: 2, una región variable de cadena ligera CDR2 que comprende los restos de aminoácidos 50 a 56 de SEQ ID NO: 2 y una región variable de cadena ligera CDR3 que comprende los restos de aminoácidos 89 a 97 de SEQ ID NO: 2;
donde el inmunoconjugado ha de administrarse en un régimen de múltiples dosis, donde la dosis de agregado a administrarse dentro de un ciclo de tratamiento activo es una dosis tolerable máxima agregada (AMTD) o una fracción de AMTD y donde dicha AMTD y/o dicha fracción excede la dosis que resulta en toxicidad limitante de dosis (DLT) cuando el inmunoconjugado se administra como una dosis única, incluyendo como parte de un régimen de dosis única múltiple dentro de dicho ciclo de tratamiento activo y/o excede la dosis tolerable máxima (MTD) cuando el inmunoconjugado se administra como una sola dosis, incluyendo como parte de un régimen de dosis única múltiple dentro de dicho ciclo de tratamiento activo,
donde la dosis tolerable máxima agregada es al menos 240 mg/m2, preferentemente 300 mg/m2, preferentemente 360 mg/m2, preferentemente 420 mg/m2,
donde la dosis que resulta en dicha toxicidad limitante de dosis es 200 mg/m2 y/o la dosis tolerable máxima al menos 160 mg/m2 o al menos 180 mg/m2,
donde el inmunoconjugado ha de administrarse en un ciclo de tratamiento activo de 21 días, al menos tres veces dentro de dichos 21 días,
donde el ciclo de tratamiento activo incluye la administración del inmunoconjugado realizándose al menos una vez a la semana,
donde la enfermedad asociada a las células diana que expresan CD138 es mieloma múltiple, carcinoma de células renales, cáncer de endometrio, cáncer cervical, adenocarcinoma de próstata,
carcinoma pancreático, cáncer gástrico, cáncer de vejiga, carcinoma mamario, hepato-carcinoma, carcinoma colorrectal, carcinoma de colon, carcinoma de células escamosas, cáncer de pulmón, linfoma no Hodgkiniano, carcinoma de timo, carcinoma de útero, carcinoma urinario o carcinoma de ovario.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2012/074867.
Solicitante: BIOTEST AG.
Nacionalidad solicitante: Alemania.
Dirección: LANDSTEINERSTR. 5 63303 DREIEICH ALEMANIA.
Inventor/es: UHEREK,CHRISTOPH, BRUECHER,CHRISTOPH, DAELKEN,BENJAMIN, OSTERROTH,FRANK, SCHULZ,GREGOR, HAEDER,THOMAS, WARTENBERG-DEMAND,ANDREA, ZUBER,CHANTAL, ENGLING,ANDRÉ, NIEMANN,GABRIELE, GUTSCHER,MARCUS, BERNOESTER,KATRIN, KOENIG,MARTIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K47/68 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › siendo el agente modificador un anticuerpo, una inmunoglobulina o un fragmento de los mismos, p. ej. un fragmento Fc.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
PDF original: ES-2684950_T3.pdf
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]