Conjugación de polisacárido con enterotoxina termolábil (LT) de E. coli desintoxicada usada como vacuna.
Un conjugado covalente de un polisacárido y una enterotoxina termolábil (LT) de E.
coli desintoxicada, en el que la LT es una holotoxina y es una proteína mutante LTS61K que tiene una sustitución de lisina en la posición correspondiente a la posición 61 de SEC ID Nº: 5.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2011/001429.
Solicitante: DCB-USA LLC.
Inventor/es: HSU,YU-SHEN, YUAN,TA-TUNG, KOU,I-LING, HUNG,KUO-CHAN, LU,YUAN-HSIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/02 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos bacterianos.
- A61K39/108 A61K 39/00 […] › Escherichia; Klebsiella.
- A61K39/38 A61K 39/00 […] › Antígenos de serpientes.
- A61K39/385 A61K 39/00 […] › Haptenos o antígenos, unidos a soportes.
- A61P1/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 1/00 Medicamentos para el tratamiento de trastornos del tracto alimentario o del aparato digestivo. › Antidiarreicos.
- A61P31/04 A61P […] › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
- C12N1/20 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › Bacterias; Sus medios de cultivo.
PDF original: ES-2550853_T3.pdf




Fragmento de la descripción:
Conjugación de polisacárido con enterotoxina termolábil (LT) de E. coli desintoxicada usada como vacuna Descripción Antecedentes de la invención:
Las vacunas de polisacárido, cuando se preparan sin proteína transportadora, carecen de respuestas de memoria inmunitaria. Las vacunas conjugadas actualmente conocidas incluyen polisacáridos capsulares bacterianos tales como Haemophilus influenzae tipo b, Neisseria meningitidis grupo C y Streptococcus pneumoniae serotipos 1, 3, 4, 5, 6B, 7F, 9V, 14, 19F, 23F. Estas vacunas están conjugadas covalentemente con una proteína transportadora, tal como el toxoide tetánico, toxoide diftérico, CRM197, una toxina diftérica no tóxica mutante, o proteína de la membrana externa de Neisseria meningitidis. Estas vacunas de conjugado de polisacárido podrían inducir respuesta dependiente de linfocitos T, especialmente en bebés por debajo de la edad de dos años; y podrían sensibilizar la memoria inmunológica a largo plazo, producir anticuerpo de alta afinidad y podrían reducir la tasa de colonización y transmisión nasofaríngea.
Sin embargo, la mayoría de las vacunas de conjugado de polisacárido bacterianas actualmente comercializadas aplicaron toxoide tetánico (TT) o toxoide diftérico (DT) como proteína transportadora. TT y DT, estas dos proteínas de toxoide, son vacunas habituales para bebés/niños; la vacunación de alta frecuencia de TT y DT dentro de un corto tiempo podría tener un impacto sobre la inmunogenicidad y seguridad (Reduced response to multiple vaccines sharing common protein epitopes that are administered simultaneously to infants. Infect. Immun. 1998; 66 (5) :20938; Immunogenicity and safety of a combination pneumococcalmeningococcal vaccine in infants: a randomized controlled trial. JAMA 2005; 293 (14) : 17518) . Por tanto, la presente invención proporciona un nuevo tipo de la proteína transportadora LTS61K para su uso en la vacuna de conjugado.
El documento EP 0 172 107 A1 desvela un conjugado de una subunidad de LTB no tóxico (LTBNT) y un polisacárido capsular bacteriano. El conjugado obtenido de LTBNT y polisacárido estuvo en forma agregada, y así se usó urea 5 M en el proceso de conjugación para eliminar los agregados. Como la urea es un desnaturalizante de proteínas, la utilización de urea afectaría la estructura y actividad de la subunidad de LTB, y así la subunidad de LTB tratada ya no se presenta como una estructura pentámera completa en su forma natural.
Resumen de la invención:
La presente invención incluye la conjugación de polisacáridos con una enterotoxina termolábil (LT) de E. coli desintoxicada en la que LT es una holotoxina y es una proteína mutante LTS61K que tiene una sustitución de lisina en la posición correspondiente a la posición 61 de SEC ID Nº: 5 útil como vacuna para proteger o inmunizar contra los efectos de bacterias infecciosas tales como Haemophilus influenzae y Streptococcus pneumoniae y aliviar la diarrea del viajero producida por E. coli enterotoxigénica.
Un aspecto de la presente invención se refiere a vacunas de polisacáridoLTS61 K covalentemente conjugadas aisladas en forma purificada. Estos productos conjugados tienen inesperadamente propiedades inmunogénicas y bactericidas superiores en mamíferos. Otro aspecto se refiere al uso de polisacáridoLTS61K conjugado para la preparación de una vacuna para un mamífero en necesidad de protección de Haemophilus influenzae tipo b (Hib) . Las vacunas de la presente invención estimulan la respuesta de linfocitos T colaboradores, presentan fuerte respuesta al refuerzo tras la reexposición y tienen altos títulos de anticuerpos.
Todavía otro aspecto de la invención se refiere al método de producción de polisacáridoLTS61K conjugado por aminación reductora y aislamiento del producto conjugado purificado. Según la presente invención, se descubrió que el método preferido de conjugar polisacárido y LTS61K para preparar la vacuna de la presente invención es la oxidación con per y odato del PS nativo, seguido de aminación reductora.
La LTS61K empleada en los conjugados de la presente invención se describe en la solicitud PCT número PCT/US2007/075801, presentada el 13 de agosto de 2007; en las solicitudes de EE.UU. Números US 1 1/779419 presentada el 18 de julio de 2007, US 12/120.953 presentada el 15 de mayo de 2008 y US 12/729.649 presentada el 23 de marzo de 2010; y en la solicitud de patente de Taiwán Nº 95139707 presentada el 27 de octubre de 2006 y concedida en enero de 2009.
Breve descripción de las figuras:
La Figura 1 es una representación generalizada de una proteína transportadora LT.
La Figura 2 es la representación estructural de sacáridos de PRP de Hib.
La Figura 3 muestra varios métodos de conjugación.
La Figura 4 muestra un método de aminación reductora según la presente invención.
La Figura 5 representa la conjugación de PRP y LTS61K por aminación reductora. La Figura 6 muestra el perfil de elución de HPLCSECRI de PRP oxidado después del tratamiento con NaIO4. La Figura 7 es un espectro de RMN de PRP oxidado. Esto confirma la formación de grupos aldehído sobre PRP después de la oxidación con per y odato. La Figura 8 muestra espectros de CD de UV lejano que confirman que no hay diferencia en la estructura secundaria entre muestras de LTS61K y conjugadas de PRPLTS61K; y también espectros de fluorescencia que confirman que no hay diferencia de la estructura terciaria máx [lambda] entre muestras de LTS61K y conjugadas de PRPLTS61K. La Figura 9 muestra análisis de aminoácidos que confirman la conjugación satisfactoria de PRP con LTS61K y la formación de un enlace covalente.
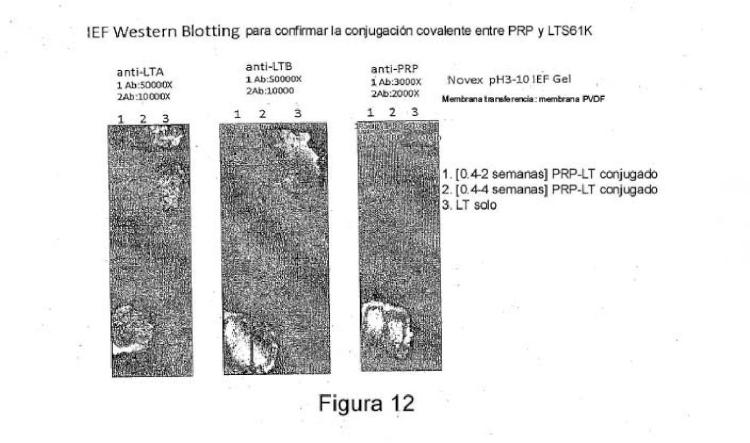
La Figura 10 muestra el análisis de transferencia Western por SDSPAGE para confirmar la conjugación covalente entre PRP y LTS61K. La Figura 11 muestra conjugados de PRPLTS61K purificados analizados por IEF PAGE. La Figura 12 muestra la transferencia Western IEF para confirmar la conjugación covalente entre PRP y LTS61K. La Figura 13 confirma la pureza de la vacuna de conjugado purificada mediante HPLCSECUVMALLSRI. La Figura 14 muestra los conjugados de PRPLTS61K purificados analizados por IEF PAGE para confirmar la pureza de la vacuna de conjugado purificada.
La Figura 15 resume un estudio de inmunogenicidad de rata de conjugados de PRP de HibLTS61 de la presente invención. La Figura 16 resume un estudio de inmunogenicidad de conejo de conjugados de PRP de HibLTS61 K de la presente invención. La Figura 17 ilustra los resultados de un estudio de inmunogenicidad de conejo de conjugados de PRP de Hib
LTS61K de la presente invención, resultados del ensayo de títulos bactericidas en sueros de conejo y títulos de Ab antiIgG de PRP. La Figura 18 ilustra información adicional sobre el estudio de inmunogenicidad de conejo. La Figura 19 ilustra resultados de un estudio de inmunogenicidad de conejo de conjugados de PRP de Hib
LTS61K de la presente invención, resultados de los títulos bactericidas en sueros de conejo (BA) y títulos de Ab
antiIgG de PRP (DO) . La Figura 20 muestra resultados de ELISA de inmunogenicidad de conejo adicional de estudios de respuestas de anticuerpos antiPRP y antiLTS61K.
La Figura 21 muestra los resultados del ensayo bactericida en sueros de conejo adicional y Ab antiIgG de PRP. La Figura 22 muestra resultados de ensayo bactericida en sueros de conejo adicional y Ab antiIgG de PRP después de una cuarta inmunización.
La Figura 23 muestra la inmunogenicidad en ratón sobre conjugados de PS de serotipo 14 neumocócicoLTS61K.
Descripción detallada de la invención: Los presentes inventores han descubierto ahora que las vacunas de polisacáridoLTS61K conjugadas hechas según la presente invención inducen sorprendentemente mayores títulos de anticuerpos IgG específicos de polisacárido y mayor actividad bactericida en sueros que las de polisacárido o polisacárido mezclado con LTS61K.
Una lista de abreviaturas empleada en el presente documento es la siguiente: CFU: unidad formadora de colonias ELISA: enzimoinmunoanálisis de adsorción
Hib: tipo Haemophilus influenzae bIEF: isoelectroenfoque LT: enterotoxina termolábil MALLS: dispersión de luz láser a múltiples ángulos DO: densidad óptica PNPS: polisacárido neumocócico PRP: polirribosil ribitol fosfato PS: polisacárido SDSPAGE: electroforesis en gel de dodecilsulfato de sodiopoliacrilamida SEC_HPLC: cromatografía líquida de alta presión de exclusión de tamaño RI: índice de refracción La nueva proteína transportadora empleada en los conjugados de la presente invención es el mutante de la enterotoxina termolábil de E. coli recombinante desintoxicada LTS61K. En el mutante de LT, las subunidades A y B
forman... [Seguir leyendo]
Reivindicaciones:
Reivindicaciones
10 15 20 25 30 1. Un conjugado covalente de un polisacárido y una enterotoxina termolábil (LT) de E. coli desintoxicada, en el que la LT es una holotoxina y es una proteína mutante LTS61K que tiene una sustitución de lisina en la posición correspondiente a la posición 61 de SEC ID Nº: 5. 2. El conjugado covalente de la reivindicación 1, en el que el polisacárido es polirribosil ribitol fosfato (PRP) . 3. Una vacuna que comprende un conjugado covalente purificado de la reivindicación 1 o 2. 4. Uso de un conjugado covalente purificado de la reivindicación 1 o 2 en la fabricación de un medicamento para proteger o inmunizar mamíferos de los efectos de bacterias infecciosas. 5. Un método de preparación de un conjugado covalente de la reivindicación 1 o 2 que comprende oxidación con per y odato del polisacárido, seguido de aminación reductora del polisacárido resultante y la proteína mutante LTS61K, y aislamiento del conjugado resultante. 6. El método de la reivindicación 5, en el que el polisacárido es PRP. 7. El método de la reivindicación 6, en el que el intervalo de relaciones molares de PRP:LT está entre aproximadamente 3:1 y aproximadamente 60:1. 8. Uso de un conjugado covalente purificado de la reivindicación 1 o 2 en la fabricación de un medicamento para proteger o inmunizar mamíferos de los efectos de la diarrea del viajero. 9. Uso de un conjugado covalente purificado de la reivindicación 1 o 2 en la fabricación de un medicamento para proteger o inmunizar mamíferos de los efectos de la diarrea de E. coli enterotoxigénica. 10. Uso de un conjugado covalente purificado de la reivindicación 1 o 2 en la fabricación de un medicamento para proteger o inmunizar mamíferos de la infección de Haemophilus influenzae o Streptococcus pneumoniae.
Patentes similares o relacionadas:
Formulación de inmunoglobulina y procedimiento de preparación de la misma, del 17 de Junio de 2020, de Biogen MA Inc: Una formulación acuosa estable que comprende natalizumab en una concentración de 15 mg/mL a 50 mg/mL, un tampón fosfato, polisorbato 80 en […]
Composiciones y métodos terapéuticos, del 6 de Mayo de 2020, de INSTITUT PASTEUR: Un compuesto para su uso en un método para tratar una inmunodeficiencia de células T CD4 en un sujeto que lo necesita, en el que el compuesto es […]
Nanoportadores sintéticos tolerogénicos para reducir las respuestas de anticuerpos, del 1 de Abril de 2020, de Selecta Biosciences, Inc: Una composición para usar en un método que promueve una respuesta inmunitaria tolerogénica a un antígeno que de otro modo causaría una respuesta inmunitaria […]
Composiciones y procedimientos para identificar especies de Ehrlichia, del 18 de Marzo de 2020, de Abaxis, Inc: Un procedimiento de identificación de las especies de Ehrlichia que infectan a un sujeto, si están presentes, comprendiendo el procedimiento: poner en contacto una […]
Composiciones de vacunas y adyuvantes y métodos para el tratamiento de infecciones del tracto urinario, del 10 de Junio de 2019, de Sequoia Vaccines, Inc: Una composición que comprende disacárido de hexaacilo fosforilado (PHAD), al menos una fosfatidilcolina y un tampón citrato de 10 mM a 50 mM; en donde la fosfatidilcolina […]
Empleo de una composición que comprende un prebiótico para disminuir el proceso inflamatorio y activación anormal de parámetros inmunológicos no específicos, del 13 de Mayo de 2019, de SOCIETE DES PRODUITS NESTLE S.A.: Empleo de por lo menos un prebiótico en la elaboración de un medicamento o un alimento o una composición para pienso de animales domésticos, para la disminución de […]
Vacunas de filovirus basadas en un vector adenovírico de chimpancé, del 6 de Mayo de 2019, de THE GOVERNMENT OF THE UNITED STATES OF AMERICA AS REPRESENTED BY THE SECRETARY OF THE DEPARTMENT OF HEALTH AND HUMAN SERVICES: Un vector de adenovirus de chimpancé recombinante de serotipo ChAd3 que comprende un ácido nucleico que codifica una glicoproteína del virus Ébola, o una composición […]
Composiciones vacunales con una matriz proteica que incluye policationes, del 27 de Marzo de 2019, de Matrivax, Inc: Un método para producir una composición inmunógena que lleva un antígeno útil atrapado en la matriz de proteína transportadora/policatión, el cual está unido de […]