Uso de p97 como sistema de administración de enzimas para la administración de enzimas lisosómicas terapéuticas.
Una composición farmacéutica para uso en el tratamiento de un sujeto que tiene una enfermedad de almacenamiento lisosómico;
comprendiendo dicha composición una molécula de p97 unida covalentemente a una proteína cuya deficiencia provoca la enfermedad; en donde la proteína está seleccionada de entre el grupo que consiste en a-L-iduronidasa, iduronato-2-sulfatasa, heparan-N-sulfatasa, a-N-acetilglucosaminidasa, arilsulfatasa A, galactosilceramidasa, a-glucosidasa ácida, tioesterasa, hexosaminidasa A, esfingomielinasa ácida y a- galactosidasa; y en donde la composición se administra a un lisosoma en una célula del sujeto.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/000894.
Solicitante: biOasis Technologies Inc.
Nacionalidad solicitante: Canadá.
Dirección: Suite 125-10551 Shellbridge Way Richmond, BC V6X 2W9 CANADA.
Inventor/es: STARR, CHRISTOPHER M., ZANKEL,TODD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/70 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Hidratos de carbono; Azúcares; Sus derivados (sorbitol A61K 31/047).
- A61K38/17 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K38/44 A61K 38/00 […] › Oxidoreductasas (1).
- A61K38/46 A61K 38/00 […] › Hidrolasas (3).
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K47/48
- C07K1/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Procedimientos generales de preparación de péptidos.
- C12P21/04 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
- C12P21/06 C12P 21/00 […] › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/566 G01N 33/00 […] › utilizando un soporte específico o proteínas receptoras como reactivos para la formación de uniones por ligando.
PDF original: ES-2496493_T3.pdf
Fragmento de la descripción:
Uso de p97 como sistema de administración de enzimas para la administración de enzimas lisosómicas terapéuticas
Campo de la invención
La presente memoria descriptiva está relacionada con el campo de la farmacia y específicamente con el tratamiento de enfermedades a través de la introducción en un sujeto de la proteína o polipéptido p97 conjugado con un agente terapéutico o de diagnóstico. En particular, esta memoria descriptiva se refiere a conjugados de p97 y proteínas deficientes en una enfermedad de almacenamiento lisosómico y métodos para el tratamiento, la mejora o la prevención de enfermedades de almacenamiento lisosómico mediante la administración de los conjugados a sujetos afectados por tales enfermedades.
Antecedentes de la invención
Las enfermedades de almacenamiento lisosómico (EAL) surgen como resultado de la ausencia o reducción de la actividad de enzimas específicas dentro de los lisosomas de una célula. Se ha identificado un gran número de estas enzimas y se han correlacionado con sus enfermedades relacionadas. Una vez identificada la enzima ausente o deficiente, el tratamiento se puede reducir al problema de administrar una enzima de reemplazo (fármaco) a los tejidos afectados de un paciente. Dentro de las células, el efecto de la enzima ausente se puede observar como una acumulación de "material de almacenamiento" no degradado dentro del lisosoma intracelular. Esta acumulación provoca que los lisosomas se hinchen y funcionen mal, lo que se traduce en daño celular y tisular. Puesto que las enfermedades de almacenamiento lisosómico típicamente tienen una etiología genética, muchos tejidos carecerán de la enzima en cuestión. Sin embargo, diferentes tejidos sufren la ausencia de la misma enzima de manera diferente. La magnitud de la afectación adversa de un tejido viene determinada, en cierta medida, por el grado en el que el tejido genere el sustrato de la enzima ausente. Los tipos de tejido que soportan la mayor carga del almacenamiento, a su vez, dictan cómo se debe administrar el fármaco al paciente. Mientras que la terapia de reemplazo enzimático (TRE) por vía intravenosa resulta beneficiosa para la EAL (por ejemplo, MPS I, MPS II) , contar con medios para la mejora de la administración de la enzima terapéutica a los lisosomas en estas enfermedades resultaría ventajoso en términos de reducción de costes y aumento de la eficacia terapéutica.
Además, la barrera hematoencefálica (BHE) bloquea la libre transferencia de muchos agentes de la sangre al cerebro. Por esta razón, no se espera que las EAL que presentan una afectación neurológica significativa (por ejemplo, MPS III, MLD, GM1) sean tan sensibles a la TRE intravenosa. Para tales enfermedades, sería altamente deseable disponer de un método de administración de la enzima a través de la BHE y hasta los lisosomas de las células afectadas.
A principios de los 1980, se identificó la melanotransferrina (MTf) o p97 como un antígeno oncofetal que o bien no se expresa o solo se expresa ligeramente en los tejidos normales, pero que se encuentra en cantidades mucho más grandes en las células neoplásicas (en particular en las células de melanoma malignas) y en los tejidos fetales (Woodbur y , y cols., P.N.A.S. USA, 77:2183-2187 (1980) ) . Más recientemente, se han documentado informes adicionales que describen la identificación de la MTf humana en tejidos normales, tales como los conductos de las glándulas sudoríparas, las células endoteliales del hígado, y el endotelio y la microglía reactiva del cerebro (Jefferies, y cols., Brain Res., 712:122-126 (1996) ; and Rothenberger, y cols., Brain Res., 712:117-121 (1996) ) .
Curiosamente, el suero normal contiene niveles muy bajos de MTf soluble circulante, pero se ha encontrado un aumento de la MTf sérica soluble en pacientes con enfermedad de Alzheimer avanzada (Kennard, y cols., Nat. Med., 2:1230-1235 (1996) ; patente de EE.UU. nº 5981194) .
Ha resultado difícil de elucidar la función bioquímica y el metabolismo de la MTf. A juzgar por su aspecto, la MFt es engañosamente similar a la transferrina (Tf) y a la lactotransferrina (lactoferrina o Lf) . En los seres humanos, estas proteínas comparten una homología de la secuencia de aminoácidos del 37-39 %. En particular, cada una de estas proteínas se une reversiblemente al hierro, y sus dominios N-terminales de unión al hierro son bastante similares (Baker, y cols., TIBS, 12:350-353 (1987) ) .
Sin embargo, no se ha confirmado la existencia de paralelismos funcionales entre estas proteínas. Por un lado, a diferencia de la Tf y la Lf, la MTf existe tanto en forma unida a la membrana como en forma soluble en suero. Además, en contraste con la Tf y la Lf, no se ha identificado receptor celular para la MTf. Se sabe que la Tf soluble en suero es absorbida por las células en un proceso dependiente de la energía mediado por el receptor de la transferrina (Tf-R) (Cook, y cols., Annu. Rev. Med., 44:63-74) (1993) ) . Asimismo, es probable que la internalización de la Lf esté mediada por un proceso mediado por receptor (Fillebeen, y cols., J. Biol. Chem., 274 (11) :701-7017 (1999) ) . Dos receptores conocidos para la Lf son LRP-1 y RAGE, aunque podrían existir otros (Melinger, y cols., FEBS Letters, 360:70-74 (1995) ; Schmidt, J. Biol. Chem., 269 (13) :9882-9888 (1994) .
Con respecto al sistema nervioso central (por ejemplo, cerebro, médula espinal) , existen al menos tres formas de 65 mejorar la administración: inyección, permeabilización de la BHE y modificación del fármaco. La inyección directa implica la inyección del fármaco en el tejido cerebral, evitando por completo la vasculatura. Este método adolece
principalmente del riesgo de complicaciones (infección, daño tisular) relacionado con las inyecciones intracraneales. Este riesgo se agrava cuando se considera en el contexto de una pauta de tratamiento regular aplicada a lo largo de la vida del paciente. También resulta difícil, usando un número limitado de inyecciones en un único sitio, lograr la misma penetración que los vasos sanguíneos (y por lo tanto, potencialmente, los fármacos) tienen en todo el cerebro.
El segundo método consiste en alterar la BHE de forma no específica mediante la inyección concomitante de fármacos por vía intravenosa. La permeabilización de la BHE se lleva a cabo químicamente. Este método adolece de una falta de especificidad. Todos aquellos componentes de la sangre que quedan necesariamente excluidos por la BHE entrarán en el cerebro junto con el fármaco. En estas condiciones, el cerebro se vuelve vulnerable y es previsible que se produzcan daños en el transcurso de una pauta de tratamiento durante toda la vida.
El tercer medio de aumento de la disponibilidad cerebral del fármaco transportado por la sangre implica la funcionalización específica del fármaco con radicales que faciliten el transporte a través de una BHE no alterada.
Este método tiene las ventajas de lograr una infiltración específica en la BHE y de una cómoda administración intravenosa. En la patente de EE.UU. nº 6455494 se muestra un método para aumentar la capacidad de un agente terapéutico para cruzar la barrera hematoencefálica, y se describe el uso de p97 como vehículo para administrar un fármaco terapéutico a través de la barrera hematoencefálica.
La p97 (melanotransferrina) es una proteína humana natural. La p97 fue descubierta y caracterizada como un marcador de la superficie celular del melanoma humano (antígeno asociado al melanoma) , pero más recientemente se ha encontrado en otros tipos de tumores, así como en el cerebro humano normal y en el tejido hepático, en cantidades traza en otros tejidos del cuerpo y en el suero. Se desconoce la función de p97 en el cuerpo, pero a juzgar por su estructura y propiedades de unión, que se cree que está implicada en el transporte de iones metálicos (por ejemplo, hierro) hasta las células. Jefferies, y cols. han estado trabajando con la p97 desde 1992 (patente de EE.UU. nº 5981194) . Estas investigaciones se han centrado en la p97 como marcador de diagnóstico para la enfermedad de Alzheimer (EA) . Synapse ha desarrollado una prueba en sangre (suero) para la EA que se basa en el descubrimiento de que la concentración sérica de la p97 aumenta a medida que avanza la enfermedad. Durante el desarrollo de esta prueba, se descubrió que la p97 se transporta de forma activa desde la sangre hacia el tejido cerebral de los individuos normales. Este descubrimiento fue el impulso para el desarrollo de la p97 como posible sistema de transporte para administrar moléculas desde la sangre, a través de la BHE, para llegar hasta los líquidos intersticiales cerebrales.
El acontecimiento clave para la administración... [Seguir leyendo]
Reivindicaciones:
1. Una composición farmacéutica para uso en el tratamiento de un sujeto que tiene una enfermedad de almacenamiento lisosómico; comprendiendo dicha composición una molécula de p97 unida covalentemente a una proteína cuya deficiencia provoca la enfermedad; en donde la proteína está seleccionada de entre el grupo que consiste en α-L-iduronidasa, iduronato-2-sulfatasa, heparan-N-sulfatasa, α-N-acetilglucosaminidasa, arilsulfatasa A, galactosilceramidasa, α-glucosidasa ácida, tioesterasa, hexosaminidasa A, esfingomielinasa ácida y αgalactosidasa; y en donde la composición se administra a un lisosoma en una célula del sujeto.
3. La composición farmacéutica para uso de acuerdo con la reivindicación 1 ó 2, en la que la composición se usa por vía intravenosa. 5. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 4, en la que la molécula de p97 es p97 soluble. 20 6. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en la que la proteína es α-L-iduronidasa 7. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en la que la 25 proteína es iduronato-2-sulfatasa. 8. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en la que la molécula de p97 está unida covalentemente a la proteína por un enlazador extendido. 9. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en la que el conjugado es una proteína de fusión de p97 y de la proteína. 10. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 9, en la que el sujeto sufre manifestaciones neurológicas de la enfermedad. 35 11. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en la que la composición comprende el conjugado en una cantidad terapéuticamente eficaz. 12. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 11, en la que la enfermedad se selecciona entre el grupo compuesto por mucopolisacaridosis I (MPS I) , MPS II, MPS IIIA, MPS IIIB, leucodistrofia metacromática (LDM) , Krabbe, Pompe, CLN2, Tay-Sachs y Niemann-Pick A y B. 13. Un uso de un compuesto que comprende una molécula de p97 unida covalentemente a una proteína cuya deficiencia provoca una enfermedad de almacenamiento lisosómico en la fabricación de un medicamento para el 45 tratamiento de un sujeto que tiene una enfermedad de almacenamiento lisosómico; en donde la proteína se selecciona de entre el grupo que consiste en α-L-iduronidasa, iduronato-2-sulfatasa, heparan-N-sulfatasa, α-Nacetilglucosaminidasa, arilsulfatasa A, galactosilceramidasa, α-glucosidasa ácida, tioesterasa, hexosaminidasa A, esfingomielinasa ácida y α-galactosidasa; y en donde el medicamento se administra a un lisosoma en una célula del sujeto. 14. El método de la reivindicación 13, en el que la proteína es α-L-iduronidasa. 15. El uso de la reivindicación 13 ó 14, en el que la molécula de p97 es p97 soluble. 16. El uso de una cualquiera de las reivindicaciones 13 a 15, en el que el compuesto es una proteína de fusión de la molécula de p97 y la proteína. 17. El uso de acuerdo con una cualquiera de las reivindicaciones 13 a 16, en el que la molécula de p97 está unida covalentemente a la proteína por un enlazador extendido. 60 18. El uso de acuerdo con una cualquiera de las reivindicaciones 13 a 17, en el que el conjugado es capaz de pasar a través de la barrera hematoencefálica y entrar en un lisosoma de una célula del sistema nervioso central. 19. Un método de detección de la actividad terapéutica de un compuesto en el tratamiento de una enfermedad de 65 almacenamiento lisosómico, comprendiendo dicho método: poner en contacto una célula que tiene un lisosoma in vitro con el compuesto, en donde el compuesto comprende p97 unida covalentemente a una proteína deficiente en una enfermedad de almacenamiento lisosómico; en donde la proteína se selecciona entre el grupo formado por α-L-iduronidasa, iduronato-2-sulfatasa, heparan-N-sulfatasa, α-N acetilglucosaminidasa, arilsulfatasa A, galactosilceramidasa, α-glucosidasa ácida, tioesterasa, hexosaminidasa A, esfingomielinasa ácida y α-galactosidasa; y el seguimiento de la administración del compuesto al lisosoma. 20. El método de acuerdo con la reivindicación 19, en el que el compuesto está marcado y el seguimiento detecta el marcador. 10 21. El método de acuerdo con la reivindicación 19, en el que la célula es humana. 22. El método de una cualquiera de las reivindicaciones 19 a 21, en el que la célula es deficiente en la proteína. 23. El método de acuerdo con una cualquiera de las reivindicaciones 19 a 22, en el que el seguimiento se realiza determinando el efecto del compuesto sobre el material de almacenamiento lisosómico. 24. Una composición farmacéutica para uso en la administración de una proteína a una célula en un sujeto que tiene una enfermedad de almacenamiento lisosómico; comprendiendo dicha composición una cantidad terapéuticamente 20 eficaz de un compuesto que comprende una molécula de p97 unida covalentemente a una proteína cuya deficiencia provoca una enfermedad de almacenamiento lisosómico y un excipiente farmacéuticamente aceptable; en donde la proteína está seleccionada de entre el grupo formado por α-L-iduronidasa, iduronato-2-sulfatasa, heparan-Nsulfatasa, α-N-acetilglucosaminidasa, arilsulfatasa A, galactosilceramidasa, α-glucosidasa ácida, tioesterasa, hexosaminidasa A, esfingomielinasa ácida y α-galactosidasa; y en donde el compuesto se administra a un lisosoma en una célula del sujeto. 25. La composición de acuerdo con la reivindicación 24, en la que el sujeto sufre manifestaciones neurológicas de la enfermedad. 2. La composición farmacéutica para uso de acuerdo con la reivindicación 1, en la que el sujeto es humano.
4. La composición farmacéutica para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en la que la molécula de p97 es p97 humana.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
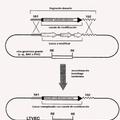 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]