Inhibición de la metástasis tumoral por anticuerpos anti neuropilina 2.
Un anticuerpo anti Nrp2B o fragmento de anticuerpo anti Nrp2B biológicamente activo,
en donde el anticuerpo o fragmento de anticuerpo comprende:
(a) la secuencia de región variable de cadena ligera:
y la secuencia de región variable de cadena pesada:
del anticuerpo YW68.4.2 cuya secuencia de aminoácidos se muestra en la Figura 10A; o
(b) la secuencia de región variable de cadena ligera:
y la secuencia de dominio variable de cadena pesada
: del anticuerpo YW68.4.2.36 cuya secuencia de aminoácidos se muestran en la Figura 10B.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/069179.
Solicitante: GENENTECH, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1 DNA WAY SOUTH SAN FRANCISCO, CA 94080 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LIANG,Wei-ching, WU,Yan, WATTS,RYAN JEFFERSON, BAGRI,ANIL DURGADAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
PDF original: ES-2469743_T3.pdf
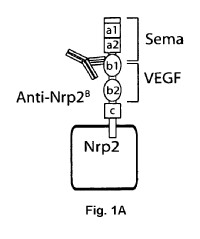
Fragmento de la descripción:
Inhibiciïn de la metïstasis tumoral por anticuerpos anti neuropilina 2.
Campo de la invenciïn La presente invenciïn se refiere a antagonistas de neuropilina 2 (Nrp2) , especialmente anticuerpos anti Nrp2, y su uso en la prevenciïn y tratamiento de metïstasis tumoral.
Antecedentes de la invenciïn Se ha establecido bien ahora que la angiogïnesis estï implicada en la patogïnesis de diversos trastornos. Estos incluyen tumores sïlidos y metïstasis, aterosclerosis, fibroplasia retrolental, hemangiomas, inflamaciïn crïnica, enfermedades neovasculares intraoculares tales como retinopatïas proliferativas, por ejemplo, retinopatïa diabïtica, degeneraciïn macular relacionada con la edad (AMD) , glaucoma neovascular, rechazo inmunitario de tejido corneal trasplantado y otros tejidos, artritis reumatoide y psoriasis. Folkman et al., J. Biol. Chem., 267: 10931-10934 (1992) ; Klagsbrun et al., Annu. Rev. Physiol. 53: 217-239 (1991) ; y Garner A., “Vascular diseases”, En: Pathobiology of Ocular Disease. A Dynamic Approach, Garner A., Klintworth GK, eds., 2ï Ediciïn (Marcel Dekker, NY, 1994) , pp 1625-1710.
En el caso del crecimiento tumoral, la angiogïnesis parece ser crucial para la transiciïn de hiperplasia a neoplasia, y para proporcionar alimento para el crecimiento o metïstasis del tumor. Folkman et al., Nature 339: 58 (1989) . La neovascularizaciïn permite que las cïlulas tumorales adquieran una ventaja de crecimiento y autonomïa proliferativa en comparaciïn con las cïlulas normales. Un tumor habitualmente comienza como una ïnica cïlula aberrante que puede proliferar solamente hasta un tamaïo de unos pocos milïmetros cïbicos debido a la distancia de los lechos capilares disponibles, y puede permanecer “durmiente” sin crecimiento adicional y diseminaciïn durante un periodo de tiempo largo. Algunas cïlulas tumorales cambian despuïs al fenotipo angiogïnico para activar cïlulas endoteliales que proliferan y maduran a nuevos vasos sanguïneos capilares. Estos vasos sanguïneos de nueva formaciïn no solamente permiten el crecimiento continuado del tumor primario, sino tambiïn la diseminaciïn y recolonizaciïn de cïlulas tumorales metastïsicas. En consecuencia, se ha observado una correlaciïn entre la densidad de microvasos en secciones tumorales y la supervivencia del paciente en cïncer de mama asï como en varios otros tumores. Weidner et al., N. Engl. J. Med 324: 1-6 (1991) ; Horak et al., Lancet 340: 1120-1124 (1992) ; Macchiarini et al., Lancet 340: 145-146 (1992) . Los mecanismos precisos que controlan el cambio angiogïnico no se entienden bien, pero se cree que la neovascularizaciïn de la masa tumoral resulta del equilibrio neto de una multitud de estimuladores e inhibidores de la angiogïnesis (Folkman Nat Med 1 (1) : 27-31 (1995) ) .
Se acepta actualmente que las metïstasis son responsables de la amplia mayorïa, estimado en el 90 %, de las muertes de tumores sïlidos (Gupta y Massague, Cell 127, 679-695 (2006) ) . El complejo proceso de metïstasis implica una serie de etapas distintas que incluyen la separaciïn de cïlulas tumorales del tumor primario, intravasaciïn de cïlulas tumorales en vasos linfïticos o sanguïneos, y extravasaciïn y crecimiento de cïlulas tumorales en sitios secundarios. El anïlisis de ganglios linfïticos regionales en muchos tipos tumorales sugiere que la vasculatura linfïtica es una vïa importante para la diseminaciïn de cïnceres humanos. Ademïs, en casi todos los carcinomas, la presencia de cïlulas tumorales en ganglios linfïticos es el factor de pronïstico adverso mïs importante. Aunque se ha pensado previamente que dichas metïstasis implicaban exclusivamente el paso de cïlulas malignas a lo largo de vasos linfïticos preexistentes cerca de los tumores, estudios experimentales e informes clïnico patolïgicos recientes (revisados en Achen et al., Br J Cancer 94 (2006) , 1355-1360 y Nathanson, Cancer 98, 413-423 (2003) ) sugieren que la linfangiogïnesis puede inducirse por tumores sïlidos y pueden promover la propagaciïn tumoral. Estos y otros estudios recientes sugieren que la direcciïn a vasos linfïticos y linfangiogïnesis puede ser una estrategia terapïutica ïtil para restringir el desarrollo de metïstasis de cïncer, lo que tendrïa un beneficio significativo para muchos pacientes.
VEGFC, un miembro de la familia del factor de cïlulas endoteliales vasculares (VEGF) , es uno de los mediadores mejor estudiados del desarrollo linfïtico. Se ha mostrado que la sobreexpresiïn de VEGFC en cïlulas tumorales promueve la linfoangiogïnesis asociada a tumor, dando como resultado metïstasis potenciada a ganglios linfïticos regionales (Karpanen et al., Faseb J20, 1462-1472 (2001) ; Mandriota et al., EMBOJ 20, 672-682 (2001) ; Skobe et al., Not Med 7, 192-198 (200) ) ; Stacker et al., Nat Rev Cancer 2, 573-583 (2002) ; Stacker et al., Faseb J 16, 922-934 (2002) ) . La expresiïn de VEGFC tambiïn se ha correlacionado con linfangiogïnesis asociada a tumor y metïstasis de ganglios linfïticos para varios cïnceres humanos (revisado en Achen et al., 2006. mencionado anteriormente) . Ademïs, se ha mostrado que el bloqueo de la seïalizaciïn mediada por VEGFC suprime la linfangiogïnesis tumoral y la metïstasis de ganglios linfïticos en ratones (Chen et al., Cancer Res 65, 9004-9011 (2005) ; He et al., J. Natl Cancer Inst 94, 8190825 (2002) ; Krishnan et al., Cancer Res 63, 713-722 (2003) ; Lin et al., Cancer Res 65, 69016909 (2005) ) .
Se sabe que el VEGFC se une con al menos dos familias de receptores de superficie celular, los receptores tirosina quinasa de VEGF y los receptores neuropilina (Nrp) .
De los tres receptores de VEGF, VEGFC puede unirse con VEGFR2 y VEGFR3 lo que conduce a dimerizaciïn del receptor (Shinkai et al., J Biol Chem 273, 31283-31288 (1998) ) , activaciïn de quinasa y autofosforilaciïn (Heldin, Cell 80, 213-223 (1995) ; Waltenberger et al., J Biol Chem 269, 26988-26995 (1994) ) . El receptor fosforilado induce la activaciïn de mïltiples sustratos lo que conduce a angiogïnesis y linfangiogïnesis (Ferrara et al., Nat Med 9, 669676 (2003) ) .
La familia de la neuropilina (Nrp) comprende dos proteïnas homïlogas, neuropilina 1 (Nrp1) y neuropilina 2 (Nrp2) . Ademïs de los receptores de VEGF, VEGFC tambiïn se une con Nrp2, que se identificï inicialmente como receptor de semaforina de clase 3 y mediador de la orientaciïn de axones (Favier et al., Blood 108, 1243-1250 (2006) ; Soker et al., J Cell Biochem 85, 357-368 (2002) ) . Mïltiples lïneas de pruebas implican a Nrp2 en el desarrollo de los sistemas vascular y linfïtico. Los mutantes de Nrp2 homocigotos muestran una grave reducciïn de vasos linfïticos pequeïos y capilares de forma prenatal (Yuan et al., Development 129, 4797-4806 (2002) ) . Ademïs, el defecto vascular letal embrionario y drïstico visto en ratones mutantes para Nrp1 homocigotos se potencia por la pïrdida de la funciïn de Nrp2 lo que conduce a letalidad mïs temprana (Takashima et al., Proc Natl Acad Sci USA 99, 36573662 (2002) ) . Sin embargo, el papel de Nrp2 en la modulaciïn de la biologïa vascular y linfïtica del adulto, y mïs especïficamente la metïstasis se desconoce.
Las Nrp tienen dominios intracelulares cortos que no se conoce que tengan ninguna actividad enzimïtica o de seïalizaciïn. Se ha propuesto que las Nrp actïan para potenciar la seïalizaciïn de VEGFR potenciando la uniïn del receptor de VEGF-ligando (Favier et al., 2006, mencionado anteriormente; Soker et al., 2002, mencionado anteriormente) . Adicionalmente, se ha mostrado que sema3F, el ligando de semaforina de Nrp2, modula el comportamiento celular endotelial in vitro e in vivo (Bielenberg et al., J Clin Invest 114, 1260-1271 (2004) ; Favier et al., Blood 1243-1250, (2006) ) . Sin embargo, informes recientes han sugerido una posibilidad alternativa de que las Nrp puedan actuar de forma independiente de los receptores de VEGF o la funciïn de semaforina para modular la migraciïn de cïlulas endoteliales (EC) (Murga et al., Blood 105, 1992-1999 (2005) ; Pan et al., Cancer Cell 11, 53-67 (2007) ; Wang et al., J Biol Chem 278, 48848-48860 (2003) ) .
Los anticuerpos neutralizadores anti VEGF suprimen el crecimiento de diversas lïneas celulares tumorales humanas en ratones desnudos (Kim et al., Nature 362: 841-844 (1993) ; Warren et al., J. Clin. Invest. 95: 1789-1797 (1995) ; Borgstrïm et al., Cancer Res. 56: 4032-4039 (1996) ; Melnyk et al., Cancer Res. 56: 921-924 (1996) ) y tambiïn inhiben la angiogïnesis intraocular en modelos de trastornos retinales isquïmicos. Adamis et al., Arch. Ophthalmol.
114: 66-71 (1996) . Por lo tanto, los anticuerpos monoclonales anti VEGF u otros inhibidores de la acciïn de VEGF son candidatos prometedores para el tratamiento de tumores... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo anti Nrp2B o fragmento de anticuerpo anti Nrp2B biolïgicamente activo, en donde el anticuerpo o fragmento de anticuerpo comprende:
(a) la secuencia de regiïn variable de cadena ligera:
y la secuencia de regiïn variable de cadena pesada:
del anticuerpo YW68.4.2 cuya secuencia de aminoïcidos se muestra en la Figura 10A; o (b) la secuencia de regiïn variable de cadena ligera:
y la secuencia de dominio variable de cadena pesada:
del anticuerpo YW68.4.2.36 cuya secuencia de aminoïcidos se muestran en la Figura 10B.
2. El anticuerpo anti Nrp2B o fragmento de anticuerpo de la reivindicaciïn 1, que comprende las secuencias de regiïn variable de cadenas pesada y ligera del anticuerpo YW68.4.2.36 cuya secuencia de aminoïcidos se muestra en la Figura 10B.
3. El anticuerpo anti Nrp2B o fragmento de anticuerpo de la reivindicaciïn 1, que: 30
(i) comprende el anticuerpo YW68.4.2 cuya secuencia de aminoïcidos se muestra en la Figura 10A o el anticuerpo YW68.4.2.36 cuya secuencia de aminoïcidos se muestra en la Figura 10B; o
(ii) es un fragmento anti Nrp2B biolïgicamente activo del anticuerpo de (i) .
(i) comprende el anticuerpo YW68.4.2.36 cuya secuencia de aminoïcidos se muestra en la Figura 10B; o
(ii) es un fragmento anti Nrp2B biolïgicamente activo del anticuerpo de (i) .
6. El anticuerpo o fragmento de anticuerpo de una cualquiera de las reivindicaciones 1-4, que es biespecïfico.
8. El anticuerpo anti Nrp2B o fragmento de anticuerpo de cualquier reivindicaciïn anterior, que es quimïrico o humanizado.
9. Una composiciïn que comprende el anticuerpo o fragmento de anticuerpo de una cualquiera de las reivindicaciones 1 a 5, en mezcla con un vehïculo farmacïuticamente aceptable.
10. Una composiciïn farmacïutica para la prevenciïn o el tratamiento de metïstasis tumoral que comprende una cantidad eficaz de un anticuerpo anti Nrp2B o fragmento de anticuerpo de una cualquiera de las reivindicaciones 1 a 8, en mezcla con un vehïculo farmacïuticamente aceptable.
11. El anticuerpo anti Nrp2B o fragmento de anticuerpo de una cualquiera de las reivindicaciones 1 a 8, para uso en un mïtodo de tratamiento mïdico en un sujeto mamïfero.
12. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con la reivindicaciïn 11, en donde el sujeto mamïfero es un paciente humano.
13. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con la reivindicaciïn 12 en donde se ha diagnosticado cïncer a dicho paciente humano.
14. El anticuerpo anti Nrp2B o fragmento de anticuerpo de una cualquiera de las reivindicaciones 1 a 8, para uso en un mïtodo para inhibir la linfangiogïnesis tumoral en un sujeto mamïfero portador de tumor.
15. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con la reivindicaciïn 14, en donde sujeto mamïfero es un paciente de cïncer humano.
16. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con la reivindicaciïn 13 o la reivindicaciïn 15, en donde dicho paciente humano ha desarrollado o estï en riesgo de desarrollar metïstasis tumoral.
17. El anticuerpo anti Nrp2B o fragmento de anticuerpo de una cualquiera de las reivindicaciones 1 a 8, para uso en un mïtodo de tratamiento terapïutico, profilïctico o preventivo de metïstasis tumoral en un paciente de cïncer humano.
18. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con una cualquiera de las reivindicaciones 13 o 15 a 17, en donde dicho cïncer se selecciona del grupo que consiste en cïncer de cïlulas escamosas, cïncer de pulmïn de cïlulas pequeïas, cïncer de pulmïn de cïlulas no pequeïas, adenocarcinoma del pulmïn, carcinoma escamoso del pulmïn, cïncer del peritoneo, cïncer hepatocelular, cïncer gïstrico, cïncer gastrointestinal, cïncer pancreïtico, glioblastoma, cïncer del cuello uterino, cïncer ovïrico, cïncer de hïgado, cïncer de vejiga, hepatoma, cïncer de mama, cïncer de colon, cïncer colorrectal, carcinoma endometrial o uterino, carcinoma de glïndulas salivares, cïncer de riïïn o renal, cïncer de hïgado, cïncer de prïstata, cïncer vulvar, cïncer de tiroides, carcinoma hepïtico y diversos tipos de cïncer de cabeza y cuello, linfoma de linfocitos B, leucemia linfocïtica crïnica (CLL) ; leucemia linfoblïstica aguda (ALL) ; leucemia de tricoleucitos; y leucemia mieloblïstica crïnica.
19. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con una cualquiera de las reivindicaciones 16 a 18, en donde dicha metïstasis estï en el sistema linfïtico o en un ïrgano distante.
20. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con una cualquiera de las reivindicaciones 11 a 19, en donde dicho uso comprende ademïs la administraciïn de un anticuerpo antagonista anti VEGF.
21. El anticuerpo anti Nrp2B o fragmento de anticuerpo para uso de acuerdo con la reivindicaciïn 20, en el que dicho anticuerpo anti VEGF es bevacizumab.
Patentes similares o relacionadas:
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Conectores autoinmolativos no lineales y conjugados de los mismos, del 22 de Julio de 2020, de Byondis B.V: Compuesto conector-farmaco con la formula (I) **(Ver fórmula)** o sal, hidrato o solvato farmaceuticamente aceptables del mismo, donde […]