Anticuerpo que sustituye la función del factor VIII de coagulación sanguínea.
Un anticuerpo biespecífico que puede sustituir funcionalmente al factor VIII de coagulación y que presenta la actividad para mejorar la activación del factor X,
que comprende:
un primer dominio que reconoce al factor de coagulación IX y/o al factor de coagulación IX activado; y
un segundo dominio que reconoce al factor de coagulación X, donde
el primer dominio comprende un primer polipéptido que comprende la cadena H de un anticuerpo contra el factor de coagulación IX y/o el factor de coagulación IX activado; el segundo dominio comprende un segundo polipéptido que comprende la cadena H de un anticuerpo contra el factor de coagulación X;
y tanto el primero como el segundo dominio comprenden un tercer polipéptido que comprende una cadena L compartida en común de un anticuerpo contra el factor de coagulación IX, el factor de coagulación IX activado o el factor de coagulación X,
donde el tercer polipéptido comprende un sitio de unión a antígenos que comprende las CDR1, 2 y 3 seleccionadas individualmente de CDR1, 2 y 3 de cada cadena L de dos o más anticuerpos;
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2006/306821.
Solicitante: CHUGAI SEIYAKU KABUSHIKI KAISHA.
Nacionalidad solicitante: Japón.
Dirección: 5-1, UKIMA 5-CHOME, KITA-KU TOKYO, 115-8543 JAPON.
Inventor/es: MIYAZAKI, TARO, SAITO, HIROYUKI, HATTORI, KUNIHIRO, KOJIMA,Tetsuo, SOEDA,Tetsuhiro.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P7/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Antihemorrágicos; Procoagulantes; Hemostáticos; Antifibrinolíticos.
- C07K16/40 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra enzimas.
- C07K16/46 C07K 16/00 […] › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C12N15/09 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
PDF original: ES-2494921_T3.pdf



Fragmento de la descripción:
Anticuerpo que sustituye la función del factor VIII de coagulación sanguínea Campo técnico
La presente invención se refiere a anticuerpos biespecificos que sustituyen funcionalmente al factor VIII de coagulación, un cofactorque mejora las reacciones enzimáticas, a procedimientos para producir dichos anticuerpos y a composiciones farmacéuticas que comprenden dicho anticuerpo como ingrediente activo.
Técnica antecedente
Los anticuerpos son altamente estables en la sangre y tienen una antigenicidad baja; por consiguiente, han atraído mucha atención como farmacéuticos. Los anticuerpos biespecificos, es decir, anticuerpos que reconocen dos tipos de antígenos simultáneamente, se encuentran entre dichos anticuerpos. Los anticuerpos biespecificos han sido propuestos durante algún tiempo. No obstante, a la fecha, los únicos anticuerpos biespecificos informados en la bibliografía son aquellos en los que dos tipos de sitios de unión a antígenos simplemente se encuentran unidos, como los utilizados para redirigir las células NK, los macrófagos y las células T (documento 3 que no es patente). Por ejemplo, el MDX-21, un anticuerpo que actualmente se encuentra en investigación clínica, es un anticuerpo biespecífico que simplemente redirecciona los monocitos que expresan FcyRI y similares contra las células cancerígenas que expresan HER-2/neu. Por consiguiente, hasta ahora, no hubo ejemplos de anticuerpos biespecificos utilizados como sustitutos funcionales para cofactores que mejoran las reacciones enzimáticas.
Un cofactor es una molécula auxiliar necesaria para que una enzima sea funcional y un componente proteico o no proteico que se une a la enzima y que es necesario para su actividad catalítica. Los ejemplos de cofactores proteicos incluyen, a modo no taxativo, factor VIII de coagulación (F. VIII), factor VIII activado de coagulación (F. Villa), factor V de coagulación (F. V), factor V activado de coagulación (F. Va), factor tisular (TF), trombomodulina (TM), proteína S (PS), proteína Z (PZ), heparina, complemento C4b, factor regulador Fl complementario, cofactor proteico de membrana (MCP) y receptor 1 complementario (CR1).
Entre estos, el F. Vlll/F. Villa es un cofactor necesario para la expresión suficiente de la actividad del factor de
coagulación IX activado (F. IXa). Mediante el uso de ensayos cromogénicos, Scheiflinger F, et al. descubrió que un
cierto tipo de anticuerpo anti-F. IX/F. IXa puede mejorar la activación del factor de coagulación X (F. X) mediante F. IXa (documento de patente 1). No obstante, las mediciones de recuperación de coagulación en plasma con carente de F. VIII mostraron que no se observó recuperación de coagulación cuando se agregó este anticuerpo solo; en su lugar, la recuperación de coagulación se observó únicamente cuando F. IXa se agregó exógenamente.
El F. Villa es conocido por interactuar no solamente con el F. IXa sino también con el F. X (documentos 1 y 2 que no son patente). A este respecto, el anticuerpo de Scheiflinger F. et al. no sustituyó de forma suficiente a nivel funcional al F. Vlll/F. Villa, y su actividad también se considera insuficiente. [Documento de patente 1]WO 1/19992 [documento 1 que no es patente] Mertens K et al., Thromb. Haemost., 1999, Vol. 82, páginas 29 a 217
[documento 2 que no es patente] Lapan KA et al., Thromb. Haemost., 1998, Vol. 8, páginas 418 a 422
[documento 3 que no es patente] Segal DM et al., Journal of Immunological Methods, 21, Vol. 248, páginas 1 a 6.
Descripción de la invención
[Problemas que deben ser resueltos con la invención]
Un objetivo de la presente invención es proporcionar anticuerpos biespecificos que sustituyan funcionalmente al factorVIII de coagulación, un cofactorque mejora las reacciones enzimáticas.
[Medios para resolver los problemas]
Tras una minuciosa investigación, los presentes inventores descubrieron varios anticuerpos biespecificos que se unen específicamente al F. IX/F. IXa y al F. X, y que sustituyen funcionalmente al F. Villa, más específicamente, tienen funciones de cofactor para mejorar la activación del F. X con F. IXa.
De estos anticuerpos, los presentes inventores seleccionaron además un anticuerpo (A44/B26) que redujo el tiempo de coagulación en 5 segundos o más en comparación con el observado cuando no se agregó ningún anticuerpo a un sistema de medición de tiempo de coagulación que utiliza suero humano carente de F. VIII. Los presentes inventores posteriormente utilizaron este anticuerpo para producir un anticuerpo de cadena L compartida en común mediante la unión de sus cadenas H con las cadenas L de A44. Como resultado, los presentes inventores mostraron que el anticuerpo de cadena L compartida en común puede producirse con A4L; no obstante, la actividad de este anticuerpo se vio atenuada en comparación con la actividad del anticuerpo biespecífico original (A44HL-B26HL).
Además, las CDR derivadas de la cadena L de A44 y la cadena L de B26 se combinaron con el marco (Fr) derivado de la cadena L de A44 para producir cadenas L híbridas y estas cadenas L se utilizaron para producir anticuerpos compartidos en común cuyo propósito es la recuperación de la actividad del F. VIII. Como resultado, cuando la
combinación de las CDR1, 2 y 3 fue BBA(G) (CDR1, 2 y 3 fueron CDR derivada de la cadena L de B26, CDR derivada de la cadena L de B26 y CDR derivada de la cadena L de A44, respectivamente), la actividad del F. VIII aumentó de forma significativa en comparación con la actividad observada con A44/B26. Además, el tiempo de coagulación se redujo en 7 segundos o más en comparación con el observado cuando no se agregó ningún anticuerpo. Este anticuerpo no atenuó las funciones del F. VIII (,1; 1 U/mL) y de hecho, actuó de forma aditiva. Además, cuando las CDR1, 2 y 3 fueron ABA(G) o BBA(G), sus tiempos de coagulación se redujeron en 6 segundos o más en comparación con los observados cuando no se agregó ningún anticuerpo.
Cuando las cadenas H de los anticuerpos A5 y A69, que son altamente homólogos a A44, se combinaron con B26H y las cadenas L híbridas mencionadas anteriormente y se evaluaron sus actividades, se obtuvieron anticuerpos que tenían actividades superiores a las con A44H. Asimismo, cuando se produjeron las cadenas L híbridas mediante la combinación de las CDR de A44L, B26L, A5L y A69L y se examinaron sus actividades, se obtuvieron anticuerpos altamente activos; no obstante, ninguno superó la actividad de la cadena L híbrida derivada de A44/B26 (BBA(G)).
Cuando se combinaron varias cadenas L híbridas (BBA, aAA, AAa, ABa, BBa, aBA, BAA, BAa y ABA)) con A69H y B26H y se evaluaron sus actividades, se obtuvieron anticuerpos altamente activos y particularmente en el caso de la combinación BBA o BBa, el tiempo de coagulación se redujo en 8 segundos o más en comparación con el observado cuando no se agregó ningún anticuerpo.
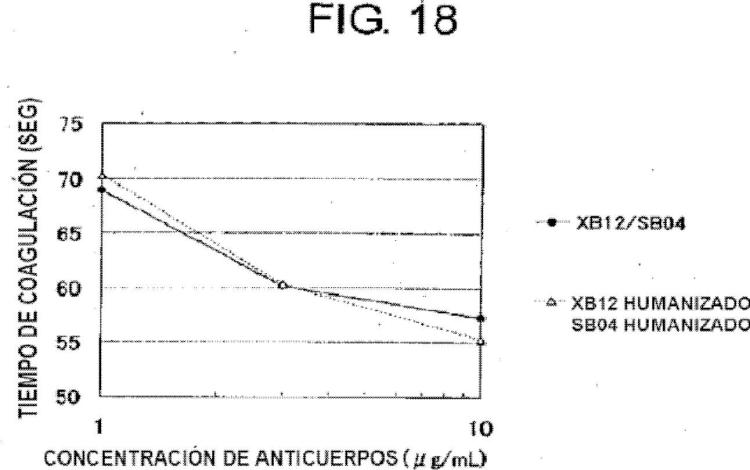
Cuando la humanización de estos anticuerpos se examinó de forma adicional, se logró una actividad igual a la de los anticuerpos originales mediante la combinación de (1) A69H humanizado, (2) B26H humanizado y (3) cadenas L híbridas humanizadas.
Por lo tanto, como se describe anteriormente, los presentes inventores lograron producir anticuerpos biespecíficos altamente activos que sustituyen a nivel funcional al factor VIII de coagulación y de ese modo completaron la presente invención.
La presente invención también proporciona procedimientos para recuperar o aumentar las actividades de estos anticuerpos, que disminuyeron debido a las cadenas L compartidas en común de cada anticuerpo.
Es decir, la presente invención se refiere a anticuerpos biespecíficos que sustituyen funcionalmente al factor VIII de coagulación, un cofactorque mejora las reacciones enzimáticas, a procedimientos para producir dichos anticuerpos y a procedimientos para recuperar o aumentar sus actividades que disminuyeron debido a las cadenas L compartidas en común de cada anticuerpo. Más específicamente, la presente invención proporciona:
[1] Un anticuerpo biespecífico que puede sustituir funcionalmente al factor VIII de coagulación y que presenta la actividad para mejorar la activación del factor X, que comprende:
un primer dominio que reconoce al factor de coagulación IX y/o al factor de coagulación IX activado; y un segundo dominio que reconoce al factor de coagulación X, donde
el primer dominio comprende un primer polipéptido que comprende la cadena H de un anticuerpo contra el factor de coagulación IX y/o el factor de coagulación IX activado; el segundo dominio comprende un segundo polipéptido que comprende la cadena H de un anticuerpo contra el factor de coagulación X;
y tanto... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo biespecífico que puede sustituir funcionalmente al factor VIII de coagulación y que presenta la actividad para mejorar la activación del factor X, que comprende:
un primer dominio que reconoce al factor de coagulación IX y/o al factor de coagulación IX activado; y un segundo dominio que reconoce al factor de coagulación X, donde
el primer dominio comprende un primer polipéptido que comprende la cadena H de un anticuerpo contra el factor de coagulación IX y/o el factor de coagulación IX activado; el segundo dominio comprende un segundo polipéptido que comprende la cadena H de un anticuerpo contra el factor de coagulación X;
y tanto el primero como el segundo dominio comprenden un tercer polipéptido que comprende una cadena L compartida en común de un anticuerpo contra el factor de coagulación IX, el factor de coagulación IX activado o el factor de coagulación X,
donde el tercer polipéptido comprende un sitio de unión a antígenos que comprende las CDR1, 2 y 3 seleccionadas individualmente de CDR1,2 y 3 de cada cadena L de dos o más anticuerpos;
2. El anticuerpo biespecífico de la reivindicación 1, donde el primer polipéptido comprende un sitio de unión a antígenos que comprende las secuencias de aminoácidos de las CDR de (a1), (a2), o (a3) y el segundo polipéptido comprende un sitio de unión a antígenos que comprende las secuencias de aminoácidos de (b), donde:
(a1) Las CDR1, 2 y 3 de cadena H comprenden las secuencias de aminoácidos de las SEQ ID NO: 3, 5 y 7, respectivamente;
(a2)Las CDR1, 2 y 3 de cadena H comprenden las secuencias de aminoácidos de las SEQ ID NO: 21, 5 y 22, respectivamente;
(a3)Las CDR1, 2 y 3 de cadena H comprenden las secuencias de aminoácidos de las SEQ ID NO: 16, 17 y 18, respectivamente; y
(b) Las CDR1, 2 y 3 de cadena H comprenden las secuencias de aminoácidos de las SEQ ID NO: 26, 28 y 3, respectivamente.
3. El anticuerpo biespecífico de la reivindicación 1 que reconoce al factor de coagulación IX y/o al factor de coagulación IX activado y al factor de coagulación X, donde la función sustitutiva del factor VIII de coagulación es reducir el tiempo de coagulación en 5 segundos o más en comparación con el tiempo de coagulación observado en la ausencia de un anticuerpo en una prueba de tiempo de tromboplastina parcial (APTT) que implica el calentamiento de una solución mixta de 5 pL, de solución de anticuerpos, 5 pL de plasma carente de F. VIII (Biomerieux) y 5 pL de reactivo de APTT (Dade Behring) a 37°C durante 3 minutos, mediante la adición de 5 pL de CaCÍ2 2 mM a la solución mixta y después la medición del tiempo de coagulación.
4. Una composición que comprende el anticuerpo de cualquiera de las reivindicaciones 1 a 3 y un vehículo farmacéuticamente aceptable.
5. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable y el anticuerpo de cualquiera de las reivindicaciones 1 a 3, para su uso en la prevención y/o tratamiento del sangrado, una enfermedad que acompañe al sangrado, o una enfermedad causada por el sangrado, donde el sangrado, la enfermedad que acompaña al sangrado, o la enfermedad causada por el sangrado es una enfermedad que se desarrolla y/o progresa debido a la reducción o carencia de actividad del factor VIII de coagulación y/o del factor VIII activado de coagulación.
6. El uso del anticuerpo de cualquiera de las reivindicaciones 1 a 3, para producir una composición farmacéutica que contenga un vehículo farmacéuticamente aceptable para prevenir y/o tratar el sangrado, una enfermedad que acompañe al sangrado, o una enfermedad causada por el sangrado, donde el sangrado, la enfermedad que acompaña al sangrado, o la enfermedad causada por el sangrado es una enfermedad que se desarrolla y/o progresa debido a la reducción o carencia de actividad del factor VIII de coagulación y/o del factor VIII activado de coagulación.
7. La composición para el uso de la reivindicación 5 o el uso de la reivindicación 6, donde la enfermedad que se desarrolla y/o progresa debido a la reducción o carencia de actividad del factor VIII de coagulación y/o del factor VIII activado de coagulación es hemofilia A.
8. La composición para el uso de la reivindicación 5 o el uso de la reivindicación 6, donde la enfermedad que se desarrolla y/o progresa debido a la reducción o carencia de actividad del factor VIII de coagulación y/o del factor VIII
activado de coagulación es una enfermedad que implica la aparición de un inhibidor contra el factor VIII de coagulación y/o el factor VIII activado de coagulación.
9. La composición para el uso de la reivindicación 5 o el uso de la reivindicación 6, donde la enfermedad que se desarrolla y/o progresa debido a la reducción o carencia de actividad del factor VIII de coagulación y/o del factor VIII
activado de coagulación es hemofilia adquirida.
1. La composición para el uso de la reivindicación 5 o el uso de la reivindicación 6, donde la enfermedad que se desarrolla y/o progresa debido a la reducción en la actividad del factor VIII de coagulación y/o del factor VIII activado de coagulación es la enfermedad de von Willebrand.
11. Un kit que comprende al menos el anticuerpo de cualquiera de las reivindicaciones 1 a 3 o la composición de la
reivindicación 4.
12. El kit de la reivindicación 11 que comprende además el factor VIII de coagulación.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]
Biblioteca de péptidos y su uso, del 8 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Una biblioteca de péptidos que comprende una pluralidad de péptidos diferentes en la que los péptidos comprenden cada uno una secuencia de aminoácidos […]
Producción de vectores de expresión y selección de células de alta capacidad de procesamiento, del 8 de Julio de 2020, de Kymab Limited: Un método para producir células que codifican un repertorio de anticuerpos que comprende cadenas pesadas y cadenas ligeras de anticuerpo cognadas, comprendiendo dicho […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Anticuerpo anti-Notch 4 humano, del 1 de Julio de 2020, de EISAI R&D MANAGEMENT CO., LTD: Un anticuerpo anti-Notch4 o un fragmento de unión a Notch4 de este, donde dicho anticuerpo o un fragmento de unión a Notch4 de este comprende cadenas pesadas y ligeras y […]
Vacuna de ADN contra pseudotuberculosis en peces marinos, del 1 de Julio de 2020, de NATIONAL UNIVERSITY CORPORATION TOKYO UNIVERSITY OF MARINE SCIENCE AND TECHNOLOGY: Una vacuna de ADN para peces, caracterizada por: - impartir inmunidad contra la pseudotuberculosis causada por Photobacterium damselae subsp. piscicida - que comprende, […]