Vectores víricos recombinantes para la prevención y la protección contra la infección por alfavirus.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2008/000343.
Solicitante: HER MAJESTY THE QUEEN IN RIGHT OF CANADA AS REPRESENTED BY THE MINISTER OF NATIONAL DEFENCE.
Nacionalidad solicitante: Canadá.
Dirección: 305 RIDEAU STREET OTTAWA, ON K1A 0K2 CANADA.
Inventor/es: WU,JOSH QIAOHUA, NAGATA,LESLIE P.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/76 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Virus; Partículas subvirales; Bacteriófagos.
- A61K38/21 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Interferones.
- A61K39/12 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos virales.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- A61P31/14 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para virus ARN.
- A61P37/04 A61P […] › A61P 37/00 Medicamentos para el tratamiento de problemas inmunológicos o alérgicos. › Inmunoestimulantes.
PDF original: ES-2439954_T3.pdf
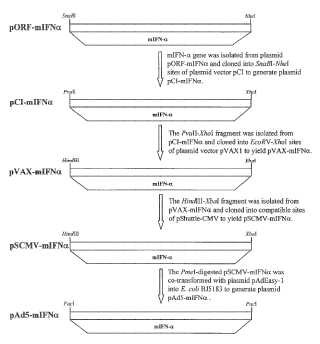
Fragmento de la descripción:
Vectores víricos recombinantes para la prevención y la protección contra la infección por alfavirus La presente solicitud reivindica los beneficios de prioridad de la solicitud de patente provisional de Estados Unidos Nº 60/902.957 presentada el 23 de febrero de 2007.
CAMPO DE LA INVENCIÓN
La presente invención se refiere a vectores víricos recombinantes y a vacunas para usar en un procedimiento de protección después de la exposición frente a la infección por alfavirus.
ANTECEDENTES DE LA INVENCIÓN
Las encefalitis inducidas por alfavirus están provocadas por virus de la encefalitis equina de Venezuela (VEEV) , oriental (EEEV) y occidental (WEEV) (Griffin, 2001) . Esta enfermedad se caracteriza por fiebre, cefalea persistente, confusión, agitación, dificultad al caminar y convulsiones. En casos graves, pueden acontecer lesiones neurológicas persistentes y la muerte. El VEEV, el EEEV y el WEEV provocan encefalitis en seres humanos con tasas de letalidad diferentes. El EEEV es el más virulento con tasas de letalidad del 30 % al 40 %. En casos mortales, los pacientes mueren habitualmente dentro de un periodo de 2 a 10 días después de la aparición de la encefalitis. En comparación con el EEEV, el WEEV parece ser menos virulento con tasas de letalidad del 10 %. La encefalitis mortal aparece a menudo en niños de pecho y niños pequeños. El VEEV provoca habitualmente una enfermedad de incapacitación aguda con fiebre, escalofríos, cefaleas, dolor muscular, diarrea y vómitos. La encefalitis aparece habitualmente en niños con una tasa de letalidad inferior al 1 %. Aparte de las encefalitis mortales en seres humanos, el VEEV, el EEEV y el WEEV también provocan brotes de la enfermedad en equinos y otros animales domésticos con tasas de letalidad altas. Por lo tanto, estos virus son patógenos emergentes y reemergentes importantes en medicina y veterinaria.
La estructura de alfavirus consiste en una cubierta proteica denominada envoltura, una cápside y dentro de la cápside un genoma de ARN monocatenario de sentido positivo (Schlesinger y Schlesinger, 2001) . Los dos tercios 5' del genoma de ARN vírico codifican las proteínas no estructurales requeridas para la transcripción y la replicación de los virus. El tercio 3' del genoma vírico codifica las proteínas de la cápside y la envoltura. Las proteínas de la envoltura se codifican mediante un ARNm subgenómico y se derivan mediante la escisión proteolítica del polipéptido E3-E2-6K-E1 en las proteínas E2 y E1 (Strauss y Strauss, 1994) . La proteína E2 se une a E1 para formar los picos sobre la superficie del virión. Las proteínas E2 y E1 de alfavirus desencadenan respuestas inmunitarias en el huésped frente a los virus (Das y col., 2004; Hodgson, Ludwig y Smith, 1999; Mathews y Roehrig, 1982) .
El VEEV, el EEEV y el WEEV se trasmiten por mosquitos. Los brotes naturales de la enfermedad aparecen cuando los mosquitos que portan los virus pican seres humanos o animales domésticos. No existen trasmisiones de ser humano a ser humano de los virus. Por lo tanto, los seres humanos se consideran huéspedes finales. Los brotes de encefalitis inducidas por alfavirus pueden tener un efecto enorme en la salud humana. Por ejemplo, un brote de VEEV en Venezuela y Colombia en 1995 causó más de 75.000 casos con 300 muertes comunicadas (Weaver y col., 1996) . Aproximadamente 1.000 casos en seres humanos se registraron en 1941 en el mayor brote de WEEV que ha tenido lugar en Canadá occidental (Reisen y Monath, 1989) .
Aparte de brotes naturales, el VEEV, el EEEV y el WEEV son agentes potenciales de guerra biológica y terrorismo biológico debido a que son muy infecciosos mediante trasmisión en aerosol. Por ejemplo, solo 10 a 100 del VEEV en aerosol son suficientes para provocar una infección y se ha informado de al menos 150 casos en seres humanos de infecciones adquiridas en laboratorio (Sidwell y Smee, 2003) . Los Centros para el Control y la Prevención de Enfermedades de Estados Unidos han clasificado el VEEV, el EEEV y el WEEV como agentes de terrorismo biológico de categoría "B".
Actualmente no existen vacunas, fármacos antivíricos o productos terapéuticos para la prevención rápida antes de la exposición o la protección después de la exposición frente a encefalitis inducida por alfavirus. Para la prevención antes de la exposición se ha desarrollado una vacuna de VEEV atenuados vivos, denominada TC-83. La vacuna protege operarios de laboratorio de la infección por VEEV. No obstante, del 15 % al 30 % de los receptores de la vacuna desarrollan fiebre, malestar y cefalea y estos efectos secundarios son tan graves que se requiere descanso en cama en aproximadamente la mitad de los receptores de la vacuna (Hoke, 2005) . Las vacunas de EEEV y WEEV muertos con estatus de nuevo fármaco en investigación (IND) están disponibles solo para operarios de laboratorio con riesgo a exposición a estos virus. Sin embargo, para ser eficaces, estas vacunas de EEEV y WEEV requieren múltiples inyecciones y refuerzos anuales. Por lo tanto, se necesitan vacunas mejoradas para la prevención rápida antes de la exposición de encefatilis inducidas por alfavirus.
Debido a que no hay disponibilidad de ningún fármaco o producto terapéutico para la protección después de la exposición frente a encefalitis inducidas por alfavirus, el tratamiento se enfoca en aliviar síntomas clínicos usando procedimientos antihipertérmicos para fiebre y fármacos anticonvulsivos.
Se han propuesto varias estrategias para la protección después de la exposición frente a encefalitis inducidas por alfavirus. La primera es el uso de anticuerpos monoclonales (mAb) de ratón que neutralizan alfavirus. Dichos mAb protegieron aproximadamente el 50 % de ratones frente a la infección por VEEV cuando se les administró 24 h después de la exposición por vía aérea al VEEV virulento (Phillpotts, 2006; Phillpotts, Jones y Howard, 2002) . Debido a que los mAb de ratón son muy inmunógenos en seres humanos y no son adecuados para uso humano, estos mAb de ratón se humanizan reemplazando gran parte de la secuencia de aminoácidos de mAb de ratón por los de seres humanos. El noventa por ciento de los ratones infectados por VEEV se curaron después de que se les administró los mAb humanizados dentro de un periodo de 1 h después de la exposición a VEEV y el 75 % se curaron cuando se les administró los mAb humanizados 24 horas después de la exposición al virus (Hunt y col., 2006) . Sin embargo, una desventaja de usar mAb para la protección después de la exposición contra encefalitis inducida por alfavirus es que se requiere una cantidad grande de mAb purificado. Por ejemplo, se necesitan hasta 4 mg/kg de mAb para proteger el 50 % de ratones de la infección por VEEV (Phillpotts, Jones y Howard, 2002) . Aunque se han desarrollado mAb contra el WEEV (documento de patente de Estados Unidos Nº 6.812.329) (Long y col., 2000a; Long y col., 2000b; Yamamoto y col., 1985) , no existen informes con respecto a la protección con los mismos de animales frente a la infección por WEEV.
Otra estrategia para la protección después de la exposición frente a encefalitis inducida por alfavirus es el uso de interferón alfa (IFN-α) . El IFN-α se produce por parte de células inmediatamente después de la infección por virus. Inhibe la replicación de un espectro amplio de virus induciendo células para sintetizar diversas proteínas antivíricas. La solicitud de patente de Estados Unidos Nº 11/231.433 (número de publicación US2006/0024270) divulga procedimientos para tratar pacientes con encefalitis víricas mediante la inyección de IFN-α. En comparación con pacientes que no recibieron IFN-α, pacientes que recibieron IFN-α dio como resultado una función neurológica y una supervivencia significativamente mejoradas. Sin embargo, el uso clínico de IFN-α para encefalitis vírica está limitado por el requerimiento de inyecciones frecuentes (normalmente cada 24 h durante hasta 14 días) con una dosis grande de IFN-α (3 millones de unidades) y toxicidades asociadas con el IFN-α que incluyen un síndrome similar a la gripe con fiebre, malestar y cefalea. El IFN-α conjugado con polietilenglicol (PEG) prolonga la semivida in vivo de IFN-α y su potencia. Por ejemplo, el tratamiento antes de la exposición de ratones con IFN-α conjugado con PEG previno ratones de una exposición por vía subcutánea o en aerosol al VEEV mientras que el tratamiento antes de la exposición con IFN-α no modificado no lo hizo (Grieder y Vogel, 1999; Lukaszewski y Brooks, 2000) . Sin embargo, no existen informes que definan si el IFN-α conjugado con PEG podría proteger ratones de encefalitis después de la exposición a VEEV, WEEV o EEEV.... [Seguir leyendo]
Reivindicaciones:
1. Vector vírico recombinante que contiene una secuencia de ADN que codifica interferón-alfa para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus en el que se inocula a dicho animal dicho vector vírico recombinante en una cantidad eficaz para conferir una respuesta protectora a dicho animal y en el que se inocula también a dicho animal una vacuna que comprende un vector vírico recombinante que contiene una secuencia de ADN que codifica las proteínas estructurales de alfavirus en una cantidad eficaz para conferir una respuesta protectora a dicho animal.
2. Vacuna que comprende un vector vírico recombinante que contiene tanto una secuencia de ADN que codifica interferón-alfa y una secuencia de ADN que codifica las proteínas estructurales de alfavirus para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus, en el que se inocula a dicho animal dicha vacuna en una cantidad eficaz para conferir una respuesta protectora a dicho animal.
3. Vector vírico recombinante según la reivindicación 1 para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus, o vacuna según la reivindicación 2 para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus, en el que dicho vector vírico es un vector de transferencia vírica seleccionado del grupo que consiste en vectores víricos derivados de adenovirus, virus adenoasociados, parvovirus, virus de vacuna, herpesvirus, poxvirus, poliovirus y retrovirus.
4. Vector vírico recombinante según la reivindicación 1 o 3, para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus o vacuna según la reivindicación 2 o 3, para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus para usar en un procedimiento en el que dicho animal susceptible se selecciona del grupo que consiste en ratones, equinos y seres humanos.
5. Vector vírico recombinante según cualquiera de las reivindicaciones 1, 3 y 4 para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus, o vacuna según cualquiera de las reivindicaciones 2, 3 y 4, para usar en un procedimiento de protección después de la exposición de un animal susceptible a la infección por alfavirus en el que dicho alfavirus es el virus de la encefalitis equina de Venezuela (VEEV) , oriental (EEEV) u occidental (WEEV) .
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Ratón nuligénico para Pint que muestra un fenotipo asociado a envejecimiento prematuro, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón cuyo genoma comprende una inactivación de un locus del ARN no codificante largo (ARNlnc) Pint endógeno, en donde la inactivación (i) da como resultado que el […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]