Variantes multiples de protenia NMB 1870 de meningococo.
Una composición inmunogénica de dos proteínas que comprende (a) una sal de aluminio adyuvante;
(b)una primera proteína que comprende una secuencia aminoácida que tiene, al menos, un 85 % de identidad desecuencia respecto a SEC ID Nº 24 y (c) una segunda proteína, que comprende una secuencia aminoácida quetiene, al menos, un 85 % de identidad de secuencia respecto a SEC ID Nº 33; en la que la proteína (b) tiene menosdel 70 % de identidad de secuencia respecto a la proteína (c).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2003/006320.
Solicitante: NOVARTIS VACCINES AND DIAGNOSTICS S.R.L..
Nacionalidad solicitante: Italia.
Dirección: VIA FIORENTINA 1 53100 SIENA (SI) ITALIA.
Inventor/es: PIZZA, MARIAGRAZIA, COMANDUCCI, MAURIZIO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/095 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Neisseria.
PDF original: ES-2436747_T3.pdf
Fragmento de la descripción:
CAMPO TÉCNICO DE LA INVENCIÓN
La presente invención se encuentra en el campo de la vacunación y, en particular, en la vacunación contra enfermedades causada por bacterias patógenas del género Neisseria tales que N.meningitidis (meningococos) .
ANTECEDENTES DE LA INVENCIÓN
Neisseria meningitidis es una bacteria encapsulada gram negativa que coloniza el tracto respiratorio superior de, aproximadamente, el 10 % de la población. Aproximadamente, en una de cada 10.000 personas colonizadas (o una de 100.000) la bacteria se introduce en el torrente sanguíneo, donde se multiplica y causa sepsis. Desde el torrente sanguíneo, la bacteria puede atravesarla barrera hematocefálica y causar meningitis. Ambas enfermedades son devastadoras y pueden matar del 5 % al 15 % de los niños y jóvenes adultos en horas, a pesar de que existen antibióticos efectivos. Más del 25 % de los que sobreviven a la enfermedad sufren secuelas permanentes.
La prevención de la enfermedad se ha conseguido parcialmente gracias a la vacunación. La inmunización se hizo posible en 1969 cuando se descubrió que la protección de la enfermedad está relacionada con la presencia de anticuerpos del suero capaces de inducir la destrucción bacteriana mediada por complemento y que los polisacáridos capsulares conjugados eran capaces de inducir estos anticuerpos. Aunque existen vacunas de polisacáridos y las vacunas conjugadas contra los serotipos A, C, W135 e Y, este enfoque no puede aplicarse al serotipo B ya que el polisacárido capsular es un polímero de ácido polisiálico, un autoantígeno en humanos. Para desarrollar una vacuna contra el serotipo B se han utilizado las proteínas expuestas en la superficie de vesículas de la membrana externa. Estas vacunas provocaron respuestas de anticuerpos bactericidas en el suero y protegían de la enfermedad, pero no inducían protección cruzada de cepas [1].
La secuencia genómica completa del serotipo B N. meningitidis ya se ha publicado [2] y ha sido sujeto de análisis para identificar antígenos de la vacuna [3]. También se conoce la secuencia genómica completa del serotipo A N. meningitidis [4], y la secuencia genómica completa de la cepa FA1090 de Neisseria gonorrhoeae se encuentra disponible [5]. Las referencias de la 6 a la 9 describen proteínas de Neisseria meningitidis y Neisseria gonorrhoeae, y se describen enfoques de la expresión a estas proteínas en las referencias 10 a 12.
Es objeto de la presente invención proporcionar y mejorar composiciones que otorguen inmunidad contra enfermedades y / o infecciones por meningococos, en particular para el serotipo B.
DESCRIPCIÓN DE LA INVENCIÓN
Una de las, aproximadamente, 2.200 proteínas descritas en la referencia 2 es “NMB1870”. En un principio, la proteína se describió como proteína “741” de la cepa MC58 (SECs ID Nº 2535 y 2536 de la referencia 8M SEC ID Nº 1) y también se ha nombrado como “GNA1870” [referencia 3] o como “ORF2086” [13].
La referencia 13 describe diversas secuencias de NMB1870 y las divide en subfamilias “A” y “B”. Estas subfamilias pueden combinarse. La referencia 13 no describe combinaciones adyuvantes con una sal de aluminio y no describe la unión de las subfamilias A y B como una proteína de fusión.
Se ha descubierto que NMB1870 es un antígeno extremadamente efectivo para provocar respuestas de anticuerpos frente al meningococo y que es expresado por todos los serotipos meningococo. Se ha encontrado NMB1870 en todas las cepas meningocócicas probadas hasta la fecha. Se han identificado cuarenta y dos secuencias meningocócicas diferentes de NMB1870, y se ha descubierto que esas secuencias se agrupan en tres variantes. Además, se ha descubierto que el suero producido contra una variante dada es bactericida dentro del mismo grupo de variante, pero no es activo contra cepas que expresen una de las otras dos variantes, es decir, hay protección cruzada dentro de las variantes pero no entre variantes. Por lo tanto, para una mayor eficacia cruzada de las cepas, debería utilizarse más de una variante para inmunizar un paciente.
La invención presenta además una composición que comprende, al menos, los siguientes dos antígenos:
(a) Una primera proteína compuesta de una secuencia aminoácida que tiene una identidad de secuencia de, al menos, el a % respecto a la SEC ID Nº 24; y
(b) Una segunda proteína compuesta de una secuencia aminoácida que tiene una identidad de secuencia de, al menos, el b % respecto a la SEC ID Nº 33 y también incluyen una sal de aluminio adyuvante.
El valor de a es, al menos, 85, por ejemplo 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 99, 5 o más. El valor de b es, al menos, 85, por ejemplo 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 99, 5 o más. Los valores de a y b no están intrínsecamente relacionados unos con otros.
Las proteínas (a) y (b) están estrechamente relacionadas a sus secuencias “prototipo·, pero no están tan estrechamente relacionadas la una con la otra.
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a, al menos, una cepa de N. meningitidis de cada grupo, al menos dos, de los siguientes tres grupos de cepas:
(a) MC58, gb185 (= M01 – 240185) , m4030, m2197, m2937, iss1001, NZ394 / 98, 67/00, 93 / 114, b198, m1390, nge28, lnp17592, 00-241341, f6124, 205900, m198 / 172, bz133, gb149 (= M01 – 240149) , nm008, nm092, 30 / 00, 39 / 99, 72 / 00, 95330, bz169, bz83, cu385, h44 / 76, m1590, m2934, m2969, m3370, m4215, m4318, n44 / 89, 14847.
(b) 961 – 5945, 2996, 96217, 312294, 11327, a22, gb013 (= M01 – 240013) , e32, m1090, m4287, 860800, 599, 95N477, 90 – 18311, c11, m986, m2671, 1000, m1096, m3279, bz232, dk353, m3697, ngh38, L93 / 4286.
(c) M1239, 16889, gb355 (= M01 – 240355) , m3369, m3813, ngp165.
Por ejemplo, la mezcla puede obtener una respuesta bactericida efectiva frente a cada serotipo B de las cepas MC58, 961 – 5945 y M1239 de N. meningitidis.
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a, al menos, el 50 % de las cepas meningocócicas clínicamente relevantes del serotipo B (por ejemplo, al menos 60 %, 70 %, 80 %, 90 %, 95 %
o más) .
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a cepas del serotipo B y cepas de, al menos, uno (por ejemplo 1, 2, 3 o 4) de los serotipos A, C, W135 e Y.
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a cepas de N. gonococcus y /
o N. cinerea.
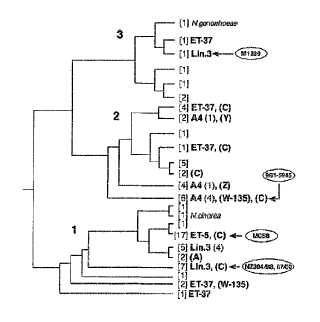
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a cepas de, al menos, dos de las tres ramas principales del dendrograma mostrado en la Figura 9 (es decir, el dendrograma obtenido por el análisis de las SECs ID 1 a 23 mediante el algoritmo de Kimura & Jukes – Cantor) .
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a cepas N. meningitidis en, al menos, 2 (por ejemplo 2, 3, 4, 5, 6 o 7) de las razas hipervirulentas ET – 37, ET – 5, el cúmulo A4, la raza 3 y los subgrupos I, III y IV – 1 [14, 15].
Las composiciones de la presente invención puede inducir adicionalmente respuestas anticuerpo bactericidas frente a una o más razas hiperinvasivas.
La mezcla puede preferiblemente obtener una respuesta anticuerpo bactericida frente a cepas de N. meningitidis en, al menos, 2 (por ejemplo 2, 3, 4, 5, 6 o 7= de los siguientes tipos de secuencia multilocus: ST1, ST4, ST5, ST8, ST11, ST32 y ST41 [16]. La mezcla puede también obtener una respuesta anticuerpo bactericida frente a las cepas ST44.
Las respuestas anticuerpo bactericidas se han medido convenientemente en ratones y son un indicador estándar de la eficacia de la vacuna [véase, por ejemplo, la nota final de la referencia 3]. La composición no necesita inducir anticuerpos bactericidas frente a todas y cada una de las cepas MenB en las razas especificadas o MLST; más bien, para cualquier grupo dado de cuatro o más cepas del serotipo B meningococos en una raza hipervirulenta en particular o un MLST, los anticuerpos inducidos por la composición son bactericidas frente a, al menos, el 50 % (por ejemplo el 60 %, 70%, 80 %, 90 % o más) del grupo. En la forma preferente, los grupos de cepas incluirán cepas aisladas en, al menos, cuatro de los siguientes países: GB, AU, CA, NO, IT, US, NZ, NL, BR y CU. Preferiblemente, el suero tiene un título bactericida de, al menos, 1024 (por ejemplo 210, 211, 212, 213, 214, 215, 216, 217, 218 o superior, preferiblemente de, al menos, 214) ,... [Seguir leyendo]
Reivindicaciones:
1. Una composición inmunogénica de dos proteínas que comprende (a) una sal de aluminio adyuvante; (b) una primera proteína que comprende una secuencia aminoácida que tiene, al menos, un 85 % de identidad de secuencia respecto a SEC ID Nº 24 y (c) una segunda proteína, que comprende una secuencia aminoácida que tiene, al menos, un 85 % de identidad de secuencia respecto a SEC ID Nº 33; en la que la proteína (b) tiene menos del 70 % de identidad de secuencia respecto a la proteína (c) .
2. La composición según la reivindicación 1, en la que la composición puede obtener una respuesta anticuerpo bactericida contra cepas de N. meningitidis en, al menos, 2 líneas hipervirulentas ET – 37, ET – 5, grupo A4, línea 3, subtipo I, subtipo III y subtipo IV – 1.
3. La composición según cualquiera de las reivindicaciones anteriores, en la que la primera proteína tiene, al
menos, un 88 % de identidad respecto a la SEC ID Nº 24. 15
4. La composición según cualquiera de las reivindicaciones anteriores, en la que la segunda proteína tiene, al menos, un 88 % de identidad respecto a la SEC ID Nº 33.
5. La composición según cualquiera de las reivindicaciones anteriores, en la que dicha primera y / o segunda 20 proteína (s) es / son proteínas meningocócicas.
6. La composición según cualquiera de las reivindicaciones anteriores, en la que una o más de las proteínas es una lipoproteína.
7. La composición según cualquiera de las reivindicaciones anteriores, en la que, al menos, una de las proteínas no incluye la secuencia aminoácida TKSKP (SEC ID Nº 70) o TRSKPV (SEC ID Nº 71) en los 10 aminoácidos de sus extremos N – Terminal.
8. La composición según cualquiera de las reivindicaciones anteriores, en la que, al menos, una de las proteínas no incluye la secuencia aminoácida PSEPPFG (SEC ID Nº 72) en los 10 aminoácidos de sus extremos N – Terminal.
9. La composición según cualquiera de las reivindicaciones anteriores, en la que, al menos, una de las proteínas incluye la secuencia aminoácida GGGG (SEC ID Nº 73) . 35
10. La composición según cualquiera de las reivindicaciones anteriores, en la que, al menos, una de las proteínas se utiliza en forma de proteína de fusión.
11. La composición según la reivindicación 10, en la que la proteína de fusión incluye la SEC ID Nº 46 y / o la 40 secuencia de lipoproteína líder P4 de H. influenzae.
12. La composición según cualquiera de las reivindicaciones anteriores, que comprende una o más proteínas que contienen una secuencia aminoácida seleccionada de SECs ID Nº 1 a 45 y 77.
13. Una composición que contiene una proteína híbrida con fórmula NH2 –A –
Patentes similares o relacionadas:
Procedimientos y composiciones de glucoconjugación, del 13 de Mayo de 2020, de PFIZER INC.: Un glucoconjugado unido a (2-((2-oxoetil)tio)etil)carbamato (eTEC) de acuerdo con la fórmula (I): **(Ver fórmula)** en la que los átomos que comprenden el espaciador […]
Bacterias mutantes para la producción de módulos generalizados para antígenos de membrana, del 13 de Mayo de 2020, de GLAXOSMITHKLINE BIOLOGICALS SA: Un procedimiento para preparar vesículas a partir de una bacteria gramnegativa en el que al menos una proteína que contiene un dominio catalítico LytM se inactiva […]
Proteína de enlace del factor H meningocócico utilizada como adyuvante, del 6 de Mayo de 2020, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que comprende dos antígenos meningocócicos fHBP diferentes, ambos adsorbidos al adyuvante de hidroxifosfato de aluminio, en donde (i) […]
Nuevas composiciones inmunogénicas para la prevención y tratamiento de enfermedad meningocócica, del 11 de Marzo de 2020, de WYETH HOLDINGS LLC: Una composición que comprende al menos una proteína que comprende una secuencia de aminoácidos que tiene identidad de secuencia mayor de 80 % con la […]
Vacunas de polipéptidos para protección amplia contra linajes meningocócicos hipervirulentos, del 18 de Diciembre de 2019, de GLAXOSMITHKLINE BIOLOGICALS SA: NadA de N.meningitidis recombinante en forma trimérica, en donde la NadA consiste de la secuencia de aminoácidos de la SEQ ID NO: 2.
Meningococo que sobreexpresa NadA y/o NHBA y vesículas de la membrana externa derivadas del mismo, del 23 de Octubre de 2019, de GLAXOSMITHKLINE BIOLOGICALS SA: Un meningococo que expresa NadA y opcionalmente NHBA, en el que el meningococo es isogénico con una cepa parental, excepto por una modificación genética […]
Composiciones y métodos para mejorar la inmunogenicidad de los conjugados de polisacárido-proteína, del 23 de Octubre de 2019, de Kanvax Biopharmaceuticals Ltd: Un conjugado de polisacárido-proteína que comprende una proteína transportadora quimérica y un antígeno polisacárido, en donde la proteína […]
Polipéptidos de fHbp meningocócicos modificados, del 16 de Agosto de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Un polipéptido que comprende una secuencia de aminoácidos que tiene al menos un 80 % de identidad de secuencia con la SEQ ID NO: 5, en el […]