Una terapia celular para degeneración ocular.
Células madre mesenquimales para usar en un procedimiento de tratamiento de un paciente que tiene unaafección degenerativa ocular,
comprendiendo el procedimiento administrar al paciente dichas células madremesenquimales en una cantidad efectiva para tratar la afección ocular degenerativa, en el que las células madremesenquimales se caracterizan por la expresión de los siguientes marcadores de superficie: CD29, CD44, CD105 yCD166 y la falta de expresión de CD14, CD34 y CD45.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/021671.
Solicitante: Janssen Biotech, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 800/850 RIDGEVIEW DRIVE HORSHAM, PA 19044 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MISTRY,SANJAY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/28 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Médula ósea; Células madre hematopoyéticas; Células madre mesenquimales de cualquier origen, por ejemplo células madre derivadas de tejido adiposo.
- C12N5/074 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre adultas.
- C12N5/077 C12N 5/00 […] › Células mesenquimales, p. ej. Células óseas, células cartilaginosas, Células del estroma de la médula ósea, células adiposas o células musculares.
PDF original: ES-2400916_T3.pdf
Fragmento de la descripción:
Una terapia celular para degeneración ocular
Antecedentes Como un órgano complejo y sensible del cuerpo que es, el ojo puede experimentar numerosas enfermedades y otras afecciones deletéreas que afectan su capacidad para funcionar normalmente. Muchas de estas afecciones están asociadas con daño o degeneración de células oculares específicas y de tejidos elaborados de esas células. Como un ejemplo, las enfermedades y las afecciones degenerativas del nervio óptico y la retina son las principales causas de ceguera en todo el mundo. Daño o degeneración de la córnea, el cristalino y tejidos oculares asociados representan otra causa significativa de pérdida de visión. La retina contiene siete capas de células alternantes y de procedimientos que convierten una señal de luz en una señal neuronal. Los fotorreceptores retinales y el epitelio de pigmento retinal (RPE) forman una unidad funcional que, en muchos trastornos, llega a estar desequilibrada debido a mutaciones genéticas o a condiciones ambientales (incluyendo la edad) . Esto resulta en pérdida de fotorreceptores: por apoptosis o degeneración secundaria, que conduce a deterioro progresivo de visión y en algunos casos, a ceguera (para una revisión, véase, por ejemplo, Lund, R.D. y cols., 2001, Progress in Retinal and Eye Research 20: 415-449) . Dos fases de trastornos oculares que tienen dentro este patrón son degeneración macular relacionada con la edad (AMD) y retinitis pigmentosa (RP) .
AMD es la causa más común de pérdida de visión en los Estados Unidos en aquellos de 50 años o mayores; y su prevalencia se incrementa con la edad. El trastorno principal en AMD parece deberse a disfunción de RPE y a cambios en membranas de Bruch, por ejemplo, deposición de lípidos, reticulación proteica y permeabilidad a nutrientes (Lund y
cols., 2001) . Diversos elementos pueden contribuir a degeneración macular, incluyendo conformación genética, edad, nutrición, fumar y exposición a luz solar.
RP se considera principalmente una enfermedad hereditaria: más de 100 mutaciones se han asociados con pérdida de fotorreceptores (Lund y cols., 2001) . Aunque la mayoría de las mutaciones van dirigidas a los fotorreceptores, algunas afectan directamente a las células de RPE. Conjuntamente, estas mutaciones afectan a procesos tales como tráfico molecular entre fotorreceptores y células de RPE y fototransducción, por ejemplo.
Otras retinopatías menos comunes, pero no obstante debilitantes pueden implicar también degeneración celular progresiva que conduce a pérdida de visión y a ceguera. Estas incluyen, por ejemplo, retinopatía diabética y membrana neovascular coroidea (CNVM) . La retinopatía diabética se puede clasificar como (1) retinopatía no proliferativa o retinopatía de fondo, caracterizada por permeabilidad capilarmente incrementada, edema, hemorragia,
microaneurismas y exudados, o 2) retinopatía proliferativa, caracterizada por neovascularización que se extiende a partir de la retina hasta la formación de tejido fibroso, de cicatrización, vítreo y potencial para el desprendimiento de retina. En CNVM, vasos sanguíneos anormales que se derivan del coroide crecen a través de las capas retinales. Los vasos nuevos frágiles se rompen fácilmente, causando que sangre y fluido se almacenen dentro de las capas de la retina.
El daño o la degeneración progresiva del nervio óptico y los nervios relacionados del ojo constituye otra causa principal de pérdida de visión y ceguera. Un ejemplo excelente es glaucoma, una afección ocular que está formada por una colección de enfermedades oculares que causan pérdida de visión con daño al nervio óptico. La presión intraocular elevada (IOP) debida al drenaje ocular inadecuado es una causa principal de glaucoma, pero puede también desarrollarse en la ausencia de IOP elevada.
El glaucoma puede desarrollarse según el ojo envejece, o puede tener lugar como resultado de una lesión ocular, inflamación ocular, tumor ocular, o en casos avanzados de cataratas o diabetes, o pueden causarse por ciertos fármacos, tales como, por ejemplo esteroides. Las características primarias de la neuropatía óptica en el glaucoma incluyen cambios característicos en la cabeza del nervio óptico, un decrecimiento en número de células de ganglios retinales supervivientes y pérdida de visión. Se ha propuesto que una cascada de eventos une la degeneración del
nervio óptico con la muerte lenta de células glanglionares retinales observada en la enfermedad y esta cascada de eventos puede ralentizarse o evitarse por el uso de agentes neuroprotectores (Osborne y cols., 2003, Eur. J. Ophthalmol, 13 (Supl. 3) : S19-S26) .
El daño celular y las afecciones degenerativas también afectan otras partes del ojo. Por ejemplo, las cataratas resultan de la opacificación gradual del cristalino del ojo. Se cree que una vez que comienza, el desarrollo de cataratas continúa 50 a lo largo de una o más rutas comunes que culminan en daño a las fibras del cristalino. Esta afección se trata actualmente por eliminación quirúrgica y reemplazo del cristalino afectado. Otro ejemplo se refiere a la córnea y a la conjuntiva circundante que forma la superficie ocular. El epitelio límbico, localizado entre la córnea y la conjuntiva bulbar, contiene células madre epiteliales corneales. La deficiencia celular del epitelio límbico (LECD) es una afección que tiene lugar, por ejemplo, en el síndrome de Stevens-Johnson y en las quemaduras térmicas o químicas. LECD
conduce a menudo a un desequilibrio entre el epitelio córneo y el epitelio conjuntival en el que la córnea se reviste por células epiteliales conjuntivales invasoras, lo que compromete gravemente la superficie córnea y afecta la agudeza visual (Nakamura, T. y Kinoshita, S., 2003. Cornea 22 (Supl. 1) : S75-S80) .
La reciente aparición de la terapia basada en células madre para reparación y regeneración tisular proporciona tratamientos prometedores para un número de patologías degenerativas celulares mencionadas anteriormente y para otros trastornos oculares. Las células madre son capaces de autorrenovación y diferenciación para generar diversos linajes de células maduras. El trasplante de tales células puede usarse como una herramienta clínica para reconstruir un tejido diana, restaurando de este modo funcionalidad fisiológica y anatómica. La aplicación de tecnología de células madre es de amplio intervalo, incluyendo ingeniería tisular, desarrollo de terapia génica y productos terapéuticos celulares, es decir, administración de agentes bioterapéuticos a una localización diana por medio de células vivas suministradas exógenamente o de componentes celulares que producen o contienen esos agentes (para una revisión, véase Tresco, P.A. y cols., 2000, Advanced Drug Deliver y Reviews 42: 2-37) .
Un obstáculo para realización del potencial terapéutico de tecnología de células madre ha sido la dificultad en obtener cantidades suficientes de células madre. Una fuente de células madre es el tejido embrionario o fetal. Las células madre y progenitoras embrionarias se han aislado a partir de un número de especies de mamíferos, incluyendo seres humanos y varios de tales tipos celulares se han mostrado capaces de autorrenovación y expansión, así como de diferenciación en diversos linajes celulares. En sistemas de modelos animales, se ha comunicado que las células madre embrionarias se diferencian en un fenotipo celular RPE, así como que potencian la supervivencia de los fotorreceptores del huésped tras trasplante (Haruta M. y cols. 2004, Investig. Ophthalmol. Visual Sci. 45: 1020-1025; Schraermeyer, U. y cols., 2001, Cell Transplantation 10: 673-680) . Pero la derivación de células madre a partir de fuentes embrionarias o fetales ha planteado muchos problemas éticos que es deseable evitar identificando otras fuentes de células multipotentes o pluripotenciales.
El tejido adulto también puede proporcionar células madre útiles para la terapia ocular basada en células. Por ejemplo, las células madre retinales y corneales por sí mismas pueden usarse para terapia de reemplazo celular en el ojo. Además, se ha comunicado que las células madre neuronales del hipocampo se integran con la retina del huésped, adoptando ciertas características neuronales y gliales (véase la revisión de Lund, R.L. y cols., 2003, J. Leukocyte Biol.
74: 151-160) . Las células madre neuronales preparadas a partir del córtex de rata fetal estaban mostrando diferenciarse a lo largo de una ruta celular de RPE tras trasplante en el espacio subretinal del adulto (Enzmann, V. y cols., 2003, Investig. Ophthalmol. Visual Sci.: 5417-5422) .
Se ha comunicado que las células madre de la médula ósea se diferencian... [Seguir leyendo]
Reivindicaciones:
1. Células madre mesenquimales para usar en un procedimiento de tratamiento de un paciente que tiene una afección degenerativa ocular, comprendiendo el procedimiento administrar al paciente dichas células madre mesenquimales en una cantidad efectiva para tratar la afección ocular degenerativa, en el que las células madre mesenquimales se caracterizan por la expresión de los siguientes marcadores de superficie: CD29, CD44, CD105 y CD166 y la falta de expresión de CD14, CD34 y CD45.
2. Las células madre mesenquimales de la reivindicación 1, en donde las células madre mesenquimales, una vez trasplantadas en una localización diana en el ojo, promueven la supervivencia de las células oculares in situ pero las células madre no forman estructuras similares a la capa fotorreceptora y no expresan un marcador específico de fotorreceptores.
3. Las células madre mesenquimales de la reivindicación 1, en donde las células madre mesenquimales, una vez trasplantadas en una localización diana en el ojo, promueven la formación de fotorreceptores a partir de células oculares in situ pero las células madre no se diferencian en fotorreceptores por sí mismas.
4. Las células madre mesenquimales de la reivindicación 1, siendo la afección ocular degenerativa una afección ocular degenerativa aguda.
5. Las células madre mesenquimales de la reivindicación 4, siendo la afección ocular degenerativa aguda un traumatismo craneoencefálico, traumatismo del nervio óptico o lesión ocular.
6. Las células madre mesenquimales de la reivindicación 1, siendo la afección ocular degenerativa una afección ocular degenerativa crónica o progresiva.
7. Las células madre mesenquimales de la reivindicación 6, siendo la afección ocular degenerativa crónica o progresiva degeneración macular, retinitis pigmentosa, retinopatía diabética, glaucoma, deficiencia celular epitelial límbica.
8. Las células madre mesenquimales de la reivindicación 1, en donde las células se administran con al menos un tipo celular distinto.
9. Las células madre mesenquimales de la reivindicación 8, siendo el al menos un tipo celular distinto un astrocito, un oligodendrocito, una neurona, un progenitor neuronal, una célula madre neuronal, célula madre epitelial retinal, célula madre epitelial corneal u otra célula multipotente o pluripotente.
10. Las células madre mesenquimales de la reivindicación 8, administrándose el al menos un tipo celular distinto simultáneamente con, o antes de, o después de, las células madre mesenquimales.
11. Las células madre mesenquimales de la reivindicación 1, administrándose las células con al menos un agente distinto.
12. Las células madre mesenquimales de la reivindicación 11, administrándose el al menos un agente distinto simultáneamente con, o antes de, o después de, las células.
13. Las células madre mesenquimales de la reivindicación 1, administrándose las células a la superficie de un ojo.
14. Las células madre mesenquimales de la reivindicación 1, administrándose las células al interior de un ojo.
15. Las células madre mesenquimales de la reivindicación 14, administrándose las células a través de una cánula o a partir de un dispositivo implantado en el cuerpo del paciente dentro del ojo o en la proximidad del mismo.
16. Las células madre mesenquimales de la reivindicación 14, administrándose las células por implantación de una matriz o un soporte tridimensionales que contienen las células.
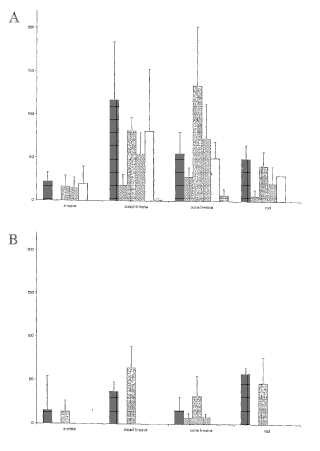
Figura 1:
Figura 2:
Figura 3:
sensibilidad umbral (unidades logarítmicas/candelas)
Figura 4:
Patentes similares o relacionadas:
Una terapia de combinación para un injerto estable y a largo plazo usando protocolos específicos para el agotamiento de los linfocitos T/B, del 20 de Mayo de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Una dosis de células hematopoyéticas inmaduras de linfocitos T agotados, en donde dichas células hematopoyéticas inmaduras de linfocitos T agotados comprenden menos de 5 x 105 […]
Función promotora del crecimiento del cabello de células madre de tamaño pequeño y uso de las mismas, del 6 de Mayo de 2020, de MEDIPOST, CO., LTD.: Una composición para su uso en la terapia de pérdida de cabello para prevenir la pérdida de cabello y estimular el crecimiento del cabello, que comprende: células […]
Terapia con células madre basada en células madre procedentes de tejido adiposo, del 6 de Mayo de 2020, de RIGSHOSPITALET: Una composición que comprende una suspensión de una población sustancialmente homogénea e inmunosupresora de células madre procedentes de tejido adiposo (ASC) humanas adultas […]
Métodos y composiciones para el tratamiento de beta talasemia, del 15 de Abril de 2020, de Sangamo Therapeutics, Inc: Una célula madre hematopoyética CD34+ modificada genéticamente, que comprende: un par de nucleasas con dedos de zinc, comprendiendo el par: (i) una primera […]
Composiciones y métodos de células grasas marrones, del 1 de Abril de 2020, de Biorestorative Therapies, Inc: Un método para generar una célula grasa marrón, el método comprende: aislar una célula madre de un tejido graso marrón obtenido; y cultivar la célula […]
Péptido para inducir regeneración de tejido y uso del mismo, del 4 de Marzo de 2020, de StemRIM Inc: Un péptido que consiste en una porción de una proteína HMGB1 y tiene una actividad de estimulación de la migración de una célula, donde dicho péptido consiste en una cualquiera […]
Métodos para inducir apoptosis parcial utilizando polipéptidos de caspasa, del 4 de Marzo de 2020, de Bellicum Pharmaceuticals, Inc: Un ligando multimérico para usar en un método para el tratamiento del cáncer; comprendiendo dicho método controlar la supervivencia de las células terapéuticas en un […]
Método de proliferación celular y agente farmacéutico para reparación y regeneración de tejido, del 12 de Febrero de 2020, de Sapporo Medical University: Método para hacer crecer células madre mesenquimatosas humanas en una muestra recogida de un sujeto vivo cultivando las células en un medio, comprendiendo […]