SISTEMAS NANOPARTICULARES ELABORADOS A BASE DE ÉSTERES DE SORBITÁN.
Sistemas nanoparticulares elaborados a base de ésteres de sorbitán.
La presente invención se refiere a sistemas que comprenden nanopartículas homogéneas con un tamaño medio inferior a 1 micrómetro que comprenden, al menos un éster de sorbitán, un éster de macrogol, un éter de macrogol o un derivado de los mismos y, opcionalmente, al menos un componente derivado de oxietileno y/o al menos un componente dotado de carga eléctrica (positiva o negativa); donde los componentes se incorporan en una única etapa consistente en la mezcla de dos disoluciones. Al uso de los mismos como medicamentos, productos sanitarios o en ingeniería de tejidos o medicina regenerativa, o con aplicaciones cosméticas, de higiene, nutricionales y de recubrimiento de superficies así como a procedimientos para su preparación.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201131812.
Solicitante: UNIVERSIDADE DE SANTIAGO DE COMPOSTELA.
Nacionalidad solicitante: España.
Inventor/es: SANCHEZ BARREIRO,ALEJANDRO, KONAT ZORZI,GIOVANNI, SEIJO REY,BEGOÑA, SANTANA CARVALHO,Edison Luis.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K47/14 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Esteres de ácidos carboxílicos, p. ej. monoglicéridos de ácidos grasos, triglicéridos de cadenas medianas, parabenos o ésteres de ácidos grasos y de polietilenglicol (PEG).
- A61K9/51 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Nanocápsulas.
- B82Y5/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B82 NANOTECNOLOGIA. › B82Y USOS O APLICACIONES ESPECIFICOS DE NANOESTRUCTURAS; MEDIDA O ANALISIS DE NANOESTRUCTURAS; FABRICACION O TRATAMIENTO DE NANOESTRUCTURAS. › Nano- biotecnología o nano-medicina, p. ej. ingeniería de proteínas o administración de fármaco.
Fragmento de la descripción:
Sistemas nanoparticulares elaborados a base de ésteres de sorbitán
CAMPO DE LA INVENCIÓN
La presente invención se refiere a sistemas que comprenden nanopartículas capaces de encapsular sustancias. Más concretamente, se refiere a sistemas nanoparticulares que comprenden ésteres de sorbitán. También se refiere a un procedimiento de preparación de estos sistemas y a sus aplicaciones en el campo de la medicina.
ANTECEDENTES DE LA INVENCIÓN
Dentro de los sistemas coloidales propuestos para el transporte de ingredientes activos que han sido descritos en literatura, destacan las micelas, micelas mixtas, emulsiones, micro y nanopartículas y liposomas que pueden estar constituidos de materias primas de distinta naturaleza y que pueden ser obtenidos mediante las más variadas técnicas de preparación. En cualquier caso, las materias primas empleadas en la elaboración de sistemas para la liberación de fármacos serán seleccionadas dependiendo de la vía de administración preferida y teniendo en cuenta su aprobación por parte de los organismos competentes.
Una materia común a algunos de estos vehículos farmacéuticos son las sustancias tensioactivas que habitualmente intervienen en los procesos de preparación de los mismos y se incorporan en pequeñas cantidades.
Sólo en algunos casos se ha conseguido emplear tensioactivos como ingredientes fundamentales de dichos vehículos farmacéuticos. Uno de estos tensioactivos son los ésteres de sorbitán, de gran interés debido a su biocompatibilidad. Los ésteres de sorbitán son frecuentemente utilizados en la industria farmacéutica. El empleo de los mismos se debe a sus propiedades como tensioactivos no iónicos lipofílicos. Precisamente por ello, el experto en la técnica sabe que dichas propiedades se manifiestan a concentraciones bajas del agente tensioactivo (Owen I. Corrigan and Anne Marie Healy, Surfactants in Pharmaceutical Products and Systems, Encyclopedia of Pharmaceutical Technology, Vol. 14 (Swarbrick, J. And Boylan, J.C., Eds.) . Concretamente, en la literatura se recoge para los ésteres de sorbitán concentraciones que no superan el 15% (Handbook of Pharmaceutical Excipients, Sixth Edition, Rowe, R.C., Sheskey, P.J. and Weller, P.J (Eds.) , Pharmaceutical Press, Chicago, 2009) .
En el contexto descrito es necesario mencionar que ha habido autores que, pese a referirse a los ésteres de sorbitán como a tensioactivos, los han empleado como componente principal en los sistemas por ellos desarrollados. Así por ejemplo, podemos citar el desarrollo de sistemas milimétricos tipo pellets o de sistemas macroscópicos tipo gel, concretamente denominados organogeles.
En el primero de los casos se describe que la máxima concentración que se ha empleado para obtener los sistemas tipo pellet ha estado comprendida entre un 50% para el sorbitan monoestearato (span 60) y el 80% para el sorbitan monooleato (span 80) (Podczeck, F., Alessi, P. And Newton, J, M., Int. J. Pharm., 361, 2008, 33-40) . Pese a ello, los autores citados han podido comprobar que lejos de desarrollarse sistemas constituidos exclusivamente por dichos componentes, la máxima cantidad de éster de sorbitán que se ha conseguido incorporar en los sistemas finales no llega al 23%.
En el segundo de los casos, lo que se consigue es obtener geles macroscópicos empleando elevados porcentajes de ésteres de sorbitán (Bari, H., International Journal of Pharmaceutical Sciences Review and Research, Volume 3, Issue 1, July – August 2010; Article 001) , (Murdan, Gregoriadis and Florence, International Journal of Pharmaceutics 180 (1999) 211–214) (Murdan, Gregoriadis and Florence , J Pharm Sci., Vol. 88, No. 6, June 1999) .
En base a lo anteriormente expuesto, cuando pensamos en el empleo de ésteres de sorbitán y lo citamos como tensioactivo, el experto en la técnica no piensa en su empleo a una elevada proporción, ya que dicha proporción no haría posible sus propiedades como tensioactivo. Pero incluso si el experto en la técnica lo pretende considerar como componente único o incluso mayoritario de una formulación, de lo que se describe en la literatura se desprende que únicamente sistemas de tamaño superior a micrómetros pueden ser desarrollados con tal componente.
Los únicos sistemas que han podido ser desarrollados hasta la actualidad empleando los ésteres de sorbitán como principal componente son los siguientes:
A) Sistemas microparticulares, con un diámetro medio superior a un micrómetro;
B) Microemulsiones (LIU Hai-shui, LI Tie-long, JIN Zhao-hui, GONG Yan-zhang, ZHANG Yunxia, Microemulsion with Span®/Tween as Mixed-surfactant and Synthesis of Iron Nanoparticles, The Chinese Journal of Process Engineering, DOI CNKI-ISSN: 1009-606X.0.2007-01-013) (EP1961412A1) ;
C) Nanosistemas vesiculares tipo reservorio (ej. liposomas o niosomas o nanocápsulas) como es el caso de los sistemas nanovesiculares descritos por Shilpa Kakkar, Indu Pal Kaur en el International Journal of Pharmaceutics, doi:10.1016/j.ijpharm.2011.04.027.
Los liposomas son vesículas coloidales en las que una membrana de estructura bilaminar compuesta de lípidos de diferentes naturaleza, encierra o encapsula una parte de la fase acuosa en la que los propios liposomas se encuentran dispersos. La unidad básica de la estructura de los liposomas es, por tanto, la bicapa lipídica que constituye la membrana vesicular, cuya formación tiene lugar espontáneamente en presencia de agua. A esta formación espontánea se han ido incorporando niveles de sofisticación en su estructura y procedimiento de obtención, mejorando de esta forma su capacidad para actuar como sistemas de liberación de fármacos y, en la misma medida, sus posibles aplicaciones terapéuticas. La composición lipídica, el tamaño de partícula o vesícula, el número de lamelas o bicapas que forman la pared, así como la composición de las fases acuosas interna y externa o el método de preparación, determinan las características físico-químicas de las vesículas, su capacidad para la encapsulación de fármacos, y también su estabilidad y comportamiento tanto in vivo como in vitro. Los liposomas son considerados sistemas transportadores de fármacos. Sin embargo, a pesar del gran interés, existen importantes problemas, relacionados sobre todo con la estabilidad del sistema en los fluidos corporales y, en particular, en el torrente sanguíneo, en donde se produce una excesiva pérdida de fármaco y una rápida intercepción del sistema, con la consiguiente retirada del mismo de la circulación, por las células del sistema fagocítico mononuclear (MPS) Andresen et al., Progress in Lipid Research 44 (2005) 68–97. Tal constatación representa un obstáculo para los liposomas como sistemas de transporte de fármacos. Además se comprobó que, en general, los liposomas presentan una capacidad de encapsulación limitada, sobre todo frente a fármacos hidrofílicos, así como un tamaño heterogéneo, observándose con frecuencia una falta de reproducibilidad de las formulaciones elaboradas, siendo, esas características también relacionadas con los métodos de preparación de los mismos Lian y Ho, JOURNAL OF PHARMACEUTICAL SCIENCES, VOL. 90, NO. 6, JUNE 2001, 667-680.
Los tres tipos de sistemas anteriores presentan un grave problema en lo que respecta a su estabilidad. Los sistemas vesiculares y emulsiones son conocidos por experimentar fenómenos de agregación y la dificultad para obtener formulaciones más estables mediante procesos como la liofilización sin alterar significativamente sus características iniciales. En este sentido, no debemos olvidar que para la propia formación de tales sistemas es preciso un considerable aporte energético y/o el empleo de combinaciones específicas de agentes tensioactivos, por lo que el producto obtenido se encuentra en una situación energéticamente desfavorable o inestable. Además, se trata de sistemas especialmente sensibles a variaciones en el entorno como la temperatura.
Por otro lado, los sistemas microparticulados poseen cierta tendencia a la sedimentación debido a la influencia de la fuerza gravitacional.
Las nanopartículas, en cuanto a que se trata de nanosistemas de tipo matricial, son sistemas adecuados para la liberación de fármacos, ya que son más estables que los citados anteriormente, en general presentan mayor capacidad de encapsulación, es posible prepararlas con un tamaño homogéneo.
Sin embargo, no es posible preparar nanopartículas en base a ésteres de sorbitán siguiendo las enseñanza del estado de la técnica, considerando como más próximo las nanopartículas constituidaspor componentes lipofílicos como las nanopartículas lipídicas sólidas (SLN) (Rainer H. MuÈller, Karsten MaÈder,...
Reivindicaciones:
1. Nanopartícula que comprende un éster de sorbitán en una proporción en peso de entre 60% y 100%.
2. Nanopartícula según la reivindicación 2, caracterizada por ser una matriz sólida, homogénea, cuyo tamaño medio está comprendido entre 1 y 999 nm.
3. Nanopartícula, según las reivindicaciones 1 a 2, donde el tamaño promedio está comprendido entre 50 y 600 nm.
4. Nanopartícula, según cualquiera de las reivindicaciones 1 a 3, cuya carga varía entre –50 mV y +60 mV.
5. Nanopartícula, según cualquiera de las reivindicaciones 1 a 4, donde el éster de sorbitán se selecciona de entre el grupo consistente en mono-, di-, tri- o sesqui-oleato de sorbitán, mono-, di-, tri- o sesqui-laurato de sorbitán, mono-, di-, tri- o sesqui-palmitato de sorbitán, mono-, di-, tri- o sesqui-estearato de sorbitán y mono-, di-, tri- o sesqui-isoestearato de sorbitán, y sus combinaciones.
6. Nanopartícula según cualquiera de las reivindicaciones 1 a 5, que además comprende una sustancia catiónica, una sustancia aniónica, un derivado de óxido de etileno, o combinaciones de los mismos.
7. Nanopartícula según la reivindicación 6, donde la sustancia catiónica se selecciona entre sales de amonio, polímeros catiónicos y aminas grasas.
8. Nanopartícula según la reivindicación 7, donde el polímero catiónico se selecciona entre protamina, poliglutámico, dextrano cationizado, poliaminoácidos y proteínas cationizadas, y sus sales.
9. Nanopartícula según la reivindicación 6, donde la sustancia aniónica es un polímero aniónico seleccionado de entre el grupo constituido por ácido hialurónico, ácido colomínico, polisiálico, condroitina, queratano, dextranos, heparina, carragenanos, furceleranos, alginatos, agar agar, glucomanano, goma gelano, goma garrofín, goma guar, goma tragacanto, goma arábiga, goma xantano, goma karaya, pectinas, celulosas, almidones, sus sales, fragmentos, derivados o combinaciones de los mismos.
10. Nanopartícula según la reivindicación 6, donde el derivado de óxido de etileno se selecciona de entre polietilenglicol dodecil éter (Brij 30) , polietilenglicol hexadecil éter (Brij 56) , polietilenglicol 2-octadecil éter (Brij 72) , polietilenglicol 8-octadecil éter (Brij 78) , polietilenglicol 8-estearato (Myrj 45) , 2-hidroxietil octadecanoato (Myrj 52) , monoestearato de etilen glicol, monoestearato de trietilen glicol.
11. Nanopartícula según cualquiera de las reivindicaciones 1 a 10, que además comprende un ingrediente activo.
12. Nanopartícula según cualquiera de las reivindicaciones 1 a 11, que además comprende un compuesto seleccionado de entre un marcador, un adyuvante, un inmunomodulador, un anticuerpo, un aptámero, un receptor de superficie, un compuesto estabilizante, un compuesto sensible a la polimerización química o combinaciones de los mismos.
13. Nanopartícula según cualquiera de las reivindicaciones 1 a 11, que se encuentra en forma liofilizada.
14. Composición farmacéutica que comprende una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, y un vehículo farmacéuticamente aceptable.
15. Composición cosmética que comprende una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12.
16. Composición nutricional que comprende una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12.
17. Producto sanitario que comprende una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12.
18. Sustancia para el recubrimiento de superficies que comprende una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12.
19. Uso de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12 en la preparación de un medicamento.
20. Uso de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12 en la preparación de un medicamento para terapia combinada.
21. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12 en la preparación de una vacuna.
22. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, en ingeniería de tejidos, medicina regenerativa y terapia celular.
23. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, como marcador.
24. Uso de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para fines diagnósticos.
25. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para su administración por vía oral, bucal, sublingual, tópica, ocular, nasal, pulmonar, ótica, vaginal, intrauterina, rectal, entérica o parenteral.
26. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, en la preparación de un producto cosmético o de higiene personal para la administración sobre piel, sistema piloso y capilar, uñas, labios, órganos genitales externos, dientes o mucosas.
27. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para terapia génica, silenciamiento o interferencia genética, o vacunación genética.
28. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para producir la asociación, expansión o activación de poblaciones celulares o para manipular o alterar las características biológicas de células vivas tanto autólogas, como alogénicas, xenogénicas
29. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para facilitar, estimular o modificar la producción de compuestos por células, con fin de producción biotecnológica.
30. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, con la finalidad de higiene o estética, para neutralizar o eliminar ectoparásitos, para perfumar, modificar el aspecto de la superficie corporal y/o corregir olores corporales y/o protegerla o mantenerla en buen estado.
31. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para modificar, corregir o introducir propiedades organolépticas o mejorar la estabilidad en un medicamento o en un producto cosmético o de higiene personal.
32. Uso de de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, para acondicionar, modificar o restablecer las características de agua, alimentos o suplementos nutricionales, así como para modificar, corregir o introducir nuevas propiedades organolépticas o mejorar la estabilidad de los mismos y para facilitar o hacer posible la administración de alimentos
o nutrientes a seres vivos.
33. Procedimiento para la preparación de una nanopartícula como se ha descrito en cualquiera de las reivindicaciones de 1 a 12, que comprende las siguientes etapas:
a) preparar una fase orgánica que comprende un éster de sorbitán en una proporción en peso de entre 60% y 100%;
b) mezclar bajo agitación la disolución obtenida en a) con una disolución acuosa.
34. Procedimiento según la reivindicación 33, donde la fase orgánica de la etapa a) y/o la disolución acuosa de la etapa b) además comprende una sustancia catiónica, una sustancia aniónica o ambas.
35. Procedimiento según las reivindicaciones 33 a 34, que comprende además una etapa c) que comprende la incubación de la dispersión de nanopartículas formadas en la etapa b) con una disolución que comprende una sustancia catiónica, un polímero aniónico o una combinación de ambos.
36. Procedimiento según cualquiera de las reivindicaciones de 33 a 35, donde la fase orgánica de la etapa a) comprende además un derivado de óxido de etileno.
37. Procedimiento según cualquiera de las reivindicaciones de 33 a 36, donde el disolvente de la fase orgánica es un solvente hidromiscible.
38. Procedimiento según cualquiera de las reivindicaciones de 33 a 37, donde el éster de sorbitán se disuelve en la fase orgánica en una concentración de entre 0, 1 y 10 mg/ml.
39. Procedimiento según cualquiera de las reivindicaciones de 34 a 35, donde la sustancia catiónica, aniónica o ambas, se disuelven a una concentración de entre 0, 01 y 1, 0 mg/mL.
40. Procedimiento según cualquiera de las reivindicaciones de 33 a 39, que comprende además la adición de un ingrediente activo, y/o un compuesto seleccionado de entre un marcador, un adyuvante, un inmunomodulador, un anticuerpo, un aptámero, un receptor de superficie, un compuesto estabilizante, un compuesto sensible a la polimerización química o combinaciones de los mismos, en una de las disoluciones a) o b) dependiendo de su carácter lipofílico o hidrofílico.
41. Procedimiento según cualquiera de las reivindicaciones de 33 a 39 que comprende además la adición de un ingrediente activo, y/o un compuesto seleccionado de entre un marcador, un adyuvante, un inmunomodulador, un anticuerpo, un aptámero, un receptor de superficie, un compuesto estabilizante, un compuesto sensible a la polimerización química o combinaciones de los mismos, en una etapa c) posterior a la etapa b) .
42. Procedimiento según cualquiera de las reivindicaciones de 33 a 41, que comprende una etapa adicional después de la etapa b) o de la etapa c) en la que las nanopartículas se someten a un proceso de deshidratación total o parcial.
43. Procedimiento según la reivindicación 42, que comprende una etapa adicional en la que se regeneran las nanopartículas deshidratadas parcialmente o liofilizadas.
Figura 1
Figura 2
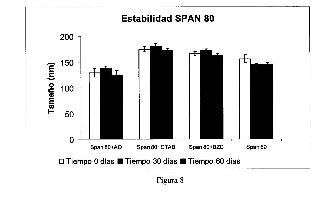
Figura 3
Figura 5
Figura 6
Figura 7
Figura 8
Figura 9
Figura 10
Figura 11
Figura 12
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Preparación externa líquida, del 29 de Julio de 2020, de HISAMITSU PHARMACEUTICAL CO. INC.: Una preparación tópica líquida, que comprende: agua; oxibutinina o una sal farmacéuticamente aceptable de la misma; y un éster de ácido dicarboxílico, […]
Método de tratamiento del cáncer, del 22 de Julio de 2020, de Intensity Therapeutics, Inc: Una composición que comprende una cantidad terapéuticamente efectiva de un agente terapéutico y un agente mejorador de la permeación intracelular para uso en el tratamiento […]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Composiciones tópicas que comprenden un corticosteroide y un retinoide para tratar la psoriasis, del 1 de Julio de 2020, de Bausch Health Ireland Limited: Una composición farmacéutica tópica para usar en el tratamiento de la psoriasis, la composición que comprende: (a) propionato de halobetasol […]
Cápsulas blandas entéricas de liberación controlada de ésteres de fumarato, del 1 de Julio de 2020, de Banner Life Sciences LLC: Una composición farmacéutica oral que comprende una cápsula blanda entérica que encapsula fumarato de monometilo suspendido en una matriz líquida […]
Composiciones de mentol líquido, del 1 de Julio de 2020, de Ddrops Company: Una composición para usar como remedio en el tratamiento de la tos o síntomas de resfriados, con o sin síntomas de gripe, donde dicha composición comprende: […]
Composición autoemulsionante de ácidos grasos omega-3, del 24 de Junio de 2020, de MOCHIDA PHARMACEUTICAL CO., LTD.: Una preparación autoemulsionante encapsulada que tiene una composición autoemulsionante que comprende, cuando se define que la composición autoemulsionante […]