Síntesis enzimática de carba-NAD.
Un método para la síntesis de carba-NAD o un análogo del mismo,
comprendiendo el método los pasos dea) fosforilar el compuesto de Fórmula I con la ayuda de una enzima quinasa nicotinamida ribosa (NRK),
Fórmula I
en la que R1 es OH, NH2, O-metilo o N-dimetilo, metilo, Y-es un contraión y X es O o S,
b) adenilar el producto fosforilado del paso (a) con un compuesto de Fórmula II con la ayuda de una enzima NMNAT.
Fórmula II
en el que R2 es NH2, OH, o NHalquilo,
en el que R3 es H, OH, NH2,
obteniendo de este modo carba-NAD o un análogo del mismo de fórmula III.
Fórmula III
en el que, R1, R2, R3, Y y X son como se han definido anteriormente.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/004523.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Inventor/es: HEINDL, DIETER, HORN, CARINA, MEIER, THOMAS, SCHMUCK,RAINER,DR, DUEFEL,Hartmut.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12P19/32 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › con un sistema cíclico condensado, que contiene un ciclo de seis miembros, con dos átomos de nitrógeno en el mismo ciclo, p. ej. nucleótidos púricos, dinucleótido de la nicotinamida-ademina.
PDF original: ES-2425631_T3.pdf
Fragmento de la descripción:
Síntesis enzimática de carba-NAD
Campo de la invención La invención se refiere a la síntesis enzimática de los análogos estables de nicotinamida adenina dinucleótido NAD / NADH y nicotinamida adenina dinucleótido fosfato NADP / NADPH, denominados "carba-NAD", es decir, análogos de NAD / NADH o NADP / NADPH, respectivamente, que comprende un azúcar carbacíclico en lugar de ribosa.
Antecedentes de la invención Los sistemas de medición para análisis bioquímicos son componentes importantes de los métodos de análisis clínicamente relevantes. Esto se refiere principalmente a la medición de analitos, por ejemplo, metabolitos o sustratos que se determinan directa o indirectamente con la ayuda de una enzima. Con frecuencia un analito de interés se convierte con la ayuda de un complejo enzima-coenzima y posteriormente se cuantifica a través de esta reacción enzimática. En este proceso, el analito a determinar en condiciones de reacción apropiadas se pone en contacto con una enzima adecuada y una coenzima mediante las cuales se cambia la coenzima por ejemplo, oxidada o reducida por la reacción enzimática. Este proceso se puede detectar electroquímicamente o fotométricamente ya sea directamente o por medio de un mediador. Por lo general, una curva de calibración proporciona una correlación directa entre el valor medido y la concentración del analito de interés y la concentración del analito se puede determinar de este modo.
Las coenzimas son moléculas orgánicas que están covalentemente o no covalentemente unidas a una enzima y están modificadas por la conversión del analito. Ejemplos prominentes de coenzimas son la dinucleótido de nicotinamida adenina (NAD) y nicotinamida adenina dinucleótido fosfato (NADP) de la que el NADH y el NADPH, respectivamente, se forman por reducción.
Como se describe en US 2008/0213809, las desventajas de los sistemas de medición convencionales, por ejemplo, un período de validez limitado, requisitos especiales para las condiciones de almacenamiento como la refrigeración o el almacenamiento liofilizado con el fin de lograr una mejor vida en estantería puede, al menos en gran medida, ser superados por los derivados estables de nicotinamida adenina dinucleótido (NAD / NADH) y nicotinamida adenina dinucleótido fosfato (NADP / NADPH) descritos allí. Estos análogos estables de NAD (P) H son apropiados para evitar resultados erróneos causados por un almacenamiento incorrecto, desapercibido, o defectuoso que es especialmente importante, por ejemplo, en el caso de los ensayos que se llevan a cabo por los usuarios finales así como la automonitorización de glucosa.
Como se describe en US 2008/0213809 la síntesis química de carba-NAD es extremadamente difícil, requiere al menos 8 etapas de síntesis, tiene lugar un bajo rendimiento global y por lo tanto es bastante caro. La ruta química para la síntesis de carba-NAD se representa en la Figura 1. Se necesitan con urgencia rutas alternativas de síntesis.
Por lo tanto un objeto de la presente invención es proporcionar carba-NAD de una manera menos engorrosa, con altos rendimientos y a un coste atractivamente bajo.
Se ha encontrado ahora sorprendentemente que es posible utilizar enzimas en lugar de la química convencional con el fin de proporcionar carba-NAD de una forma adecuada y coste-efectiva.
Resumen de la invención La presente invención se refiere a un método para la síntesis de carba-NAD o un análogo del mismo, comprendiendo el método los pasos de a) fosforilar un 3-carbamoil-1- (2, 3-dihidroxi-4-hidroximetil-ciclopentil) piridinio-metanosulfonato o un análogo del mismo por la ayuda de una enzima NRK, b) adenilar el producto fosforilado del paso (a) con adenosina o un compuesto estructuralmente relacionado, con la ayuda de una enzima NMN-AT obteniendo de este modo carba-NAD o un análogo de la misma.
Descripción detallada de la invención La presente invención se refiere a un método para la síntesis de carba-NAD o un análogo del mismo, comprendiendo el método los pasos de a) fosforilar el compuesto de Fórmula I con la ayuda de una enzima quinasa nicotinamida ribosa (NRK) ,
Fórmula I
en la que R1 es OH, NH2, O-metilo o N-dimetilo, metilo, Y-es un contraión y X es O o S, b) adenilar el producto fosforilado del paso (a) con un compuesto de Fórmula II con la ayuda de una enzima NMN-AT. 10 Fórmula II
en el que R2 es NH2, OH, o NHalquilo,
en el que R3 es H, OH, NH2, obteniendo de este modo carba-NAD o un análogo del mismo de fórmula III. Fórmula III
en el que, R1, R2, R3, Y y X son como se han definido anteriormente.
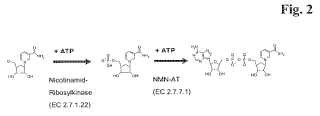
El método anterior también se ilustra por el esquema de reacción mostrado en la Figura 2.
El término "carba-" se utiliza para indicar que en lugar de un residuo de azúcar ribosilo está presente un 2, 3dihidroxiciclopentano. En otras palabras, un carba-análogo oxidado de nicotinamida adenina dinucleótido (NAD ') , por ejemplo, es un compuesto por lo demás idéntico a (NAD') , excepto que un anillo de 2, 3-dihidroxiciclopentano reemplaza el anillo D-ribonucleótido de la porción nicotinamida ribósido (Slama, JT y Simmons, AM, Biochemistr y 27
(1988) 1831) .
Las enzimas se conocen como catalizador altamente específico para permitir que se produzcan reacciones en condiciones más o menos fisiológicas que en su ausencia requieren condiciones severas o que incluso a veces son casi imposible de alcanzar. Con el fin de realizar este tipo de reacciones específicas y, como resultado de la evolución a través de generaciones y generaciones bajo presión selectiva, las enzimas tienden a ser muy específicas tanto con respecto a la especificidad de sustrato, así como con respecto a la reacción catalizada. Ahora se ha encontrado sorprendentemente que quinasas de nicotinamida ribosa aceptan los compuestos de piridinio de fórmula I que comprenden un anillo en lugar de un residuo ribosil como un sustrato de 2, 3 dihidroxiciclopentano y son capaces de fosforilar estos compuestos.
Las quinasas nicotinamida ribosa (NRK) según la nomenclatura de las enzimas internacionales se agrupan en la clase EC 2.7.1.22 (ATP: N-ribosilnicotinamida 5'-fosfotransferasas) . Una enzima escogida de la clase EC 2.7.1.22 se utiliza en un método de acuerdo con la presente invención con el fin de fosforilar un compuesto de Fórmula I. Las NRK preferidas son las que se conocen a partir de Saccharomyces cerevisiae, Pseudomonas aeruginosa, Streptococcus Sanguinius y Homo sapiens. También se prefieren las NRK utilizadas en un método de acuerdo con la presente invención son las conocidas de Streptococcus Sanguinius y de Homo sapiens. En una forma de realización preferida, la NRK1 como se conoce a partir de Homo sapiens se utiliza con el fin de llevar a cabo el primer paso en un método de acuerdo con la presente invención.
Como se indica en la Fórmula I no sólo carba-nicotinamida con R1 siendo NH2, sino también otros compuestos como los análogos de carba-nicotinamida definidos y resumidos por las alternativas dadas para R1 representa un sustrato apropiado para ciertas enzimas NRK. Armado con la descripción de la presente invención, el experto en la materia no tendrá ningún problema para investigar los compuestos de Fórmula I, así como compuestos relacionados por su capacidad para ser fosforilados eficazmente por una enzima NRK. Los compuestos de piridinio tal como se definen en la Fórmula I se utilizan para la fosforilación enzimática en un método de acuerdo con la presente invención. Un análogo de nicotinamida es un compuesto tal como se define en la Fórmula I, en el que R1 no es NH2. Preferiblemente R1 de la fórmula I se selecciona de entre el grupo que consiste en OH, NH2 y O-metilo. En una forma de realización preferida R1 es OH y en otra realización preferida R1 es NH2. Alquilo en R1 o R2 es preferiblemente alquilo C1 a C6 lineal o ramificado, preferiblemente alquilo lineal.
El residuo X en la fórmula I pueden ser o bien O o S. En una forma de realización preferida X en la Fórmula I es O.
El contraión Y- se selecciona preferiblemente del grupo que consiste de metilsulfonato, Cl-, PF6-, BF4-, y ClO4-. También se prefiere el contraión es BF4- o metilsulfonato.
Sorprendentemente, las adeniltransfereasas de nucleótidos de nicotinamida (NMN-AT) pueden utilizar la carbanicotinamida fosforilada obtenida como se ha descrito anteriormente como moléculas aceptoras y son capaces de adenilar estos compuestos. En el segundo paso la síntesis enzimática de carba-NAD o un análogo del mismo un mononucleótido de nicotinamida adeniltransferasa se utiliza así para transferir un residuo de adenilo o un análogo del mismo a la carbo-nicotinamida fosforilada o un análogo del mismo,... [Seguir leyendo]
Reivindicaciones:
1. Un método para la síntesis de carba-NAD o un análogo del mismo, comprendiendo el método los pasos de a) fosforilar el compuesto de Fórmula I con la ayuda de una enzima quinasa nicotinamida ribosa (NRK) , Fórmula I
en la que R1 es OH, NH2, O-metilo o N-dimetilo, metilo, Y-es un contraión y X es O o S,
b) adenilar el producto fosforilado del paso (a) con un compuesto de Fórmula II con la ayuda de una enzima NMN-AT.
Fórmula II
en el que R2 es NH2, OH, o NHalquilo,
en el que R3 es H, OH, NH2,
obteniendo de este modo carba-NAD o un análogo del mismo de fórmula III. 25 Fórmula III
en el que, R1, R2, R3, Y y X son como se han definido anteriormente.
2. El método de la reivindicación 1, en el que dicha enzima NRK se selecciona de NRK conocidas a partir de Saccharomyces cerevisiae, Pseudomonas aeruginosa, Streptococcus Sanguinius y Homo sapiens.
3. El método de la reivindicación 1 o 2, en el que dicho NMN-AT se selecciona del grupo que consiste en el NMN-AT
conocido de Bacillus subtilis, Escherichia coli, janashii Methanococcus, Sulfolobus solfataricus, Saccharomyces 35 cerevisiae y Homo sapiens.
4. El método de acuerdo con cualquiera de las reivindicaciones 1 a 3, en el que en el compuesto R1 de fórmula I se selecciona del grupo que consiste en OH, NH2 y O-metilo.
5. El método de acuerdo con cualquiera de las reivindicaciones 1 a 3, en el que en el compuesto R2 de fórmula II es NH2 u OH.
6. El método de acuerdo con cualquiera de las reivindicaciones 1 a 3, en el que el compuesto R3 de fórmula II es H 5 o OH.
7. El método de acuerdo con cualquiera de las reivindicaciones 1 a 3, en el que en el compuesto X de la Fórmula I es O.
8. El método de acuerdo con cualquiera de las reivindicaciones anteriores, en el que R1 es NH2, R2 es NH2, R3 es H y X es O.
Patentes similares o relacionadas:
Genes y proteínas para la síntesis de alcanoil-CoA, del 6 de Diciembre de 2017, de NATIONAL RESEARCH COUNCIL OF CANADA: Una molécula de ácido nucleico aislada o purificada que comprende una secuencia de nucleótidos que tiene al menos un 77 % de identidad de […]
Base de sabor para la intensificación del gusto natural y proceso para su obtención, del 16 de Noviembre de 2016, de NESTEC S.A.: Un proceso de fabricación de una base de sabor que intensifica el gusto, dicha base contiene: - entre el 8 y el 80 % de compuestos derivados de modo natural elegidos […]
Microorganismo que tiene un ciclo de fijación de dióxido de carbono introducido en el mismo, del 14 de Septiembre de 2016, de MITSUI CHEMICALS, INC.: Un microorganismo productor de acetil-CoA que comprende un ciclo de producción de acetil-CoA obtenido confiriendo al menos un tipo de actividad enzimática […]
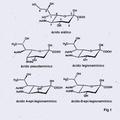 Biosíntesis de ácido CMP-legionamínico a partir de fructosa-6-P, del 16 de Diciembre de 2015, de NATIONAL RESEARCH COUNCIL OF CANADA: Un método de síntesis que comprende:
(a) hacer reaccionar GDP-N-acetil-glucosamina, dinucleótido nicotinamida adenina (NAD) y LegB (4,6- 5 deshidratasa […]
Biosíntesis de ácido CMP-legionamínico a partir de fructosa-6-P, del 16 de Diciembre de 2015, de NATIONAL RESEARCH COUNCIL OF CANADA: Un método de síntesis que comprende:
(a) hacer reaccionar GDP-N-acetil-glucosamina, dinucleótido nicotinamida adenina (NAD) y LegB (4,6- 5 deshidratasa […]
Mutante de aminasa 5''-xmp específico de amoníaco, del 16 de Abril de 2014, de CJ CHEILJEDANG CORPORATION: Un mutante de aminasa 5'-XMP específico de amoníaco, preparado sustituyendo cisteína en la posición 86 de aminasa 5'-XMP con alanina, serina o glicina, […]
Bacteria que puede producir una sustancia de purina y procedimiento para producir una sustancia de purina, del 23 de Abril de 2013, de AJINOMOTO CO., INC.: Procedimiento para producir una sustancia derivada de purina, que comprende: cultivar una bacteria perteneciente al género Bacillus que presenta una capacidad de […]
Una base sabrosa potenciadora del sabor natural y un proceso para su preparación, del 15 de Abril de 2013, de NESTEC S.A.: Una base sabrosa potenciadora del sabor que incluye: - una cantidad de entre el 10 y el 80 % del peso de compuestos derivados de manera natural seleccionados […]
 PROCEDIMIENTO PARA PRODUCIR METABOLITOS SINTETIZADOS BIOLÓGICAMENTE MEDIANTE PIROFOSFATO DE FOSFORRIBOSILO, del 7 de Enero de 2011, de KYOWA HAKKO BIO CO., LTD: Se proporciona un procedimiento industrial más ventajoso para la producción de metabolitos sintetizados biológicamente vía fosforibosil pirofosfato (PRPP), haciendo […]
PROCEDIMIENTO PARA PRODUCIR METABOLITOS SINTETIZADOS BIOLÓGICAMENTE MEDIANTE PIROFOSFATO DE FOSFORRIBOSILO, del 7 de Enero de 2011, de KYOWA HAKKO BIO CO., LTD: Se proporciona un procedimiento industrial más ventajoso para la producción de metabolitos sintetizados biológicamente vía fosforibosil pirofosfato (PRPP), haciendo […]