Separación de estereoisómeros de N,N-dialquilamino-2-alquil-3-hidroxi-3-fenil-alcanos.
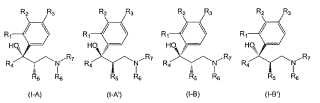
Procedimiento para aislar un estereoisómero de una mezcla que incluye los dos estereoisómeros de fórmulasgenerales (I-A) y (I-A') y/o los dos estereoisómeros de fórmulas generales (I-B) y (I-B')
donde
R1,
R2 y R3, iguales o diferentes, se seleccionan de entre el grupo consistente en -H, -F, -Cl, -alquilo(C1-C6), -Salquilo(C1-C6), -OH, -O-alquilo(C1-C6), -O-alquilen(C1-C6)fenilo, -OCO-alquilo(C1-C6), -OCON(alquilo(C1-C6))2 y-O-SiR8R9R10 (siendo R8, R9 y R10, iguales o diferentes, -alquilo(C1-C6) o -fenilo);
R4 es -H o -alquilo(C1-C6);
R5 es -alquilo(C1-C6); y
R6 y R7, iguales o diferentes, son -H o -alquilo(C1-C6);
siendo "alquilo(C1-C6)" un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógenos, iguales o diferentes,seleccionados entre -F, -Cl y -Br; y siendo "alquileno(C1-C6)" un grupo hidrocarburo saturado, lineal oramificado, cíclico o de cadena abierta, de 1 a 6 átomos de carbono, en caso dado sustituido con 1 a 6 átomosde halógenos, iguales o diferentes, seleccionados entre -F, -Cl y -Br;
o sus sales con ácidos orgánicos o inorgánicos;
que incluye los pasos de:
a) influir en la proporción de mezcla de los estereoisómeros mezclados de modo que al menos uno de losestereoisómeros, preferentemente el estereoisómero a aislar, esté presente en un exceso enantiomérico; y
b) añadir ácido fosfórico bajo condiciones que provocan la precipitación del estereoisómero presente en unexceso enantiomérico desde una solución en forma de fosfato, hidrogenofosfato o dihidrogenofosfato.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/005101.
Solicitante: GRUNENTHAL GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ZIEGLERSTRASSE 6 52078 AACHEN ALEMANIA.
Inventor/es: BUSCHMANN, HELMUT, HEINRICH, HELL, WOLFGANG.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C213/10 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 213/00 Preparación de compuestos que contienen grupos amino e hidroxi, amino e hidroxi eterificados o amino e hidroxi esterificados unidos a la misma estructura carbonada. › Separación; Purificación; Estabilización; Empleo de aditivos.
- C07C217/72 C07C […] › C07C 217/00 Compuestos que contienen grupos amino e hidroxi eterificados unidos a la misma estructura carbonada. › unidos a través de cadenas carbonadas con al menos tres átomos de carbono entre los grupos amino y el ciclo aromático de seis miembros o el sistema cíclico condensado que contiene este ciclo.
PDF original: ES-2403418_T3.pdf
Fragmento de la descripción:
Separación de estereoisómeros de N, N-dialquilamino-2-alquil-3-fenil-alcanos
La invención se refiere a un procedimiento para separar estereoisómeros de N, N-dialquilamino-2-alquil-3-hidroxi-3-fenilalcanos.
Los opioides vienen utilizándose hace años como analgésicos para el tratamiento del dolor, aunque presentan una serie de efectos secundarios, por ejemplo adicción y dependencia, depresión respiratoria, inhibición gastrointestinal y estreñimiento. Por ello, sólo se pueden administrar en dosis altas durante un período de tiempo prolongado con medidas de precaución especiales, tales como normas de prescripción especiales.
Es conocido que determinados N, N-dialquilamino-2-alquil-3-hidroxi-3-fenil-alcanos (en particular compuestos 1-fenil-3dimetilaminopropano) tienen efecto analgésico y no provocan los efectos secundarios típicos de los opioides. Estas sustancias se caracterizan por un marcado efecto analgésico claramente reforzado, por ejemplo en comparación con el opioide tramadol.
Estos N, N-dialquilamino-2-alquil-3-hidroxi-3-fenil-alcanos de efecto analgésico son quirales. Dado que en la mayoría de los casos tienen dos centros quirales, los compuestos se presentan en forma de 4 estereoisómeros, esto es dos pares de enantiómeros que son diastereoisoméricos entre sí.
Con frecuencia, la eficacia de un analgésico se atribuye a su interacción con un receptor determinado de una célula humana o animal. Debido a que estos receptores están formados por aminoácidos quirales, y en caso dado también glucósidos quirales, su interacción con medicamentos quirales es estereoselectiva. Por ello, los estereoisómeros individuales de los medicamentos quirales frecuentemente tienen diferente eficacia farmacológica.
J.R. Dehli y col. (Tetrahedron: Asymmetr y , vol. 12, nº 10, 2001, páginas 1485-1492) describieron la obtención estereoselectiva mediante biocatalizadores de a-alquil-1-hidroxinitrilos a partir de 1-cetonitrilos por introducción de un grupo alquilo y reducción del grupo carbonilo. Los a-alquil-1-hidroxinitrilos quirales pueden ser utilizados como precursores para obtener aminoalcoholes.
L. Angliolini y col. (Tetrahedron, vol. 25, 1969, páginas 4211-4216) describieron la síntesis estereoespecífica de (±) -1fenil-1, 2-dimetil-3-dimetilaminopropan-1-oles mediante reacción de un reactivo de Grignard adecuado con a-metil-1dimetilamino-propiofenona o 3-metil-4-dimetilamino-2-butanona.
Ninguno de estos dos procedimientos incluye la separación de mezclas estereoisoméricas.
Por consiguiente, es necesario un procedimiento para separar los estereoisómeros, esto es los diastereoisómeros y enantiómeros de N, N-dialquilamino-2-alquil-3-hidroxi-3-fenil-alcanos.
El documento EP-A 693 475 describe la síntesis de (2RS, 3RS) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol. La separación de los diastereoisómeros, es decir de los dos pares de enantiómeros, se lleva a cabo por precipitación en forma de clorhidrato con trimetilclorosilano/agua en 2-butanona. La separación de la mezcla racémica de los dos enantiómeros de configuración (2R, 3R) y (2S, 3S) tiene lugar en columna HPLC quiral.
Sin embargo, en general, la separación cromatográfica de enantiómeros en fases estacionarias quirales no es adecuada para grandes cantidades de principio activo, sirviendo, en la mayoría de los casos, sólo para fines analíticos. Por ello es necesario un procedimiento que también sea adecuado para separar los enantiómeros de N, N-dialquilamino-2-alquil-3hidroxi-3-fenil-alcanos quirales a escala preparativa.
Así, la invención tiene por objeto proporcionar un procedimiento para la separación de los estereoisómeros, preferentemente enantiómeros, de N, N-dialquilamino-2-alquil-3-hidroxi-3-fenil-alcanos quirales que también se pueda llevar a cabo a escala de gramos y kilogramos. El procedimiento debería ser económico, tener un alto rendimiento y asegurar una alta pureza enantiomérica.
Este objetivo se resuelve según el objeto de las reivindicaciones. Sorprendentemente se ha comprobado que es posible aislar un estereoisómero de una mezcla que incluye los dos estereoisómeros de fórmulas generales (I-A) y (I-A’) y/o los dos estereoisómeros de fórmulas generales (I-B) y (I-B’) ,
donde R1, R2 y R3, iguales o diferentes, se seleccionan de entre el grupo consistente en -H, -F, -Cl, -alquilo (C1-C6) , -Salquilo (C1-C6) , -OH, -O-alquilo (C1-C6) , -O-alquilen (C1-C6) fenilo, -OCO-alquilo (C1-C6) , -OCON (alquilo (C1-C6) ) 2 y -O-SiR8R9R10 (siendo R8, R9 y R10, iguales o diferentes, -alquilo (C1-C6) o -fenilo) ;
R4 es -H o -alquilo (C1-C6) ;
R5 es -alquilo (C1-C6) ; y
R6 y R7, iguales o diferentes, son -H o -alquilo (C1-C6) ;
siendo "alquilo (C1-C6) " un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6 átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógenos, iguales o diferentes, seleccionados entre -F, -Cl y -Br; y siendo "alquileno (C1-C6) " un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6 átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógenos, iguales o diferentes, seleccionados entre -F, -Cl y -Br;
o sus sales con ácidos orgánicos o inorgánicos;
mediante un procedimiento que incluye los pasos de:
a) influir en la proporción de mezcla de los estereoisómeros mezclados de modo que al menos uno de los estereoisómeros, preferentemente el estereoisómero a aislar, esté presente en un exceso enantiomérico; y
b) añadir ácido fosfórico bajo condiciones que provocan la precipitación del estereoisómero presente en un exceso enantiomérico desde una solución en forma de fosfato, hidrogenofosfato o dihidrogenofosfato.
Sorprendentemente se ha comprobado que es posible cristalizar los estereoisómeros individuales con una alta estereoselectividad a partir de la mezcla de los estereoisómeros cuando al menos uno de ellos no está presente en mezcla racémica, sino con un exceso enantiomérico.
Los compuestos de fórmula general (I) presentan al menos dos centros quirales. Los compuestos se pueden sintetizar de diferentes modos. Por ejemplo, en primer lugar se puede producir una base de Mannich según una reacción de Mannich, con lo que se genera el primer centro quiral:
Cuando la reacción de Mannich se lleva a cabo sin inducción quiral, es decir en ausencia de sustancias auxiliares quirales, catalizadores quirales, disolventes quirales, etc., la base de Mannich se obtiene en forma de una mezcla racémica, ya que los estados de transición que conducen a las dos bases de Mannich enantioméricas son enantiomorfos y, en consecuencia, de igual energía.
El segundo centro quiral se puede introducir por ejemplo sometiendo a reacción el carbonilo de la base de Mannich con un reactivo de Grignard:
Así, a partir de la base de Mannich racémica se forman los cuatro estereoisómeros de N, N-dialquilamino-2-alquil-3hidroxi-3-fenil-alcanos de fórmula general (I-A) , (I-A’) , (I-B) e (I-B’) . Dependiendo del patrón de sustitución en los dos centros quirales se obtiene respectivamente la configuración R o S.
En principio también es posible la presencia de otros centros quirales en una de las cadenas laterales. En caso de tres centros quirales, la cantidad de estereoisómeros aumenta a ocho en total, existiendo cuatro pares de enantiómeros. Preferentemente, los N, N-dialquilamino-2-alquil-3-hidroxi-3-fenil-alcanos sólo presentan dos centros quirales.
Preferentemente, por un lado los estereoisómeros (I-A) y (I-A’) por un lado y por otro los estereoisómeros (I-B) y (I-B’) son en cada caso enantioméricos entre sí. Por lo demás, los estereoisómeros son diastereoisoméricos entre sí. Por consiguiente, preferentemente el estereoisómero (I-A) es enantiomérico con respecto a (I-A’) y diastereoisomérico con respecto a (I-B) y (I-B’) , el estereoisómero (I-A’) es enantiomérico con respecto a (I-A) y diastereoisomérico con respecto a (I-B) y (I-B’) , el estereoisómero (I-B) es diastereoisomérico con respecto a (I-A) y (I-A’) y enantiomérico con respecto a (I-B’) y, por último, el estereoisómero (I-B’) es diastereoisomérico con respecto a (I-A) y (I-A’) y enantiomérico con respecto a (I-B) .
Si en el paso (a) del procedimiento según la invención se influye en la proporción de mezcla de los estereoisómeros en la mezcla de modo que el estereoisómero de fórmula general (I-A’) esté presente en un exceso enantiomérico, el exceso se refiere a la cantidad de su enantiómero, es decir preferentemente al estereoisómero... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para aislar un estereoisómero de una mezcla que incluye los dos estereoisómeros de fórmulas generales (I-A) y (I-A’) y/o los dos estereoisómeros de fórmulas generales (I-B) y (I-B’)
donde R1, R2 y R3, iguales o diferentes, se seleccionan de entre el grupo consistente en -H, -F, -Cl, -alquilo (C1-C6) , -Salquilo (C1-C6) , -OH, -O-alquilo (C1-C6) , -O-alquilen (C1-C6) fenilo, -OCO-alquilo (C1-C6) , -OCON (alquilo (C1-C6) ) 2 y -O-SiR8R9R10 (siendo R8, R9 y R10, iguales o diferentes, -alquilo (C1-C6) o -fenilo) ;
R4 es -H o -alquilo (C1-C6) ;
R5 es -alquilo (C1-C6) ; y
R6 y R7, iguales o diferentes, son -H o -alquilo (C1-C6) ;
siendo "alquilo (C1-C6) " un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6 átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógenos, iguales o diferentes,
seleccionados entre -F, -Cl y -Br; y siendo "alquileno (C1-C6) " un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6 átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógenos, iguales o diferentes, seleccionados entre -F, -Cl y -Br;
o sus sales con ácidos orgánicos o inorgánicos;
que incluye los pasos de:
a) influir en la proporción de mezcla de los estereoisómeros mezclados de modo que al menos uno de los estereoisómeros, preferentemente el estereoisómero a aislar, esté presente en un exceso enantiomérico; y b) añadir ácido fosfórico bajo condiciones que provocan la precipitación del estereoisómero presente en un exceso enantiomérico desde una solución en forma de fosfato, hidrogenofosfato o dihidrogenofosfato.
2. Procedimiento según la reivindicación 1, caracterizado porque la influencia ejercida en el paso (a) se produce 25 por
adición del estereoisómero que ha de estar presente en exceso, o por síntesis enantioselectiva de los estereoisómeros.
3. Procedimiento según la reivindicación 1 o 2, caracterizado porque el exceso enantiomérico es de al menos un 1, 0% ee.
4. Procedimiento según cualquiera de las reivindicaciones anteriores, caracterizado porque R1 y R3 son en cada caso -H y R2 es -OCH3.
5. Procedimiento según cualquiera de las reivindicaciones anteriores, caracterizado porque R4 es -CH3CH3 y R5, R6 y R7 son en cada caso -CH3.
6. Procedimiento según cualquiera de las reivindicaciones anteriores, caracterizado porque incluye el paso de 35 c) separar la sal precipitada obtenida en el paso (b) de la solución sobrenadante.
7. Procedimiento según la reivindicación 6, caracterizado porque incluye el paso de d) transformar la sal separada en el paso (c) en el clorhidrato.
8. Sal de adición de un estereoisómero de fórmula general (I-A) , (I-A’) , (I-B) o (I-B’) tal como se define en la 5 reivindicación 1, 4 o 5 y ácido fosfórico.
9. Sal de adición según la reivindicación 8, seleccionada de entre el grupo consistente en fosfato de (2R, 3R) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, hidrogenofosfato de (2R, 3R) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, dihidrogenofosfato de (2R, 3R) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol,
fosfato de (2S, 3S) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, hidrogenofosfato de (2S, 3S) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, dihidrogenofosfato de (2S, 3S) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, fosfato de (2R, 3S) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, hidrogenofosfato de (2R, 3S) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol,
dihidrogenofosfato de (2R, 3S) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, fosfato de (2S, 3R) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, hidrogenofosfato de (2S, 3R) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol, dihidrogenofosfato de (2S, 3R) -1-dimetilamino-3- (3-metoxifenil) -2-metil-3-pentanol.
10. Procedimiento para preparar un estereoisómero de fórmula general (I-A) , (I-A’) , (I-B) o (I-B’)
donde
R1, R2 y R3, iguales o diferentes, se seleccionan de entre el grupo consistente en -H, -F, -Cl, -alquilo (C1-C6) , -S
alquilo (C1-C6) y -OH, con la condición de que al menos uno de los grupos R1, R2 y R3 sea -OH;
R4 es -H o -alquilo (C1-C6) ;
25 R5 es -alquilo (C1-C6) ; y
R6 y R7, iguales o diferentes, son -H o -alquilo (C1-C6) ;
o sus sales con ácidos orgánicos o inorgánicos;
que incluye el procedimiento según una de las reivindicaciones 1 a 9 donde al menos uno de los grupos R1, R2
30 y R3 es -O-alquilo (C1-C6) , -O-alquilen (C1-C6) fenilo, -OCON (alquilo (C1-C6) ) 2 u -O-SiR8R9R10; -OCO-alquilo (C1-C6) , -OCO2-alquilo (C1-C6) ,
siendo "alquilo (C1-C6) " un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6
átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógeno, iguales o diferentes, seleccionados
entre -F, -Cl y -Br; y
35 siendo "alquileno (C1-C6) " un grupo hidrocarburo saturado, lineal o ramificado, cíclico o de cadena abierta, de 1 a 6 átomos de carbono, en caso dado sustituido con 1 a 6 átomos de halógeno, iguales o diferentes,
seleccionados entre -F, -Cl y -Br.
11. Procedimiento según la reivindicación 10, caracterizado porque incluye el paso de:
e) transformar al menos uno de los grupos R1, R2 y R3, que consisten en -O-alquilo (C1-C6) , -O-alquilen (C1C6) fenilo, -OCO-alquilo (C1-C6) , -OCO2-alquilo (C1-C6) , -OCON (alquilo (C1-C6) ) 2 u -O-SiR8R9R10, en un grupo -OH.
Patentes similares o relacionadas:
Polimorfos de clorhidrato de 4-metilbenzoato de 4-[2-dimetilamino-1-(1-hidroxiciclohexil)etil]fenilo, métodos para la preparación de los mismos y uso de los mismos, del 6 de Noviembre de 2019, de Shan Dong Luye Pharmaceutical Co., Ltd: Una Forma Cristalina II de [clorhidrato de 4-metilbenzoato de 4-[2-dimetilamino-1-(1-hidroxiciclohexil)etil]fenilo], caracterizada porque la Forma Cristalina II muestra […]
Procedimiento para la preparación de cristales de clorhidrato de fingolimod, del 3 de Julio de 2019, de SYNTHON BV: Un procedimiento de preparación de la Forma 1 del clorhidrato de fingolimod cristalino de fórmula (1a):**Fórmula** representada por el patrón de […]
Síntesis de compuestos de carbomoilpiridona policíclica, del 27 de Febrero de 2019, de GILEAD SCIENCES, INC.: Un proceso para preparar un compuesto de Fórmula ß-1•J-1 de acuerdo con el siguiente esquema:**Fórmula** en el 15 que el proceso comprende hacer […]
Método para producir tensioactivo catiónico, del 10 de Diciembre de 2018, de KAO CORPORATION: Método para producir un tensioactivo catiónico que comprende las siguientes etapas: etapa 1: una etapa de obtener un éster de alcanolamina […]
Procedimiento para la fabricación de Ivabradina y de intermediarios de síntesis de la misma, del 27 de Abril de 2016, de LABORATORIO CHIMICO INTERNAZIONALE S.P.A.: Procedimiento para la preparación de (1S)-4,5-dimetoxi-1-(amoniometil)-benzociclobutano de fórmula (B) que comprende: (i) hacer reaccionar 4,5-dimetoxi-1-(amoniometil)-benzociclobutano […]
Compuestos que tienen una actividad antagonista de un receptor muscarínico y agonista de un receptor beta-2 adrenérgico, del 30 de Noviembre de 2015, de CHIESI FARMACEUTICI S.P.A.: Un compuesto de fórmula general I**Fórmula** En donde Q es un grupo de fórmula Q1, Q2, Q3, Q4, Q5 o Q6**Fórmula** Z es H u OH; Y es seleccionado […]
Separación de una mezcla de enantiómeros de (R)- y (S)-3-amino-1-butanol, del 30 de Julio de 2014, de BASF SE: Procedimiento para la separación de una mezcla de enantiómeros de (R)- y (S)-3-amino-1-butanol dado el caso protegidos en el átomo de oxígeno, que comprende […]
Separación de N,N,N''-trimetilbisaminoetiléter de mezclas que comprenden aminas terciarias o aminoalquiléteres terciarios, del 16 de Abril de 2014, de HUNTSMAN INTERNATIONAL LLC: Método para recuperar N,N,N'-trimetilbisaminoetiléter (A) a partir de su amida (B) que comprende las siguientes etapas: (a) transamidación […]