Proceso para la preparación de pimozide.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11159364.
Solicitante: INSTITUT UNIV. DE CIENCIA I TECNOLOGÍA, S.A.
Inventor/es: CASTELLS BOLIART,JOSEP, BAYARRI FERRER,Navidad, ECHEVERRÍA BEISTEGUI,Begoña, ESTÉVEZ COMPANY,CARLOS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D211/52 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 211/00 Compuestos heterocíclicos que contienen ciclos hidrogenados de piridina, no condensados con otros ciclos. › que tienen un radical arilo como el segundo sustituyente en posición 4.
PDF original: ES-2398740_T3.pdf
Fragmento de la descripción:
Proceso para la preparación de pimozide La presente invención se refiere al campo de los disolventes inertes útiles para llevar a cabo reacciones químicas y más concretamente, a su utilización para la preparación de pimozide.
ANTECEDENTES DE LA INVENCiÓN
Una adecuada selección del disolvente en las diferentes etapas de síntesis o de purificación puede mejorar el rendimiento del principio activo o determinar características tales como la forma cristalina del mismo, la pureza y la solubilidad. Por tanto, el disolvente es un parámetro crítico en la obtención de fármacos. Además, el nivel de disolventes residuales en el producto final debe reducirse hasta una cantidad aceptable que cumpla las especificaciones del producto conforme a los requisitos de seguridad. La directriz de disolventes residuales (CPMPIICH/283/95) y las ampliaciones posteriores establecen una clasificación y unos límites en los disolventes residuales basados en consideraciones de seguridad.
Algunos disolventes conocidos pueden producir toxicidades inaceptables o tener efectos medioambientales altamente perjudiciales, por lo que deben evitarse en la producción tanto del principio activo como del producto farmacéutico final. Entre este tipo de disolventes se encuentran el tetracloruro de carbono, 1, 2-dicloroetano, 1, 1dicloroeteno y 1, 1, 1-tricloroetano.
Otros disolventes asociados con un nivel de toxicidad inferior deben limitarse para proteger a los pacientes de potenciales efectos secundarios. Entre estos disolventes se encuentran el xileno, tolueno, metanol, hexano, N, Ndimetilformamida (DMF) , N, N-dimetilacetamida (DMA) , diclorometano, cloroformo, yacetonitrilo.
Entre los disolventes considerados menos tóxicos se encuentran la acetona, el etanol, el alcohol isopropílico (IPA) , el acetato de etilo, el dimetilsulfóxido (DMSO) , el éter etílico, la metiletilcetona (MEC) , la metilisobutilcetona (MISC) , el propanol y el tetrahidrofurano (THF) . Estos disolvente deben utilizarse cuando su uso esté justificado por el proceso o las características del producto.
Aunque debido a su inferior toxicidad, los disolventes pertenecientes al tercer grupo mencionado anteriormente son los preferidos, deben seguir utilizándose de acuerdo con la legislación vigente que establece los parámetros que permiten minimizar su impacto tanto sobre la salud humana como sobre el medio ambiente. De este modo, tomando como ejemplo la MISC, puesto que es uno de los disolventes más ampliamente utilizados en la industria química debido, entre otras razones, a su facilidad para solubilizar compuestos orgánicos y de ser eliminado del medio por evaporación, se puede observar que su utilización lleva asociada algunos riesgos. La peligrosidad intrínseca de la MISC se refleja esencialmente en sus propiedades físicas (P. eb.: 117-118 oC; Pv: 15 mmHg (20 OC) ) Y toxicológicas (LD5º (oral ratas) : 2.1 g/kg) , de tal forma que la legislación europea ha establecido valores límite ambientales y biológicos indicativos. En consecuencia, la legislación española ha incluido la MISC en la lista general de valores límite ambientales de exposición profesional, estableciendo un valor de exposición diaria 45 (VLA-ED) de 83 mg/m3 y un valor de exposición de corta duración (VLA-EC) de 208 mg/m3. La MISC presenta las siguientes frases de riesgo R: 11-20-36/37-66 ("Fácilmente inflamable. Nocivo por inhalación. Irrita los ojos y las vías respiratorias. La exposición repetida puede provocar sequedad o formación de grietas en la piel") . Desde el punto de vista de la seguridad, la MISC exhibe las siguientes frases S: 9-16-29 ("Consérvese el recipiente en lugar bien ventilado. Conservar alejado de toda llama o fuente de chispas -No fumar. No tirar los residuos por el desagüe") . Los códigos de peligrosidad de la "National Fire Protection Association" (NFPA) , puntúa con un 3 la inflamabilidad de la MISC y con un 2 su peligrosidad sobre la salud humana.
En el desarrollo de un principio activo farmacéutico, el objetivo inicial es encontrar una o varias rutas sintéticas que permitan obtener el compuesto de interés con un rendimiento aceptable. Esto conlleva utilizar condiciones de 55 reacción, incluidos los disolventes, que permitan conseguir dicho objetivo a escala de laboratorio. Además, deben tenerse en cuenta otros aspectos adicionales (por ejemplo, limitación de disolventes para cumplir con los requisitos del producto farmacéutico, de seguridad y medioambientales) , en una posterior etapa de optimización del proceso y, especialmente, en su escala industrial.
De este modo, en general, resulta de alto interés para la industria farmacéutica identificar y utilizar disolventes alternativos que permitan minimizar los problemas asociados a los disolventes habitualmente empleados en procesos conocidos de preparación de principios activos.
El documento 00243284 A 1 se refiere a un proceso para la preparación de pimozide con rendimientos entre el 75 y 65 el 80% usando como reactivos 1-cloro-4, 4-bis- ( 4-fluorofenil) -butano y 1- ( 4-piperidil) -2-benzimidazolinona y una mezcla de alcoholes C6-C9 como disolvente.
El documento JP5011373A 1 se refiere a un proceso de 2 etapas para la preparación de pimozide usando como reactivos 1-haI0-4, 4-di- (4-fluorofenil) butano (4) Y 1- (1-benzilpiperidin-4-il) -1 H-benzo[d]imidazol-2 (3H) -ona y DMF como disolvente.
DESCRIPCiÓN DE LA INVENCiÓN
Sorprendentemente, se ha encontrado que el glicerol formal permite llevar a cabo reacciones de obtención de 5
principios activos farmacéuticos en condiciones altamente seguras y no contaminantes. De este modo, el producto final, además de cumplir sobradamente con los requisitos de seguridad exigidos por la normativa existente debido a su baja toxicidad, presenta diversas ventajas adicionales.
El glicerol formal es una mezcla de dos isómeros, el 4-hidroximetil-1, 3-dioxolano y el 5-hidroxi-1, 3-dioxano. Estos 10 dos isómeros están presentes en una proporción constante del 40% y 60%, respectivamente. El glicerol formal es muy estable tanto bajo condiciones neutras como básicas y es inerte frente a los productos solubilizados que sean compatibles con las funciones alcohol y acetal. En medio ácido fuerte puede descomponerse liberando formaldehído y glicerol. Para evitar su descomposición es preferible que el pH del medio sea superior a 4. Es totalmente miscible en éter, acetona, aceites esenciales, alcoholes yagua. Además, es prácticamente inodoro, 15 presenta una muy baja toxicidad y es moderadamente biodegradable. Se conoce el uso del glicerol formal en áreas de la técnica como en la industria de la fundición y de fabricación de productos de uso doméstico, tintas y pinturas. En el campo farmacéutico y veterinario se ha utilizado como excipiente o vehículo en la fabricación de productos tales como soluciones inyectables. Sin embargo, en el estado de la técnica no se menciona o sugiere nada relacionado con el uso del glicerol formal como disolvente inerte en reacciones químicas para la obtención o purificación de fármacos.
En la Tabla 1 se muestran las propiedades físico-químicas de la MISC en comparación con las del glicerol formal. Los datos para la MISC han sido obtenidos a partir de la Ficha Internacional de Seguridad Química publicada por el Instituto Nacional de Seguridad e Higiene en el Trabajo. Los datos para el glicerol formal han sido obtenidos a partir
de la ficha de seguridad más reciente del fabricante de referencia.
Se puede observar que los puntos de ebullición y de inflamación del glicerol formal son aproximadamente 80°C superiores a los de la MISC y que la presión de vapor del glicerol formal es inferior a la de MISC, lo cual favorece un menor riesgo por exposición. Además, el glicerol formal presenta un mejor perfil toxicológico como lo demuestra la ausencia de frases R y de valores límite ambientales, así como una dosis letal por ingestión en ratas cinco veces superior. La menor inflamabilidad del glicerol formal, como indican los códigos de riesgo de la NFPA, ofrece ventajas en relación a la seguridad de su manipulación en planta química.
Tabla 1. Propiedades de la MISC y del glicerol formal 35
PROPIEDAD MIBC GLICEROL FORMAL
Color Líquido incoloro Líquido incoloro
Olor Olor característico Líquido inodoro
Punto de ebullición (oC) 117-118 192-193
Punto de inflamación (oC) 18 98
Punto de auto-inflamación (oC) 449 >400
Límites de explosividad (% v/v) 1.7 -7.6 No disponible
Presión de vapor (mmHg) 15 (exp., 20°C) 0.13 (calc., 25°C)
Densidad (25°C, g/mL) ) : 0, 801 1, 203
Solubilidad en H20 (gIL) 20 Miscible en todas proporciones
LD50 (oral, ratas, g/kg) 2.1 10
VLA-ED... [Seguir leyendo]
Reivindicaciones:
1. Proceso para la preparación de pimozide, caracterizado porque la reacción de obtención de dicho principio activo se lleva a cabo en glicerol formal como disolvente inerte a un pH superior a 4 y en el que dicha reacción es una sustitución nucleofílica SN2.
2. Proceso según la reivindicación 1, que comprende la reacción de la 4- (2-oxo-1-benzimidazolinil) -piperidina y 1cloro-4, 4-di- ( 4-fluorofenil ) butano.
3. Proceso según la reivindicación 2, en el que la reacción se lleva a cabo en presencia de una base en una cantidad comprendida entre 1 y 1, 2 equivalentes con respecto a la 4- (2-oxo-1-benzimidazolinil) -piperidina.
4. Proceso según cualquiera de las reivindicaciones 2 ó 3, en el que se añade yoduro potásico a la reacción como catalizador.
5. Proceso según cualquiera de las reivindicaciones 2 a 4, en el que la reacción se lleva a cabo a una temperatura comprendida entre 60 y 95°C.
6. Proceso según la reivindicación 5, en el que la reacción se lleva a cabo a una temperatura comprendida entre 80 Y 95°C.
7. Proceso según cualquiera de las reivindicaciones 2 a 6, en el que el glicerol formal está presente en una cantidad comprendida entre 3 y 10 mi por cada gramo de 4- (2-oxo-1-benzimidazolinil) -piperidina.
8. Proceso según la reivindicación 7, en el que dicho glicerol formal está presente en una cantidad comprendida entre 3 y 5 mi por cada gramo de 4- (2-oxo-1-benzimidazolinil) -piperidina.
Patentes similares o relacionadas:
Procedimiento para la preparación del éster etílico del ácido 1-(2-halogen-etil)-4-piperidina-carboxílico, del 24 de Julio de 2019, de OLON S.p.A: Un procedimiento para la preparación de un compuesto de fórmula (I) **Fórmula** en el que X es un grupo saliente seleccionado de un átomo […]
Profármacos de sales de amonio cuaternario, del 16 de Agosto de 2017, de Alkermes Pharma Ireland Limited: Un compuesto profármaco de un fármaco pariente que contiene aminaa terciariaa en el que dicho compuesto profármaco del fármaco pariente tiene la fórmula:**Fórmula** en el […]
Agentes antivirales para la hepatitis B, del 26 de Julio de 2017, de Novira Therapeutics Inc: Un compuesto de fórmula IV: **Fórmula** o sales farmacéuticamente aceptables del mismo; en donde R4 es H o alquilo C1-C6; cada R5 se selecciona independientemente […]
Derivado de piperidina novedoso, del 30 de Marzo de 2016, de MSD K.K: El compuesto 4-(2-metoxipirimidin-5-il)-9-(4-{3-[(2R)-2-metilpirrolidin-1-il]propoxi}fenil)-1-oxa-4,9-diazaespiro- [5,5]undecan-3-ona, o una sal farmacéuticamente […]
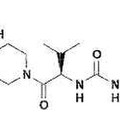 Derivado de piperidinilo como modulador de la actividad de los receptores de quimiocinas, del 1 de Enero de 2014, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Fórmula (I):**Fórmula**
o un estereoisómero o forma salina farmacéuticamente aceptable del mismo.
Derivado de piperidinilo como modulador de la actividad de los receptores de quimiocinas, del 1 de Enero de 2014, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Fórmula (I):**Fórmula**
o un estereoisómero o forma salina farmacéuticamente aceptable del mismo.
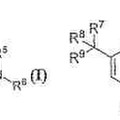 Derivados de benzamida y usos relacionados con los mismos, del 11 de Abril de 2013, de AMGEN INC.: Compuesto que tiene la fórmula (I):
o una sal, solvato o estereoisómero farmacéuticamente aceptable del mismo, en la que:
R1 es -OH;
R2 es metilo;
R3 […]
Derivados de benzamida y usos relacionados con los mismos, del 11 de Abril de 2013, de AMGEN INC.: Compuesto que tiene la fórmula (I):
o una sal, solvato o estereoisómero farmacéuticamente aceptable del mismo, en la que:
R1 es -OH;
R2 es metilo;
R3 […]
Proceso para la preparación de loperamida, del 2 de Mayo de 2012, de INSTITUT UNIV. DE CIENCIA I TECNOLOGÍA, S.A: Procedimiento para la preparación de loperamida o una sal de adición de ácido de la misma, caracterizado porquela reacción de obtención de dicha loperamida […]
DERIVADOS DE ARIL Y HETEROARIL-PIPERIDINCARBOXILATOS, SU PREPARACIÓN Y SU APLICACIÓN COMO INHIBIDORES DE LA ENZIMA FAAH, del 13 de Octubre de 2011, de SANOFI: Compuesto que responde a la fórmula general (I) : **Fórmula** elegido entre los compuestos de la siguiente tabla : en forma de base, de sal de adición a un ácido, de hidrato […]