Métodos y composiciones para suministrar polinucleótidos.
Un polipéptido recombinante del grupo de movilidad elevada, o un fragmento del mismo,
que comprende:
un polipéptido del factor de transcripción mitocondrial A (TFAM) que comprende al menos una caja HMGoperablemente enlazada a un dominio de transducción de proteína que está enlazado operablemente a unaseñal seleccionadora de dianas para un orgánulo no nuclear, en el que el polipéptido recombinante del grupode movilidad elevada se puede asociar con un polinucleótido para empaquetar el polinucleótido para elsuministro al orgánulo no nuclear.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/035137.
Solicitante: GENCIA CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 706 B FOREST ST. CHARLOTTESVILLE, VA 22903 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KHAN,SHAHARYAR.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01N37/18 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › A01N 37/00 Biocidas, productos que atraen o repelen a los animales perjudiciales, o reguladores del crecimiento de los vegetales, que contienen compuestos orgánicos que tienen un átomo de carbono que posee tres enlaces a heteroátomos, con a lo más dos enlaces a un halógeno, p. ej. ácidos carboxílicos (conteniendo ácidos ciclopropanocarboxílicos o sus derivados, p. ej. nítrilos de ácidos ciclopropanocarboxílicos, A01N 53/00). › que contienen el grupo —CO—N , p. ej. amidas o imidas de ácido carboxílico; Sus tioanálogos.
- A01N43/04 A01N […] › A01N 43/00 Biocidas, productos que atraen o repelen a los animales perjudiciales, o reguladores del crecimiento de los vegetales, que contienen compuestos heterocíclicos (que contienen anhídridos cíclicos, imidas cíclicas A01N 37/00; que contienen compuestos de fórmula , que no tienen más que un heterociclo en los que m≥1 y n≥0 y es una pirrolidina, una piperidina, una morfolina, una tiomorfolina, una piperazina o una polimetilenoimina, no sustituida o sustituida por un alcoilo, que tiene al menos cuatro grupos CH 2 A01N 33/00 - A01N 41/12; que contienen ácidos ciclopropanocarbhoxílicos o sus derivados, p. ej. ésteres con heterociclos, A01N 53/00). › con un heteroátomo.
- A61K38/00 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07H21/02 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con ribosilo como radical sacárido.
- C07K14/72 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › para hormonas.
- C12N15/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N15/62 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
- C12N15/63 C12N 15/00 […] › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N9/22 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Ribonucleasas.
- C12P19/34 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polinucleótidos, p. ej. ácidos nucleicos, oligorribonucleótidos.
- C12P21/06 C12P […] › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
PDF original: ES-2411962_T3.pdf
Fragmento de la descripción:
Métodos y composiciones para suministrar polinucleótidos ANTECEDENTES
1. CAMPO TÉCNICO
La presente descripción se refiere generalmente a composiciones y métodos para el suministro de polinucleótidos, más particularmente a composiciones y métodos para la transfección, por ejemplo transfección de orgánulos.
2. TÉCNICA RELACIONADA
Se han descrito muchas enfermedades mitocondriales que surgen de mutaciones homoplásmicas individuales en ADN mitocondrial (mtDNA) . Estas enfermedades afectan típicamente a tejidos no mitóticos (cerebro, retina, músculo) , presentes con fenotipos variables, y pueden aparecer esporádicamente y son intratables. Cada vez más pruebas implican a las anomalías del mtDNA en enfermedades tales como Parkinson y diabetes tipo II, pero siguen sin estar definidas las mutaciones etiológicas específicas para estas patologías. La comprensión de las relaciones genotipo-fenotipo de mtDNA y el desarrollo de un tratamiento específico para enfermedades a base de mtDNA está impedido por la incapacidad de manipular el genoma mitocondrial.
En el transcurso de la evolución, muchos organismos abordaron la tarea de introducir macromoléculas en células vivas. Aparte de los mecanismos de captación activos o mediados habitualmente por receptores, específicos de células, la solución general que ha surgido independientemente en muchas estirpes se basa en péptidos desarrollados específicamente para interaccionar con e insertarse en membranas bicapa lipídicas. De este modo, las colicinas bacterianas, las porinas humanas, y los dominios de transducción de proteína (PTD) de diversas especies comparten el motivo de una hélice alfa cargada positivamente, frecuentemente con una estructura anfipática, que es capaz de insertarse en membranas lipídicas, y suministrar intracelularmente cargas más grandes. Informes de investigación recientes confirman el uso exitoso de PTD fusionados a proteínas para su suministro a través de fronteras biológicas, incluyendo la barrera hematoencefálica, y la placenta.
Otro aspecto de gran importancia en el suministro de macromoléculas en organismos es la necesidad de protegerlas de la degradación proteolítica, nucleolítica e inmunitaria y su eliminación mientras atraviesan espacios extracelulares. Un enfoque usado a menudo es revestir ADN con proteínas capaces de sobrevivir al duro viaje hasta la diana. Las proteínas de la cápside vírica han tenido bastante éxito, aunque, para los fines de suministrar ADN a seres humanos, sufren un inconveniente significativo – la inmunogenicidad, la capacidad para provocar una fuerte reacción inmunitaria, reduciendo enormemente la eficacia de la terapia génica.
De este modo, existe la necesidad de composiciones y métodos mejorados para el suministro de polinucleótidos al interior de la célula.
Matsuhima et al, J. Biol. Chem., 278 (33) :31149-31158 (2003) en el documento titulado “functional domains of chicken mitochondrial transcription factor A for the maintenance of mitochondrial DNA copy number in lymphoma cell line DT40”, explica los dominios funcionales de varios polipéptidos TFAM.
El documento DE19856052 describe proteínas de fusión obtenidas entre las cadenas pesadas de la toxina tetánica y HMG 1.
En un primer aspecto de la presente invención, se proporciona un polipéptido del grupo de movilidad elevada recombinante, o un fragmento del mismo, que comprende:
un polipéptido del factor de transcripción mitocondrial A (TFAM) que comprende al menos una caja HMG operablemente enlazada a un dominio de transducción de proteína que está enlazado operablemente a una señal seleccionadora de dianas para un orgánulo no nuclear, en el que el polipéptido del grupo de movilidad elevada recombinante se puede asociar con un polinucleótido para empaquetar el polinucleótido para el suministro al orgánulo no nuclear.
Se proporcionan vehículos de suministro de polinucleótidos no víricos, y métodos para su uso. En general, la descripción proporciona proteínas de unión a polinucleótidos modificadas que comprenden un dominio de transducción de proteína operablemente enlazado a una señal seleccionadora de dianas, por ejemplo una señal seleccionadora de orgánulos no nucleares. Un aspecto proporciona un polipéptido que comprende al menos un dominio de la caja HMG, más típicamente al menos dos dominios de la caja HMG y al menos un dominio de transducción de proteína. El polipéptido se puede asociar con un polinucleótido, haciendo que el polinucleótido se condense. El polipéptido también puede revestir al polinucleótido. El revestimiento y/o condensación del polinucleótido ayuda a proteger de la degradación al polinucleótido. El dominio de transducción de proteína ayuda al complejo polipéptido-polinucleótido a atravesar membranas y a entrar en el interior de la célula o un orgánulo. La señal seleccionadora de dianas ayuda a dirigir el complemento hacia un sitio de interés, y suministrar de ese modo el polinucleótido.
Las composiciones descritas se pueden usar para suministrar polinucleótidos a localizaciones específicas en una célula, incluyendo, pero sin limitarse a, mitocondrias y cloroplastos. En algunos aspectos, los polinucleótidos codifican una proteína terapéutica o una proteína que compensa proteínas no funcionales o la ausencia de proteínas. En consecuencia, algunos aspectos proporcionan métodos para tratar enfermedades, por ejemplo enfermedades relacionadas con mitocondrias o cloroplastos.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
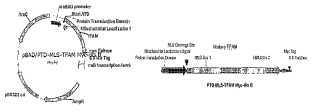
La Figura 1 es un diagrama de un diseño de plásmido ejemplar (izquierda) y una estructura proteica ejemplar (derecha) para TFAM con un dominio PTD seguido de una MLS.
La Figura 2 es un panel de micrografías de fluorescencia que muestra el transcurso de tiempo de mtDNA marcado con Alexa 488 (verde) complejado con PTD-MLS-TFAM añadido a células Sy5y. Red = MitoTracker Red.
Las Figuras 3A-C son micrografías de fluorescencia que muestran la tinción con MtRed y BrdU (FITC) de células rho0 (A) , SY5Y normales (B) y rho0 16 h después de la transfección con mtDNA complejado con PTD-MLS-TFAM (C) .
La Figura 4 es un gel de agarosa de productos de la PCR que amplifica la región alrededor de la mutación LHON 11778A después de SfaN1. Línea 1 - cíbrido LHON; Línea 2 - Sy5y; Línea 3 - Rho0; Línea 4 - Rho0 transfectada con LHON mtDNA; Línea 5 - Rho0 transfectada sin ADN.
La Figura 5A es una micrografía de fluorescencia que muestra células SY5Y normales 24 horas después de la transfección con mtDNA-MtEGFP clonada como un gen de fusión con ND6 en el sitio BamHI de mtDNA y coteñida con MiitoTracker Red.
La Figura 5B es una inmunotransferencia para EGFP usando anticuerpo JL-8 (Clontech) que muestra un producto de fusión proteico de 45 kDa entre ND6 y EGFP (flecha superior) , así como la EGFP de 33 kDa (flecha inferior) .
La Figura 6 es una inmunotransferencia de mtEGFP al silenciar con siRNA a PoIG después de cinco días. La línea final muestra el fracaso de EGFP siRNA para lograr el silenciamiento en un marco de tiempo similar.
La Figura 7A es un diagrama esquemático ejemplar de mtEGFP que contiene una señal de localización nuclear (NLS) y PTD clonado en mtDNA que contiene nuevos sitios de restricción, BgIII y NotI.
Las Figuras 7B-C son micrografías de fluorescencia que muestran células Sy5y que expresan NLS-mtEGFP-PTD que localiza a mitocondrias y el núcleo. (C) Las células se contratiñen con Mito Tracker Red.
La Figura 8A es un diagrama esquemático ejemplar del sitio BamHI erradicado en mtDNA, y BamHI-cDNA clonado en mtDNA.
La Figura 8B es un gel 24 horas después de la transfección, que muestra el fragmento de la PCR de mtDNA procedente de células que se digirieron con BamHI. La línea 1 no se digirió, y la línea 2 de mtDNA de control se digirió.
La Figura 8C es un gel que muestra lisados mitocondriales de células que se incubaron con ADN que contiene un sitio BamHI. Las células del control (línea 1) no muestran actividad de BamHI, mientras que las células transfectadas (línea 2) poseen actividad de BamHI.
La Figura 9 es un gel que muestra PTD-BgIII recombinante dirigido a mitocondrias que provocó la eliminación rápida de la proteína mtEGFP en células que expresan un mtDNA que posee un sitio de restricción BgIIImtEGFP, durante un período de tiempo de 5 días.
DESCRIPCIÓN DETALLADA
1. Definiciones Al describir y reivindicar la materia objeto descrita, se usará la siguiente terminología según las definiciones expuestas más abajo.
El término “polipéptidos” incluye proteínas y sus fragmentos. Los polipéptidos... [Seguir leyendo]
Reivindicaciones:
1. Un polipéptido recombinante del grupo de movilidad elevada, o un fragmento del mismo, que comprende:
un polipéptido del factor de transcripción mitocondrial A (TFAM) que comprende al menos una caja HMG operablemente enlazada a un dominio de transducción de proteína que está enlazado operablemente a una señal seleccionadora de dianas para un orgánulo no nuclear, en el que el polipéptido recombinante del grupo de movilidad elevada se puede asociar con un polinucleótido para empaquetar el polinucleótido para el suministro al orgánulo no nuclear.
2. El polipéptido de la reivindicación 1, en el que el polipéptido recombinante del grupo de movilidad elevada se asocia con 10 a 100 nucleótidos de un polinucleótido que se va a suministrar a un orgánulo seleccionado como diana, y de ese modo empaqueta el polinucleótido para el suministro al orgánulo seleccionado como diana.
3. El polipéptido de la reivindicación 1, en el que el polipéptido recombinante del grupo de movilidad elevada comprende una secuencia seleccionada de SEC ID NO. 210, o un fragmento de la misma, suficiente para la unión a un polinucleótido.
4. El polipéptido de la reivindicación 1, en el que la señal seleccionadora de dianas comprende una señal de localización mitocondrial o una señal de localización de cloroplastos.
5. El polipéptido de la reivindicación 4, en el que la señal de localización mitocondrial comprende una secuencia que tiene una homología de.
8. 100% con una señal de localización mitocondrial derivada de una proteína seleccionada del grupo que consiste en hexocinasa I, amino oxidasa (que contiene flavina) A, hexocinasa IV, forma celular beta pancreática, proteína relacionada con el receptor periférico de benzodiazepinas, metaxina 2, receptor de importación de proteína de membrana externa mitocondrial putativa (hTOM) , glutationa transferasa; canal aniónico 2 dependiente del voltaje (proteína de membrana mitocondrial externa porínica) , citocromo b5, receptor periférico de benzodiazepinas, anclaje de cinasa de célula germinal S-AKAP84, proteína de anclaje de cinasa A, precursor de carnitina O-palmitoiltransferasa I, hexocinasa II, amino oxidasa (que contiene flavina) B, ácido graso de cadena larga-CoA ligasa 2, ácido graso de cadena larga-CoA ligasa 1 (palmitoil-CoA ligasa) , canal aniónico 1 dependiente del voltaje, metaxina 1, translocasa de 34 kDa de membrana mitocondrial externa putativa humana hTOM34, canal aniónico 4 dependiente del voltaje (proteína porínica de la membrana mitocondrial externa) , citocromo-b5 reductasa, canal aniónico 3 dependiente del voltaje (proteína porínica de la membrana mitocondrial externa) , homólogo de la subunidad TOM20 del receptor de importación mitocondrial (proteína de la membrana externa de 20 kd mitocondrial) (receptor de la membrana mitocondrial externa TOM20) , precursor del homólogo de discos marginales tumorosos (HTID-1) , SEC ID Nos. 18-51, SEC ID Nos.
5. 188 y el polipéptido codificado por SEC ID No: 52.
6. El polipéptido de la reivindicación 4, en el que la señal de localización de cloroplastos tiene una homología del 80100% con una señal de localización de cloroplastos derivada de una proteína seleccionada del grupo que consiste en el dominio peptídico de tránsito de la proteína ribosomal de apicoblasto S9, péptido de señal de glutationa reductasa (GR) del guisante, término NH2 de Cr-RSH que codifica una guanosina 3’, 5’-bispirofosfato (ppGpp) sintasa-degradasa putativa, proteínas 14-3-3, partícula de reconocimiento de la señal de cloroplastos que incluye las subunidades cpSRP54, cpSRP43 o un fragmento de las mismas, péptidos de tránsito de cloroplastos AtOEP7 que incluye el dominio transmembránico (TMD) y su región de siete aminoácidos vecinos C-terminal, péptido de tránsito cloroplástico N-terminal THI 1, SEC. ID Nos.
19. 203, el polipéptido codificado por SEC ID No: 189, el polipéptido codificado por SEC ID No: 204 y el polipéptido codificado por SEC ID No: 205.
7. El polipéptido de la reivindicación 1, en el que el dominio de transducción de proteína comprende una pluralidad de restos de aminoácidos que tienen una carga neta positiva en condiciones fisiológicas.
8. El polipéptido de la reivindicación 7, en el que el dominio de transducción de proteína comprende 8-15 restos de aminoácidos.
9. El polipéptido de la reivindicación 1, en el que el dominio de transducción de proteína comprende 11 restos de arginina.
10. El polipéptido de la reivindicación 1, en el que el dominio de transducción de proteína se selecciona del grupo que consiste en YGRKKRRQRRR (SEC. ID. NO.: 1) , RKKRRQRRR (SEC. ID. NO. 2) , aminoácido.
4. 60 de la proteína de HIV-1 TAT, la tercera hélice de homeodominio de Antennapedia, RQIKIWFQNRRMKWKK (SEC. ID. NO.: 207) , una región de poliarginina, 7 restos de arginina, RRQRRTSKLMKR (SEC. ID. NO.: 7) , GWTLNSAGYLLGKINLKALAALAKKIL (SEC. ID. NO.: 8) , WEAKLAKALAKALAKHLAKALAKALKACEA (SEC. ID. NO.: 9) , un fragmento de los mismos, o una combinación de los mismos.
11. El polipéptido de cualquiera de las reivindicaciones 1-10, en el que el dominio de transducción de proteína facilita el atravesamiento de una membrana, y en el que la membrana es una membrana celular, una membrana plasmática, una membrana de orgánulo, una membrana de micela, una membrana bicapa, una membrana de una sola capa, una membrana de vesícula, una membrana nuclear, o una membrana mitocondrial.
12. Una composición que comprende:
(a) un polipéptido recombinante del grupo de movilidad elevada, o un fragmento del mismo, en el que el polipéptido recombinante del grupo de movilidad elevada, o un fragmento del mismo, comprende un polipéptido del factor A de transcripción mitocondrial (TFAM) que comprende al menos una caja HMG enlazada operablemente a un dominio de transducción de proteína que está enlazado operablemente a una señal seleccionadora de dianas para un orgánulo no nuclear, y
(b) un polinucleótido,
en la que el polinucleótido está asociado físicamente con el polipéptido recombinante del grupo de movilidad elevada, o fragmento del mismo.
13. La composición de la reivindicación 12, en la que la asociación física protege al polinucleótido de la degradación.
14. La composición de la reivindicación 12, en la que el polipéptido recombinante del grupo de movilidad elevada, o un fragmento del mismo, se une de forma reversible a una región del polinucleótido.
15. La composición de la reivindicación 12, en la que el polinucleótido comprende un promotor enlazado operablemente a una secuencia de ácido nucleico que codifica un polipéptido, siRNA, o un polinucleótido antisentido.
16. La composición de la reivindicación 12, en la que el polinucleótido comprende ARN, ADN, o una combinación de los mismos.
17. La composición de la reivindicación 12, en la que el polinucleótido comprende un dominio enzimático.
18. La composición de la reivindicación 12, en la que el polinucleótido comprende ARN enzimático o ADN enzimático.
19. La composición de la reivindicación 12, en la que el polinucleótido es monocatenario o multicatenario.
20. El polipéptido o composición de una cualquiera de las reivindicaciones 1 a 19, para uso en terapia.
21. Un método in vitro de empaquetamiento de un polinucleótido, que comprende:
combinar un polinucleótido con una cantidad de un polipéptido recombinante del grupo de movilidad elevada suficiente para empaquetar el polinucleótido,
en el que el polipéptido recombinante del grupo de movilidad elevada comprende un polipéptido TFAM que comprende al menos un dominio de la caja HMG operablemente enlazado a un dominio de transducción de proteína que está enlazado operablemente a una señal seleccionadora de dianas para un orgánulo no nuclear,
en el que el dominio de transducción de proteína y la señal seleccionadora de dianas se presentan sobre una superficie exterior del polinucleótido empaquetado.
22. El método de la reivindicación 21, en el que el polipéptido recombinante del grupo de movilidad elevada se asocia reversiblemente con el polinucleótido.
23. El método de la reivindicación 21, en el que el polipéptido recombinante del grupo de movilidad elevada reviste al polinucleótido.
24. El método de la reivindicación 21, en el que la asociación del polipéptido recombinante del grupo de movilidad elevada con el polinucleótido induce a un cambio conformacional en el polinucleótido.
25. El método de la reivindicación 21, en el que el dominio de la caja HMG se asocia con el polinucleótido de una manera específica de la secuencia.
26. El método de la reivindicación 21, en el que el dominio de la caja HMG se asocia de forma no específica con el polinucleótido.
27. El método de la reivindicación 21, en el que la etapa de combinación se produce in vitro.
28. Un complejo de polinucleótido-polipéptido, comprendiendo el complejo de polinucleótido-polipéptido:
(1) un polipéptido recombinante del grupo de movilidad elevada que comprende un polipéptido TFAM que comprende al menos una caja HMG operablemente enlazada a un dominio de transducción de proteína que está operablemente enlazado a una señal seleccionadora de orgánulos no nucleares, y
(2) un polinucleótido que codifica un primer polipéptido enzimático o un ácido nucleico enzimático y al menos un segundo polipéptido.
29. El complejo de la reivindicación 28, en el que el polinucleótido comprende un genoma mitocondrial o un fragmento del mismo.
30. El complejo de la reivindicación 28, en el que el orgánulo no nuclear es una mitocondria.
31. El complejo de la reivindicación 28, en el que el primer polipéptido enzimático es una endonucleasa.
32. El complejo de la reivindicación 28, en el que el ácido nucleico enzimático comprende ADN, ARN, o una combinación de los mismos.
33. El complejo de la reivindicación 28, en el que el polinucleótido codifica más de un polipéptido mitocondrial.
Patentes similares o relacionadas:
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]
Ratón nuligénico para Pint que muestra un fenotipo asociado a envejecimiento prematuro, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón cuyo genoma comprende una inactivación de un locus del ARN no codificante largo (ARNlnc) Pint endógeno, en donde la inactivación (i) da como resultado que el […]