Inhibidores ODCasa para el tratamiento de malaria.
Un compuesto seleccionado de un compuesto de fórmula I, tautómeros del mismo y sales,
solvatos y profármacosfarmacéuticamente aceptables del mismo, en el que el profármaco se selecciona de un éster fenílico, un éster de alquiloC8-C24, un éster alcoximetílico, un carbamato y un éster de aminoácido, de cualquier grupo hidroxilo, 5 tiol, amino ocarboxilo disponible en el compuesto de fórmula I:
en la que
R1 se selecciona de CN, N3, I, Br, NH2, NO2, C(O)alquilo C1-6, NH-alquilo C1-C6, N(alquilo C1-C6)2, NHC(O)alquilo C1-C6 yNHC(O)O-alquilo C1-C6;
R2 se selecciona de H, halógeno, alquilo C1-C6, alcoxi C1-6, fluoro-alquilo C1-C6 sustituido, fluoro-alcoxi C1-C6 sustituido,N3, NH2 y CN;
R3 se selecciona de OH, NH2, H y NHC(O)alquilo C1-C6;
Z se selecciona de:**Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2006/001620.
Solicitante: UNIVERSITY HEALTH NETWORK.
Nacionalidad solicitante: Canadá.
Dirección: R. FRASER ELLIOTT BUILDING, ROOM 1S-417 190 ELIZABETH STREET TORONTO, ON M5G 2C4 CANADA.
Inventor/es: KOTRA,LAKSHMI P, PAI,EMIL F, BELLO,ANGELICA M, FUJIHASHI,MASAHIRO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/7064 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo pirimidinas condensadas o no condensadas.
- A61P33/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 33/00 Agentes antiparasitarios. › Contra la malaria.
- C07H19/067 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 19/00 Compuestos que contienen un heterociclo que comparten un heteroátomo del ciclo con un radical sacárido; Nucleósidos; Mononucleótidos; Sus anhidro-derivados. › con un ribosilo como radical sacárido.
- C07H19/073 C07H 19/00 […] › con un desoxi-2-ribosilo como radical sacárido.
PDF original: ES-2436404_T3.pdf
Fragmento de la descripción:
Inhibidores ODCasa para el tratamiento de malaria
CAMPO DE LA INVENCIÓN
La presente invención se refiere a ciertos compuestos de uridina sustituidos en 6 para su uso en el tratamiento y la prevención de malaria. La invención también se refiere a novedoso compuestos de uridina que tienen actividad inhibidora de ODCasa y a composiciones farmacéuticas que comprenden estos compuestos.
ANTECEDENTES DE LA INVENCIÓN
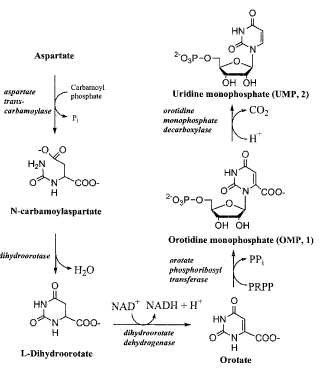
La ODCasa (EC 4.1.1.23) desempeña una función central en la síntesis de novo de uridina-5'-O-monofosfato (UMP) . La UMP es un bloque estructural, sintetizado de novo a partir de ácido aspártico, para la síntesis de otros nucleótidos de 15 pirimidina tales como uridina-5'-O-trifosfato (UTP) , citidina-5'-O-trifosfato (CTP) , timidina-5'-O-trifosfato (TMP) y 2'-desoxicitidina-5'-O-trifosfato (dCTP) (Figura 1) . Los nucleótidos de pirimidina son los elementos estructurales para la síntesis de ARN y ADN, las moléculas esenciales para la replicación y supervivencia celular. Debido a su importante función en la síntesis de ácidos nucleicos de novo de células, la ODCasa está presente en bacterias, archea, parásitos y en seres humanos, es decir, casi en cualquier especie, excepto en virus. Esta enzima cataliza la descarboxilación de orotidina monofosfato (OMP) a uridina monofosfato (UMP) (compuestos 1 y 2 en la etapa final en la Figura 1) . Esta enzima es particularmente interesante para los enzimólogos debido a que presenta un nivel extraordinario de potenciamiento de la tasa catalítica de más de 17 órdenes de magnitud en comparación con la reacción de descarboxilación sin catalizar en agua a pH neutro de 7, 0, 25 ºC.i, ii Una descarboxilación sin catalizar de OMP dura aproximadamente 78 millones de años, y la descarboxilación enzimática en una escala de tiempo de milisegundos. Así, la ODCasa es uno de los miembros más capaces del mundo enzimático.ii, iii, iv, v
De forma interesante, las descarboxilasas encontradas en la naturaleza usan tanto un cofactor como productos intermedios covalentes durante la catálisis de reacciones de descarboxilación.vi, vii Por ejemplo, la indol piruvato descarboxilasa (IPDC) dependiente de tiamina difosfato usa tiamina como cofactor y se forman productos intermedios covalentes con el cofactor durante el procedimiento de descarboxilación. Se cree que la ODCasa es bastante inusual en catalizar la descarboxilación con tal capacidad sin la ayuda ningún co-factor, metal o producto intermedio covalente.i, ii, iii Una diferencia interesante cuando se mira esta enzima a través de las especies es que en ciertos organismos de nivel superior tales como el ser humano o ratón, la ODCasa es una parte de la enzima bifuncional, UMP sintasa.viii En organismos patógenos tales como bacterias, hongos y parásitos, la ODCasa es una enzima monofuncional.ix, x En todas las especies, la ODCasa (tanto si es monofuncional como bifuncional) es activa como una unidad dimérica.
En general, las investigaciones que eligen ODCasa como diana se basaron en la malaria, cáncer y algunas investigaciones antivirales. En las últimas dos décadas se investigaron ampliamente varios análogos de OMP para entender el mecanismo catalítico de ODCasa.iii, xi Entre estos análogos, 6-aza-UMP (3) y 6-hidroxi-UMP (o BMP, 4) , pirazofurina, xantosina-5'-monofosfato (XMP, 12) y 6-tiocarboxamido-UMP (13) son algunos de los potentes inhibidores que se estudiaron contra ODCasa (Figura 2) .xii, xiii, xiv Sin embargo, el desarrollo de candidatos a inhibidores se ha limitado debido a sus toxicidades y falta de especificidad.xii También hay investigaciones de relación estructura-actividad muy limitadas o inexistentes y diseño de inhibidores contra ODCasa. Así, la ODCasa no ha ganado mucha adherencia en los 80 y los 90 como diana de fármaco.
Aparte de su obvio interés farmacológico, la ODCasa ha sido una enzima favorita para bioquímicos y biólogos estructurales debido a sus inusuales propiedades catalíticas. Se propusieron varios mecanismos antes de y después de la disponibilidad de las estructuras cristalinas de rayos X para varias ODCasas en 2000.xv, xvi, xvii, xviii Aunque se trataron ideas de catálisis covalente, ninguno de los mecanismos presentado incluyó una formación de especies covalentes como etapa clave durante la descarboxilación por ODCasa. Un análisis del sitio catalítico de ODCasa de Metanobacterium thermoautotrophicum (Mt) reveló dos residuos aspartato (Asp70 y Asp75B, el último contribuido por la segunda subunidad de la ODCasa dimérica) y dos residuos de lisina (Lys42 y Lys72) que se mantienen mediante una fuerte red de enlaces de hidrógeno (Figura 3) . Los análisis de varias estructuras de co-cristales de ODCasa con una variedad de ligandos confirman que estos residuos se mantienen estrechamente en sus posiciones respectivas en el sitio activo y hay
menos de 0, 5 A de movimiento en las posiciones de las cadenas laterales de estos residuos. La prueba existente no soporta ningún residuo de sitio activo que forme un enlace covalente tanto con el sustrato durante la catálisis como con cualquier inhibidor conocido.iii, xvi, xix, xx, xxi
Los cuatro residuos anteriores se proponen para ejercer tensión estérica y electrostática fuerte sobre el grupo carboxilato C-6 de OMP y eliminar el grupo carboxilo.xvi Hoy en día se conocen las estructuras cristalinas de rayos X de ODCasa de diez especies diferentes. En 2000, cuatro estructuras cristalinas de rayos X de ODCasa incluyeron el mecanismo catalítico de esta enzima. Basándose en la estructura de ODCasa de S. cerevisiae complejada con el análogo de estado de transición BMP (4) , se propuso un mecanismo de estabilización del estado de transición de descarboxilación de OMP.xviii También se sugirió una propuesta similar por Appleby y col. basándose en la estructura cristalina de ODCasa (Bacillus subtilis) complejada con el producto, 65 UMP.xvii Estos autores sugirieron que la reacción de descarboxilación avanza mediante una sustitución electrófila en la que C-6 está protonado por Lys62 a medida que se libera la molécula de dióxido de carbono.xvii La estructura de la enzima ODCasa de E. coli co-cristalizada con BMP era la base de la propuesta presentada por Harris y col.xxii Basándose en la proximidad del resto carboxilato sobre OMP (1) y el residuo Asp71 en el sitio activo de ODCasa, se propuso que la descarboxilación de OMP depende de la existencia de un protón compartido entre Asp71 y el grupo carboxilo del sustrato.xxii Se postuló un mecanismo similar que implica repulsión electrostática por Wu y col.xvi Este mecanismo de 5 descarboxilación de OMP se basa en los principios del efecto de Circe descrito por Jencks en 1975.xxiii El efecto de Circe establece que sólo el grupo reactivo del sustrato necesita estar desestabilizado. La fuerte interacción entre la parte no reactiva del sustrato y el sitio activo de la enzima proporciona la energía para desestabilizar directamente el grupo reactivo del sustrato.xxiii El mecanismo de repulsión electrostática señala al residuo de aspartato de sitio activo. En cuatro especies diferentes la localización y función de este residuo está altamente conservada. Los residuos catalíticos Asp70 y 10 Lys72 se localizan próximos al centro de reacción C-6 del anillo de pirimidina del sustrato OMP y se postuló que Asp70
(M. thermoautotrophicum) proporcionaba la desestabilización electrostática del complejo enzima-sustrato. Lys72 en el sitio activo provee el protón para neutralizar el carbanión desarrollado después de la salida del carboxilato.xvi A pesar de varias estructuras de rayos X y enzimología en profundidad en las dos últimas décadas, la ODCasa continúa retando a los bioquímicos con mecanismo todavía sin resolver y nuevos giros (véase más adelante) .
En el sitio activo de ODCasa se propone que el grupo monofosfato de OMP se une primero y este grupo contribuye a la mayor energía requerida para la unión del sustrato a ODCasa.xxiv La eliminación de fosfato de la molécula de sustrato produjo una eficiencia catalítica significativamente menor medida como la constate de segundo orden (kcat/KM) para la catálisis de sustrato a producto.xxiv En un interesante experimento, la unión del dianión fosfito (HPO32-) a ODCasa (de S.
cerevisiae) produjo un aumento de 80.000 veces en la constante de segundo orden para la descarboxilación del sustrato truncado que carece de un resto fosfato.xxv Así, el grupo fosfato es un componente importante para la unión de ODCasa. Así, con el fin de que los fármacos de nucleósido (la correcta terminología es profármacos) sean activos contra ODCasa in vivo, el compuesto de nucleósido tiene que convertirse en su forma de monofosfato dentro de la célula por cualquier nucleósido cinasa y luego... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto seleccionado de un compuesto de fórmula I, tautómeros del mismo y sales, solvatos y profármacos farmacéuticamente aceptables del mismo, en el que el profármaco se selecciona de un éster fenílico, un éster de alquilo C8-C24, un éster alcoximetílico, un carbamato y un éster de aminoácido, de cualquier grupo hidroxilo, tiol, amino o carboxilo disponible en el compuesto de fórmula I:
en la que R1 se selecciona de CN, N3, I, Br, NH2, NO2, C (O) alquilo C1-6, NH-alquilo C1-C6, N (alquilo C1-C6) 2, NHC (O) alquilo C1-C6 y NHC (O) O-alquilo C1-C6; R2 se selecciona de H, halógeno, alquilo C1-C6, alcoxi C1-6, fluoro-alquilo C1-C6 sustituido, fluoro-alcoxi C1-C6 sustituido,
N3, NH2 y CN; R3 se selecciona de OH, NH2, H y NHC (O) alquilo C1-C6; Z se selecciona de:
en las que R4 se selecciona de H, alquilo C1-C6 e hidroxi-alquilo C1-C6 sustituido; uno de R5 y R6 es hidrógeno y el otro se selecciona de H, OH y F y uno de R5' y R6' es hidrógeno y el otro se selecciona de H, OH y F o R5 y R6 o R5' y R6' juntos pueden ser =O o =CH2; R7 se selecciona de H, F y OH; R8 se selecciona de H, C (O) alquilo C1-C6, P (O) (OH) 2, P (O) (O-alquilo C1-C6) 2 y P (O) (O-alquilo C1-C6) OH;
R9 se selecciona de H, N3, CN, alquilo C1-C6; y X-Y se selecciona de -CH2-O-, -O-CH2- y -S-CH2-;
para su uso en el tratamiento o prevención de malaria en un sujeto.
2. Un compuesto para su uso según la reivindicación 1, en el que R1 en los compuestos de fórmula I se selecciona de I, Br, NO2, N (alquilo C1-C4) 2, NHC (O) alquilo C1-C4 y NHC (O) O-alquilo C1-C4.
3. Un compuesto para su uso según la reivindicación 2, en el que R1 en los compuestos de fórmula I se selecciona de I,
Br, NO2, N (CH3) 2, NHC (O) CH3 y NHC (O) CH3. 40
4. Un compuesto para su uso según la reivindicación 3, en el que R1 en los compuestos de fórmula I se selecciona de I, Br y N (CH3) 2.
5. Un compuesto para su uso según la reivindicación 4, en el que R1 en los compuestos de fórmula I es I. 45
6. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-5, en el que R2 en los compuestos de fórmula I se selecciona de H, halógeno, alquilo C1-C4, alcoxi C1-C4, fluoro-alquilo C1-C4 sustituido, fluoro-alcoxi C1-C4 sustituido, N3, NH2 y CN.
7. Un compuesto para su uso según la reivindicación 6, en el que R2 en los compuestos de fórmula I se selecciona de H, fluoro, cloro, bromo, CH3, OCH3, CF3, CF3O, N3, NH2 y CN.
8. Un compuesto para su uso según la reivindicación 7, en el que R2 en los compuestos de fórmula I se selecciona de H, fluoro, cloro, bromo, OCH3 y CF3, CF3O.
9. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-8, en el que R3 en los compuestos de fórmula I se selecciona de OH y NH2.
10. Un compuesto para su uso según la reivindicación 9, en el que R3 en los compuestos de fórmula I es OH y el compuesto de fórmula I tiene la siguiente estructura tautómera:
11. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-10, en el que en los compuestos de fórmula I Z es la fórmula II.
12. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-11, en el que R4 en los compuestos de fórmula I es H.
13. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-12, en el que R5 y R5' son ambos OH y R6 y R6' son ambos H.
14. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-12, en el que R5 es H, R5' es OH y R6 y R6' son ambos H.
15. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-10, en el que R7 en los compuestos de fórmula I es H u OH.
16. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-15, en el que R8 en los compuestos de fórmula I se selecciona de H, C (O) alquilo C1-C4, P (O) (OH) 2, P (O) (O-alquilo C1-C4) 2 y P (O) (O-alquilo C1-C4) OH.
17. Un compuesto para su uso según la reivindicación 16, en el que R8 en los compuestos de fórmula I se selecciona de 35 H, C (O) CH3, P (O) (OH) 2, P (O) (OCH3) 2 y P (O) (OCH3) OH.
18. Un compuesto para su uso según la reivindicación 17, en el que R8 en los compuestos de fórmula I se selecciona de H, C (O) CH3 y P (O) (OH) 2.
19. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-18, en el que R9 en los compuestos de fórmula I es H.
20. Un compuesto para su uso según la reivindicación 1, en el que X-Y es -O-CH2-.
21. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-20, en el que el compuesto de fórmula I tiene la siguiente estructura:
22. Un compuesto para su uso según una cualquiera de las reivindicaciones 1-21, en el que el compuesto de fórmula I se selecciona de: 6-Cianouridina;
6-Cianouridina-5'-monofosfato; 6-Azidouridina; 6-Azidouridina-5'-O-monofosfato; 6-Aminouridina-5'-O-monofosfato; 6-Aminouridina;
6-Metil-uridina; 6-Metil-uridina-5'-O-monofosfato; 6-Yodo-uridina; 6-N-Metilaminouridina; 6-N, N-Dimetilaminouridina;
6-N Metilaminouridina-5'-O-monofosfato; 6-Yodo-uridina-5'-O-monofosfato; 5-Fluoro-6-aminouridina; 5-Bromo-6-yodo-uridina; 5-Fluoro-6-azidouridina;
5-Fluoro-6-yodo-uridina; 5-Fluoro-6-aminouridina-5'-O-monofosfato; 5-Bromo-6-yodo-uridina-5'-O-monofosfato; 5-Fluoro-6-azidouridina-5'-O-monofosfato; 5-Fluoro-6-yodo-uridina-5'-O-monofosfato;
6-Metoxicarbonil-uridina; 6-Etoxicarbonil-uridina; 6-Metoxicarbonil-uridina-5'-O-monofosfato; 6-Etoxicarbonil-uridina-5'-O-monofosfato; 1'-Hidroximetil-6-yodo-uridina;
1'-Hidroximetil-6-yodo-uridina-5'-monofosfato, y sales, solvatos y profármacos farmacéuticamente aceptables de los mismos, en los que el profármaco se selecciona de un éster fenílico, un éster de alquilo C8-C24, un éster alcoximetílico, un carbamato y un éster de aminoácido, de cualquier grupo hidroxilo, tiol, amino o carboxilo disponible en el compuesto de fórmula I.
23. Un compuesto seleccionado de un compuesto de fórmula I, y sales, solvatos y profármacos farmacéuticamente aceptables del mismo, como se define en una cualquiera de las reivindicaciones 1-22, para su uso en prevenir o tratar una infección de un parásito palúdico en un sujeto.
24. Un procedimiento para inhibir ODCasa en una muestra de plasma o de sangre aislada de un sujeto que comprende añadir a dicha muestra de plasma o de sangre una cantidad eficaz inhibidora de un compuesto seleccionado de un compuesto de fórmula I, y sales, solvatos y profármacos farmacéuticamente aceptables del mismo, como se define en una cualquiera de las reivindicaciones 1-22.
25. Un compuesto de fórmula I seleccionado de:
6. (dimetilamino) uridina; 5-fluoro-6-aminouridina; 5-bromo-6-aminouridina; 5-fluoro-6-azidouridina; 1'-hidroximetil-6-yodo-uridina;
6. (dimetilamino) -2'-desoxiuridina; 5-fluoro-6-amino-2'-desoxiuridina; 5-bromo-6-amino-2'-desoxiuridina; 5-fluoro-6-azido-2'-desoxiuridina; 5-cloro-6-yodo-2'-desoxiuridina;
5. cloro-6-azido-2'-desoxiuridina; 5-metoxi-6-yodo-2'-desoxiuridina; 5-metoxi-6-azido-2'-desoxiuridina; 5-metoxi-6-amino-2'-desoxiuridina; 5-bromo-6-yodo-2'-desoxiuridina;
5. bromo-6-azido-2'-desoxiuridina; 6- (dimetilamino) uridina-5'-monofosfato; 5-fluoro-6-aminouridina-5'-monofosfato; 5-bromo-6-aminouridina-5'-monofosfato; 5-fluoro-6-azidouridina-5'-monofosfato;
1'-hidroximetil-6-yodo-uridina-5'-monofosfato 6- (dimetilamino) -2'-desoxiuridina-5'-monofosfato; 5-fluoro-6-amino-2'-desoxiuridina-5'-monofosfato; 5-bromo-6-amino-2'-desoxiuridina-5'-monofosfato; 5-fluoro-6-azido-2'-desoxiuridina-5'-monofosfato;
5. cloro-6-yodo-2'-desoxiuridina-5'-monofosfato; 5-cloro-6-azido-2'-desoxiuridina-5'-monofosfato; 5-metoxi-6-yodo-2'-desoxiuridina-5'-monofosfato; 5-metoxi-6-azido-2'-desoxiuridina-5'-monofosfato; 5-metoxi-6-amino-2'-desoxiuridina-5'-monofosfato;
5. bromo-6-yodo-2'-desoxiuridina-5'-monofosfato;
5. bromo-6-azido-2'-desoxiuridina-5'-monofosfato;
5. fluoro-6-yodo-uridina-5'-monofosfato; 5 6-yodo-uridina-5'-acetato;
6. yodo-2'-desoxiuridina-5'-acetato, y
sales, solvatos y profármacos farmacéuticamente aceptables de los mismos en los que el profármaco se selecciona de un éster fenílico, un éster de alquilo C8-C24, un éster alcoximetílico, un carbamato y un éster de aminoácido, de cualquier grupo hidroxilo, tiol, amino o carboxilo disponible en el compuesto de fórmula I.
26. Una composición farmacéutica que comprende uno o más de un compuesto según la reivindicación 25 y un vehículo 15 farmacéuticamente aceptable para el mismo.
27. Uso de un compuesto seleccionado de un compuesto de fórmula I, tautómeros del mismo y sales, solvatos y profármacos farmacéuticamente aceptables del mismo, como se define en una cualquiera de las reivindicaciones 1 a 22, en la preparación de un medicamento para tratar o prevenir malaria.
Patentes similares o relacionadas:
Derivados de iminotetrahidropirimidinona como inhibidores de plasmepsina V, del 27 de Mayo de 2020, de UCB Biopharma SRL: Un compuesto de fórmula (IIA) o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde el anillo X representa un anillo […]
Procedimiento para el tratamiento de infecciones de Plasmodium resistentes a los medicamentos y producto utilizado, del 20 de Abril de 2020, de MEDALAB RESEARCH S.L: Procedimiento para el tratamiento de infecciones de Plasmodium resistentes a los medicamentos y producto utilizado. La invención se refiere al uso de un gas producido por […]
COMPLEJO DE INCLUSIÓN DE ORIGEN NATURAL Y BIODISPONIBLE PARA EL TRATAMIENTO DE ENFERMEDADES DE ORIGEN PARASITARIO, del 15 de Noviembre de 2019, de UNIVERSIDAD DE VALLADOLID: Complejo de inclusión de origen natural y biodisponible para el tratamiento de enfermedades de origen parasitario. Complejo de inclusión que comprende […]
Análogos de salinomicina que contienen nitrógeno, síntesis y utilización contra células troncales cancerosas y paludismo, del 14 de Agosto de 2019, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS): Compuesto de fórmula (I), enantiómeros, mezcla de enantiómeros, diastereoisómeros y mezcla de diastereoisómeros del mismo:**Fórmula** en el que: - W se selecciona […]
Activador de las placas de Peyer, del 31 de Julio de 2019, de Mitsui Sugar Co., Ltd. (100.0%): Un polisacárido obtenido de caña de azúcar que es adecuado para activar las placas de Peyer, en el que el polisacárido contiene α-glucano como componente […]
Derivados azepanilo y composiciones farmacéuticas que los comprenden con actividad antiparasitaria, del 18 de Junio de 2019, de MERCK PATENT GMBH: Un compuesto según la fórmula (i)**Fórmula** donde W se selecciona entre un enlace C-Sp2-Sp2-C, O, SO2, S, N Z se selecciona entre C o N, Z' se selecciona […]
Intervenciones basadas en angiopoyetina para el tratamiento de la malaria cerebral, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de una proteína angiopoyetina modificada para su uso en un método de tratamiento, prevención […]
Compuestos de triaminopirimidina útiles para evitar o tratar la malaria, del 15 de Enero de 2019, de MMV Medicines for Malaria Venture: Un compuesto de Fórmula (I):**Fórmula** o un complejo, hidrato, solvato, o polimorfo, tautómero, isómero geométrico, forma ópticamente activa, o una sal farmacéuticamente […]