Inhibidores de serina proteasa tipo tripsina, su preparación y uso.
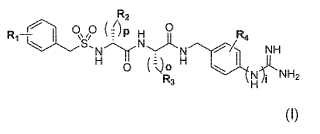
Compuestos de la fórmula general (I)**Fórmula**
con
R1 opcionalmente presente una vez o más veces e independientemente entre sí,
representa un residuo COOR5, conR5 igual a hidrógeno o a un grupo de alquilo inferior, ramificado o lineal, con 1-6 átomos de carbono, un residuoaminoalquilo ramificado o lineal con 1-6 átomos de carbono, un residuo de halógeno o pseudohalógeno, o unresiduo de polietilenglicol de la fórmula (II) o (III)
CH3-O-(CH2-CH2-O-)n-CH2-CH2-(C≥O)-NH-CH2- (II)
CH3-O-(CH2-CH2-O-)n-CH2-CH2-NH-(C≥O)-CH2-CH2-(C≥O)-NH-CH2- (III)
Con n definido de tal manera que los residuos de polietilenglicol tienen un peso molecular promedio de 10000 Da,5000 Da, 3400 Da, 2000 Da, 1000 Da o 750 Da;
R2 representa un ciclo o biciclo no sustituido o sustituido, aromático o no aromático, con 5-13 átomos de carbono oheterociclo aromático con 4-5 átomos de carbono y un átomo de nitrógeno, óxido de nitrógeno, átomo de oxígeno oátomo de azufre, donde la sustitución es un residuo de halógeno, un residuo alquilo ramificado o lineal, sustituidoopcionalmente con flúor, con 1-6 átomos de carbono, un residuo alquiloxi ramificado lineal, opcionalmente sustituidocon flúor, con 1-6 átomos de carbono, un residuo hidroxilo o un residuo ciano; o un residuo de la estructura.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/009220.
Solicitante: THE MEDICINES COMPANY (LEIPZIG) GMBH.
Nacionalidad solicitante: Alemania.
Dirección: Deutscher Platz 5 A 04103 Leipzig ALEMANIA.
Inventor/es: STURZEBECHER, JORG, STEINMETZER,TORSTEN, SCHWEINITZ,ANDREA, REICHELT,CLAUDIA, SCHULZE,ALEXANDER, HEINICKE,JOCHEN, STEINMETZER,PETER, SÖFFING,ANETT, VAN DE LOCHT,ANDREAS, NICKLISCH,SILKE, LUDWIG,FRIEDRICH-ALEXANDER, DAGHISCH,MOHAMMED.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/18 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Sulfamidas (compuestos que contienen un grupo para N-benceno-sulfonil-N A61K 31/63).
- A61K31/44 A61K 31/00 […] › Piridinas no condensadas; Sus derivados hidrogenados.
- A61P7/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Agentes antitrombóticos; Anticoagulantes; Inhibidores de la agregación plaquetaria.
- C07C311/33 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 311/00 Amidas de ácidos sulfónicos, es decir, compuestos en los que átomos de oxígeno, unidos por enlaces sencillos, de grupos sulfónicos han sido sustituidos por átomos de nitrógeno que no forman parte de grupos nitro o nitroso. › de una estructura carbonada saturada que contiene ciclos.
- C07D213/56 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 213/00 Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos. › Amidas.
- C07D213/89 C07D 213/00 […] › con heteroátomos directamente unidos al átomo de nitrógeno del ciclo.
- C07D233/64 C07D […] › C07D 233/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, no condensados con otros ciclos. › con radicales hidrocarbonados sustituidos, unidos a los átomos de carbono del ciclo, p. ej. histidina.
PDF original: ES-2439244_T3.pdf
Fragmento de la descripción:
Inhibidores de serina proteasa tipo tripsina, su preparación y uso. La invención se refiere a inhibidores de serina proteasas tipo tripsina de la fórmula general:
los cuales, además de plasmina, también inhiben calicreína plasmática, así como a la preparación y uso de éstos como medicamentos, preferentemente para el tratamiento de pérdida de sangre, especialmente en estados hiperfibrinolíticos, en trasplantes de órganos y procedimientos quirúrgicos cardiacos, especialmente con derivación o bypass cardiopulmonar, o como constituyente de un adhesivo de fibrina.
Ya son conocidos inhibidores de plasmina y calicreína plasmática (PK) . La plasmina es una serina proteasa tipo tripsina y desdobla numerosos sustratos C terminalmente de los aminoácidos básicos arginina o lisina. La plasmina se forma a partir del zimógeno plasminógeno por la acción catalítica de los activadores de plasminógeno urocinasa o tPA. Los sustratos de plasmina incluyen diversas proteínas de la matriz extracelular y la membrana basal, por ejemplo fibronectina, laminina, colágeno tipo IV o fibrina, pero también numerosos zimógenos como preformas de metaloproteasas de matriz o el activador del plasminógeno urocinasa. En la sangre, la plasmina es responsable, ante todo, de la fibrinólisis por desdoblamiento de fibrina en productos solubles.
Los inhibidores de plasmina endógenos incluyen α, 2-macroglobulina y la serpina α, 2-antiplasmina. En ciertos estados patológicos puede haber activación espontánea de la fibrinólisis. En el caso de tal hiperplasminemia, no solo se degrada la fibrina cerradora de heridas, sino existe también formación de productos de degradación de fibrinógeno anticoagulante. Con ello pueden surgir serios deterioros de la hemostasis. Los antifibrinolíticos que se utilizan en la clínica son ácidos aminocarboxílicos sintéticos como el ácido £-aminocapróico, ácido paminometilbenzóico o ácido tranexámico (ácido trans-4- (aminometil) ciclohexancarboxílico) . Estos compuestos bloquean la unión del zimógeno plasminógeno a la fibrina y de este modo inhiben la activación de éste en plasmina. Estos compuestos, por tanto, no son inhibidores directos de plasmina y son incapaces de inhibir plasmina la cual ya ha sido formada. Otro antifibrinolítico empleado es aprotinina (Trasylol®, Bayer AG, Leverkusen) , un polipéptido de 58 aminoácidos que se obtiene de pulmón bovino. La aprotinina inhibe plasmina con una constante de inhibición de 1 nM, pero es relativamente no específica y también inhibe eficazmente tripsina (Ki = 0.1 nM) y calicreína plasmática (Ki = 30 nM) . La aprotinina también inhibe otras enzimas, aunque con actividad reducida.
Un uso importante de aprotinina es reducir la pérdida de sangre, especialmente en procedimientos quirúrgicos cardiacos con bypass o derivación cardiopulmonar (CPB) , reduciendo ostensiblemente la necesidad de transfusiones sanguíneas perioperatorias (Sodha et al., 2006) . Además, la aprotinina también se emplea en otras operaciones, por ejemplo en trasplantes de órgano, para inhibir la pérdida de sangre o se utiliza como aditivo en adhesivos de fibrina.
El uso de aprotinina tiene varias desventajas. Puesto que se aísla de órganos bovinos, en teoría existe el riesgo de contaminación patógena reacciones alérgicas. El riesgo de un shock anafiláctico es relativamente bajo con la primera administración de aprotinina (< 0, 1 %) , aunque aumenta con administración repetida a los 200 días a 4-5 %.
Recientemente se documentó que la administración de aprotinina en comparación directa con ácido £-aminocapróico o ácido tranexámico induce una cantidad aumentada de efectos secundarios (Mangano et al., 2006) . La administración de aprotinina dio origen a una duplicación del número de casos de daño renal, por lo que se hizo necesaria la diálisis. Del mismo modo, el riesgo de infarto de miocardio y accidente cerebrovascular apopléjico se aumentó por la administración de aprotinina en comparación con los grupos testigo.
A la fecha sólo se conocen algunos inhibidores sintéticos de plasmina. Sanders y Seto (1999) describieron derivados de 4-heterociclohexanona con actividad relativamente débil, con constantes de inhibición º 50 μM para plasmina. Xue y Seto (2005) reportaron derivados peptídicos de ciclohexanona con valores IC50 º 2 μM, pero se desconoce su desarrollo posterior. Okada y Tsuda describieron diferentes derivados con un residuo de 4-aminometilciclohexanoilo que inhiben plasmina con valores IC50 º 0, 1 μM, pero no se conoce una aplicación clínica de estos inhibidores (Okada et al., 2000; Tsuda et al., 2001) .
Las constantes de inhibición de plasmina han sido publicadas en numerosas publicaciones sobre el desarrollo de inhibidores de proteasas de coagulación como antitrombóticos, donde el objetivo en estos casos fue inhibir plasmina tan débilmente como fuera posible. En ninguno de estos documentos se mencionó un uso posible de estos compuestos para reducir la pérdida de sangre en procedimientos quirúrgicos cardiacos. De este modo, por ejemplo, el inhibidor de trombina melagatran inhibe plasmina con un valor Ki de 0.7 μM, mientras que los compuestos estructural y estrechamente relacionados H317/86 tienen una constante de inhibición de 0.22 μM para plasmina (Gustafsson et al., 1998) . Sin embargo, ambos compuestos inhiben la proteasa trombina ostensiblemente más fuerte con valores Ki º 2 nM, por lo cual la administración de melagatran da como resultado una fuerte anticoagulación.
Como se describe en la introducción la aprotinina inhibe no solo plasmina sino también calicreína plasmática (PK) . La PK es una serina proteasa tipo tripsina multifuncional para la cual se conocen varios sustratos fisiológicos. De esta manera, la PK puede liberarse por desdoblamiento proteolítico del péptido vasoactivo bradicinina a partir de cininógeno de peso molecular alto y activar los zimógenos factor de coagulación XII, prourocinasa, plasminógeno y pro-MMP 3. Por lo tanto, se supone que el sistema PK/cinina tiene una función importante en diversos síntomas, por ejemplo, en situaciones tromboembólicas, coagulación intravascular diseminada, shock séptico, alergias, el síndrome de postgastrectomía, artritis y ARDS (síndrome de distrés respiratorio del adulto) (Tada et al., 2001) .
Por consiguiente, la aprotinina inhibe, por su efecto inhibidor sobre PK, la liberación de la hormona peptídica bradicinina. La bradicinina tiene, por activación del receptor de bradicinina B2, diversos efectos. La liberación inducida por bradicinina de tPA, NO y prostaciclina a partir de las células endoteliales (ver la revisión de Schmaier, 2002) tiene influencia sobre la fibrinólisis, presión arterial y episodios inflamatorios. Se discute que los procesos inflamatorios sistémicos que pueden ocurrir como efectos colaterales en operaciones se reducen por la inhibición de la liberación de bradicinina.
Diversas bisbenzamidinas como pentamidina y compuestos relacionados, y ésteres de ácidos w-amino y wguanidinoalquilcarboxílicos con valores Ki micromolares han sido descritos como inhibidores de PK (Asghar et al., 1976; Muramatu y Fuji, 1971; Muramatu y Fuji, 1972; Ohno et al, 1980; Muramatu et al., 1982; Satoh et al., 1985; Tena et al., 1991) .
Los primeros inhibidores competitivos, selectivos, que se derivan de arginina o fenilalalanina fueron desarrollados por Okamoto et al., (1988) e inhiben PK con valores Ki alrededor de 1 μM. Varios documentos sobre el desarrollo de inhibidores de PK competitivos han sido publicados por el grupo de Okada, en cuyo caso los compuestos más activos que se derivan del trans-4-aminometilciclohexancarbonil-Phe-4-carboximetilanilida tienen constantes de inhibición alrededor de 0.5 μM (Okada et al., 1999; Okada et al., 2000, Tsuda et al., 2001) . Los inhibidores de PK tienen en común su valor Ki relativamente alto. La Patente US 6, 472, 393 describe inhibidores de PK potentes con constantes de inhibición alrededor de 1 nM y con una 4-amidinoanilina como residuo P1. Los inhibidores de PK también han sido descritos en US 5, 602, 253. US 2006/0148901 describe inhibidores de PK cuyo efecto inhibidor sobre plasmina, sin embargo, es relativamente pequeño, por lo cual estos inhibidores difieren de los inhibidores descritos en la presente solicitud.
En WO 2005/026198 A1 se describen análogos de bencilamina sustituidos básicamente como inhibidores del factor de coagulación Xa, su producción y uso para la terapia y profilaxis de enfermedades cardiovasculares y eventos tromboembólicos.
En WO 2004/062657 A1 se describen el uso de 4-amidino- o 4-guanidinobencilamina acilada según la fórmula general (I) P4- P3- P2- P1 (I) en cuyo caso... [Seguir leyendo]
Reivindicaciones:
1. Compuestos de la fórmula general (I)
con R1 opcionalmente presente una vez o más veces e independientemente entre sí, representa un residuo COOR5, con R5 igual a hidrógeno o a un grupo de alquilo inferior, ramificado o lineal, con 1-6 átomos de carbono, un residuo aminoalquilo ramificado o lineal con 1-6 átomos de carbono, un residuo de halógeno o pseudohalógeno, o un residuo de polietilenglicol de la fórmula (II) o (III)
CH3-O- (CH2-CH2-O-) n-CH2-CH2- (C=O) -NH-CH2- (II)
CH3-O- (CH2-CH2-O-) n-CH2-CH2-NH- (C=O) -CH2-CH2- (C=O) -NH-CH2- (III)
Con n definido de tal manera que los residuos de polietilenglicol tienen un peso molecular promedio de 10000 Da, 5000 Da, 3400 Da, 2000 Da, 1000 Da o 750 Da;
R2 representa un ciclo o biciclo no sustituido o sustituido, aromático o no aromático, con 5-13 átomos de carbono o heterociclo aromático con 4-5 átomos de carbono y un átomo de nitrógeno, óxido de nitrógeno, átomo de oxígeno o átomo de azufre, donde la sustitución es un residuo de halógeno, un residuo alquilo ramificado o lineal, sustituido opcionalmente con flúor, con 1-6 átomos de carbono, un residuo alquiloxi ramificado lineal, opcionalmente sustituido con flúor, con 1-6 átomos de carbono, un residuo hidroxilo o un residuo ciano; o un residuo de la estructura:
R3 se selecciona de o R4 representa opcionalmente un residuo de halógeno presente una o varias veces;
o = 1 o 2; p = 0, 1, 2, 3 o 4; y
i = 0 o 1; así como sus mezclas racémicas y sales con ácidos orgánicos o inorgánicos.
2. Compuestos según la reivindicación 1, caracterizados porque en R1 el residuo de alquilo inferior es metilo o etilo, preferentemente metilo, el residuo de aminoalquilo es metilo, y el residuo halógeno o pseudohalógeno es cloro o un grupo ciano; y n es un número entero de cerca de 25 a cerca de 250, preferentemente cerca de 18, cerca de 25,
cerca de 50, cerca de 85, cerca de 125 o cerca de 250;
En R2 el heterociclo aromático contiene un átomo de nitrógeno u óxido de nitrógeno;
En R4 el residuo halógeno es flúor;
o = 1;
p = 3; y 15 i = 0.
3. Compuestos según la reivindicación 1 o 2, caracterizados porque R1 está presente una vez y en posición meta o para, preferentemente R1 es un residuo COOH, principalmente R1 está presente una vez y se selecciona de hidrógeno, de un grupo 4-COOH o principalmente de un grupo 3-COOH.
4. Compuestos según una de las reivindicaciones 1-3, caracterizados porque R2 es un ciclo o biciclo aromático con 20 6-13 átomos de carbono o heterociclo con 5 átomos de carbono y un átomo de nitrógeno.
5. Compuestos según una de las reivindicaciones 1-3, caracterizados porque R2 es un ciclo no aromático con 6 átomos de carbono.
6. Compuestos según una de las reivindicaciones 1-5, caracterizados porque R3 es
7. Compuestos según una de las reivindicaciones 1-6, caracterizados porque las sales se forman a partir de ácido clorhídrico, HBr, ácido acético, ácido trifluoroacético o ácido toluenosulfónico.
8. Compuestos según una de las reivindicaciones 1-7, caracterizados porque R2 se selecciona de los siguientes residuos:
9. Compuestos según una de las reivindicaciones 1-8, caracterizados porque R3 tiene la estructura 10. Compuestos según una de las reivindicaciones 1-9, caracterizados porque el compuesto se define de la siguiente manera:
Compuesto No. R1 R2 p R3 o i R4
1 H 3 1 0 -
2 4-COOH 3 1 0 -
3 3-COOH 3 1 0 -
4 3-COOH 3 1 1 -
5 3-COOH 3 1 0 2-F
6 H 3 1 0 -
7 H 3 1 0 -
Compuesto No. R1 R2 p R3 o i R4
8 H 3 1 0 -
9 H 3 1 0 -
10 H 3 1 0 -
11 H 3 1 0 -
12 H 3 1 0 -
13 H 1 1 0 -
14 H 1 1 0 -
15 H 1 1 0 -
16 4-COOH 1 1 0 -
17 H 1 1 0 -
18 3-COOH 1 1 0 -
19 4-COOH 1 1 0 -
20 H 1 1 0 -
21 H 3 1 0 -
22 H 0 1 0 -
23 3-COOH 0 1 0 -
24 H 2 1 0 -
25 3-COOH 2 1 0 -
26 H 2 2 0 -
Compuesto No. R1 R2 p R3 o i R4
27 H 2 2 0 -
28 H 3 1 0 -
29 4-COOH 3 1 0 -
30 3-COOH 3 1 0 -
31 H 3 2 0 -
32 H 3 1 0 -
33 3-COOH 3 1 0 -
34 H 3 2 0 -
35 4-COOH 3 2 0 -
36 3-COOH 3 2 0 -
37 H 1 2 0 -
38 H 1 2 0 -
39 H 3 2 0 -
40 3-COOH 3 2 0 -
41 H 3 2 0 -
42 3-COOH 3 2 0 -
43 H 1 2 0 -
44 H 2 2 0 -
45 H 1 2 0 -
46 H 0 2 0 -
47 H 2 2 0 -
49 H 3 2 0 -
50 3-COOH 3 2 0 -
51 H 3 2 0 -
52 3-COOH 3 2 0 -
53 H 3 2 0 -
54 3-COOH 3 2 0 -
Compuesto No. R1 R2 p R3 o i R4
55 H 3 2 0 -
56 3-COOH 3 2 0 -
11. Compuesto según la reivindicación 10, caracterizado porque el compuesto se define de la siguiente manera:
R1 R2 p R3 o I R4
3-COOH 3 1 0 -
12. Compuestos de la fórmula general (IV)
con R1 presente opcionalmente una o varias veces e independientemente entre sí representa un COOR5, con R5 igual a hidrógeno o a un grupo alquilo inferior, ramificado o lineal, con 1-6 átomos de carbono, un residuo aminoalquilo ramificado o lineal con 1-6 átomos de carbono, un residuo halógeno o pseudohalógeno o un residuo de polietilenglicol de la fórmula (V) o (VI)
CH3-O- (CH2-CH2-O-) n-CH2-CH2- (C=O) -NH-CH2- (V)
CH3-O- (CH2-CH2-O-) n-CH2-CH2-NH- (C=O) -CH2-CH2- (C=O) -NH-CH2- (VI)
Con n definida de tal manera que los residuos de polietilenglicol tienen un peso molecular promedio de 10000 Da, 5000 Da, 3400 Da, 2000 Da, 1000 Da o 750 Da;
R2 es un residuo alquiloxi ramificado o lineal, con 1-6 átomos de carbono, un residuo hidroxilo, un residuo amino o un residuo alquiloxicarbonilamido ramificado o lineal, con 1-6 átomos de carbono;
R3 se selecciona de los siguientes residuos:
R4 representa un residuo halógeno presente opcionalmente una o varias veces, 20 o = 1 o 2;
p = 1, 2, 3 o 4, i = 0 o 1; así como sus mezclas racémicas y sales con ácidos orgánicos o inorgánicos.
13. Compuestos según la reivindicación 12, caracterizados porque en R1 el residuo de alquilo inferior es metilo o etilo, preferentemente metilo, el residuo aminoalquilo es metilo, y el residuo halógeno o pseudohalógeno es cloro o un grupo ciano; y n es un número entero de cerca de 25 a cerca de 250, preferentemente cerca de 18, cerca de 25, cerca de 50, cerca de 85, cerca de 125 o cerca de 250;
En R2 el residuo de alcoxi y el residuo de alquiloxicarbonilamida son butilo terciario;
R3 es En R4 el residuo halógeno es flúor;
o = 1; p = 3; y i =0.
14. Compuestos según la reivindicación 13, caracterizados porque R1 está presente una vez y en posición meta o para, R1 es preferentemente hidrógeno o un residuo COOH, R1 está presente principalmente una vez y se selecciona de hidrógeno, de un grupo 4-COOH o un grupo 3-COOH.
15. Compuestos según una de las reivindicaciones 13-14, caracterizados porque la sales se forman a partir de ácido clorhídrico, HBr, ácido acético, ácido trifluoroacético o ácido toluenosulfónico.
16. Compuestos según una de las reivindicaciones 13-15, caracterizados porque el compuesto se define de la siguiente manera:
Compuesto No. R1 R2 p R3 o
57 H 4 1
58 4-COOH 4 1
59 H *-NH2 4 1
60 H 1 1
Compuesto No. R1 R2 p R3 o
61 H *-NH2 1 1
62 H 4 1
63 H 1 1
64 4-COOMe 1 1
65 4-COOH 1 1
66 3-COOMe 1 1
67 3-COOH 1 1
68 H *-OH 1 1
69 4-COOMe *-OH 1 1
70 4-COOH *-OH 1 1
71 H 1 1
72 H *-OH 1 1
73 H 1 2
74 H *-OH 1 2
Compuesto No. R1 R2 p R3 o
75 H 1 1
76 H *-OH 1 1
77 H 1 2
78 H *-OH 1 2
17. Método para producir un compuesto según una de las reivindicaciones 1-16, caracterizado porque los correspondientes aminoácidos se acoplan secuencialmente a una amidina o guanidinobencilamina protegidas en el grupo amidino o guanidino, en cuyo caso el aminoácido N-terminal, o bien ya porta el residuo P4, donde P4 es o bien éste se enlaza a continuación al mismo y a continuación Los compuestos resultantes se purifican y opcionalmente se PEGilan.
18. Método para producir un compuesto según una de las reivindicaciones 1-16 el cual comprende las siguientes etapas:
(a) Amidación de un aminoácido, Na-protegido de manera correspondiente, que tiene el residuo R3, donde R3 se define tal como en la reivindicación 1, con una aminometilbenzamidina o -guanidina protegida correspondiente,
(b) Disociación del grupo protector Na del aminoácido que tiene R3 y reacción del producto resultante con el correspondiente bencilsulfonilaminoácido que tiene los residuos R1 y R2, donde R1 y R2 son tal como se definen en la reivindicación 1, y disociación de los grupos protectores restantes para obtener el compuesto de la fórmula (I) , y
después de una posible purificación
(c) opcionalmente PEGilación del compuesto resultante.
19. Medicamento que contiene al menos un compuesto según una de las reivindicaciones 1-16.
20. Medicamento según la reivindicación 19 para el tratamiento de la pérdida de sangre, principalmente en estados
hiperfibrinolíticos, en trasplantes de órganos o intervenciones quirúrgicas en el corazón, ante todo con derivación 20 (bypass) cardiopulmonar.
21. Adhesivo de fibrina que contiene al menos un compuesto según una de las reivindicaciones 1-16.
22. Uso de al menos un compuesto según una de las reivindicaciones 1-16 para producir un medicamento según la reivindicación 19 o 20 o de un adhesivo de fibrina según la reivindicación 21.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Procedimiento de compuestos antifúngicos, del 22 de Julio de 2020, de NQP 1598, Ltd: Procedimiento para preparar un compuesto de fórmula 5 ó 5*, o una mezcla de los mismos: **(Ver fórmula)** comprendiendo el método: (a) hacer reaccionar un compuesto […]
Productos terapéuticos basados en la lantionina sintetasa 2 tipo C, del 15 de Julio de 2020, de LANDOS BIOPHARMA, INC: Un compuesto de la fórmula: **(Ver fórmula)** o una sal o éster farmacéuticamente aceptable de este, en donde: Q es piperazina-1,4-diilo; […]
Derivados de piperidina en calidad de inhibidores de HDAC1/2, del 8 de Julio de 2020, de Regenacy Pharmaceuticals, Inc: Un compuesto de Fórmula IIIa: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde R1 se selecciona del grupo que consiste […]
Compuestos orgánicos, del 17 de Junio de 2020, de INTRA-CELLULAR THERAPIES, INC: Un compuesto de Fórmula I: **(Ver fórmula)** en forma libre o de sal, donde: R1 y R2 son independientemente H o alquilo C1-4 (por ejemplo, metilo o […]
Compuestos ahorradores de PPAR para el tratamiento de enfermedades metabólicas, del 3 de Junio de 2020, de Metabolic Solutions Development Company LLC (100.0%): Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: cada uno de R1 y R2 se selecciona independientemente entre […]
Uso de inhibidores de la PDE4 para la profilaxis y/o la terapia de la dislipoproteinemia y trastornos relacionados, del 27 de Mayo de 2020, de Albert-Ludwigs-Universität Freiburg: Inhibidor específico de la fosfodiesterasa 4 (PDE 4) para uso en el tratamiento profiláctico o terapéutico de la dislipoproteinemia, en donde el inhibidor […]
Nuevos usos terapéuticos de derivados de la bencilidenguanidina para el tratamiento de proteopatías, del 20 de Mayo de 2020, de InFlectis BioScience: Compuesto de la fórmula (I), o una sal farmacéuticamente aceptable del mismo, **(Ver fórmula)** o un tautómero de los mismos donde: […]