Derivado de indolizina y su utilización para fines médicos.
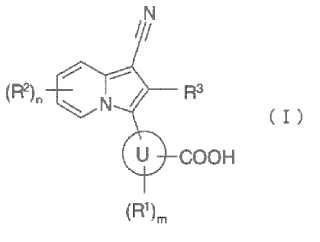
Un derivado de indolizina representado por la fórmula (I):**Fórmula**
en la que
el anillo U representa arilo o heteroarilo;
R1 representa un átomo de halógeno, un grupo hidroxi, nitro, amino o alquilo C1-6 que puede estar sustituido por unátomo de flúor;
R2 representa cualquiera de los siguientes (1) a (7)
(1) un átomo de halógeno
(2) un grupo hidroxi;
(3) amino;
(4) carbamoílo;
(5) ciano;
(6) carboxi;
(7) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, mono(di) alquilamino C1-6, acilo C2-7, acilamino C2-7, mono(di)alquilcarbamoílo C1-6, alquilsulfonilo C1-6, alquilsulfonilamino C1-6, mono(di) alquilsulfamoílo C1-6, alquiltio C1-6,alquenil C2-6 alcoxi C1-6, cicloalquilo C3-8, heterocicloalquilo de 3 a 8 miembros, cicloalquenilo C5-8,heterocicloalquenilo de 5 a 8 miembros, cicloalquiloxi C3-8, cicloalquilamino C3-8, cicloalquil C3-8 alquilo C1-6,cicloalquil C3-8 alcoxi C1-6, cicloalquil C3-8 alquilamino C1-6, arilo, heteroarilo, ariloxi, arilamino, arilcarbonilo,arilcarbonilamino, aril alcoxi C1-6, heteroariloxi, heteroarilamino, heteroarilcarbonilo o heteroarilcarbonilaminocualquiera de los cuales puede tener cualquier grupo seleccionado del grupo sustituyente α;
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2010/055692.
Solicitante: KISSEI PHARMACEUTICAL CO., LTD..
Nacionalidad solicitante: Japón.
Dirección: 19-48, YOSHINO MATSUMOTO-SHI NAGANO 399-8710 JAPON.
Inventor/es: SHIMIZU, KAZUO, TAKIGAWA,YASUSHI, IIZUKA,MASATO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/437 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo el sistema heterocíclico un ciclo de cinco eslabones teniendo el nitrógeno como heteroátomo del ciclo, p. ej. indolicina, beta-carbolina.
- A61P13/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 13/00 Medicamentos para el tratamiento del aparato urinario (diuréticos A61P 7/10). › de la orina o del tracto urinario p.ej.acidificadores de la orina.
- A61P13/12 A61P 13/00 […] › de los riñones.
- A61P19/02 A61P […] › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para problemas de las articulaciones, p.ej. artritis, artrosis.
- A61P19/06 A61P 19/00 […] › Agentes antigotosos, p.ej.agentes antihiperuricémicos o uricosúricos.
- A61P43/00 A61P […] › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- C07D471/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
PDF original: ES-2429148_T3.pdf
Fragmento de la descripción:
Derivado de indolizina y su utilización para fines médicos
Campo técnico [0001] La presente invención se refiere a derivados de indolizina útiles como medicamentos.
De forma más particular, la presente invención se refiere a derivados de indolizina que tienen actividades inhibidoras de la xantina oxidasa y son útiles como agentes para la prevención o el tratamiento de una enfermedad asociada con la anomalía del nivel de ácido úrico en suero, o sus profármacos, o sus sales farmacéuticamente aceptables.
Antecedentes de la técnica [0003] El ácido úrico es el producto final del metabolismo de la purina en seres humanos. En muchos mamíferos, a diferencia del ser humano, el ácido úrico se descompone adicionalmente mediante la urato oxidasa (uricasa) en el hígado a alantoína, que se excreta a través del riñón. En seres humanos, la ruta principal de excreción del ácido úrico es el riñón, en el que aproximadamente las dos terceras partes de ácido úrico se excretan en la orina. El resto se excreta en las heces, Cuando se produce una producción excesiva o una excreción disminuida de ácido úrico, se produce hiperuricemia. La hiperuricemia se clasifica en un tipo de producción en exceso de ácido úrico, un tipo de excreción en exceso de ácido úrico y un tipo mixto de ambas. Esta clasificación de la hiperuricemia es clínicamente importante. En un intento de reducir los efectos adversos de los agentes terapéuticos, los agentes terapéuticos se escogen de acuerdo con cada clase (por ejemplo, véase la referencia 1 no de patente) .
En la hiperuricemia con un tipo de producción en exceso de ácido úrico, aumenta la excreción urinaria de ácido úrico, y cuando la excreción urinaria de ácido úrico aumenta adicionalmente utilizando un fármaco uricosúrico, es posible que se desarrollen complicaciones de cálculos urinarios. Por tanto, en principio, alopurinol, un inhibidor de la producción de ácido úrico (o denominado algunas veces un inhibidor de la síntesis de ácido úrico, denominado a parir de ahora en el presente documento como “inhibidor de la producción de ácido úrico”) , se utiliza en un tipo de producción en exceso de ácido úrico.
El ácido úrico se produce a partir de cuerpos de purina, que se derivan de la dieta y se sintetizan de forma endógena, finalmente, oxidando la xantina mediante la xantina oxidasa. El alopurinol se desarrolla como un inhibidor de la xantina oxidasa y un inhibidor único de la producción de ácido úrico utilizado en la práctica médica. Aunque sin embargo, se ha informado de que el alopurinol es eficaz en la hiperuricemia y diversas enfermedades producidas por la misma, se han notificado también graves efectos adversos tales como síndrome de envenenamiento (angilitis hipersensible) , síndrome de Stevens-Johnson, dermatitis exfoliativa, anemia aplásica, disfunción hepática y similares. (por ejemplo, véase la referencia 2 no de patente) . Como una de las causas, se ha apuntado que alopurinol tiene una estructura de tipo ácido nucleico e inhibe una ruta del metabolismo de la pirimidina (por ejemplo, referencia 3 no de patente) .
Por otra parte, en la hiperuricemia con un tipo de excreción defectiva de ácido úrico, disminuye la excreción de ácido úrico. Se ha notificado que cuando se utiliza alopurinol, que se metaboliza a oxipurinol y se excreta a través del riñón por el mismo mecanismo que el ácido úrico, disminuye también la excreción de oxipurinol y aumenta la incidencia de trastornos hepáticos (por ejemplo, véase la referencia 4 no de patente) . Por tanto, en principio, se utilizan fármacos uricosúricos tales como probenecid, benzbromarona y similares en un tipo de excreción defectiva de ácido úrico. Estos fármacos uricosúricos, sin embargo, ejercen también efectos tales como trastornos gastrointestinales, cálculos urinarios o similares. Particularmente, benzbromarona es conocido como causa posible de hepatitis fulminante en el caso de pacientes idiosincráticos (por ejemplo, véanse las referencias 5 y 6 no de patente) .
De esta manera, se dice que tanto el inhibidor de la producción de ácido úrico existente como el fármaco uricosúrico tienen restricciones de utilización en pacientes o graves efectos adversos. De este modo, se ha deseado el desarrollo de un agente fácil de usar para el tratamiento de la hiperuricemia o similar.
El ácido úrico se elimina principalmente por el riñón, y se ha investigado hasta el momento la dinámica del urato en el riñón en algunos experimentos utilizando vesículas de membrana de borde de cepillo (BBMV) preparadas a partir de la corteza renal (por ejemplo, véanse las referencias 7 y 8 no de patente) . Se sabe que, en seres humanos, el ácido úrico pasa a través de los glomérulos del riñón libremente, y existen mecanismos de reabsorción y secreción de ácido úrico en el túbulo proximal (por ejemplo, véase la referencia 9 no de patente) .
En años recientes se ha identificado el gen (SLC22A12) que codifica el transportador de urato del riñón humano (por ejemplo, véase la referencia 10 no de patente) . El transportador codificado por este gen (transportador 1 de urato, denominado a partir de ahora en el presente documento como “URAT1”) es una molécula de tipo 12transmembrana que pertenece a la familia OAT. El ARNm de URAT1 se expresa de forma específica en el riñón, y se ha observado la localización de URAT1 en el lado apical del túbulo proximal en la sección de tejido de riñón humano. En un experimento que utilizaba un sistema de expresión en oocitos de Xenopus, se ha demostrado la captación de ácido úrico a través de URAT 1. Además, se ha demostrado que la captación de ácido úrico es transportada por el intercambio con aniones orgánicos tales como ácido láctico, ácido pirazinacarboxílico (PZA) , ácido nicotínico y similares, y que la captación de ácido úrico a través de URAT 1 está inhibida por los fármacos uricosúricos, probenecid y benzbromarona. Por tanto, tal como se esperaba del experimento que utilizaba vesículas de membrana, se ha sugerido con fuerza que URAT1 es un intercambiador de urato/anión. Esto es, se ha demostrado que URAT 1 es un transportador que juega un importante papel en la reabsorción del ácido úrico en el riñón (por ejemplo, véase la referencia 10 no de patente) .
Además, se ha aclarado la relación entre URAT 1 y las enfermedades. La hipouricemia renal idiopática es una enfermedad en la que la excreción del ácido úrico está aumentada debido a la dinámica anormal del urato en el riñón y el nivel del ácido úrico en suero se vuelve bajos. Se sabe que la enfermedad está a menudo asociada con los cálculos urinarios o insuficiencia renal aguda después del ejercicio. Se ha identificado URAT 1 como un gen causante de la hipouricemia renal (por ejemplo, véase la referencia 10 no de patente) . Estas incidencias sugieren también con fuerza que URAT 1 es responsable de controlar el nivel de ácido úrico en suero.
Por tanto, una sustancia que tiene una actividad inhibidora de URAT1 es útil como un agente para el tratamiento y la prevención de enfermedades asociadas con elevados niveles de ácido úrico en suero, esto es, hiperuricemia, tofo gotoso, artritis gotosa, trastorno renal asociado con hiperuricemia, cálculos urinarios o similares.
En el tratamiento de la hiperuricemia, se ha notificado que una combinación de alopurinol de un inhibidor de la producción de ácido úrico y un agente que tiene una actividad uricosúrica que disminuye el nivel de ácido úrico en suero más fuertemente que el uso individual de alopurinol (por ejemplo, véanse las referencias 11 y 12 no de patente) . Por tanto, cuando el tratamiento con un agente individual existente puede no ejercer suficiente efecto, se puede esperar un efecto terapéutico mayor mediante el uso de una combinación de un inhibidor de la producción de ácido úrico y un agente uricosúrico. Además, para la hiperuricemia con el tipo de excreción defectiva de ácido úrico, se considera que debido a que se puede disminuir la excreción urinaria disminuyendo el nivel de ácido úrico en suero, se puede reducir el riesgo de cálculos urinarios producidos por la monoterapia con un agente uricosúrico. Además, para la hiperuricemia con el tipo mixto, se espera un elevado efecto terapéutico. De esta manera, se espera que un agente que tenga una actividad inhibidora de la producción de ácido úrico y una actividad uricosúrica llegue a ser un agente extremadamente útil para la prevención o el tratamiento de la hiperuricemia o similar.
Como compuesto que tiene actividad inhibidora de la xantina oxidasa y actividad inhibidora de URAT1, se conoce la morina, un producto natural (véase... [Seguir leyendo]
Reivindicaciones:
1. Un derivado de indolizina representado por la fórmula (I) :
en la que el anillo U representa arilo o heteroarilo; R1 representa un átomo de halógeno, un grupo hidroxi, nitro, amino o alquilo C1-6 que puede estar sustituido por un átomo de flúor;
R2 representa cualquiera de los siguientes (1) a (7)
(1) un átomo de halógeno
(2) un grupo hidroxi; 20
(3) amino;
(4) carbamoílo; 25 (5) ciano;
(6) carboxi;
(7) alquilo C1-6, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, mono (di) alquilamino C1-6, acilo C2-7, acilamino C2-7, mono (di)
alquilcarbamoílo C1-6, alquilsulfonilo C1-6, alquilsulfonilamino C1-6, mono (di) alquilsulfamoílo C1-6, alquiltio C1-6, alquenil C2-6 alcoxi C1-6, cicloalquilo C3-8, heterocicloalquilo de 3 a 8 miembros, cicloalquenilo C5-8, heterocicloalquenilo de 5 a 8 miembros, cicloalquiloxi C3-8, cicloalquilamino C3-8, cicloalquil C3-8 alquilo C1-6, cicloalquil C3-8 alcoxi C1-6, cicloalquil C3-8 alquilamino C1-6, arilo, heteroarilo, ariloxi, arilamino, arilcarbonilo, arilcarbonilamino, aril alcoxi C1-6, heteroariloxi, heteroarilamino, heteroarilcarbonilo o heteroarilcarbonilamino cualquiera de los cuales puede tener cualquier grupo seleccionado del grupo sustituyente a;
m representa un número entero entre 0 y 2, y cuando m es 2, estos R1 son opcionalmente diferentes entre sí; n representa un número entero entre 0 y 3, y cuando n es 2 o 3, estos R2 son opcionalmente diferentes entre sí; y cuando dos R2 unidos a los átomos adyacentes en el anillo de indolizina existen y representan de forma independiente un grupo seleccionado entre el grupo que consiste en alquilo C1-6, que se puede sustituir por un átomo de flúor y alcoxi C1 , que se puede sustituir por un átomo de flúor, estos dos R2 forman opcionalmente un anillo de 5 a 8 miembros junto con los átomos de unión en el anillo de indolizina;
R3 representa un átomo de hidrógeno, un átomo de cloro o un átomo de flúor; y el grupo sustituyente a consiste en 45 un átomo de flúor, un átomo de cloro, un grupo hidroxi, amino, carboxi, carbamoílo, ciano, alquilo C1-6, alcoxi C1-6 y mono (di) alquilamino C1-6, o uno de sus profármacos, o una de sus sales farmacéuticamente aceptables, en el que “profármaco” significa un compuesto en el que uno o más grupos carboxi de un compuesto representado por la fórmula general anterior (I) está sustituido por un grupo formador de un profármaco, en el que el grupo formador de un profármaco se selecciona entre el grupo constituido por alquilo C1-6, alquil C1-6-COO-alquileno C1-6, alquil C1-6OCOO-alquileno C1-6, cicloalquil C3-8-OCOO-alquileno C1-6, mono (di) hidroxialquil C1-6-OCOO-alquileno C1-6, alcoxi C1-6 alcoxi C1-6 alquilo C1-6, mono (di) alquilamino C1-6 alquilo C1-6, heterocicloalquilalquilo C1-6 de 3 a 8 miembros, y alquil C1-6-OCO-aminoalquileno C1-6.
2. Un derivado de indolizina tal como se reivindica en la reivindicación 1, representado por la fórmula (Ia) :
en la que el anillo U representa arilo o heteroarilo; 15 R1a representa un átomo de hidrógeno, un átomo de flúor, un grupo hidroxi, amino, metilo o trifluorometilo; R2a y R2b representan de forma independiente cualquiera de los siguientes (a1) a (a4) : 20 (a1) un átomo de hidrógeno; (a2) un átomo de halógeno; (a3) un grupo hidroxi; 25 (a4) alquilo C1-6, alcoxi C1-6, mono (di) alquilamino C1-6, acilo C2-7, alquiltio C1-6, cicloalquilo C3-8, heterocicloalquilo de 3 a 8 miembros, arilo o heteroarilo, cada uno de los cuales puede tener algún grupo seleccionado entre el grupo sustituyente a; R2c
representa un átomo de hidrógeno, un átomo de halógeno, un grupo hidroxi, alquilo C1-6 que puede tener cualquier grupo seleccionado entre el grupo sustituyente a o alcoxi C1-6 que puede tener cualquier grupo seleccionado entre el grupo sustituyente a; o cuando R2a y R2b, o R2b y R2c representan de forma independiente un grupo seleccionado entre el grupo que consiste en alquilo C1-6 que puede estar sustituido por un átomo de flúor y alcoxi C1-6, que puede estar sustituido por un átomo de flúor, forman opcionalmente un anillo de 5 a 8 miembros junto con los átomos en el anillo de indolizina;
R2d representa un átomo de hidrógeno o un átomo de flúor;
R3a representa un átomo o un átomo de flúor; y
el grupo sustituyente a tiene el mismo significado que se ha descrito en la reivindicación 1 o uno de sus profármacos, o una de sus sales farmacéuticamente aceptables en el que “profármaco” significa un compuesto en el que uno o más grupos carboxi de un compuesto representado 45 por la fórmula general anterior (Ia) está sustituido por un grupo formador de un profármaco, en el que el grupo formador de un profármaco se selecciona entre constituido por alquilo C1-6, alquil C1-6-COO-alquileno C1-6, alquil C1-6OCOO-alquileno C1-6, cicloalquil C3-8-OCOO-alquileno C1-6, mono (di) hidroxialquil C1-6-OCOO-alquileno C1-6, alcoxi C1-6 alcoxi C1-6 alquilo C1-6, mono (di) alquilamino C1-6 alquilo C1-6, heterocicloalquilalquilo C1-6 de 3 a 8 miembros, y alquil C1-6-OCO-aminoalquileno C1-6.
3. Un derivado de indolizina tal como se reivindica en la reivindicación 2, en el que el anillo U representa un anillo de benceno, un anillo de piridina, un anillo de tiofeno o un anillo de tiazol, o uno de sus profármacos o una de sus sales farmacéuticamente aceptable 4. Un derivado de indolizina tal como se reivindica en la reivindicación 2, en el que el grupo representado por la fórmula:
es un grupo representado por la fórmula:
y R1a representa un átomo de hidrógeno o un grupo hidroxi, o uno de sus profármacos, o una de sus sales 20 farmacéuticamente aceptable.
5. Un derivado de indolizina tal como se reivindica en la reivindicación 3 o 4, en el que R2a y R2b representan cualquiera de los siguientes (b1) a (b4) :
(b1) un átomo de hidrógeno;
(b2) un átomo de halógeno;
(b3) un grupo hidroxi; 30
(b4) alquilo C1-6, alcoxi C1-6, mono (d) alquilamino C1-6 o hidroxialquilo C1-6 cada uno de los cuales puede estar
sustituido por un átomo de flúor; y
R2c
representa un átomo de hidrógeno, un átomo de halógeno, un grupo hidroxi, alquilo C1-6 que puede estar 35 sustituido por un átomo de flúor o alcoxi C1-6 que puede estar sustituido por un átomo de flúor, o uno de sus profármacos, o una de sus sales farmacéuticamente aceptables;
6. Un derivado de indolizina tal como se reivindica en una cualquiera de las reivindicaciones 2 a 5, en el que R2d representa un átomo de hidrógeno, o uno de sus profármacos, o una de sus sales farmacéuticamente aceptable.
7. Un derivado de indolizina tal como se reivindica en una cualquiera de las reivindicaciones 1 a 6, en el que R3 o R3a representa un átomo de hidrógeno, o uno de sus profármacos, o una de sus sales farmacéuticamente aceptable.
8. Un derivado de indolizina tal como se reivindica en l reivindicación 6 o 7, en el que R1a representa un átomo de hidrógeno o un grupo hidroxi;
R2a representa un átomo de hidrógeno, un átomo de flúor, un átomo de cloro, metilo, etilo, metoxi, monofluorometilo, difluorometilo, trifluorometilo, difluorometoxi, o trifluorometoxi;
R2b representa un átomo de hidrógeno, un átomo de flúor, un átomo de cloro, metilo, etilo, metoxi, monofluorometilo, difluorometilo, trifluorometilo, difluorometoxi o trifluorometoxi; opcionalmente R2b
en el que representa un átomo de hidrógeno, metilo, etilo, metoxi, monofluorometilo, difluorometilo, trifluorometilo, difluorometoxi o trifluorometoxi; y
R2c
representa un átomo de hidrógeno, un átomo de flúor, un átomo de cloro, metilo, monofluorometilo, difluorometilo, o trifluorometilo, o uno de sus profármacos o una de sus sales farmacéuticamente aceptables;
9. Un derivado de indolizina tal como se reivindica en la reivindicación 8, en el que R1a representa un átomo de hidrógeno, o uno de sus profármacos o una de sus sales farmacéuticamente aceptable.
10. Un derivado de indolizina tal como se reivindica en la reivindicación 8, en el que R1a representa un grupo hidroxi, o uno de sus profármacos, o una de sus sales farmacéuticamente aceptable.
11. Un derivado de indolizina tal como se reivindica en la reivindicación 8, que se selecciona entre el grupo que consiste en
Ácido 4- (1cianoindolizina-3-il) benzoico Ácido 4- (1-ciano-7-metilindolizina-3-il) benzoico, Ácido 4- (8-cloro-1-cianoindolizina-3-il) benzoico, Ácido 4- (1-ciano-8-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-6-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-6, 8-dimetilindolizina-3-il) benzoico, Ácido 4- (1-ciano-8-fluoro-7-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-6-fluoro-7-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-7-etilindolizina-3-il) benzoico, Ácido 4- (1-ciano-8-etilindolizina-3-il) benzoico, Ácido 4- (1-ciano-8-fluoroindolizina-3-il) benzoico, Ácido 4- (1-ciano-6-fluoroindolizina-3-il) benzoico, Ácido 4- (1-ciano-7-trifluorometilindolizina-3-il) benzoico, Ácido 4- (1-cianoindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-7-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-8-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-6-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-6, 8-dimetilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-6-fluoro-7-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-8-fluoro-7-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-8-etilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-8-fluoroindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-6-fluoroindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-7-trifluorometilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-7-fluorometilindolizina-3-il) benzoico,
Ácido 4- (6-cloro-1-ciano-7-metilindolizina-3-il) benzoico, Ácido 4- (8-cloro-1-ciano-7-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-7, 8-dimetilindolizina-3-il) benzoico, Ácido 4- (7-cloro-1-ciano-8-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-6, 8-difluoroindolizina-3-il) benzoico, Ácido 4- (1-ciano-8-metoxiindolizina-3-il) benzoico, Ácido 4- (1-ciano-7-metoxiindolizina-3-il) benzoico, Ácido 4- (1-ciano-7-metoxi-6-metilindolizina-3-il) benzoico, Ácido 4- (1-ciano-6-fluoro-7-trifluorometilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (6-cloro-1-ciano-7-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (8-cloro-1-ciano-7-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-7, 8-dimetilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (7-cloro-1-ciano-8-metilindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-6, 8-difluoroindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-7-metoxiindolizina-3-il) -2-hidroxibenzoico, Ácido 4- (1-ciano-7-metoxi-6-metilindolizina-3-il) -2-hidroxibenzoico, y Ácido 4- (1-ciano-7-fluorometilindolizina-3-il) -2-hidroxibenzoico, o una de sus sales farmacéuticamente aceptable.
12. Un derivado de indolizina o un profármaco o una de sus sales farmacéuticamente aceptable tal como se reivindica en una cualquiera de las reivindicaciones 1 a 11, que es un inhibidor de la xantina oxidasa.
13. Una composición farmacéutica que comprende como un principio activo un derivado de indolizina o un profármaco o una de sus sales farmacéuticamente aceptable tal como se reivindica en una cualquiera de las reivindicaciones 1 a 11
14. Una composición farmacéutica tal como se reivindica en la reivindicación 13, para uso en la prevención o el tratamiento de una enfermedad seleccionada entre el grupo que consiste en hiperuricemia, tofo gotoso, artritis gotosa, trastorno renal asociado con hiperuricemia y cálculos urinarios opcionalmente para uso en la prevención o el tratamiento de la hiperuricemia, opcionalmente para uso en la disminución del nivel de ácido úrico en suero.
15. Una composición farmacéutica tal como se reivindica en la reivindicación 13, que es un inhibidor de la producción de ácido úrico.
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Derivado de dihidroindolizinona, del 1 de Julio de 2020, de ONO PHARMACEUTICAL CO., LTD.: (3S)-3-[2-(6-amino-2-fluoro-3-piridinil)-4-fluoro-1H-imidazol-5-il]-7-[5-cloro-2-(1H-tetrazol-1-il)fenil]-2,3-dihidro- (1H)-indolizinona, una…
Inhibidor de fibrosis, del 1 de Julio de 2020, de NIPPON SHINYAKU CO., LTD.: Composición farmacéutica que comprende un derivado heterocíclico seleccionado de ácido 2-{4-[N-(5,6-difenilpirazin-2-il)-N-isopropilamino]butiloxi}acético […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Compuestos utilizados como inhibidores de la quinasa reordenada durante la transfección (RET), del 1 de Julio de 2020, de GlaxoSmithKline Intellectual Property Development Limited: Un compuesto de acuerdo con la Fórmula (I), o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde: X es N o CR5; Y es un enlace; […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]