Procedimiento de cristalización de eritromicina.
Un procedimiento para la recristalización de eritromicina, caracterizado por las etapas que comprenden:
1) en primer lugar, disolver eritromicina o una sal de eritromicina en diclorometano o una mezcla disolventeque comprende diclorometano en condiciones alcalinas para formar una solución de eritromicina;
2) después, enfriar la solución de eritromicina gradualmente desde 37 ºC hasta -5 5 ºC para formar unasuspensión de cristales de eritromicina;
3) después, separar los cristales de eritromicina de la suspensión; y
4) finalmente lavar y secar los cristales,
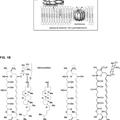
en el que la eritromicina tiene la siguiente estructura: **Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CN2009/001204.
Solicitante: Sunshine Lake Pharma Co., Ltd .
Nacionalidad solicitante: China.
Dirección: Northern Industrial Area Songshan Lake Dongguan Guangdong 523000 CHINA.
Inventor/es: MA,XIAOPING, SONG,LUNING.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H17/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 17/00 Compuestos que contienen radicales heterocíclicos unidos directamente a los heteroátomos de los radicales sacárido. › Heterociclos que contienen ocho o más miembros cíclicos, p. ej. eritromicinas.
PDF original: ES-2423795_T3.pdf
Fragmento de la descripción:
Procedimiento de cristalización de eritromicina Campo de la invención La presente invención se refiere a un procedimiento para la recristalización de eritromicina.
Antecedentes de la invención La eritromicina, C37H67NO13, peso molecular de 733, 94, es un antibiótico con un anillo macrólido de 14 miembros. Tiene un espectro antimicrobiano similar o ligeramente más amplio que el de la penicilina, y tiene un fuerte efecto antibacteriano frente a bacterias G +. Puede usarse como material de partida para la preparación de material que contenga eritromicina, o como material de partida para la preparación de derivados de eritromicina.
El documento CN1513864A desvela un procedimiento de recristalización dinámica para la preparación de eritromicina a partir de una sal de eritromicina, que usa acetona y agua como disolventes. La cantidad de eritromicina A en el producto formado es menor del 93 %. La cantidad de agua en los cristales de eritromicina es mayor del 3, 5 %. El título microbiológico de los cristales de eritromicina es menor de 930 μ/mg.
El documento RO 99 792 B1 (INST DE CERCETARI CHIMICO FARMA) del 29 de junio 1990 desvela un procedimiento para la cristalización de eritromicina que se disuelve en diclorometano en condiciones alcalinas.
La presente invención usa un nuevo disolvente para obtener eritromicina con una mejor calidad. La cantidad de eritromicina A en los cristales de eritromicina (procedimiento de detección mediante HPLC) es mayor del 94, 5 %. La cantidad de diclorometano en los cristales de eritromicina es menor de 600 ppm. La cantidad de agua en los cristales de eritromicina es menor del 2, 5 %. El título microbiológico de los cristales de eritromicina es mayor de 940 μ/mg.
Descripciones de la invención El fin de la presente invención es proporcionar un procedimiento de recristalización de eritromicina que sea capaz de formar un producto con una mayor cantidad de eritromicina A. 25 Para conseguir el fin de la presente invención, el procedimiento para la recristalización de eritromicina de la presente invención comprende las etapas: 1) en primer lugar, disolver eritromicina o una sal de eritromicina en diclorometano o una mezcla disolvente que comprende diclorometano en condiciones alcalinas para formar una solución de eritromicina;
2) después, enfriar la solución de eritromicina gradualmente desde 37 ºC hasta -5 ºC para formar una 30 suspensión de cristales de eritromicina; 3) después, separar los cristales de eritromicina de la suspensión; 4) y finalmente lavar y secar los cristales. en el que la sal de eritromicina puede ser tiocianato de eritromicina o lactato de eritromicina. La mezcla disolvente que comprende diclorometano puede comprender adicionalmente uno cualquiera de etanol, 35 acetona, acetato de etilo o acetato de butilo, u otros alcoholes, cetonas o ésteres similares. El contenido en volumen
de diclorometano en la mezcla disolvente es del 60 al 100 %.
La condición alcalina se refiere a que el pH de la solución de eritromicina es de 8, 6 - 12.
La cantidad de eritromicina A en la solución de eritromicina es del 4 al 20 %, preferentemente del 14 al 16 %.
La temperatura se enfría gradualmente desde 37 ºC hasta -5 ºC a una velocidad de enfriamiento de 1 a 10 ºC por hora, para un periodo de tiempo de recristalización desde 2 hasta 36 horas. Preferentemente, la temperatura de la solución de eritromicina se mantiene a 23 - 28 ºC durante entre 1 y 10 horas durante el enfriamiento gradual.
La etapa de separación puede realizarse mediante el equipo usado habitualmente en la técnica, tal como centrífugas, equipo de filtración y similares.
Los cristales de eritromicina separados mediante centrifugación puede lavarse con un disolvente orgánico o agua pura, y el residuo del disolvente en los cristales de eritromicina puede retirarse mediante un procedimiento de secado.
El disolvente orgánico comprende más del 90 % de diclorometano, y otros componentes orgánicos tales como alcoholes, cetonas o ésteres.
Mediante un ensayo, la cantidad de eritromicina A en los cristales de eritromicina (procedimiento de detección mediante HPLC) es mayor del 94, 5 %. La cantidad de diclorometano en los cristales de eritromicina es menor de 600 ppm. La cantidad de agua en los cristales de eritromicina es menor del 2, 5 %. El título microbiológico de los cristales de eritromicina es mayor de 940 μ/mg.
La presente invención utiliza el hecho de que la solubilidad de la eritromicina en el disolvente que comprende diclorometano disminuye al disminuir la temperatura. La eritromicina disuelta en el disolvente de diclorometano se enfría gradualmente desde una temperatura elevada hasta una temperatura baja para formar los cristales de eritromicina y para formar un producto con una mayor cantidad de eritromicina A.
Ejemplos Los ejemplos experimentales solo pretenden ser ilustrativos de la presente invención, pero no deben usarse para limitar el ámbito de la presente invención.
Ejemplo 1
Se añadió tiocianato de eritromicina (200 g) en diclorometano (500 ml) , se agitó con calor a 37 ºC y se ajustó a un pH de 12 hasta que la solución se volvió transparente. La fase acuosa superior se separó y se retiró para obtener una solución de diclorometano con aproximadamente un 14 % de eritromicina A. La solución de diclorometano se enfrió hasta 24 ºC, se mantuvo durante 2 horas y se enfrió hasta -4 ºC en 5 horas. Los cristales formados se filtraron. Se usó diclorometano (20 ml) para lavar los cristales, y los cristales se filtraron durante 5 minutos más. La cantidad de eritromicina A en la eritromicina seca es del 95, 2 % con un contenido de diclorometano de 150 ppm, un contenido de agua del 1, 0 % y un título microbiológico de 948 μ/mg.
Ejemplo 2
Se añadió eritromicina (100 g) en diclorometano (600 ml) , se agitó con calor a 35 ºC y se ajustó a un pH de 10 hasta que la solución se volvió transparente. La fase acuosa superior se separó y se retiró para obtener una solución de diclorometano con aproximadamente un 16 % de eritromicina A. La solución de diclorometano se enfrió hasta 28 ºC, se mantuvo durante 5 horas y después se enfrió hasta -2 ºC en 5 horas. Los cristales formados se filtraron. Se usó diclorometano (20 ml) para lavar los cristales, y los cristales se filtraron durante 5 minutos más. La cantidad de eritromicina A en la eritromicina seca es del 96, 0 % con un contenido de diclorometano de 178 ppm, un contenido de agua del 0, 9 % y un título microbiológico de 955 μ/mg.
Ejemplo 3
Se añadió una mezcla de tiocianato de eritromicina y otras impurezas (100 g) en una mezcla disolvente (300 ml) que comprende diclorometano y acetona (el contenido en volumen de diclorometano es del 60 %) , se agitó con calor a 34 ºC y se ajustó a un pH de 12 hasta que la solución se volvió transparente. La fase acuosa superior se separó y se retiró para obtener una solución de diclorometano con aproximadamente un 15 % de eritromicina A. La solución de diclorometano se enfrió hasta 23 ºC, se mantuvo durante una hora, y después se enfrió hasta 3 ºC en 16 horas. Los cristales formados se filtraron. Se usó diclorometano (20 ml) (el contenido de diclorometano es del 95 % y el de etanol es del 5 %) para lavar los cristales, y los cristales se filtraron durante 5 minutos más. La cantidad de eritromicina A en la eritromicina seca es del 94, 6 % con un contenido de diclorometano de 352 ppm, un contenido de agua del 2, 2 % % y un título microbiológico de 941 μ/mg.
Ejemplo 4
Se añadió eritromicina (100 g) en diclorometano (600 ml) . Se añadió acetona (20 ml) , se agitó con calor a 35 ºC y se ajustó a un pH de 9, 8 hasta que la solución se volvió transparente. La fase acuosa superior se separó y se retiró para obtener una solución de diclorometano con aproximadamente un 15 % de eritromicina A. La solución de diclorometano se enfrió hasta 24 ºC, se mantuvo durante 2 horas y después se enfrió hasta 0 ºC en 8 horas. Los cristales formados se filtraron. Se usó diclorometano (20 ml) para lavar los cristales, y los cristales se filtraron durante 5 minutos más. La cantidad de eritromicina A en la eritromicina seca es del 95, 4 % con un contenido de diclorometano de 247 ppm, un contenido de agua del 1, 2 % y un título microbiológico de 946 μ/mg.
Ejemplo 5
Se añadió una mezcla de tiocianato de eritromicina de eritromicina y otras impurezas (100 g) en diclorometano (300 ml) . Se añadió acetato de butilo (o acetato de etilo) (50 ml) , se agitó con calor a 34 ºC y se ajustó a un pH de 12 hasta que la solución se volvió transparente. La fase acuosa superior se separó y se retiró para obtener... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para la recristalización de eritromicina, caracterizado por las etapas que comprenden:
1) en primer lugar, disolver eritromicina o una sal de eritromicina en diclorometano o una mezcla disolvente que comprende diclorometano en condiciones alcalinas para formar una solución de eritromicina; 2) después, enfriar la solución de eritromicina gradualmente desde 37 ºC hasta -5 ºC para formar una suspensión de cristales de eritromicina; 3) después, separar los cristales de eritromicina de la suspensión; y 4) finalmente lavar y secar los cristales,
en el que la eritromicina tiene la siguiente estructura:
2. El procedimiento de la reivindicación 1, caracterizado porque la mezcla disolvente que comprende diclorometano comprende adicionalmente uno cualquiera de etanol, acetona, acetato de etilo o acetato de butilo; y el contenido en volumen de diclorometano en la mezcla disolvente es del 60 al 100 %.
3. El procedimiento de la reivindicación 1 o 2, caracterizado porque la condición alcalina se refiere a que el pH de 15 la solución de eritromicina es de 8, 6 - 12.
4. El procedimiento de una cualquiera de las reivindicaciones 1-3, caracterizado porque la cantidad de eritromicina A en la solución de eritromicina es del 4 al 20 %.
5. El procedimiento de una cualquiera de las reivindicaciones 1-4, caracterizado porque una temperatura se enfría
gradualmente desde 37 ºC hasta -5 ºC a una velocidad de enfriamiento de entre 1 y 10 ºC por hora durante un 20 periodo de tiempo de recristalización de 2 a 36 horas.
6. El procedimiento de la reivindicación 5, caracterizado porque la temperatura de la solución de eritromicina se mantiene .
2. 28 ºC durante entre 1 y 10 horas durante el enfriamiento gradual.
7. El procedimiento de una cualquiera de las reivindicaciones 1-6, caracterizado porque se usa un disolvente orgánico o agua pura para el lavado.
8. El procedimiento de la reivindicación 7, caracterizado porque el disolvente orgánico comprende más del 90 % de diclorometano y otro componente disolvente orgánico, en el que el componente disolvente orgánico es un alcohol, una cetona o un éster.
Patentes similares o relacionadas:
Polimorfos de 20,23-piperidinil-5-O-micaminosiltilonolida, del 20 de Mayo de 2020, de INTERVET INTERNATIONAL B.V: Una forma cristalina de 20,23-dipiperidinil-5-O-micaminosil-tilonolida que tiene al menos una de las siguientes características: un espectro FT-Raman que comprende […]
Derivados de azitromicina con propiedades de potenciación de la barrera epitelial, del 13 de Mayo de 2020, de EpiEndo Pharmaceuticals ehf: Un compuesto de acuerdo con la fórmula (I) **(Ver fórmula)** En donde R1 es OH; R2 es de acuerdo con la fórmula (III) **(Ver […]
Derivados de avermectina B1 que tienen un sustituyente alcoximetilo en la posición 4'''' o 4'', del 17 de Febrero de 2020, de Boehringer Ingelheim Animal Health USA Inc: Compuesto de fórmula**Fórmula** en la que n es 0 o 1; A-B es -CH=CH; R1 es sec-butilo o isopropilo; R2 es CH2CH3, p-ClC6H4, CH2(CH2)2N3 […]
Levoisovalerilespiramicina III y preparaciones, métodos de preparación y utilizaciones de la misma, del 1 de Enero de 2020, de Shenyang Fuyang Pharmaceutical Technology Co., Ltd: Compuesto cristalino de levoisovalerilespiramicina III, en el que, la fórmula estructural química de la levoisovalerilespiramicina III se representa como la fórmula […]
 Derivado de anfotericina b con toxicidad reducida, del 25 de Septiembre de 2019, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ILLINOIS: C2'epiAmB, representado por**Fórmula**
o una sal farmacéuticamente aceptable del mismo.
Derivado de anfotericina b con toxicidad reducida, del 25 de Septiembre de 2019, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ILLINOIS: C2'epiAmB, representado por**Fórmula**
o una sal farmacéuticamente aceptable del mismo.
Forma cristalina de levoisovalerilespiramicina II y preparaciones, procedimientos de preparación y utilizaciones de la misma, del 7 de Agosto de 2019, de Shenyang Fuyang Pharmaceutical Technology Co., Ltd: Compuesto de levoisovalerilespiramicina II, en el que, la fórmula estructural química de la levoisovalerilespiramicina II se representa como la fórmula (II), en condiciones […]
Derivados de la anfotericina B con índice terapéutico mejorado, del 20 de Septiembre de 2018, de The Board of Trustees of the University of Illionis: Un compuesto, o una sal farmacéuticamente aceptable del mismo, el compuesto que se selecciona de**Fórmula**
Procedimientos para tratar enfermedades gastrointestinales, del 11 de Abril de 2018, de Cempra Pharmaceuticals, Inc: Una cantidad terapéuticamente efectiva de un compuesto de fórmula **Fórmula** o una sal farmacéuticamente aceptable del mismo, donde: R10 es hidrógeno […]