Conjugados de polímero-factor von Willebrand.
Constructo proteináceo que no está unido a Factor VIII (FVIII) para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o a deficiencias de FVIII,
de FvW o de ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII endógeno en la sangre del mamífero; comprendiendo el constructo proteináceo
a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW) plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad biológica del FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno, y dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW;
teniendo dicho constructo la capacidad de unirse a la molécula de FVIII endógena del mamífero y, cuando se administra al mamífero, la vida media in vivo del constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII endógena unida a dicho constructo se incrementa en comparación con la vida media in vivo de la molécula de FVIII unida a FvW y no unida con al menos una molécula polimérica fisiológicamente aceptable.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/046879.
Solicitante: BAXTER INTERNATIONAL INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: Law Department, One Baxter Parkway Deerfield, IL 60015 ESTADOS UNIDOS DE AMERICA.
Inventor/es: TURECEK, PETER, SCHEIFLINGER, FRIEDRICH, SIEKMANN,JUERGEN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K47/48
PDF original: ES-2434035_T3.pdf
Fragmento de la descripción:
Conjugados de polímero-factor von Willebrand.
CAMPO DE LA INVENCIÓN
La presente invención se refiere a métodos para prolongar la vida media in vivo del FVIII en la sangre de un mamífero que presenta una alteración hemorrágica asociada a defectos funcionales o deficiencias de al menos uno de entre el FVIII, y el FvW.
ANTECEDENTES DE LA INVENCIÓN
El FvW es una glucoproteína adhesiva multimérica presente en el plasma de los mamíferos que tiene múltiples funciones fisiológicas. Durante la hemostasia primaria, el FvW actúa como mediador entre receptores específicos sobre la superficie plaquetaria y los componentes de la matriz extracelular, tal como el colágeno. Además, el FvW actúa como proteína transportadora y estabilizadora para el FVIII procoagulante. El FvW se sintetiza en células endoteliales y megacariocitos como una molécula precursora de 2.813 aminoácidos. El polipéptido precursor, pre-pro-FvW, consiste en un péptido señal de 22 residuos, un pro-péptido de 741 residuos y el polipéptido de 2.050 residuos hallado en FvW de plasma maduro (Fischer y col., FEBS Lett. 351: 345-348, 1994) . Después de su secreción en el plasma, el FvW circula en forma de diversas especies de diferente tamaño molecular. Estas moléculas de FvW consisten en oligómeros y multímeros de la subunidad madura de 2.050 residuos aminoácidos. El FvW se puede encontrar habitualmente en el plasma con tamaños desde un dímero hasta multímeros de 50 - 100 dímeros (Ruggeri y col. Thromb. Haemost. 82: 576-584, 1999) . La vida media in vivo del FvW humano en el sistema circulatorio humano es de aproximadamente 12 a 20 horas. El FVIII tiene una vida media in vivo relativamente corta, aproximadamente 8 a 12 horas, lo que hace necesaria una readministración frecuente para el tratamiento de pacientes con alteraciones hemorrágicas asociadas a defectos funcionales o deficiencias de al menos uno de entre FVIII y FvW.
En el estado anterior de la técnica se ha descrito que el FvW recombinante (FvWr) producido en cultivos de células eucarióticas está más intacto y menos degradado proteolíticamente que el FvW derivado de plasma (Fischer y col., FEBS Lett. 375: 259-262, 1995) . El documento EP 0 784 632 describe un método para aislar un FvW de alta pureza mediante la purificación de FvW recombinante utilizando una cromatografía de intercambio aniónico. En la técnica también se conocen métodos para producir a gran escala FvW homogéneo y estructuralmente intacto (Schlokat y col., Biotechnol. Appl. Biochem. 24: 257-267, 1996; Fischer y col., CMLS 53: 943-950, 1997) . El FvW recombinante se ha caracterizado utilizando modelos caninos, murinos y porcinos de la enfermedad de von Willebrand (EvW) (Turecek y col., Blood 90: 3555-3567, 1997; Roussi y col., Blood Coag. Fibrinol. 9: 361-372, 1998; Schwarz y col., Haemophilia 4: 53-62, 1998; Schwarz y col., Semin. Thromb. Hemost. 28: 215-225, 2002) . El documento WO 00/49047 describe un método para producir una preparación de FvW mediante el tratamiento de pro-FvW con trombina. El documento WO 98/25969 proporciona un método para purificar proteínas que se unen a FvW utilizando un FvWr inmovilizado sobre un vehículo. En el documento EP 0 977 584 se describe el uso farmacéutico de propéptidos de FvW (pro-FvW) derivado de plasma y recombinante para tratar trastornos de la coagulación sanguínea. El documento US 6.037.452 describe la unión de FVIII y factor IX (FIX) a un óxido de poli (alquileno) a través de un engarce o un agente de acoplamiento. El documento EP 0 774 261 demuestra que el uso de un FvW recombinante con una vida media biológica in vivo prolongada estabiliza el FVIII sanguíneo de un mamífero e induce la producción de FVIII endógeno. No obstante, existe la necesidad de aumentar aún más la vida media in vivo del FvW y el FVIII en pacientes con alteraciones hemorrágicas basadas en FvW y FVIII.
Ya es sabido que el FvW estabiliza el FVIII in vivo y, por consiguiente, desempeña un papel crucial en la regulación de los niveles de FVIII en plasma y siendo por ello un factor central para controlar la hemostasia primaria y secundaria. También es sabido que, después de la administración de productos terapéuticos que contienen FvW, se puede observar un aumento del FVIII:C endógeno de 1 a 3 unidades por ml en 24 horas, lo que demuestra el efecto de estabilización in vivo del FvW sobre el FVIII.
Existe una gran necesidad de una nueva sustancia para ampliar el espectro de tratamiento de deficiencias en el FVIII de coagulación, también conocidas como hemofilia A.
Así, la presente invención proporciona un nuevo sistema para prolongar la vida media in vivo del FVIII en la sangre de un mamífero. Otro objeto de la presente invención es proporcionar métodos para mejorar el tratamiento de alteraciones hemorrágicas asociadas a defectos funcionales o deficiencias de FVIII, de FvW o ambos.
Los documentos WO 97/11957, EP 1 258 497 y EP 1 260 582 dan a conocer en cada caso conjugados de un polipéptido y un polímero biocompatible y un proceso para su producción. El documento WO 94/15625 describe un FVIII modificado con PEG que tiene una vida media in vivo prolongada. El documento US 6.037.452 proporciona FVIII no inmunógeno de acción prolongada unido de forma covalente a un óxido de poli (alquileno) , tal como PEG. El documento WO 2004/075923 describe conjugados de FVIII unido de forma covalente con uno a tres polímeros solubles en agua. Lewis y col. (1994) Bioconjugate J, 5: 565-576, proporciona un método soluble en agua para la modificación de proteínas con DOTA.
Un primer aspecto de la invención proporciona un constructo proteináceo que no está unido a Factor VIII (FVIII) , para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o deficiencias de FVIII, de FvW o ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII endógeno en la sangre del mamífero; comprendiendo el constructo proteináceo:
a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW)
plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad
biológica de FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno, y
dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW; teniendo dicho constructo la capacidad de unirse a la molécula de FVIII endógena del mamífero y, cuando se administra al mamífero, la vida media in vivo del constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII endógena unida al constructo se incrementa en comparación con la vida media in vivo de la molécula de FVIII unida a FvW y no unida con al menos una molécula polimérica fisiológicamente aceptable.
Un segundo aspecto de la invención proporciona un constructo proteináceo no unido a Factor VIII (FVIII) para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o deficiencias de FVIII, FvW o ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII o de un precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII en la sangre del mamífero; comprendiendo el constructo proteináceo:
a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW)
plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad
biológica del FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno,
y dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW; administrándose al mamífero una primera dosis de al menos una molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII;
teniendo dicho constructo la capacidad de unirse a la molécula de FVIII o precursor, subunidad o fragmento de FVIII administrado y, cuando se administra al mamífero, la vida media in vivo del constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII o precursor, subunidad o fragmento de FVIII administrado unido a dicho constructo se incrementa en comparación con la vida media in vivo de la molécula o precursor, subunidad o fragmento de FVIII unido a FvW y no unido con al menos una molécula polimérica fisiológicamente aceptable.
Un tercer aspecto de la invención proporciona una molécula de FVIII... [Seguir leyendo]
Reivindicaciones:
1. Constructo proteináceo que no está unido a Factor VIII (FVIII) para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o a deficiencias de FVIII, de FvW o de ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII endógeno en la sangre del mamífero; comprendiendo el constructo proteináceo a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW) plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad biológica del FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno, y dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW;
teniendo dicho constructo la capacidad de unirse a la molécula de FVIII endógena del mamífero y, cuando se administra al mamífero, la vida media in vivo del constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII endógena unida a dicho constructo se incrementa en comparación con la vida media in vivo de la molécula de FVIII unida a FvW y no unida con al menos una molécula polimérica fisiológicamente aceptable.
2. Constructo proteináceo que no está unido a Factor VIII (FVIII) para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o a deficiencias de FVIII, de FvW o de ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII o de un precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII en la sangre del mamífero; comprendiendo el constructo proteináceo a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW) plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad biológica del FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno, y dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW; administrándose al mamífero una primera dosis de al menos una molécula de FVIII o precursor, subunidad
o fragmento de FVIII que tiene la actividad biológica del FVIII;
teniendo dicho constructo la capacidad de unirse a la molécula de FVIII o precursor, subunidad o fragmento de FVIII administrado y, cuando se administra al mamífero, la vida media in vivo del constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII o precursor, subunidad o fragmento de FVIII administrado unido a dicho constructo se incrementa en comparación con la vida media in vivo de la molécula o precursor, subunidad o fragmento de FVIII unido a FvW y no unido con al menos una molécula polimérica fisiológicamente aceptable.
3. Molécula de FVIII o un precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII, para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o deficiencias de FVIII, de FvW o de ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII o de un precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII en la sangre del mamífero;
administrándose al mamífero una primera dosis de al menos un constructo proteináceo que no está unida a FVIII y que comprende:
a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW) plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad biológica del FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno, y dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW;
teniendo dicho constructo la capacidad de unirse a la molécula de FVIII o precursor, subunidad o fragmento de FVIII administrado y, cuando se administra al mamífero, la vida media in vivo del constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII o precursor, subunidad o fragmento de FVIII administrado unido a dicho constructo se incrementa en comparación con la vida media in vivo de la molécula o precursor, subunidad o fragmento de FVIII unido a FvW y no unido con al menos una molécula polimérica fisiológicamente aceptable.
4. Complejo para su uso en el tratamiento de una alteración hemorrágica asociada a defectos funcionales o a deficiencias de FVIII, de FvW o de ambos en un mamífero, mediante la prolongación de la vida media in vivo del FVIII o de un precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII en la sangre del mamífero; comprendiendo el complejo:
un constructo proteináceo que incluye a) una molécula de FvW seleccionada de entre el grupo consistente en factor de von Willebrand (FvW) plasmático, FvW recombinante, un precursor, subunidad o fragmento de FvW que tiene una actividad biológica del FvW determinada en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno, y dímeros y multímeros de los mismos; y
b) al menos una molécula polimérica fisiológicamente aceptable unida a dicha molécula de FvW; y
una molécula de FVIII o un precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII, unido al constructo proteinácea;
y, cuando se administra al mamífero, la vida media in vivo de dicho constructo se incrementa en comparación con la vida media in vivo de la molécula de FvW, y la vida media in vivo de la molécula de FVIII o precursor, subunidad o fragmento de FVIII unido al constructo se incrementa en comparación con la vida media in vivo de la molécula o precursor, subunidad o fragmento de FVIII unido a FvW y no unido con al menos una molécula polimérica fisiológicamente aceptable.
5. Constructo proteináceo para su uso según la reivindicación 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, caracterizado porque se administra la molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII o para la administración simultánea con dicho constructo proteináceo.
6. Constructo proteináceo para su uso según la reivindicación 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, caracterizado porque se administra o se administra secuencialmente la molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII antes o después de la administración de dicho constructo proteináceo.
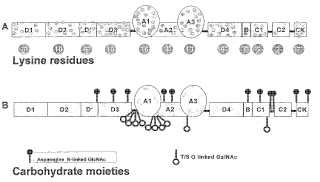
7. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, o complejo para su uso según la reivindicación 4, caracterizado porque dicha o dichas moléculas poliméricas fisiológicamente aceptables están unidas a un residuo carbohidrato de dicho FvW o dicho precursor, subunidad o fragmento de FvW.
8. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, o complejo para su uso según la reivindicación 4, caracterizado porque dicha o dichas moléculas poliméricas fisiológicamente aceptables están unidas a un residuo lisina de dicho FvW o dicho precursor, subunidad o fragmento de FvW.
9. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, o complejo para su uso según la reivindicación 4, caracterizado porque dicha molécula polimérica fisiológicamente aceptable se selecciona de entre el grupo consistente en poli (alquilenglicol) , poli (propilenglicol) , copolímeros de etilenglicol y propilenglicol, poliol poli (oxetilado) , alcohol poli (olefínico) , poli (vinilpirrolidona) , poli (hidroxialquilmetacrilamida) , poli (hidroxialquil-metacrilato) , poli (sacáridos) , poli (αhidroxiácido) , alcohol poli (vinílico) , polifosfaceno, polioxazolina y poli (N-acriloilmorfolina) .
10. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, o complejo para su uso según la reivindicación 4, caracterizado porque dicha molécula polimérica fisiológicamente aceptable es polietilenglicol (PEG) o un derivado del mismo.
11. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, o complejo para su uso según la reivindicación 4, caracterizado porque dicha molécula polimérica fisiológicamente aceptable es ácido polisiálico (PSA) o un derivado del mismo.
12. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación 3, o complejo para su uso según la reivindicación 4, caracterizado porque el FvW incluido en dicho constructo mantiene la actividad biológica de FvW de acuerdo con la determinación en un ensayo de cofactor de ristocetina o un ensayo de unión de colágeno.
13. Constructo proteináceo para su uso según la reivindicación 1 o 2, o molécula de FVIII o precursor, subunidad o fragmento de FVIII que tiene la actividad biológica del FVIII para su uso según la reivindicación
3, o complejo para su uso según la reivindicación 4, caracterizado porque el FvW o dicho precursor, subunidad o fragmento de FvW es un producto recombinante.
FvW:Ag (UI/ml plasma) ± SD
U FvW/ml plasma ± SD
Patentes similares o relacionadas:
Derivativos del ácido siálico para la derivatización y conjugación de proteínas, del 20 de Diciembre de 2019, de LIPOXEN TECHNOLOGIES LIMITED: Un procedimiento de producción de un derivativo aldehído de un ácido siálico en el que un material de partida que tiene una unidad de ácido siálico en el […]
GELES DE QUITOSANO(A) CONTENIENDO NANOPARTICULAS METALICAS DE COBRE, PLATA Y ANTIBIOTICOS (CIPROFLOXACINO, CEFOTAXIME, GENTAMICINA Y CLOXACILINA), del 12 de Diciembre de 2019, de CARDENAS Y CIA LTDA: En la presente invención se describen geles de quitosano (poli-beta-glucosamina) con propiedades bactericidas y fungicidas en mezcla con nanopartículas […]
Compuestos de polímero de polialquileno y usos de los mismos, del 20 de Noviembre de 2019, de Biogen MA Inc: Una composición farmacéutica que comprende un conjugado y un vehículo, adyuvante, diluyente, conservante y/o solubilizante farmacéuticamente […]
Composiciones y métodos para la liberación dirigida de fármacos in vitro e in vivo a células de mamíferos mediante minicélulas intactas derivadas de bacterias, del 23 de Octubre de 2019, de ENGENEIC MOLECULAR DELIVERY PTY LTD: Una composición que comprende: (a) una pluralidad de minicélulas intactas derivadas de bacterias que tienen paredes celulares intactas, en donde la pluralidad […]
Moléculas con semividas prolongadas, composiciones y usos de las mismas, del 16 de Octubre de 2019, de MEDIMMUNE, LLC: Una molécula modificada que comprende una proteína o agente no de proteína y un dominio constante de IgG, en la que el dominio constante de IgG comprende un dominio CH3 humano […]
Método para la preparación de oligo etilenglicol monodisperso, del 19 de Junio de 2019, de NEKTAR THERAPEUTICS: Un método para preparar un oligo (etilenglicol) monodisperso, comprendiendo dicho método: (i) hacer reaccionar un oligo (etilenglicol) terminado […]
Construcciones de moléculas MHC y sus usos para el diagnóstico y terapia, del 29 de Mayo de 2019, de DAKO DENMARK A/S: Una construcción de moléculas MHC en forma soluble en un medio de solubilización o inmovilizada en un soporte sólido o semi-sólido, comprendiendo dicha construcción de moléculas […]
Usos terapéuticos de anticuerpos monoclonales frente al receptor de la angiotensina II tipo 1, del 17 de Mayo de 2019, de QUEEN MARY AND WESTFIELD COLLEGE: Un anticuerpo monoclonal o un fragmento del mismo que se une al péptido que consiste en la secuencia EDGIKRIQDD para su uso en el tratamiento de la proliferación […]