Proceso para producir ácido 2-pipecólico-2'',6''-xilidida útil como un producto intermedio para la preparación de anestésicos locales.
Un proceso para la preparación del ácido 2-pipecólico-2', 6'-xilidida o uno de sus derivados que comprende la hidrogenación del ácido 2-picolínico-2',
6'-xilidida de fórmula 2 en presencia de níquel Raney como catalizador.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/000237.
Solicitante: PHARMATHEN S.A..
Nacionalidad solicitante: Grecia.
Dirección: 6, DERVENAKION STR. 15351 PALLINI ATTIKIS GRECIA.
Inventor/es: SONI,ROHIT,RAVIKANT, KOFTIS,Theocharis, GEORGOPOULOU,Ionna, KARAGIANNIDOU,Evrykleia.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D211/60 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 211/00 Compuestos heterocíclicos que contienen ciclos hidrogenados de piridina, no condensados con otros ciclos. › Atomos de carbono que tienen tres enlaces a heteroátomos, con a lo más un enlace a halógeno, p. ej. radicales éster o nitrilo.
PDF original: ES-2383715_T3.pdf
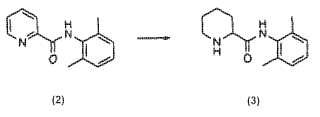
Fragmento de la descripción:
Proceso para producir ácido 2-pipecólico-2', 6'-xilidida útil como un producto intermedio para la preparación de anestésicos locales. 5 Área técnica de la invención La presente invención se refiere a un proceso mejorado para la preparación de compuestos del ácido 2-pipecólico2', 6'-xilidida o sus derivados y en particular a un método adecuado para la fabricación de una forma ópticamente activa de éste, que representa un producto intermedio importante para la preparación de anestésicos locales, como Ropivacaína o Levobupivacaína o sus sales.
Antecedentes de la invención El ácido 2-pipecólico-2', 6'-xilidida, particularmente en su forma ópticamente activa, es útil como un producto intermedio en la preparación de anestésicos locales. Por ejemplo el ácido L-2-pipecólico-2', 6'-xilidida de fórmula 1 se emplea como producto intermedio en la fabricación de anestésicos locales como Levobupivacina y Ropivacaína.
Se conocen diversos métodos para la preparación de ácido L-2-pipecólico-2', 6'-xilidida en una forma ópticamente activa. Sin embargo el estado anterior de la técnica encontró dificultades importantes en la preparación de ácido L-2pipecólico-2', 6'-xilidida o una de sus sales, debido a la formación de subproductos indeseados.
WO-A-85/00599 da a conocer la síntesis de ácido L-2-pipecólico-2', 6'-xilidida que comprende la resolución del ácido 2-pipecólico y su conversión en el clorhidrato del cloruro del ácido L-2-pipecólico con PCl5 en cloruro de acetilo como solvente, el cual al condensarse posteriormente con 2, 6-xilidina da el ácido L-2-pipecólico-2', 6'-xilidida correspondiente. Las principales desventajas de esta ruta consisten en la manipulación del cloruro de acetilo como solvente a la escala de una fábrica y también en la filtración del clorhidrato del cloruro del ácido pipecólico que es un producto intermedio del proceso. Además, el uso de PCl5 a gran escala es problemático, puesto que el PCl5 es propenso a reaccionar con la humedad atmosférica; asimismo, la separación de los residuos del cloruro de ácido intermedio es difícil. Por otra parte, los flujos de residuos del fosfato que se generan, son difíciles de tratar o de desechar en otra parte.
WO-A-96/12700 da a conocer un proceso para preparar Levobupivacina, (±) -Bupivacaína y otros análogos N
alquilo, donde el clorhidrato del ácido 2-pipecólico se clora con cloruro de tionilo o cloruro de oxalilo a clorhidrato del cloruro del ácido 2-pipecólico, y la amidación posterior con 2, 6-dimetilanilina sin aislamiento da los derivados del ácido 2-pipecólico-2', 6'-xilidida resultantes. Sin embargo, la manipulación del cloruro de tionilo a escala industrial es difícil y la reacción genera gases dañinos como dióxido de azufre que plantean problemas ambientales.
45 EP-B-0784608 da a conocer proceso para preparar Levobupivacaína y Ropivacaína, a partir de L-Lisina natural y sin costo, usando un método de mezcla de quiralidad para obtener el enantiómero S. Sin embargo, este proceso comprende una larga secuencia de reacciones que comprende la protección y desprotección del grupo α-amino e involucra también una reacción de diazotación peligrosa.
50 GB 824542 da a conocer la preparación de ácido N-alquil-2-pipecólico-2', 6'-xilidida partiendo de ácido 2-picolínico mediante su reacción con una amina aromática adecuada con POCl3; el ácido 2-picolínico-2', 6'-xilidida resultante se reduce después al ácido 2-pipecólico-2', 6'-xilidida correspondiente usando PtO2 como catalizador. La desventaja de este proceso es el uso de un catalizador de platino muy costoso.
55 En consecuencia, todavía existe la necesidad de un proceso eficiente, económico y seguro sin subproductos indeseados peligrosos.
Resumen de la invención 60 Por consiguiente, es un objetivo de la presente invención proporcionar un proceso mejorado para la preparación del ácido 2-pipecólico-2, 6-xilidida o uno de sus derivados, que supere las deficiencias del estado anterior de la técnica.
Otro objetivo de la presente invención es proporcionar un método, inocuo para el ambiente, de preparación del ácido 2-pipecólico-2, 6-xilidida en una forma ópticamente activa o uno de sus derivados que tenga elevada pureza quiral,
que sea eficiente y reduzca los costos de producción.
De conformidad con los objetivos antedichos de la presente invención, se proporciona un proceso para la preparación del ácido 2-pipecólico-2', 6'-xilidida o uno de sus derivados que comprende la hidrogenación del ácido 2picolínico-2', 6'-xilidida en presencia de níquel Raney como catalizador.
Las realizaciones preferidas de la presente invención se exponen en las reivindicaciones dependientes 2 a 9.
Otros objetivos y ventajas de la presente invención se tornarán evidentes para los expertos a la vista de la descripción detallada siguiente.
Descripción detallada de la invención La presente invención se refiere a un proceso mejorado para la fabricación del compuesto ácido 2-pipecólico-2', 6'xilidida o uno de sus derivados.
De acuerdo con la presente invención, el proceso para la preparación del ácido L-2-pipecólico-2', 6'-xilidida comprende los pasos siguientes:
- Un material de partida, sal de clorhidrato del ácido 2-picolínico se suspende en diclorometano y se hace reaccionar con cloruro de oxalilo para obtener el cloruro de ácido correspondiente;
- El cloruro de ácido generado in situ se condensa después con 2, 6-xilidina para obtener el derivado ácido 2picolínico-2', 6'-xilidida, el cual después de la hidrogenación con níquel Raney como catalizador da el ácido 2pipecólico-2', 6'-xilidida;
- El ácido 2-pipecólico-2', 6'-xilidida racémico se resuelve después en el isómero L con ácido dibenzoil-L-tartárico para obtener una pureza quiral en el rango de 90-95%.
- Se logra un incremento adicional de la pureza quiral hasta >99.5% mediante cristalización de sus sales de adición de ácido con ácido alcanoico en un solvente no cetónico y no alcohólico en un medio no acuoso.
De acuerdo con la presente invención, el ácido 2-pipecólico-2', 6'-xilidida o su derivado se prepara a partir de ácido 2picolínico comercial y menos costoso, que se usa como el material de partida clave. Su sal de HCl (es decir sal de clorhidrato del ácido 2-picolínico) preparada in situ se hace reaccionar con cloruro de oxalilo para generar el cloruro de ácido correspondiente evitando los agentes de clorinación de fósforo (PCl5, PCl3 y POCl3) y azufre (SOCl2 y SO2Cl2) y el uso de cloruro de acetilo.
El cloruro de ácido se condensa después con 2, 6-xilidina a una temperatura entre -5 y 0 °C, en presencia de una base orgánica, para obtener el ácido 2-picolínico-2', 6'-xilidida correspondiente. Se pueden emplear diversas bases orgánicas como piridina o un exceso molar de la 2, 6-xilidina o trialquilaminas como trietilamina, N-etil-N, N-diisopropilamina etc., la base orgánica que más se prefiere es piridina.
El ácido 2-picolínico-2', 6'-xilidida resultante se convierte después en el ácido 2-pipecólico-2', 6'-xilidida mediante hidrogenación selectiva del anillo de piridina a anillo de piperidina en presencia de un anillo aromático carbocíclico. Se eligió Ni Raney entre otros reactivos reductores como el menos costoso. El uso de PtO2 al 5% (ácido acéticometanol, 3.5 bar, 50 °C) demostró ser eficiente, aunque es costoso.
Se ensayaron las condiciones de reducción y probaron ser cruciales con respecto a todos los parámetros posibles (es decir, solvente, temperatura, presión y tiempo) . Cuando la reducción se llevó a cabo en metanol a 90 °C a una presión de hidrógeno de 75 psi utilizando Ni Raney, se encontró después de 24 horas el producto 3 en 73%, junto con 16% del compuesto de partida 2 y 8% del análogo metilado 4 (R = Me) (los rendimientos son de acuerdo con los resultados de HPLC) [véase Tabla 1, entrada 1]. Cuando la presión de hidrógeno se aumentó [véase Tabla 1, entradas 2-4], el compuesto de partida 2 se redujo por debajo de 1%, pero el producto metilado 4 aumentó como subproducto de la reducción. Para eliminar esta formación, se reemplazó el agua como solvente y se agregó ácido acético para aumentar la solubilidad del compuesto 2. Esa suposición probó ser correcta, pero se observó un 24.5% total de impurezas desconocidas, probablemente debido a la acetilación del nitrógeno [véase Tabla 1, entrada 5]. Usando sólo ácido acético como solvente la reducción... [Seguir leyendo]
Reivindicaciones:
1. Un proceso para la preparación del ácido 2-pipecólico-2', 6'-xilidida o uno de sus derivados que comprende la hidrogenación del ácido 2-picolínico-2', 6'-xilidida de fórmula 2 en presencia de níquel Raney como catalizador.
3. El proceso de acuerdo con la reivindicación 2, donde dicho solvente es metanol y ácido acético. 4. 80 °C y a una presión de hidrógeno de 10-30 kg/cm2, preferentemente a 50 °C y a una presión de hidrógeno de 18 kg/cm2. 5. El proceso de acuerdo con la reivindicación 1, donde el proceso comprende además los pasos siguientes: a) Hacer reaccionar clorhidrato del ácido 2-picolínico con cloruro de oxalilo para dar el cloruro de ácido correspondiente; b) Hacer reaccionar in situ el cloruro de ácido generado del paso a) con 2, 6-xilidina en presencia de una base orgánica para obtener el ácido 2-picolínico-2', 6'-xilidida deseado. 6. El proceso de acuerdo con la reivindicación 5, donde dicha base orgánica se selecciona de un grupo que consiste 30 en un derivado de piridina y trialquilamina. 7. El proceso de acuerdo con la reivindicación 6, donde dicha base orgánica es piridina. 8. El proceso de acuerdo con la reivindicación 5, donde además después de la hidrogenación el ácido 2-pipecólici 2', 6'-xilidida racémico obtenido se resuelve en el isómero L con ácido dibenzoil-L-tartárico para obtener el ácido L-2pipecólico-2', 6'-xilidida de fórmula 1, con una pureza quiral en el rango d. 9. 95%. 45 9. El proceso de acuerdo con la reivindicación 8, que comprende además la cristalización de la sal de adición de ácido del ácido L-2-pipecólico-2', 6'-xilidida en un solvente no alcohólico y no cetónico en un medio no acuoso para obtener ácido L-2-pipecólico-2', 6'-xilidida de una pureza quiral de al menos 99.5%. 15 2. El proceso de acuerdo con la reivindicación 1, donde se usa un solvente para la reducción anterior seleccionado entre alcohol y un ácido alifático inferior.
20 4. El proceso de acuerdo con la reivindicación 1, donde la reducción se lleva a cabo .
Patentes similares o relacionadas:
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Nuevas composiciones para prevenir y/o tratar trastornos degenerativos del sistema nervioso central, del 27 de Mayo de 2020, de AMICUS THERAPEUTICS, INC: Un compuesto de Fórmula III: **(Ver fórmula)** en donde: R1 es C(R2)(R3)(R4); R2 es hidrógeno, -OH o halógeno; R3 es hidrógeno, -OH, halógeno o -CH3; […]
Procedimiento de producción de derivados y productos intermedios de diazabiciclooctano, del 22 de Abril de 2020, de MEIJI SEIKA PHARMA Co., LTD: Procedimiento para producir un compuesto de fórmula (IV): **(Ver fórmula)** en la que OBn es benciloxilo, y R3 es alquilo C1-6 o heterociclilo, o forma […]
Procesos e intermedios en la preparación de antagonistas de C5aR, del 22 de Abril de 2020, de CHEMOCENTRYX, INC.: Un método de preparación de un compuesto que tiene la fórmula (I): **(Ver fórmula)** o una sal del mismo, en donde R1 es Cl o […]
Proceso para la preparación de derivados de 4-aminoindano y amidas de aminoindano relacionadas, del 15 de Abril de 2020, de Stichting I-F Product Collaboration: Un proceso para la preparación de derivados de 4-aminoindano de Fórmula (I), sales y enantiómeros de los mismos **(Ver fórmula)** que comprende […]
Profármacos de treprostinil, del 15 de Abril de 2020, de Corsair Pharma, Inc: Un compuesto según la fórmula (IA) **(Ver fórmula)** en la que, Z es -OH, -OR11 o P1; R11 es alquilo, alquilo sustituido, cicloalquilo, cicloalquilo sustituido, […]
Lípidos y composiciones lipídicas para la administración de agentes activos, del 25 de Diciembre de 2019, de NOVARTIS AG: Un compuesto de fórmula (II) o una sal farmacéuticamente aceptable del mismo, en la que: **(Ver fórmula)** R1 se selecciona del grupo que consiste en: **(Ver […]
Procedimiento para la preparación de 3-aminopiperidina enriquecida enantioméricamente, del 18 de Diciembre de 2019, de Reuter Chemische Apparatebau e.K: Un procedimiento para preparar 3-aminopiperidina, en donde el procedimiento comprende las siguientes etapas: a) poner a disposición hidrazida de ácido […]