Proceso a partir de ácido shikímico para obtener oseltamivir fosfato.
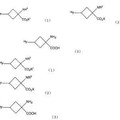
Proceso para la preparación de un derivado del ácido 4,5-diaminoshikímico de fórmula
y las sales de adición farmacéuticamente aceptables del mismo,
en el que
R', R1' son, independientemente el uno del otro, H o alquilo C1-6,
R2 es un alquilo C1-6 y
R3, R4 son, independientemente el uno del otro, H o un alcanoilo C1-6, con la condición de que R3 y R4 no seanambos H,
que se caracteriza por que
en el paso a) se da la esterificación del ácido shikímico de fórmula
con R2OH para formar un compuesto de fórmula
en el que R2 es como se ha definido anteriormente;
en el paso b)
se formula el trimesilato de fórmula IV haciendo reaccionar compuesto de fórmula III con cloruro de metanosulfonilo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/061838.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Nacionalidad solicitante: Suiza.
Dirección: GRENZACHERSTRASSE, 124 4070 BASEL SUIZA.
Inventor/es: TRUSSARDI, RENE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C227/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 227/00 Preparación de compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › a partir de productos naturales.
- C07C229/48 C07C […] › C07C 229/00 Compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › con grupos amino y grupos carboxilo unidos a átomos de carbono del mismo ciclo no condensado.
PDF original: ES-2392207_T3.pdf
Fragmento de la descripción:
Proceso a partir de ácido shikímico para obtener oseltamivir fosfato
La presente invención está relacionada con un proceso para la preparación de un derivado del ácido 4, 5-diaminoshikímico de fórmula
y de las sales de adición farmacéuticamente aceptables del mismo en las que R1, R1’ son, independientemente el uno del otro, H o alquilo, R2 es un alquilo y R3, R4 son, independientemente el uno del otro, H o a alcanoilo C1-6, con la condición de que R3 y R4 no son ambos un H.
Los derivados del ácido 4, 5-diamino-shikímico de fórmula I, especialmente el (3R, 4R, 5S) -5-amino-4-acetilamino-3 (1-etilpropoxi) -ciclohex-1-eno-carboxilato de etilo y sus sales de adición farmacéuticamente aceptables son potentes inhibidores de la neuraminidasa viral (J. C. Rohloff et al., J. Org. Chem. 63, 1998, 4545-4550; WO 98/07685) .
La problemática en la que se origina la presente invención es proporcionar un nuevo proceso para preparar los derivados del ácido 4, 5-diamino-shikímico con una calidad y rendimiento satisfactorio a partir de un material de partida que pueda obtenerse fácilmente, el ácido shikímico. El ácido shikímico puede obtenerse fácilmente mediante procesos biotecnológicos, por ejemplo la ingeniería genética o la fermentación (Sunil S. Chandran, Jian Yi, K.M. Draths, Ralph von Daeniken, Wolfgang Weber, y J.W. Frost, Biotechnologie Progress, Vol. 19, nº 3, 2003, 808-814) .
El problema se soluciona, de acuerdo con la presente invención, mediante un proceso para preparar los compuestos de fórmula I como se muestra en el esquema 1: Este nuevo proceso posee la ventaja de que consta de menos pasos para obtener los derivados del ácido 4, 5diamino-shikímico de fórmula I comparado con el proceso conocido en la materia (J.C.Rohloff et al., J.Org.Chem. 63, 1998, 4545-4550; WO 98/07685 y Abrecht et al: "The synthetic development of the anti-influenza neuraminidase
inhibitor oseltamivir phosphate (Tamiflu) : a challenge for synthesis and process research" CHIMIA Vol. 58, nº 9, 2004, págs.. 621-629) . Además, la combinación de pasos del proceso sin aislamiento y purificación de los correspondientes intermediarios descritos en el Esquema 1 permite potenciar la eficiencia y rendimiento global del proceso.
El nuevo proceso se caracteriza por
paso a) esterificación del ácido shikímico de fórmula
con R1OH para formar un compuesto de fórmula
en el que R2 es como se ha definido anteriormente;
paso b) formulación del trimesilato de fórmula IV haciendo reaccionar el compuesto de fórmula III con cloruro de metanosulfonilo
en el que R2 es como se ha definido anteriormente,
paso c) sustitución SN2 regioselectiva del grupo 3-mesilato del trimesilato IV mediante un reactivo azida para formar una azida de fórmula
en el que R2 es como se ha definido anteriormente, paso d) reducción de la azida de fórmula V con trialquilfosfito para formar la aziridina de fórmula
en el que R2 es como se ha definido anteriormente, R5 y R6, independientemente el uno del otro son alquilo C1-6, 25 paso e) apertura de la aziridina de fórmula VI para formar el compuesto de fórmula
en el que R1, R1’, R2, R5 y R6 son como se han definido anteriormente, paso f) transformación de la fosforamida de fórmula VII en el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente,
paso g) reducción de la azida de fórmula IX para formar el compuesto de fórmula I y si es necesario, formación de una sal de adición farmacéuticamente aceptable.
Existen dos formas alternativas de realizar el paso f)
1. El paso f) comprende los pasos f1) , f2) y f3) : paso f1) hidrólisis de la fosforamida de fórmula VII para formar el compuesto de fórmula
en el que R1, R1’ y R2 son como se han definido anteriormente, paso f2) acilación del compuesto de fórmula VIII-1 para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente,
paso f3) sustitución del grupo 5-mesilato del compuesto de fórmula VIII-2 por una azida para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente, 10 o alternativamente
2.1. el paso f) comprende los pasos f1) , f2) y f3) : paso f’1) sustitución del grupo 5-mesilato del compuesto de fórmula VII para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente, 20 paso f2) hidrólisis del compuesto de fórmula X para formar el compuesto de fórmula
en el que R1, R1’ y R2 son como se han definido anteriormente, paso f3) acilación del compuesto de fórmula XI para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente,
El término alquilo posee el significado de un grupo alquilo de cadena sencilla o ramificada de entre 1 y 12 átomos de C, más convenientemente de entre 1 y 6 átomos de C. Ejemplos de tales grupos alquilo son metilo, etilo, n-propilo, ipropilo, n-butilo, i-butilo, terc-butilo, pentilo y sus isómeros, hexilo y sus isómeros, heptilo y sus isómeros, octilo y sus isómeros, nonilo y sus isómeros, decilo y sus isómeros, undecilo y sus isómeros, y dodecilo y sus isómeros.
Este grupo alquilo puede sustituirse con uno o más sustituyentes como se define en, por ejemplo, la WO 98/07685. Los sustituyentes adecuados son alquilo C1-6 (como se ha definido anteriormente) , alquenilo C1-6, cicloalquilo C3-6, hidroxilo, alcoxi C1-6, alcoxicarbonilo C1-6, F, Cl, Br y I.
El término alquilo en R1, R1’ posee el significado de un grupo alquilo de cadena sencilla o ramificada de entre 1 y 12 átomos de C, más convenientemente de entre 1 y 6 átomos de C.
El significado preferible de R1 es etilo, y de R1’ es etilo.
R2 es un grupo alquilo de cadena sencilla o ramificada de entre 1 y 12 átomos de C, más convenientemente entre 1 y 6 átomos de C como se ha ejemplificado anteriormente.
El significado preferible de R2 es etilo.
R3 y R4 poseen el significado de grupos alcanoilo, más preferiblemente alcanoilo C1-6 como hexanoilo, pentanoilo, butanoilo (butirilo) , propanoilo (propionilo) , etanoilo (acetilo) y metanoilo (formilo) .
El significado preferible de R3 es acetilo y de R4 es H.
R5 y R6 son grupos alquilo de cadena sencilla o ramificada de entre 1 y 12 átomos de C, más convenientemente entre 1 y 6 átomos de C como se ha ejemplificado anteriormente.
El significado preferible de R5 y R6 son etilo.
El término "sales de adición ácida farmacéuticamente aceptable" incluye sales con ácidos inorgánicos y orgánicos, como el ácido clorhídrico, ácido bromhídrico, ácido nítrico, ácido sulfúrico, ácido fosfórico, ácido cítrico, ácido fórmico, ácido fumárico, ácido maleico, ácido acético, ácido succínico, ácido tartárico, ácido metanosulfónico, ácido p-toluenosulfónico, ácido bencenosulfónico y similares.
La formación de sal se efectúa mediante métodos que son conocidos per se y que serán familiares para cualquier experto en la materia. Se consideran tanto las sales con ácidos inorgánicos como las sales con ácidos orgánicos. Los clorhidratos, bromhidratos, sulfatos, nitratos, citratos, acetatos, maleatos, succinatos, metanosulfonatos, ptoluenosulfonatos y similares son ejemplos de tales sales.
La sal de adición ácida farmacéuticamente aceptable preferible es la sal 1:1 con ácido fosfórico que puede formarse preferiblemente y en solución etanólica a una temperatura de entre -20 °C y 60 °C.
Paso a)
El paso a) comprende la esterificación de ácido (3R, 4S, 5R) -3, 4, 5-trihidroxi-ciclohex-1-enocarboxílico de fórmula II con un alcohol de fórmula R2OH.
Normalmente, la reacción se realiza en un alcohol, preferiblemente etanol en presencia de un ácido fuerte, como ácido clorhídrico en etanol, ácido sulfúrico o la preparación in situ de ácido clorhídrico con cloruro de tionilo en etanol, preferiblemente con cloruro... [Seguir leyendo]
Reivindicaciones:
1. Proceso para la preparación de un derivado del ácido 4, 5-diaminoshikímico de fórmula
y las sales de adición farmacéuticamente aceptables del mismo, en el que
R’, R1’ son, independientemente el uno del otro, H o alquilo C1-6, R2 es un alquilo C1-6 y R3, R4 son, independientemente el uno del otro, H o un alcanoilo C1-6, con la condición de que R3 y R4 no sean ambos H, que se caracteriza por que
en el paso a) se da la esterificación del ácido shikímico de fórmula
con R2OH para formar un compuesto de fórmula
en el que R2 es como se ha definido anteriormente; en el paso b) 25 se formula el trimesilato de fórmula IV haciendo reaccionar compuesto de fórmula III con cloruro de metanosulfonilo
en el que R2 es como se ha definido anteriormente,
en el paso c) se realiza la sustitución SN2 regioselectiva del grupo 3-mesilato del trimesilato IV mediante un reactivo azida para formar una azida de fórmula
en el que R2 es como se ha definido anteriormente, en el paso d) se reduce la azida de fórmula V con trialquilfosfito para formar la aziridina de fórmula
en el que R2 es como se ha definido anteriormente, R5 y R6, independientemente el uno del otro son alquilo C1-6, 10 en el paso e)
se realiza la apertura de la aziridina de fórmula VI para formar el compuesto de fórmula
en el que R1, R1’, R2, R5 y R6 son como se han definido anteriormente, en el paso f) se transforma la fosforamida de fórmula VII en el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente, en el paso g) se reduce la azida de fórmula IX para formar el compuesto de fórmula I y si fuera necesario, se forma una sal de adición farmacéuticamente aceptable.
2. El proceso de la reivindicación 1, en el que el paso f) comprende los pasos, paso f1) hidrólisis de la fosforamida de fórmula VII para formar el compuesto de fórmula
en el que R1, R1’ y R2 son como se han definido anteriormente, paso f2) acilación del compuesto de fórmula VIII-1 para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente, 10 paso f3) sustitución del grupo mesilato del compuesto de fórmula VIII por una azida para formar el compuesto de fórmula
en el que R’, R1’, R2, R3 y R4 son como se han definido anteriormente.
3. El proceso de la reivindicación 1, en el que paso f) comprende los pasos, paso f’1) sustitución del grupo mesilato del compuesto de fórmula VII para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente, paso f’2) 25 hidrólisis del compuesto de fórmula X para formar el compuesto de fórmula
en el que R1, R1’ y R2 son como se han definido anteriormente, paso f’3) acilación del compuesto de fórmula XI para formar el compuesto de fórmula
en el que R1, R1’, R2, R3 y R4 son como se han definido anteriormente.
4. El proceso de la reivindicación 1, en el que R1, R1’ y R2 son etilo, R3 es acetilo y R4 es hidrógeno.
5. El proceso de la reivindicación 1, en el que R5 y R6 independientemente el uno del otro son etilo.
6. El proceso de la reivindicación 1, en el que la sal de adición ácida farmacéuticamente aceptable es la sal del ácido fosfórico.
7. El proceso de la reivindicación 1, en el que paso a) se realiza en un alcohol, preferiblemente etanol en presencia
de un ácido fuerte, preferiblemente cloruro de tionilo, en un rango de temperaturas de reacción de entre 60 °C y 20 150 °C, preferiblemente de 70 °C a 100 °C.
8. El proceso de la reivindicación 1, en el que paso b) se realiza en un solvente orgánico aprótico, preferiblemente acetato de etilo, y cloruro de metanosulfonilo con una base terciaria orgánica, preferiblemente trietilamina, a una temperatura de reacción en un rango de entre -20 °C y 50 °C, preferiblemente de 0 °C a 5 °C.
9. El proceso de la reivindicación 1, en el que paso c) se realiza en un solvente orgánico inerte, preferiblemente dimetilsulfóxido o con una mezcla acuosa del solvente orgánico, preferiblemente acetato de etilo y con un catalizador de la transferencia de fase, como hidrógeno sulfato de tetrabutilamonio y un reactivo azida, preferiblemente azida sódica, a temperatura ambiente.
10. El proceso de la reivindicación 1, en el que paso d) se realiza en un solvente orgánico, preferiblemente tolueno en una atmósfera de gas inerte, se añade un trialquilfosfito, como el trietilfosfito, a temperatura ambiente, y la temperatura de reacción se encuentra en el rango entre 50 °C y 150 °C, preferiblemente de 100 °C a 120 °C.
11. El proceso de la reivindicación 1, en el que paso e) se realiza en un alcohol, como el 3-pentanol y etileterato de trifluoruro de boro en una atmósfera de gas inerte en un rango de temperaturas de entre -20 ° C y 100 ° C, preferiblemente de 0 °C a 5 °C.
12. El proceso de la reivindicación 2, en el que paso f1) se realiza en un alcohol, como el etanol y un ácido fuerte,
preferiblemente ácido sulfúrico, en una atmósfera de gas inerte, en un rango de temperaturas de entre 50 °C y 150 °C, preferiblemente de 80 °C a 120 °C.
13. El proceso de la reivindicación 2, en el que paso f2) se realiza utilizando un agente de acilación, preferiblemente
bajo condiciones básicas utilizando anhídrido acético en acetato de etilo en un rango de temperaturas entre -20 °C y 45 100 °C.
14. El proceso de la reivindicación 2, en el que paso f3) se realiza en un solvente orgánico inerte, preferiblemente dimetilsulfóxido o una mezcla de solventes con dimetilsulfóxido y etanol con un reactivo azida, preferiblemente azida sódica a entre 20 °C y 120 °C, preferiblemente entre 80 °C y 100 °C.
15. El proceso de la reivindicación 3, en el que paso f1) se realiza en un solvente orgánico inerte, preferiblemente dimetilsulfóxido o una mezcla de solventes con dimetilsulfóxido y etanol, y un reactivo azida, preferiblemente azida sódica, a entre 20 °C y 120 °C, preferiblemente a entre 80 °C y 100 °C.
16. El proceso de la reivindicación 3, en el que paso f2) se realiza en un alcohol, preferiblemente etanol y un ácido
fuerte, preferiblemente ácido sulfúrico en una atmósfera de gas inerte en un rango de temperaturas de entre 20 °C y 150 °C, preferiblemente de 80 °C a 120 °C.
17. El proceso de la reivindicación 3, en el que paso f3) se realiza bajo condiciones básicas utilizando una mezcla de
anhídrido acético en acetato de etilo en un rango de temperaturas de entre -20 °C y 100 °C, preferiblemente de 0 °C 15 a 5 °C.
Patentes similares o relacionadas:
Agentes moduladores de S1p y/o ATX, del 31 de Julio de 2019, de Biogen MA Inc: Un compuesto representado por la fórmula (I):**Fórmula** o una sal farmacéuticamente aceptable del mismo, donde X es O, S, S(O), -CH2-, o S(O)2; X1, X2, y X5 son […]
Derivados de ácido 1-[7-(cis-4-metil-ciclohexiloxi)-8-trifluorometil-naftalen-2-ilmetil]-piperidin-4-carboxílico como moduladores de autotaxina (ATX) para tratar inflamaciones y trastornos autoinmunitarios, del 28 de Febrero de 2018, de Biogen MA Inc: Un compuesto representado por la fórmula (III): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que R3 es […]
Preparación de precursor de PET, del 16 de Agosto de 2017, de Blue Earth Diagnostics Limited: Un proceso de preparación de un compuesto de Fórmula IIIa:**Fórmula** en donde: R denota un grupo alquilo con de 1 a 5 átomos de carbono […]
Método para producción de un agente de representación de imágenes de diagnóstico por radiación, del 6 de Septiembre de 2013, de NIHON MEDI-PHYSICS CO., LTD.: Un método para producir un agente radiactivo de representación de imágenes de diagnóstico, quecomprende un paso de preparación de la solución que consiste en preparar una […]
Tripéptidos inhibidores de la hepatitis C, del 4 de Junio de 2013, de BOEHRINGER INGELHEIM (CANADA) LTD.: Un procedimienrto para la resolución de una mezcla enantiomérica de éster metílico de ácidos 1-amino-2-vinilcilciclopropil-carboxílicos, o una mezcla N-protegida […]
 Procedimiento para la producción de compuesto orgánico marcado con flúor radioactivo, del 14 de Marzo de 2012, de NIHON MEDI-PHYSICS CO., LTD.: Un procedimiento para la producción de un compuesto orgánico marcado con flúor radioactivo, que comprende:
una etapa de desesterificación de retener, en una columna […]
Procedimiento para la producción de compuesto orgánico marcado con flúor radioactivo, del 14 de Marzo de 2012, de NIHON MEDI-PHYSICS CO., LTD.: Un procedimiento para la producción de un compuesto orgánico marcado con flúor radioactivo, que comprende:
una etapa de desesterificación de retener, en una columna […]
CETOENOLES ESPIROCÍCLICOS SUSTITUIDOS CON TRIFLUOROMETILO Y SU USO COMO PLAGUICIDAS Y HERBICIDAS, del 14 de Noviembre de 2011, de BAYER CROPSCIENCE AG: Compuestos de fórmula (I) **Fórmula** en la que V representa hidrógeno, halógeno, alquilo o alcoxi, W representa hidrógeno, ciano, nitro, halógeno, […]
PROCEDIMIENTO PARA LA PREPARACIÓN DE AMINOALCOHOLES, del 11 de Enero de 2011, de LONZA AG: Procedimiento para preparar un aminoalcohol de fórmula en forma del racemato o de uno de sus isómeros ópticamente activos, que comprende la hidrólisis de un derivado […]