Procedimiento de preparación de un antagonista de leucotrienos y de un intermedio del mismo.
Compuesto de fórmula IIa,
o un solvato farmacéuticamente aceptable del mismo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/059965.
Solicitante: MOEHS IBERICA, S.L..
Nacionalidad solicitante: España.
Inventor/es: CAMPS RAMIREZ DE CARTAGENA,HELENA, SANCHEZ CASALS,CARLES.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/4704 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › 2-Quinolonas, p. ej. carboestirilo.
- A61P11/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Antiasmáticos.
- C07D215/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 215/00 Compuestos heterocíclicos que contienen quinoleína o quinoleína hidrogenada en el sistema cíclico. › Atomos de halógeno o radicales nitro.
PDF original: ES-2395439_T3.pdf
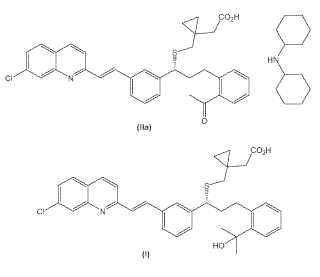
Fragmento de la descripción:
Procedimiento de preparación de un antagonista de leucotrienos y de un intermedio del mismo La presente invención se refiere a un procedimiento para la preparación de montelukast, así como a nuevos intermedios útiles para dicho procedimiento. ESTADO DE LA TÉCNICA ANTERIOR
Montelukast es la Denominación Común Internacional (DCI) del ácido (R) - (E) -1- ( ( (1- (3- (2- (7-cloro-2
quinolinil) etenil) fenil) -3- (2- (1-hidroxi-1-metiletil) fenil) propil) tio) metil) ciclopropanacético, número CAS 158966-92-8.
La sal monosódica de montelukast (CAS No 151767-02-1) de fórmula Ia Ia pertenece a un grupo de fármacos denominados antagonistas de leucotrienos. Se trata de un compuesto activo por
vía oral que se une con una gran afinidad y selectividad al receptor CysLT1. Este fármaco se utiliza actualmente en el tratamiento de asma, inflamación, angina, espasmo cerebral, nefritis glomerular, hepatitis, endotoxemia, uveitis y rechazo de transplantes.
La preparación de la sal sódica de montelukast aparece por primera vez en la EP 480717 (ejemplo 161) .
Posteriormente se describió un procedimiento alternativo para la preparación de un intermedio de montelukast en la EP 500360. Sin embargo, estos procedimientos no son particularmente adecuados para su uso a escala industrial, debido al uso de disolventes como diclorometano, reactivos como hidracina, y temperaturas por debajo de -40ºC. Además, dichos procedimientos requieren purificaciones cromatográficas tediosas de algunos intermedios y/o de los productos finales y los rendimientos del producto son bajos.
Entre las estrategias de preparación de montelukast se han descrito también procedimientos que comprenden la formación de sales de amina de montelukast, las cuales se transforman posteriormente en la sal sódica. Algunos de estos procedimientos, como los que se describen a continuación, comprenden la purificación de la sal de diciclohexilamina de montelukast:
Así, por ejemplo, la solicitud europea EP 737186 describe un procedimiento de preparación de montelukast sódico en forma cristalina a partir de la sal de diciclohexilamina de montelukast. Este procedimiento es difícilmente aplicable a escala industrial ya que emplea una base altamente inflamable (n-butil litio) y temperaturas de reacción por debajo de -10ºC. Además, en la preparación de montelukast se forma una impureza, que deriva de la deshidratación del grupo terc-butanol, y su eliminación resulta muy difícil. Adicionalmente, las etapas de purificación vía sal de diciclohexilamina son muy largas y comprenden el sembrado de la solución de montelukast y diciclohexilamina en tolueno o acetato de etilo, y posterior adición de heptano o hexano respectivamente.
En el documento WO 06/008751 se describe otro procedimiento de obtención de la sal sódica de montelukast que comprende la transformación de montelukast en la sal de diciclohexilamina del mismo. Sin embargo, este procedimiento también requiere el sembrado de la solución y se necesita un período de tiempo muy largo (más de un día) para que cristalice la sal de diciclohexilamina.
Además, la purificación vía sales de diciclohexilamina se ha aplicado también a intermedios que posteriormente se transforman en montelukast.
Así, los documentos WO 06/008751 y WO 07/004237 describen la preparación de montelukast mediante la formación de una sal de diciclohexilamina del intermedio éster metílico de fórmula:
Cl
Sin embargo, estos procedimientos presentan los mismos inconvenientes que los descritos para la formación de sales de diciclohexilamina sobre montelukast ácido.
Por tanto, debido a la dificultad de purificar montelukast y sus intermedios, es de gran interés proporcionar procedimientos alternativos para la preparación de montelukast, en particular si son de fácil industrialización.
EXPLICACIÓN DE LA INVENCIÓN 10 Los inventores han encontrado que la preparación de una sal de diciclohexilamina de fórmula IIa HN
Cl
IIa permite la obtención de montelukast, así como sus sales y solvatos, incluyendo hidratos, mediante un procedimiento fácilmente escalable que supera los inconvenientes del estado de la técnica.
La sal de diciclohexilamina de fórmula IIa, como se puede ver en los ejemplos, es mucho más insoluble en disolventes polares que las sales de diciclohexilamina conocidas de montelukast y del intermedio éster metílico. Debido a esa diferencia de solubilidad, esta sal presenta la ventaja de que cristaliza fácilmente en dichos disolventes polares, acortándose considerablemente los tiempos de formación de la sal. Asimismo, no es necesario sembrar la solución para iniciarse la cristalización, lo que, a la práctica, facilita la operatoria a escala industrial ya que se evita llevar a cabo operaciones que pueden resultar peligrosas debido a la inflamabilidad de este tipo de disolventes. Adicionalmente, el producto se obtiene con rendimiento alto y pureza elevada.
Otra ventaja de la utilización de la sal de fórmula IIa es que puede obtenerse mediante el uso de disolventes polares, sin necesidad de mezclas con disolventes apolares, lo que facilita el aislamiento del producto. Además, el uso de un único disolvente para la cristalización facilita la recuperación y reutilización del mismo en un proceso industrial.
Además, si se desea, la purificación de la sal de fórmula IIa puede llevarse a cabo en el mismo disolvente en el que se ha realizado la cristalización.
Por tanto, un primer aspecto de la invención se refiere a un compuesto de fórmula IIa,
HN
Cl
IIa o un solvato farmacéuticamente aceptable del mismo, incluyendo un hidrato.
Otro aspecto de la invención se refiere a un procedimiento de preparación de un compuesto de fórmula IIa tal como se ha definido anteriormente, que comprende la reacción de un compuesto de fórmula II
Cl
II
con diciclohexilamina en presencia de un disolvente polar. Otro aspecto de la invención se refiere a un procedimiento de preparación de un compuesto de fórmula I,
Cl
o una sal farmacéuticamente aceptable del mismo, o un solvato farmacéuticamente aceptable del mismo, incluyendo un hidrato; que comprende la transformación de un compuesto de fórmula IIa HN
Cl
IIa 10 en un compuesto de fórmula II por tratamiento acuoso en medio ácido;
Cl
II
seguido de reacción con un compuesto de fórmula III CH3MgX, donde X representa halógeno, opcionalmente en presencia de un ácido de Lewis, en un disolvente adecuado; y posterior tratamiento acuoso en medio ácido para dar el compuesto de fórmula I; y, opcionalmente, el compuesto de fórmula I se convierte en una sal farmacéuticamente aceptable del mismo por tratamiento con la correspondiente base, o una sal del compuesto de fórmula I se convierte en otra sal del compuesto de fórmula I por intercambio de iones, o el compuesto de fórmula I se convierte en un solvato farmacéuticamente aceptable del mismo, incluyendo un hidrato, por cristalización/precipitación en un disolvente adecuado.
Montelukast (compuesto de fórmula I) y sus intermedios se pueden preparar mediante los procedimientos descritos a continuación. Las condiciones más adecuadas para llevar a cabo el procedimiento pueden variar dependiendo de diversos parámetros considerados por el experto en la materia, tal como, concentración de productos de partida, temperatura, disolvente utilizado y similares. Éstos pueden ser fácilmente determinados por el experto en la materia por ensayos rutinarios y con la ayuda de las enseñanzas de los ejemplos presentes en esta descripción.
En algunas de las reacciones de la presente invención, se utiliza un tratamiento acuoso en medio ácido para el
aislamiento del producto de reacción. En general, dicho ácido puede ser un ácido orgánico. Ejemplos de ácidos orgánicos incluyen, entre otros, ácido acético, ácido metanosulfónico, ácido trifluorometanosulfónico, ácido etanosulfónico, ácido bencenosulfónico o ácido p-toluenosulfónico. En una realización particular el ácido utilizado es ácido acético.
Como se ha mencionado anteriormente, el compuesto de fórmula I se puede preparar por reacción de un compuesto de fórmula II con un compuesto de fórmula III, donde X representa halógeno, según se muestra en el siguiente esquema:
O
II
CH3MgX
III
CO2H
S
Cl N
HO
I
Esta reacción se lleva a cabo opcionalmente en presencia de un ácido de Lewis, en un disolvente adecuado, tal como tetrahidrofurano, y a una temperatura adecuada, preferiblemente a 0 ºC y posteriormente... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula IIa,
Cl HN
O
IIa o un solvato farmacéuticamente aceptable del mismo.
2. Compuesto de fórmula IIa según la reivindicación 1, donde el solvato es un hidrato.
3. Forma cristalina de la sal de diciclohexilamina del ácido (R) - (E) -1- ( ( (1- (3- (2- (7-cloro-2-quinolinil) etenil) fenil) -3- (2
acetilfenil) propil) tio) metil) ciclopropan-acético según la reivindicación 1, caracterizada porque su difractograma de Rayos X es tal como se muestra en la FIGURA 1, medido en un difractómetro de Rayos X equipado con un ánodo de cobre (A= 1.54056 A) .
4. Procedimiento de preparación de un compuesto de fórmula IIa tal como se ha definido en cualquiera de las 15 reivindicaciones 1-3, que comprende la reacción de un compuesto de fórmula II
Cl
II
con diciclohexilamina en presencia de un disolvente polar.
5. Procedimiento de preparación según la reivindicación 4, donde el disolvente polar se selecciona entre el grupo que consiste en una cetona de fórmula RCOR1, un éster de fórmula RCO2R1 donde R y R1 pueden ser iguales o diferentes y representan (C1-C4) alquilo, y un hidrocarburo aromático que es un benceno mono o disustituído, donde el sustituyente se selecciona entre halógeno o metilo.
6. Procedimiento de preparación según la reivindicación 5, donde el disolvente polar es acetona.
7. Procedimiento de preparación según cualquiera de las reivindicaciones 4-6 donde previamente se hace reaccionar un compuesto de fórmula IV
Cl
donde GS representa un grupo saliente seleccionado del grupo que consiste en metanosulfoniloxilo y ptoluenosulfoniloxilo; con un compuesto de fórmula V
O
V
donde R representa un metal alcalino, en un disolvente adecuado, seguido de tratamiento acuoso en medio ácido, para obtener el compuesto de fórmula II.
8. Procedimiento de preparación según la reivindicación 7 donde GS representa metanosulfoniloxilo.
9. Procedimiento de preparación según cualquiera de las reivindicaciones 7-8 donde R representa Na.
10. Procedimiento de preparación de un compuesto de fórmula I,
I
o una sal farmacéuticamente aceptable del mismo, o un solvato farmacéuticamente aceptable del mismo; que 10 comprende la transformación de un compuesto de fórmula IIa en un compuesto de fórmula II por tratamiento acuoso en medio ácido;
II
seguido de reacción con un compuesto de fórmula III CH3MgX, donde X representa halógeno, en un disolvente adecuado, opcionalmente en presencia de un ácido de Lewis; y posterior tratamiento acuoso en medio ácido para dar el compuesto de fórmula I; y, opcionalmente, el compuesto de fórmula I se convierte en una sal
farmacéuticamente aceptable del mismo por tratamiento con la correspondiente base, o una sal del compuesto de fórmula I se convierte en otra sal del compuesto de fórmula I por intercambio de iones, o el compuesto de fórmula I se convierte en un solvato farmacéuticamente aceptable del mismo por cristalización/precipitación en un disolvente adecuado.
11. Procedimiento de preparación según la reivindicación 10, donde X representa Cl en presencia de un ácido de Lewis.
12. Procedimiento de preparación según la reivindicación 11, donde el ácido de Lewis es CeCl3.
13. Procedimiento de preparación según cualquiera de las reivindicaciones 10-12 donde previamente se hace reaccionar un compuesto de fórmula II
II con diciclohexilamina en presencia de un disolvente polar para obtener un compuesto de fórmula IIa.
14. Procedimiento de preparación según la reivindicación 13, donde previamente se hace reaccionar un compuesto de fórmula IV
Cl
donde GS representa un grupo saliente seleccionado del grupo que consiste en metanosulfoniloxilo y ptoluenosulfoniloxilo; con un compuesto de fórmula V
O
V
donde R representa un metal alcalino, en un disolvente adecuado, seguido de tratamiento acuoso en medio ácido, para obtener el compuesto de fórmula II.
REFERENCIAS CITADAS EN LA DESCRIPCIÓN
Esta lista de referencias citadas por el solicitante es únicamente para la comodidad del lector. No forma parte del documento de la patente europea. A pesar del cuidado tenido en la recopilación de las referencias, no se pueden excluir errores u omisiones y la EPO niega toda responsabilidad en este sentido.
Documentos de patentes citados en la descripción EP 480717 A [0004] [0043] WO 07004237 A [0009] EP 500360 A [0004] WO 0608751 A [0056] EP 737186 A [0006] [0056] WO 0704237 A [0056] WO 06008751 A [0007] [0009]
Patentes similares o relacionadas:
Derivados de 5-[2-(piridin-2-ilamino)-1,3-tiazol-5-il]-2,3-dihidro-1H-isoindol-1-ona y su uso como inhibidores dobles de fosfatidilinositol··3-cinasa delta y gamma, del 15 de Julio de 2020, de ASTRAZENECA AB: Compuesto de formula (I) **(Ver fórmula)** donde X es C(O) o SO2; Y es SO2NHR5 o SO2R6; R1 se selecciona de alquilo C1-4, […]
Composiciones farmacéuticas para uso tópico basadas en ácido hialurónico sulfatado como promotor de absorción de la piel, del 1 de Julio de 2020, de FIDIA FARMACEUTICI S.P.A.: Una composición farmacéutica para uso tópico que contiene ácido hialurónico sulfatado como promotor de absorción de la piel de diclofenaco, ketoprofeno, ibuprofeno […]
Compuestos de diaminopirimidilo sustituidos, composiciones de los mismos y procedimientos de tratamiento con ellos, del 17 de Junio de 2020, de SIGNAL PHARMACEUTICALS LLC: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal, un tautómero, un isotopólogo o un estereoisómero farmacéuticamente aceptable […]
Cadena alfa del receptor de IgE de alta afinidad de fusión Fc, del 13 de Mayo de 2020, de KISSEI PHARMACEUTICAL CO., LTD.: Una proteína de fusión Fc que comprende: (i) una cadena α del receptor de IgE de alta afinidad; y (ii) la región Fc de IgG1, en donde la región del fragmento […]
Derivados de piperidin-4-IL azetidina como inhibidores de JAK1, del 6 de Mayo de 2020, de Incyte Holdings Corporation: Un compuesto, que es {1-{1-[3-Fluoro-2-(trifluorometil)isonicotinoil]piperidin-4-il}-3-[4-(7H-pirrolo[2,3-d]pirimidin-4-il)-1H-pirazol-1-il]azetidin-3-il}acetonitrilo,…
Compuestos heterocíclicos tricíclicos sustituidos, del 22 de Abril de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de fórmula (I) **(Ver fórmula)** o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo, […]
Compuestos heterocíclicos útiles como inhibidores de TNF, del 22 de Abril de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de fórmula (I) **(Ver fórmula)** o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo, […]
Compuestos heterocíclicos tricíclicos útiles como inhibidores de TNF, del 22 de Abril de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de fórmula (I) **(Ver fórmula)** o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable o un solvato del mismo, en donde: X […]