Método para obtención de anticuerpos.
Un método de obtención de al menos un anticuerpo recombinante con afinidad mejorada para un antígenoseleccionado a partir de una familia de anticuerpos generados in vivo que se unen al antígeno seleccionado,
quecomprende:
a) obtener a partir de células B una familia de dos o más anticuerpos generados in vivo que se unen almismo antígeno y conservan los apareamientos VH y VL generados in vivo en los cuales la secuenciade aminoácidos VH CDR3 de cada anticuerpo en la familia tiene una identidad de 100%;
b) re-aparear la región VH de un anticuerpo obtenido en el paso (a) con la región VL de un anticuerpo diferenteobtenido en el paso (a) para producir un nuevo anticuerpo recombinante; y
c) someter a cribado el anticuerpo recombinante producido en el paso (b) y seleccionar dicho anticuerposi tiene afinidad mejorada con respecto a la población inicial de anticuerpos obtenida en el paso (a)en donde en el paso (a) los anticuerpos se obtienen a partir de células B aisladas individuales y se obtienen lassecuencias que codifican las regiones variables de los anticuerpos.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2006/001238.
Solicitante: UCB PHARMA, S.A..
Nacionalidad solicitante: Bélgica.
Dirección: 60, ALLÉE DE LA RECHERCHE 1070 BRUSSELS BELGICA.
Inventor/es: LAWSON, ALASTAIR, DAVID, GRIFFITHS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
PDF original: ES-2388177_T3.pdf
Fragmento de la descripción:
Método para obtención de anticuerpos
La presente invención se refiere a anticuerpos de afinidad alta y métodos de producción de los mismos. En particular, la presente invención proporciona un nuevo método de mejora de la afinidad de los anticuerpos.
Las altas especificidad y afinidad de los anticuerpos hacen de los mismos agentes ideales de diagnóstico y terapéuticos, particularmente para modulación de las interacciones proteína: proteína. Los anticuerpos enteros y fragmentos de anticuerpos están demostrando ser agentes terapéuticos versátiles, como se ve por el reciente éxito de productos tales como ReoPro®, Remicade™ y Humira®.
Las inmunoglobulinas son moléculas en forma de Y que comprenden dos cadenas pesadas idénticas y dos cadenas
ligeras idénticas. Enlaces disulfuro unen los pares de cadenas pesadas y ligeras así como las dos cadenas pesadas. Cada cadena está constituida por un dominio variable que varía en secuencia y es responsable de la unión de antígeno, conociéndose los mismos como los dominios VH y VL para las cadenas pesada y ligera, respectivamente. Cada cadena está constituida también por al menos un dominio constante que se une moléculas efectoras. En la cadena ligera existe un solo dominio constante (CL) y en la cadena pesada existen tres (CH1, CH2 y CH3) .
Existen tres regiones dentro de los dominios variables que son hipervariables en secuencia dispuestos en cuatro regiones marco más altamente conservadas. Estas regiones hipervariables son fundamentalmente responsables del reconocimiento de antígeno y se hace referencia a las mismas como 'regiones determinantes de la complementariedad' (CDRs) .
Existen muchos tipos diferentes de anticuerpos y fragmentos de los mismos que pueden utilizarse en terapia, con
inclusión de anticuerpos enteros y fragmentos tales como Fab, Fab', F (ab') 2 y scFv. Todos estos comprenden un par de dominios VH y VL que son responsables de la unión del antígeno.
Los anticuerpos para uso en terapia se derivan de cierto número de fuentes que incluyen por ejemplo animales inmunizados y bibliotecas de presentación de fago. A menudo, la afinidad de estos anticuerpos cuando se aíslan por primera vez no es suficientemente alta para uso directo en terapia, habiéndose desarrollado cierto número de méto25 dos para aumentar la afinidad de los anticuerpos (maduración de la afinidad) que incluyen la mutación de las CDRs (Yang et al., J. Mol. Biol., 254, 392-403, 1995) , uso de tensiones de mutación de E. coli (Low et al., J. Mol. Biol., 250, 359-368, 1996) , desordenamiento de DNA (Patten et al., Curr. Opin. Biotechnol., 8, 724-733, 1997) y PCR sexual (Crameri et al., Nature, 391, 288-291, 1998) . Un método particular de maduración de afinidad se conoce como 'desordenamiento de cadenas', en el cual una cadena del anticuerpo se mantiene se une mientras que la otra se modifi
ca, v.g. el dominio VH de un anticuerpo de partida se desordena con una gama de otros dominios VL y las nuevas combinaciones VH y VL se someten a cribado para identificar aquéllas que poseen afinidad mejorada con respecto al anticuerpo de partida.
Los dominios VH o VL 'de reemplazamiento' utilizados en el desordenamiento de cadenas se obtienen típicamente a partir de bibliotecas de genes de región VH o VL de anticuerpos construidas a partir de, por ejemplo, el mRNA de 35 linfocitos de sangre periférica de donantes inmunizados o no inmunizados (Clackson et al., 1991, Nature, 352, 624628; Vaughan et al., 1996, Nature Biotechnology, 14, 309-314) . La presentación de fago ha sido utilizada típicamente para desordenar secuencias de anticuerpos dado que es posible que un fago acomode los grandes tamaños de biblioteca necesarios para representar todos los genes VH o VL posibles. Típicamente, las bibliotecas de genes VH
o VL se clonan en un vector que codifica el gen VH o VL complementario del anticuerpo de partida, véase, por 40 ejemplo, Marks et al., 1992, Bio/Technology, 10, 779-783; Marks JD, 2004, Methods in Molecular Biology, 248, 327
343. Las diversas nuevas combinaciones VH o VL se expresan luego como scFvs en la superficie del fago y se someten a cribado respecto a afinidad mejorada. En caso requerido, el proceso puede repetirse reemplazando esta vez la cadena opuesta.
Schier et al., (1996, Journal of Molecular Biology, Londres, 255, 28-43) describe el aislamiento de Fv monocatenario 45 anti-c-erbB-2 humano monómero de afinidad alta, utilizando selección dirigida por afinidad.
En algunos casos es todavía necesario combinar el desordenamiento con otros métodos de maduración, tales como mutagénesis CDR a fin de producir un anticuerpo de afinidad alta (Thompson et al., J. Mol. Biol. 256, 77-78, 1996) .
El desordenamiento ha sido utilizado también para investigar la promiscuidad de los apareamientos de cadenas pesada y ligera de anticuerpos (Kang et al., 1991, Proc. Natl. Acad. Sci. 88, 11120-11123) . Se obtuvieron anticuer50 pos que se unían al hapteno, NPN, a partir de bibliotecas de presentación de fago derivadas de un ratón inmunizado y se identificaron familias clonales de secuencias de anticuerpos basadas en semejanzas de secuencia y en la longitud de las regiones CDR3 de ambas cadenas pesada y ligera, que se suponía se derivaban del mismo clon inicial de células B. En cada familia, la CDR3 tenía la misma longitud. Las cadenas pesada y ligera de todas las familias de anticuerpos se desordenaron y las secuencias de los anticuerpos que se unían todavía el hapteno se determinaron y 55 se compararon con las secuencias del anticuerpo de partida para determinar de qué familias se derivaban. Se observó promiscuidad tanto incestuosa como extraclonal de las cadenas VH o VL, de tal modo que se observó que
regiones variables de cadena pesada se apareaban con cadenas ligeras procedentes de la familia de cadena ligera complementaria tanto de fuera como de dentro. No se determinó afinidad alguna para estos clones desordenados.
Suzuki et al., (2000, Biochemical and Biophysical Research Communications, 271, 1, 240-243) describe cadenas ligeras que determinan la propiedad de unión de autoanticuerpos IgG humanos anti-dsDNA.
Burton et al (US 2003/187247) describe anticuerpos monoclonales humanos neutralizantes para el virus de la inmunodeficiencia humana.
Suzuki et al., (1999, International Journal of Molecular Medicine, vol. 3, 4, 385-390) describe la clonación y el análisis funcional de autoanticuerpos IgG anti-DNA bicatenario utilizando el método de presentación de fago.
Aburatani et al., (2002, Journal of Biochemistr y , Japanese Biochemical Society, 132, 5, 775-782) describe la impor10 tancia de un residuo basal CDR H3 en la interacción VH/VL de anticuerpos humanos.
Ihle et al., (2003, Scandinavian Journal of Immunology, 57, 5, 453-462) describe la clonación, secuenciación y expresión de regiones variables de inmunoglobulina de anticuerpos monoclonales murinos específicos para los bucles de proteínas P1.7 y P1.16 PorA de Neisseria meningitidis.
Sorprendentemente, los autores de la presente invención han conseguido demostrar ahora que es posible producir
anticuerpos de afinidad alta por re-apareamiento de las regiones variables de anticuerpos dentro de una familia de anticuerpos que se unen al mismo antígeno. Sorprendentemente, la afinidad de anticuerpos de afinidad ya alta puede aumentarse aún por re-apareamiento de las regiones variables entre miembros de familias de anticuerpos afines, evitando la necesidad de grandes bibliotecas de secuencias VH y VL diversas. A pesar de diferencias sólo pequeñas en las secuencias de los anticuerpos, pueden obtenerse grandes aumentos en la afinidad de estos anticuerpos. La
frecuencia del aumento de afinidad observada es sorprendente para un número tan pequeño de combinaciones de secuencia posibles.
Por tanto, la presente invención proporciona un método de obtención de al menos un anticuerpo recombinante con afinidad mejorada para un antígeno seleccionado de una familia de anticuerpos generados in vivo que se unen al anticuerpo seleccionado, que comprende:
a) obtener a partir de células B una familia de dos o más anticuerpos generados in vivo que se unen al mismo antígeno y conservan los apareamientos VH y VL generados in vivo en los cuales la secuencia de aminoácidos VH CDR3 de cada anticuerpo en la familia tiene... [Seguir leyendo]
Reivindicaciones:
1. Un método de obtención de al menos un anticuerpo recombinante con afinidad mejorada para un antígeno seleccionado a partir de una familia de anticuerpos generados in vivo que se unen al antígeno seleccionado, que comprende:
a) obtener a partir de células B una familia de dos o más anticuerpos generados in vivo que se unen al mismo antígeno y conservan los apareamientos VH y VL generados in vivo en los cuales la secuencia de aminoácidos VH CDR3 de cada anticuerpo en la familia tiene una identidad de 100%;
b) re-aparear la región VH de un anticuerpo obtenido en el paso (a) con la región VL de un anticuerpo diferente obtenido en el paso (a) para producir un nuevo anticuerpo recombinante; y 10 c) someter a cribado el anticuerpo recombinante producido en el paso (b) y seleccionar dicho anticuerpo
si tiene afinidad mejorada con respecto a la población inicial de anticuerpos obtenida en el paso (a) en donde en el paso (a) los anticuerpos se obtienen a partir de células B aisladas individuales y se obtienen las secuencias que codifican las regiones variables de los anticuerpos.
2. El método de acuerdo con la reivindicación 1, en el cual la familia de dos o más anticuerpos obtenida en el
paso (a) se caracteriza adicionalmente porque la región VH de cada anticuerpo tiene una identidad mayor que 60% al nivel de aminoácidos y la región VL de cada anticuerpo tiene una identidad mayor que 60% al nivel de aminoácidos.
3. El método de acuerdo con la reivindicación 1 o la reivindicación 2, en el cual en el paso (b) cada región VH de los anticuerpos obtenidos en el paso (a) se re-aparea con cada región VL de tal modo que cada nueva combina
ción VH:VL se produce como un anticuerpo recombinante o fragmento del mismo y al menos uno de los anticuerpos recombinantes producidos se somete a cribado en el paso (c) .
4. El método de la reivindicación 3, en el cual cada nueva combinación de anticuerpos producida en el paso (b) se somete a cribado en el paso (c) .
5. El método de acuerdo con la reivindicación 1 o la reivindicación 2, en el cual los pasos (b) y (c) se repiten 25 para diferentes pares VH:VL hasta que se identifica un anticuerpo con afinidad mejorada en el paso (c) .
6. El método de una cualquiera de las reivindicaciones 1 a 5 en el cual se obtienen tres o más anticuerpos en el paso (a) .
7. El método de acuerdo con una cualquiera de las reivindicaciones 1 a 6 que comprende adicionalmente el paso (d) en el cual el anticuerpo obtenido en el paso (c) se humaniza.
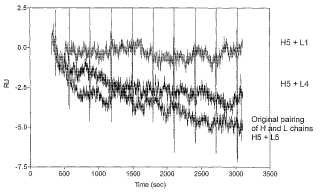
Figura 1
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Formulación anti-IFNAR1 estable, del 24 de Junio de 2020, de ASTRAZENECA AB: Una formulacion de anticuerpo que comprende: a. De 100 mg/ml a 200 mg/ml de anifrolumab; b. Lisina HCl 40 mM a 60 mM; c. Trehalosa […]
Proteínas y péptidos modificados, del 24 de Junio de 2020, de GLAXO GROUP LIMITED: Un dominio variable de inmunoglobulina único, que se une a TNFR1 y que se selecciona de cualquiera de las siguientes secuencias de aminoácidos: (a) DOM1h-131-206 caracterizada […]
Métodos para purificar una proteína objetivo de una o más impurezas en una muestra, del 17 de Junio de 2020, de EMD Millipore Corporation: Un metodo para purificar una proteina objetivo que contiene una region Fc de una o mas impurezas en una muestra, el metodo comprende las etapas de: a) poner en contacto […]
Dominios variables de inmunoglobulina, del 10 de Junio de 2020, de Ablynx NV: Dominio variable individual de inmunoglobulina de cadena pesada (ISVD), en que el residuo aminoacídico en la posición 89 es L y el residuo […]
Criterio de valoración terapéutico equivalente para inmunoterapia de enfermedades basada en antiCTLA-4, del 10 de Junio de 2020, de E. R. Squibb & Sons, L.L.C: Un anticuerpo antiCTLA-4 para su uso en el tratamiento de cáncer en un sujeto, tratamiento que comprende inducir un acontecimiento liminar […]