Derivados de tioflavina y su uso en diagnosis y terapia de la enfermedad de alzheimer.
Un compuesto fijador de amiloide de la fórmula (I) siguiente para uso en la detección de depósitos de amiloide enun individuo o una sal no tóxica soluble en agua del mismo:
en donde Z es S, NR', O o CR', en cuyo caso la forma tautómera correcta del anillo heterocíclico resulta ser un indolen el cual R' es H o un grupo C1-C8 alquilo:
Y es NR1R2, OR2 o SR2;
en donde el nitrógeno de
no es una amina cuaternaria;
cada uno de R1 y R2 se selecciona independientemente del grupo constituido por H, un grupo C1-C8 alquilo,(CH2)nOR' (en donde n ≥ 1, 2, ó 3), CF3, CH2-CH2X, CH2-CH2-CH2X (en donde X ≥ F, Cl, Br o I), (C≥O)-R', Rph,(CH2)nRph (en donde n ≥ 1, 2, 3 ó 4 y Rph representa un grupo fenilo insustituido o sustituido, en donde lossustituyentes de Rph se seleccionan del grupo constituido por F, Cl, Br, I, un grupo C1-C8 alquilo, (CH2)nOR' (endonde n ≥ 1, 2, ó 3), CF3, CH2-CH2X, O-CH2-CH2X, CH2-CH2-CH2X, O-CH2-CH2-CH2X (en donde X ≥ F, Cl, Br o I),CN, (C≥O)-R', N(R')2, NO2, (C≥O)N(R')2, O(CO)R', OR', SR', COOR' (en donde R' es H o un grupo C1-C8 alquilo), untrialquil-estaño y un grupo quelante (con o sin un grupo metálico quelado) de la forma W-L o V-W-L, en donde V seselecciona del grupo constituido por -COO-, -CO-, -CH2O- y -CH2NH-; W es -(CH2)n en donde n ≥ 0, 1, 2, 3, 4 ó 5; yL es:**Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2001/026427.
Solicitante: UNIVERSITY OF PITTSBURGH OF THE COMMONWEALTH SYSTEM OF HIGHER EDUCATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 200 GARDNER STEEL CONFERENCE CENTER THACKERAY & O'HARA STREETS PITTSBURGH, PA 15260 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KLUNK,William E, WANG,YANMING DR, MATHIS,CHESTER A. JR.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/428 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con carbociclos.
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- A61K51/04 A61K […] › A61K 51/00 Preparaciones que contienen sustancias radioactivas utilizadas para la terapia o para el examen in vivo. › Compuestos orgánicos.
- A61P25/28 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
- C07D277/64 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 277/00 Compuestos heterocíclicos que contienen ciclos de tiazol-1,3 o tiazol-1,3 hidrogenado. › con solamente radicales hidrocarbonados o hidrocarbonados sustituidos unidos en posición 2.
- C07D277/66 C07D 277/00 […] › con ciclos o sistemas cíclicos aromáticos unidos en posición 2.
- G01N33/534 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un marcador radiactivo.
PDF original: ES-2395721_T3.pdf
Fragmento de la descripción:
Derivados de tioflavina y su uso en diagnosis y terapia de la enfermedad de Alzheimer
CAMPO DE LA INVENCIÓN
La presente invención se refiere a la identificación de compuestos que son adecuados para producción de imágenes de depósitos de amiloide en pacientes vivos. Más específicamente, la presente invención se refiere a un método de producción de imágenes de depósitos de amiloide en el cerebro in vivo a fin de permitir la diagnosis ante-mortem de la enfermedad de Alzheimer. La presente invención considera también usos terapéuticos para tales compuestos.
ANTECEDENTES DE LA INVENCIÓN
La enfermedad de Alzheimer ("AD") es una enfermedad neurodegenerativa caracterizada por pérdida de memoria y
otros déficits cognitivos. McKhann et al., Neurology 34:939 (1984) . Es la causa más común de demencia en los Estados Unidos. La AD puede atacar a personas tan jóvenes como de 40-50 años, pero, debido a que la presencia de la enfermedad es difícil de determinar sin una peligrosa biopsia de cerebro, el momento de la aparición se desconoce. La prevalencia de AD aumenta con la edad, alcanzando estimaciones de la población afectada a porcentajes tan altos como 40-50% para edades de 85-90. Evans et al., JAMA 262:2551 (1989) ; Katzman,
Neurology 43:13 (1993) .
En la práctica, AD se diagnostica definitivamente por examen de tejido cerebral, usualmente en la autopsia. Khachaturian, Arch. Neurol. 42:1097 (1985) ; McKhann et al., Neurology 34:939 (1984) . Neuropatológicamente, esta enfermedad se caracteriza por la presencia de placas neuríticas (NP) , madejas neurofibrilares (NFT) , y pérdida neuronal, junto con una diversidad de otros hallazgos. Mann, Mech. Ageing Dev. 31:213 (1985) . Las rodajas de tejido cerebral tejido post-mortem de víctimas de la enfermedad de Alzheimer exhiben la presencia de amiloide en la forma de núcleos proteináceos extracelulares de las placas neuríticas que son características de AD.
Los núcleos de amiloide de estas placas neuríticas están compuestos de una proteína denominada el amiloide º (Aº) que está dispuesta en una configuración predominantemente de hoja plegada beta. Mori et al., Journal of Biological Chemistr y 267:17082 (1992) ; Kirschner et al., PNAS 83:503 (1986) . Las placas neuríticas son un aspecto precoz e invariante de la enfermedad (Mann et al., J. Neurol. Sci. 89:169; Mann, Mech. Ageing. 31:913 (1985) ; Terr y et al., J. Neuropathol. Exp. Neurol 46: 262 (1987) .
La deposición inicial de Aº ocurre probablemente mucho tiempo antes que sean apreciables los síntomas clínicos. Los "criterios microscópicos mínimos" recomendados actualmente para la diagnosis de AD están basados en el número de placas neuríticas encontradas en el cerebro. Khachaturian, Arch. Neurol. supra (1985) .
Lamentablemente, la evaluación de los recuentos de placas neuríticas tiene que demorarse hasta después de la muerte.
Las placas neuríticas que contienen amiloide son una característica prominente de áreas selectivas del cerebro en AD así como en el síndrome de Down y en personas homocigóticas para el alelo de la apolipoproteína E4 que son muy propensas a desarrollar AD. Corder et al., Science 261: 921 (1993) ; Divr y , P., J. Neurol. Psych. 27: 643-657 35 (1927) ; Wisniewski et al., in Zimmerman, H.M. (ed.) : PROGRESS IN NEUROPATHOLOGY (Grune y Stratton, N.Y. 1973) pp. 1-26. El amiloide cerebral se demuestra fácilmente por tinción de secciones de cerebro con tioflavina S o rojo Congo. Puchtler et al., J. Histochem. Cytochem. 10:35 (1962) . El amiloide teñido con rojo Congo se caracteriza por un aspecto dicroico, que exhibe un color de polarización amarillo-verde. La fijación dicroica es el resultado de la estructura de hoja plegada beta de las proteínas de amiloide. Glenner G.N. Eng. J. Med. 302:1283 (1980) . Una exposición detallada de la bioquímica e histoquímica del amiloide puede encontrarse en Glenner, N. Eng. J. Med., 302:1333 (1980) .
Hasta ahora, la diagnosis de AD se ha realizado en la mayoría de los casos por evaluación de criterios clínicos, biopsias de cerebro y estudios de tejido post-mortem. Los esfuerzos de investigación para desarrollar métodos para la diagnosis de la enfermedad de Alzheimer in vivo incluyen (1) tests genéticos, (2) métodos de inmunoensayo y (3)
técnicas de producción de imágenes.
La evidencia de que las anormalidades en el metabolismo de Aº son necesarias y suficientes para el desarrollo de AD está basada en el descubrimiento de mutaciones puntuales en la proteína precursora de Aº en varias familias raras con una forma autosómica dominante de AD. Hardy, Nature Genetics 1:233 (1992) ; Hardy et al., Science 256: 184 (1992) . Estas mutaciones ocurren cerca de los puntos de escisión N- y C-terminales necesarios para la 50 generación de Aº a partir de su proteína precursora. St. George-Hyslop et al., Science 235:885 (1987) ; Kang et al., Nature 325:733 (1987) ; Potter WO92/17152. El análisis genético de un gran número de familias AD ha demostrado, sin embargo, que AD es genéticamente heterogénea. St. George-Hyslop et al., Nature 347: 194 (1990) . La conexión con los marcadores del cromosoma 21 se demuestra sólo en algunas familias con AD de aparición precoz y en ninguna familia con AD de aparición tardía. Más recientemente, Sherrington et al han identificado un gen en el 55 cromosoma 14, cuyo producto se predice que contiene dominios transmembranales múltiples y se asemeja a una proteína de membrana integral (Sherrington et al., Nature 375:754-760 (1995) ) . Este gen puede dar cuenta de hasta el 70% de la AD dominante autosómica de aparición precoz. Datos preliminares sugieren que esta mutación en el
cromosoma 14 causa un aumento en la producción de A . Scheuner et al., Soc. Neurosci. Abstr. 21:1500 (1995) . Una mutación en un gen muy similar ha sido identificada en el cromosoma 1 en poblaciones emparentadas alemanas del Volga con AD de aparición precoz. Levy-Lahad et al., Science 269:973-977 (1995) .
El cribado para el genotipo de la apolipoproteína E ha sido sugerido como ayuda en la diagnosis de AD. Scott,
Nature 366:502 (1993) ; Roses, Ann. Neurol. 38:6-14 (1995) . Sin embargo, esta tecnología presenta dificultades, debido que el alelo de la apolipoproteína E4 es sólo un factor de riesgo para AD, no un marcador de la enfermedad. El mismo está ausente en muchos pacientes de AD y presente en muchas personas ancianas que no padecen demencia. Bird, Ann. Neurol. 38: 2-4 (1995) .
Se han desarrollado métodos de inmunoensayo para detectar la presencia de marcadores neuroquímicos en pacientes de AD y para detectar una proteína amiloide afín a AD en el líquido cefalorraquídeo. Warner, Anal. Chem. 59:1203A (1987) ; Patente Mundial No. 92/17152 por Potter; Glenner et al, Patente U.S. No. 4.666.829. No se ha demostrado que estos métodos para la diagnosis de AD detecten AD en todos los pacientes, particularmente en las etapas iniciales de la enfermedad, y son relativamente invasivos, por requerir una punción medular. Asimismo, se han realizado intentos para desarrollar anticuerpos monoclonales como sondas para producción de imágenes de A .
Majocha et al., J. Nucl. Med., 33:2184 (1992) ; Majocha et al., WO89/06242 y Majocha et al., Patente U.S. 5.231.000. La desventaja principal de las sondas de anticuerpos es la dificultad de lograr que estas grandes moléculas atraviesen la barrera hematoencefálica. La utilización de anticuerpos para diagnosis in vivo de AD requeriría anormalidades acusadas en la barrera hematoencefálica a fin de lograr acceso al cerebro. No existe ninguna prueba funcional convincente de que existan fiablemente anormalidades en la barrera hematoencefálica en AD. Kalaria,
Cerebrovascular & Brain Metabolism Reviews 4:226 (1992) .
Se ha utilizado el péptido A radiomarcado para marcar placas de tipo difuso, compacto y neurítico en secciones de cerebro AD. Véase Maggio et al., WO93/04194. Sin embargo, estos péptidos comparten todas las desventajas de los anticuerpos. Específicamente, los péptidos no atraviesan normalmente la barrera hematoencefálica en las cantidades necesarias para la producción de imágenes y dado que estas sondas reaccionan con las placas difusas,
pueden no ser específicas para AD.
La imposibilidad de evaluar la deposición de de amiloide en AD hasta después de la muerte impide el estudio de esta enfermedad devastadora. Se precisa un método de cuantificación de la deposición de amiloide antes de la muerte, no sólo como herramienta de diagnóstico en casos moderados o clínicamente confusos sino también en la monitorización de la eficacia de las terapias dirigidas a prevenir la deposición de A . Por esta razón, sigue siendo... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto fijador de amiloide de la fórmula (I) siguiente para uso en la detección de depósitos de amiloide en un individuo o una sal no tóxica soluble en agua del mismo:
en donde Z es S, NR', O o CR', en cuyo caso la forma tautómera correcta del anillo heterocíclico resulta ser un indol en el cual R' es H o un grupo C1-C8 alquilo:
Y es NR1R2, OR2 o SR2; en donde el nitrógeno de
no es una amina cuaternaria;
cada uno de R1 y R2 se selecciona independientemente del grupo constituido por H, un grupo C1-C8 alquilo, (CH2) nOR' (en donde n = 1, 2, ó 3) , CF3, CH2-CH2X, CH2-CH2-CH2X (en donde X = F, Cl, Br o I) , (C=O) -R', Rph, (CH2) nRph (en donde n = 1, 2, 3 ó 4 y Rph representa un grupo fenilo insustituido o sustituido, en donde los 15 sustituyentes de Rph se seleccionan del grupo constituido por F, Cl, Br, I, un grupo C1-C8 alquilo, (CH2) nOR' (en donde n = 1, 2, ó 3) , CF3, CH2-CH2X, O-CH2-CH2X, CH2-CH2-CH2X, O-CH2-CH2-CH2X (en donde X = F, Cl, Br o I) , CN, (C=O) -R', N (R') 2, NO2, (C=O) N (R') 2, O (CO) R', OR', SR', COOR' (en donde R' es H o un grupo C1-C8 alquilo) , un trialquil-estaño y un grupo quelante (con o sin un grupo metálico quelado) de la forma W-L o V-W-L, en donde V se selecciona del grupo constituido por -COO-, -CO-, -CH2O- y -CH2NH-; W es - (CH2) n en donde n = 0, 1, 2, 3, 4 ó 5; y
L es:
en donde M se selecciona del grupo constituido por Tc y Re;
y R' es H o un grupo C1-C8 alquilo) ; cada uno de R3-R10 se selecciona independientemente del grupo constituido por H, F, Cl, Br, un grupo C1-C8 alquilo, (CH2) nOR' (en donde n = 1, 2, ó 3) , CF3, CH2-CH2X, O-CH2-CH2X, CH2-CH2-CH2X, O-CH2-CH2-CH2X (en donde X = F, Cl, Br o I) , CN, (C=O) -R', N (R') 2, NO2, (C=O) N (R') 2, O (CO) R', OR', SR', COOR', Rph, CR'=CR'-Rph, CR2'=CR2'-Rph, un trialquil-estaño y un grupo quelante (con o sin un grupo metálico quelado) de la forma W-L o V-W-L, en donde V se selecciona del grupo constituido por -COO-, -CO-, -CH2O- y -CH2NH-; W es - (CH2) n en donde n = 0, 1, 2, 3, 4 ó 5; y L es:
en donde M se selecciona del grupo constituido por Tc y Re; 10 o en donde cada uno de R1-R10 se selecciona independientemente del grupo constituido por un grupo quelante (con
y en donde R15 se selecciona independientemente de lo siguiente: H,
en donde R15 se selecciona independientemente de lo siguiente: H,
y R16 es en donde Q se selecciona independientemente de una de las estructuras siguientes:
en donde n = 0, 1, 2, 3 ó 4,
Z es S, NR', O, o C (R') 2 en donde R' es H o un grupo C1-C8 alquilo; U es N o CR'; Y es NR1R2, OR2 o SR2; cada R17-R24 se selecciona independientemente del grupo constituido por H, F, Cl, Br, I, un grupo C1-C8 alquilo,
(CH2) nOR' (en donde n = 1, 2 ó 3) , CF3, CH2-CH2X, O-CH2-CH2X, CH2CH2CH2X, O-CH2-CH2-CH2X (en donde X = F, Cl, Br o I) , CN, (C=O) -R', N (R') 2, NO2, (C=O) N (R') 2, O (CO) R', OR', SR', COOR', Rph, CR'=CR'-Rph y CR2'-CR2-Rph; en donde al menos uno de los sustituyentes R1-R10 se selecciona del grupo constituido por 3H, 131I, 125I, 123I, 76Br, 75Br, 18F, CH2-CH2-X*, O-CH2-CH2-X*, CH2-CH2-CH2X*, O-CH2-CH2-CH2X* (en donde X* = 131I, 123I, 76Br, 75Br o 18F) , 19F, 125I, un sustituyente que contiene carbono seleccionado del grupo constituido por C1-C8 alquilo, (CH2) nOR' , CF3,
CH2-CH2X, O-CH2-CH2X, CH2-CH2-CH2X, O-CH2-CH2-CH2X (en donde X=F, Cl, Br o I) , CN, (C=O) -R', (C=O) N (R') 2, O (CO) R', COOR', CR'=CR'-Rph y CR2'-CR2'-Rph en donde al menos un carbono es 11C, 13C o 14C y un grupo quelante (con grupo metálico quelado) de la forma W-L* o V-W-L*, en donde V se selecciona del grupo constituido por -COO-, -CO-, -CH2O- y -CH2NH-; W es - (CH2) n donde n = 0, 1, 2, 3, 4 ó 5; y L* es:
en donde M* es 99mTc;
o L* es:
y en donde R15 se selecciona independientemente de lo siguiente: 20 H,
2. El compuesto de la reivindicación 1, en donde uno de los sustituyentes R3-R10 se selecciona del grupo constituido por 131I, 123I, 18F, 11C, 75Br y 76Br.
3. El compuesto de la reivindicación 2, en donde uno de los sustituyentes R3-R10 se selecciona del grupo constituido 25 por 11C y 18F.
4. El compuesto de la reivindicación 1, en donde Z = S, Y = N, R1 = H; y R2 se selecciona del grupo constituido por (CH2) nOR' (en donde n=1, 2, o 3) , CF3, CH2-CH2X, CH2-CH2-CH2X (en donde X=F, Cl, B, o I) , (C=O) -R', Rph, y (CH2) nRph (en donde n= 1, 2, 3, o 4) en donde cuando R2 es CH2Rph, R8 no es CH3.
5. El compuesto de la reivindicación 1, en donde Z=S, Y=N, R'=H, R1=H, R2=CH3 y R3-R10 son H.
6. El compuesto de la reivindicación 1, en donde Z=S, Y=O, R'=H, R2=CH3 y R3-R10 son H.
7. El compuesto de la reivindicación 1, en donde Z=S, Y=N, R'=H, R1-4=H, R5=I, y R6- R10 son H.
8. El compuesto de la reivindicación 1, en donde Z=S, Y=N, R'=H, R1-4=H, R5=I, R8=OH y R6- R7 y R9- R10 son H.
9. El compuesto de la reivindicación 1, en donde Z=S, Y=N, R'=H, R'=H, R2= CH2-CH2-CH2-F y R3- R10 son H. 35 10. El compuesto de la reivindicación 1, en donde Z=S, Y=O, R'=H, R2= CH2-CH2-F y R3- R10 son H.
11. El compuesto de la reivindicación 1, en donde Z=S, Y=N, R'=H, R1-7=H, R8=O-CH2-CH2-F y R9- R10 son H.
12. El compuesto de la reivindicación 1, en donde Z=S, Y=N, R'=H, R1=CH3, R2-7=H, R8=O-CH2-CH2-F y R9- R10 son
H.
13. El compuesto de la reivindicación 4, en donde al menos uno de los sustituyentes R3-R10 se selecciona del grupo constituido por CN, OCH3, OH y NH2.
14. El compuesto de la reivindicación 1, en donde R1 = H, R2 = CH3 y R8 se selecciona del grupo constituido por CN, OCH3, OH, OCH3 y NH2.
15. El compuesto de la reivindicación 14, en donde R3-R7 y R9-R10 son H.
16. El compuesto de la reivindicación 1, que tiene la estructura:
17. El compuesto de la reivindicación 1, que tiene la estructura:
18. El compuesto de la reivindicación 1, que tiene la estructura:
19. El compuesto de la reivindicación 1, que tiene la estructura:
20. El compuesto de la reivindicación 1, que tiene la estructura:
21. El compuesto de la reivindicación 1, que tiene la estructura:
22. El compuesto de la reivindicación 1, en donde el depósito de amiloide está localizado en el cerebro de un individuo.
23. El compuesto de la reivindicación 1, en donde se sospecha que el individuo padece una enfermedad o síndrome seleccionado del grupo constituido por Enfermedad de Alzheimer, Enfermedad de Alzheimer familiar, Síndrome de Down y homocigosis para el alelo de la apolipoproteína E4.
24. Un método para la síntesis de un compuesto de la reivindicación 1 que tiene al menos uno de los sustituyentes R3-R10 se seleccionados del grupo constituido por 131I, 125I, 123I, 76Br, 75Br, 18F y 19F, que comprende el paso de 25 marcar un compuesto de la reivindicación 1, en donde Z = S, Y = N, R1 = H y al menos uno de los sustituyentes R3-
R10 es un trialquil-estaño, por reacción del compuesto con una sustancia que contiene 131I, 125I, 123I, 76Br, 75Br, 18F o 19F.
25. Una composición farmacéutica para detectar depósitos de amiloide, que comprende (a) un compuesto fijador de amiloide de la fórmula (I) definida en la reivindicación 1 o una sal no tóxica 30 soluble en agua del mismo; y
(b) un portador farmacéuticamente aceptable.
26. Una composición farmacéutica de acuerdo con la reivindicación 25, en donde Z = S, Y = n y R1 = H.
27. Un método para detectar depósitos de amiloide en tejido de biopsia o tejido humano o animal tejido post-mortem, que comprende los pasos de:
(a) incubar tejido fijado en formalina o recién congelado con una solución de un compuesto fijador de amiloide de la fórmula (I) definida en la reivindicación 1 o una sal no tóxica soluble en agua del mismo para formar un 5 depósito marcado y a continuación,
(b) detectar los depósitos marcados.
28. El método de la reivindicación 27 en donde la solución se compone d.
2. 100% etanol, siendo el resto de la solución agua, en donde la solución está saturada con un compuesto fijador de amiloide de acuerdo con la reivindicación 1 o una sal no tóxica soluble en agua del mismo.
29. El método de la reivindicación 27 en donde la solución está compuesta de un tampón acuoso que contiene 050% etanol, en donde la solución contiene 0, 0001 a 100 !M del compuesto fijador de amiloide.
30. El método de la reivindicación 27 en donde la detección se efectúa por técnicas microscópicas seleccionadas del grupo constituido por microscopía de campo brillante, de fluorescencia, confocal láser y de polarización cruzada.
31. Un método de cuantificación de la cantidad de amiloide en tejido de biopsia o tejido post-mortem que comprende
los pasos de: a) incubar un compuesto fijador de amiloide de la fórmula (I) definida en la reivindicación 1 o una sal no tóxica soluble en agua del mismo, con un homogeneizado de tejido de biopsia o tejido post-mortem, en donde al menos uno de los sustituyentes R1-R10 del compuesto está marcado con un radiomarcador seleccionado del grupo constituido por 125I, 3H, y un sustituyente que contiene carbono especificado en la reivindicación 1, en donde al menos un carbono es 11C, 13C, o 14C, b) separar el compuesto fijado al tejido del compuesto no fijado al tejido. c) cuantificar el compuesto fijado al tejido, y d) convertir las unidades de compuesto fijado al tejido de la reivindicación 1 en unidades de microgramos de amiloide por 100 mg de tejido por comparación con un estándar.
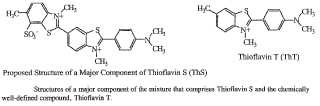
Tioflavina T (ThT)
Estructura propuesta de un Componente Principal de de Tioflavina S (ThS)
Fibrilla de A
Fibrilla de A
Tiempo (min)
Tiempo (min)
Hocico Fuera del Cerebro
Patentes similares o relacionadas:
Molécula de colorante y preparados de colorante, en particular para su uso en métodos quirúrgicos de cirugía oftálmica y para teñir proteínas, del 15 de Julio de 2020, de AL.CHI.MI.A. S.R.L.: Una molécula de colorante que tiene la estructura: **(Ver fórmula)** donde: R1 está conformado por un grupo SO3- unido con un enlace […]
Sonda fluorescente para detectar dipeptidil peptidasa IV, del 3 de Junio de 2020, de The University of Tokyo: Una sonda fluorescente para detectar la dipeptidil peptidasa IV (DPP-IV) que comprende un compuesto representado por la siguiente fórmula (I) o una sal del mismo: **(Ver […]
Kit y método para detectar hidroxiapatita dental porosa, del 27 de Mayo de 2020, de Incisive Technologies Pty Ltd: Una sonda para su uso en un método de detección de una afección in vivo que implica hidroxiapatita dental porosa, que comprende: un indicador coloreado […]
Composiciones para administración por vía oral que comprende una variante de una proteína de pliegue OB, del 29 de Abril de 2020, de AFFILOGIC: Composición para la administración por vía oral para un uso terapéutico o diagnóstico, que comprende una variante de una proteína salvaje de pliegue OB, presentando […]
Marcador molecular para células madre cancerosas, del 29 de Abril de 2020, de Sapporo Medical University: Un péptido seleccionado del grupo que consiste en: DNAJB8 : AFMEAFSSF (SEQ ID NO: 71); DNAJB8 : AYRKLALRW (SEQ ID NO: 68); y DNAJB8 : […]
Cepas bacterianas que expresan genes de metilasa y sus usos, del 22 de Abril de 2020, de LOMA LINDA UNIVERSITY: Una bacteria aislada para usar en la producción de ADN plasmídico metilado, en donde la bacteria comprende un polinucleótido exógeno que codifica una CpG metilasa […]
Variantes de clorotoxina, conjugados y métodos para su utilización, del 8 de Abril de 2020, de FRED HUTCHINSON CANCER RESEARCH CENTER: Conjugado de clorotoxina que comprende un péptido de clorotoxina acoplado covalentemente a un marcador fluorescente seleccionado del grupo que consiste […]
Composición de imagen de cartílago articular, del 8 de Abril de 2020, de Mercury Asset Management Co., Ltd: Una composición adecuada para uso en la visualización de una zona degenerativa de cartílago articular, que se caracteriza por contener una albúmina […]