COMPOSICIÓN PARA EL TRATAMIENTO DEL DOLOR Y/O LA INFLAMACIÓN.
Composiciones para el tratamiento del dolor y/o la inflamación que comprenden al menos un péptido de fórmula general (I)R1-AA-R2(I)sus estereoisómeros,
mezclas de los mismos, y sus sales cosmética y farmacéuticamente aceptables, donde AA es una secuencia de 3 a 40 aminoácido adyacentes contenida en la secuencia de aminoácidos de la proteína SNAP-25. Péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, y sus sales cosmética y farmacéuticamente aceptables para el tratamiento del dolor y/o inflamación
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200802210.
Solicitante: BCN PEPTIDES, S.A.
DIVERDRUGS, S.L.
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: FERRER MONTIEL, ANTONIO, CARREÑO SERRAIMA,CRISTINA, PONSATI OBIOLS, BERTA, FERNANDEZ CARNEADO,JIMENA, VAN DEN NEST,WIM, CAMPRUBI ROBLES,MARIA.
Fecha de Solicitud: 24 de Julio de 2008.
Fecha de Publicación: .
Fecha de Concesión: 10 de Febrero de 2012.
Clasificación Internacional de Patentes:
- A61K38/17A2
Clasificación PCT:
- A61K38/17 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
Fragmento de la descripción:
Composición para el tratamiento del dolor y/o la inflamación.
Campo de la invención
La presente invención se refiere a una composición para el tratamiento del dolor y/o la inflamación, preferentemente para el tratamiento del dolor agudo, dolor crónico, dolor inflamatorio, dolor inducido por cáncer o por el tratamiento del cáncer, dolor visceral, dolor neuropático, neuralgia post-herpética, neuropatía diabética, neuralgia del trigémino, migraña y fibromialgia. Dicha composición comprende una cantidad eficaz de al menos un péptido que posee una secuencia derivada de la secuencia de aminoácidos de la proteína SNAP-25, o de sus sales cosmética o farmacéuticamente aceptables.
Antecedentes de la invención
El dolor representa un grave problema social y económico. Se calcula que más de 2 millones de personas están incapacitadas diariamente por sufrir sensaciones dolorosas transitorias o crónicas [Williams, M., Kowaluk, E.A. y Arneric S.P (1999) "Emerging Molecular approaches to pain therapy" J. Med. Chem. 42, 1481-1500]. Claros ejemplos lo representan la algesia experimentada por pacientes de cáncer, jaqueca, artritis, quemados, accidentados y los operados quirúrgicamente. Un dolor no tratado de manera eficaz puede llegar a ser devastador para las personas, limitando sus capacidades, reduciendo su movilidad, provocando alteraciones del sueño e interfiriendo dramáticamente en su calidad de vida. A pesar de la gravedad del problema, el arsenal farmacéutico para combatirlo, prevenirlo y/o aminorar su sintomatología y su progreso es sorprendentemente limitado, debido, en parte, a la falta de dianas terapéuticas específicas sobre las que actuar, y al desconocimiento de las rutas metabólicas que median la transducción del dolor.
La integridad de nuestro organismo viene garantizada por el correcto funcionamiento acoplado de dos sistemas altamente especializados: el sistema inmune y el sistema nervioso. Ante una lesión tisular provocada por estímulos nocivos de naturaleza física o química, ambos sistemas colaboran concertadamente provocando la sensibilización de la zona afectada con el objetivo de frenar la expansión del daño y garantizar la rápida reparación de la zona deteriorada [Belmonte, C. y Cerveró, F. Eds. (1996) "Neurobiology of Nociceptors" Oxford University Press]. Este proceso se denomina inflamación y puede ser de dos tipos, bien humoral si está principalmente mediada por el sistema inmune, o bien neurogénica si está producida por el sistema nervioso. No obstante, un aspecto importante es que ambos tipos de inflamación se potencian entre sí, intensificando de esta forma la experiencia dolorosa que acompaña al proceso inflamatorio.
La sensación de dolor se inicia cuando los terminales periféricos de un grupo de neuronas sensoriales, conocidas como neuronas nociceptoras o nociceptores, se activa por estímulos nocivos de naturaleza química, mecánica o térmica. Las neuronas nociceptoras transmiten la información acerca del daño tisular a los centros procesadores de la sensación de dolor en la médula espinal y el cerebro [Belmonte, C. y Cerveró, F. Eds. (1996) "Neurobiology of Nociceptors" Oxford University Press; Baranauskas, G. y Nistri, A. (1998) "Sensitization of pain pathways in the spinal cord: cellular mechanisms" Prog. Neurobiol. 54, 349-365; Richardson, D.J. y Vasko, M.R. (2002) "Cellular mechanisms of neurogenic inflammation" J. Pharmacol. Exp. Ther. 302, 839-845]. Una característica importante de los nociceptores es que aun siendo principalmente neuronas primarias de carácter aferente, tras ser activadas, son capaces de ejercer una función eferente mediante la liberación de moléculas pro-algésicas y pro-inflamatorias como la sustancia P (SP), el péptido relacionado con la calcitonina (CGRP), la histamina, el ATP, el glutamato, y la bradiquinina (BK). Estas moléculas promueven la activación autocrina y paracrina de las neuronas vecinas así como también de otros tipos celulares como los mastocitos, los neutrófilos, y las plaquetas. Al activarse las células no neuronales circundantes liberan neurotrofinas (NGF), citoquinas (α-TNF, IL1-β, IL-6), prostaglandinas, leucotrienos y protones que dotan a la sopa inflamatoria de su carácter ácido. Todos estos factores, a su vez, actúan sobre los nociceptores potenciando la inflamación local o inflamación neurogénica, modificando la excitabilidad nociceptiva o sensibilización periférica, y provocando cambios en la percepción de los estímulos aplicados en la zona dañada como por ejemplo la hiperalgesia, entendida como una respuesta exagerada a un estímulo modestamente nocivo como, por ejemplo, temperaturas templadas de 35-40ºC, o la alodinia, entendida como el fenómeno en que se perciben como dolorosos estímulos que no son nocivos como, por ejemplo, una ligera brisa [Belmonte, C. y Cerveró, F. Eds. (1996) "Neurobiology of Nociceptors" Oxford University Press; Baranauskas, G. y Nistri, A. (1998) "Sensitization of pain pathways in the spinal cord: cellular mechanisms" Prog. Neurobiol. 54, 349-365; Richardson, D.J. y Vasko, M.R. (2002) "Cellular mechanisms of neurogenic inflammation" J. Pharmacol. Exp. Ther. 302, 839-845; Brune, K. y Handwerker, H.O. Eds. (2004) "Hyperalgesia: molecular mechanisms and clinical implications" Progress in Pain Research and Management, vol 30. IASP Press. Seatle]. Una excitabilidad persistente de los nociceptores periféricos origina alteraciones sinápticas a nivel de la médula espinal que conducen al proceso de sensibilización central que, a su vez, contribuye a potenciar la percepción dolorosa en la zona inflamada [Richardson, D.J. y Vasko, M.R. (2002) "Cellular mechanisms of neurogenic inflammation" J. Pharmacol. Exp. Ther. 302, 839-845; Brune, K. y Handwerker, H.O. Eds. (2004) "Hyperalgesia: molecular mechanisms and clinical implications" Progress in Pain Research and Management, vol 30. IASP Press. Seatle].
Las bases moleculares y celulares de la inflamación neurogénica, así como su regulación por mediadores de la inflamación son mayoritariamente desconocidas debido, fundamentalmente, a la falta de información acerca de la identidad molecular de muchos de los receptores implicados, así como a la indefinición de las rutas de señalización involucradas en los nociceptores. No obstante, se conoce que los mecanismos por los que los componentes de la sopa inflamatoria alteran la excitabilidad neuronal pueden ser directos a través de la interacción con canales iónicos en la superficie de los nociceptores o bien indirectos, a través de cascadas intracelulares [Richardson, D.J. y Vasko, M.R. (2002) "Cellular mechanisms of neurogenic inflammation" J. Pharmacol. Exp. Ther. 302, 839-845; Brune, K. y Handwerker, H.O. Eds. (2004) "Hyperalgesia: molecular mechanisms and clinical implications" Progress in Pain Research and Management, vol 30. IASP Press. Seatle]. Así la BK, las NGF y las interleuquinas producen sus acciones al activar rutas metabólicas que activan a las proteínas quinasas PKC y PKA que pueden modificar receptores de membrana que transducen estímulos ambientales, y/o modular la expresión de genes neuronales (especialmente en procesos inflamatorios crónicos). Entre los receptores diana de las rutas de señalización intracelular están los canales activados por voltaje selectivos al ión Na+ y el receptor de vanilloides TRPV1, un integrador sensorial de estímulos nocivos químicos y térmicos, así como canales mecanosensibles. La activación de dichos receptores dispara potenciales de acción que estimulan la función aferente y eferente de los nociceptores, lo que se traduce en un incremento de la sensibilización periférica y central. Por tanto, todas estas observaciones demuestran un papel clave de la inflamación neurogénica o neurológica en procesos inflamatorios agudos y crónicos. Por tanto, compuestos que reduzcan la magnitud de la inflamación neurogénica presentarán una actividad antiinflamatoria y analgésica. Así, por ejemplo, antagonistas de los receptores neuronales implicados como el TRPV1, los canales de Na+, los receptores de bradiquinina o los receptores purinérgicos se comportarán como antiinflamatorios y/o analgésicos potentes. Una prueba de ello lo constituyen los antagonistas del receptor TRPV1 [García-Martínez, C., Planells-Cases, R., Fernández, A.M. Royo, M., Albericio, F., Messeguer, A., Pérez-Payá, E., Carreño, C. y Ferrer-Montiel, A. (2003) "Small moleculas targeting the TRPV1 complex as new drugs for pain management" Drugs of...
Reivindicaciones:
1. Composición para el tratamiento del dolor y/o la inflamación que comprende al menos un péptido de fórmula general (I)
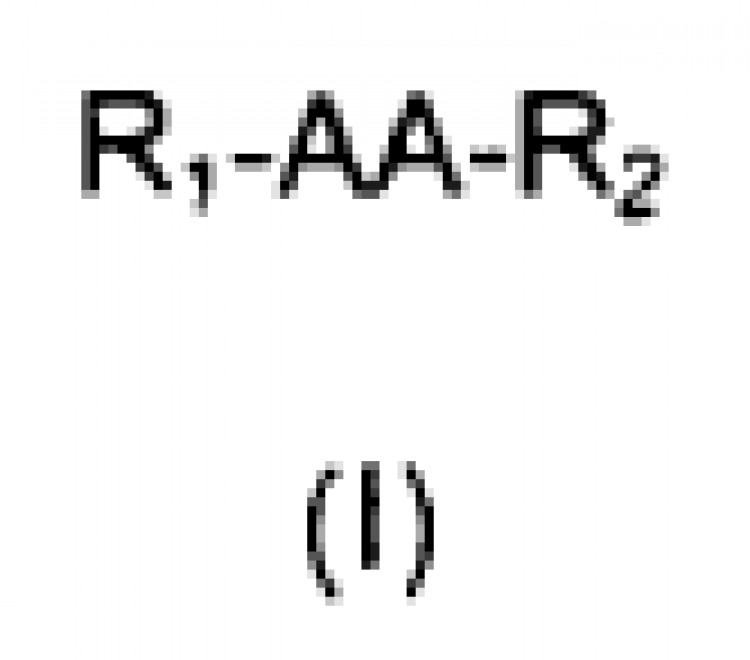
sus estereoisómeros, mezclas de los mismos, y/o sus sales cosmética y farmacéuticamente aceptables, caracterizada por que
AA es una secuencia de 6 a 40 aminoácidos adyacentes contenida en la secuencia de aminoácidos SEQ ID No. 1, que contiene la secuencia de aminoácidos SEQ ID No. 11 manteniendo la función;
R1 se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido, y R5-C(O)-; y
R2 se selecciona del grupo formado por -NR3R4, -OR3 y -SR3; donde R3 y R4 se seleccionan independientemente del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido y aralquilo sustituido o no sustituido; donde
R5 se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido, heterociclilo sustituido o no sustituido y heteroarilalquilo sustituido o no sustituido,
y al menos un adyuvante aceptable.
2. Composición según la reivindicación 1, caracterizada por que R1 es H, grupo alifático de C2 a C24 no cíclico sustituido o no sustituido, grupo aliciclilo de C2 a C24 sustituido o no sustituido o R5-C(O)-, donde R5 es grupo alifático no cíclico de C1 a C24 sustituido o no sustituido o aliciclilo de C1 a C24 sustituido o no sustituido.
3. Composición según la reivindicación 2, caracterizada por que R1 se selecciona del grupo formado por H, acetilo, terc-butanoilo, hexanoilo, 2-metilhexanoilo, ciclohexancarboxilo, octanoilo, decanoilo, lauroilo, miristoilo, palmitoilo, estearoilo, oleoilo y linoleoilo.
4. Composición según la reivindicación 1, caracterizada por que R1 es un polímero de polietilenglicol.
5. Composición según la reivindicación 4, caracterizada por que dicho polímero de polietilenglicol es
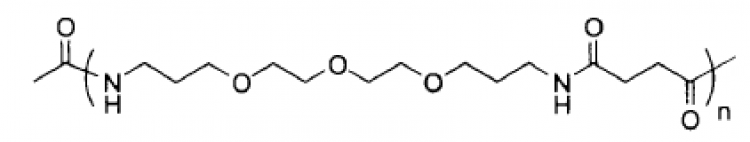
donde n puede variar entre 1 y 100.
6. Composición según la reivindicación 5, caracterizada por que n varía entre 1 y 5.
7. Composición según la reivindicación 1, caracterizada por que R2 es -NR3R4 o -OR3, donde R3 y R4 se seleccionan independientemente del grupo formado por H, grupo alifático no cíclico de C1 a C24 sustituido o no sustituido y grupo aliciclilo de C1 a C24 sustituido o no sustituido.
8. Composición según la reivindicación 7, caracterizada por que R3 y R4 se seleccionan del grupo formado por H, metilo, etilo, hexilo, dodecilo y hexadecilo.
9. Composición según la reivindicación 1, caracterizada por que AA es una secuencia de aminoácidos adyacentes contenida en una secuencia seleccionada del grupo formado por SEQ ID No.4, SEQ ID No.8, SEQ ID No.11, SEQ ID No.12, SEQ ID No.14, SEQ ID No.15, SEQ ID No.16, SEQ ID No.17, SEQ ID No.18, SEQ ID No.19, SEQ ID No.20, SEQ ID No.21, SEQ ID No.22, SEQ ID No.23, SEQ ID No.24, SEQ ID No.25 y SEQ ID No.26.
10. Composición según cualquiera de las reivindicaciones 1 a 9, caracterizada por que el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado a un vehículo o a un sistema de liberación sostenida seleccionado del grupo formado por liposomas, milicápsulas, microcápsulas, nanocápsulas, esponjas, vesículas, micelas, miliesferas, microesferas, nanoesferas, lipoesferas, microemulsiones, nanoemulsiones, milipartículas, micropartículas y nanopartículas.
11. Composición según cualquiera de las reivindicaciones 1 a 10, caracterizada por que el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra adsorbido sobre un polímero orgánico o soporte sólido mineral seleccionado del grupo formado por talco, bentonita, sílice, almidón o maltodextrina.
12. Composición según cualquiera de las reivindicaciones 1 a 11, caracterizada por que presenta una formulación seleccionada del grupo formado por cremas, emulsiones múltiples, composiciones anhidras, dispersiones acuosas, aceites, leches, bálsamos, espumas, lociones, geles, soluciones hidroalcólicas, linimentos, sueros, jabones, champús, ungüentos, mousses, pomadas, polvos, barras, lápices, vaporizadores y aerosoles.
13. Composición según cualquiera de las reivindicaciones 1 a 12, caracterizada por que el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado en productos de línea de maquillaje.
14. Composición según cualquiera de las reivindicaciones 1 a 13, caracterizada por que el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado en un tejido, un tejido-no-tejido o un producto sanitario.
15. Composición según la reivindicación 14, caracterizada por que el tejido, tejido-no-tejido o producto sanitario se selecciona del grupo formado por vendas, gasas, camisetas, medias, calcetines, ropa interior, fajas, guantes, pañales, compresas, apósitos, cubrecamas, toallitas, hidrogeles, parches adhesivos, parches no adhesivos, parches microeléctricos y mascarillas faciales.
16. Composición según cualquiera de las reivindicaciones 1 a 15, caracterizada por que el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra a una concentración entre el 0.00000001% y el 20% en peso.
17. Composición según la reivindicación 16, caracterizada por que el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra a una concentración entre el 0.0001% y el 5% en peso.
18. Composición según cualquiera de las reivindicaciones 1 a 17, caracterizada por que comprende una cantidad eficaz de al menos un principio activo seleccionado del grupo formado por un agente antioxidante, un inhibidor de la NO-sintasa, un agente dermorelajante, un agente antiinflamatorio, un agente analgésico, un agente antimicrobiano, un agente antifúngico, o mezclas de ellos.
19. Composición según cualquiera de las reivindicaciones 1 a 18, caracterizada por que se administra por vía tópica, enteral o parenteral.
20. Composición según la reivindicación 19, caracterizada por que se administra por vía tópica, transdérmica, oral, nasal, o inhalacional, o mediante inyección intramuscular, intravenosa, intraperitoneal o subcutánea.
21. Composición según la reivindicación 20, caracterizada por que la administración tópica o transdérmica se realiza mediante iontoforesis, sonoforesis, electroporación, presión mecánica, gradiente de presión osmótica, cura oclusiva, microinyecciones, inyecciones sin agujas mediante presión, parches microeléctricos o cualquier combinación de ellas.
22. Composición según la reivindicación 1, caracterizada por que el dolor y/o inflamación se seleccionan del grupo formado por dolor neuropático, dolor inflamatorio, dolor visceral, dolor abdominal, dolor del sistema digestivo, dolor del sistema respiratorio, dolor del sistema urogenital, dolor del sistema endocrino, dolor de corazón, dolor pancreático, dolor intestinal, dolor de estómago, dolor del bazo, dolor de los vasos sanguíneos, síndrome del colon irritable, dolor de cabeza tensional, dolor de cabeza asociado a sinusitis, migraña, dolor ocular, síndrome del ojo seco, dolor post-operativo, dolor post-operativo debido a las incisiones quirúrgicas, dolor post-operativo debido a la inserción de implantes en los huesos, dolor post-operativo debido a la sustitución de huesos, dolor post-operativo debido a las infecciones, dolor debido a cáncer, el dolor debido a cáncer de huesos, dolor asociado a tumores óseos benignos, dolor asociado a osteomas osteoides, dolor asociado a osteoblastomas, dolor debido al tratamiento del cáncer, dolor músculoesquelético, dolor muscular espástico, fibromialgia, dolor neurálgico, dolor de cuello asociado a distonias cervicales, dolor de espalda, lumbalgias, ciáticas, inflamación neurogénica, irritación cutánea, pieles sensibles, dermatitis atópica, dermatitis de contacto, dermatitis del pañal, eccema, artitis, artritis reumatoide, osteoartritis, neuralgia post-herpética, neuropatías periféricas, dolor fantasma, alodinia, dolor debido al síndrome del túnel carpiano, dolor quemante, parestesias, dolor facial, neuralgia del trigémino, dolor neuropático debido a diabetes, dolor asociado de procesos de tatuaje o a eliminación de tatuajes, dolor debido a juanetes, dolor testicular, dolor miofascial, dolor de la vejiga urinaria, dolor del tracto urinario, dolor vulvar, dolor vaginal, dolor escrotal, dolor perineal, dolor pélvico, dolor o irritación cutánea tras una intervención quirúrgica, tras un tratamiento con terapia de luz pulsada (IPL, Intense Pulse Light), tras un tratamiento con terapia de luz pulsada monocromática (láser), tras un tratamiento con agentes descamantes químicos o tras una sobreexposición a agentes externos agresivos.
23. Péptido de fórmula general (I)
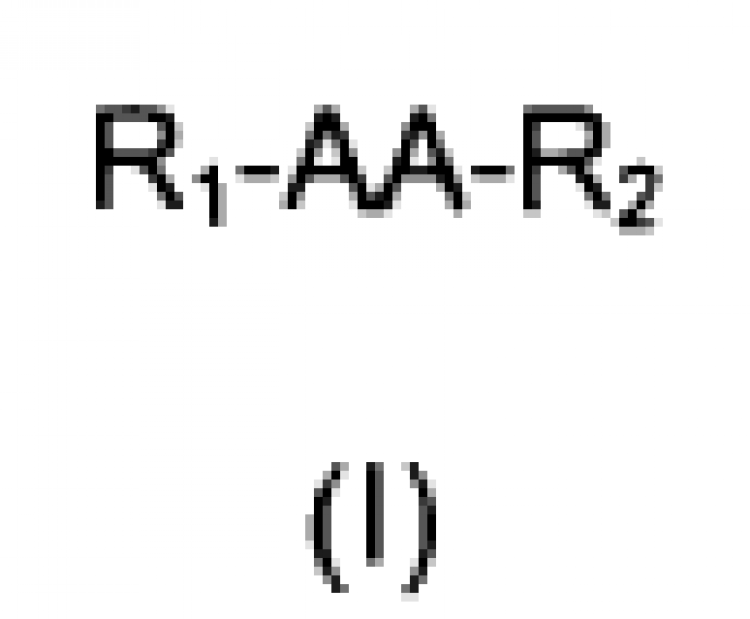
sus estereoisómeros, mezclas de los mismos, y/o sus sales cosmética y farmacéuticamente aceptables, donde
AA es una secuencia de 6 a 40 aminoácidos adyacentes contenida en la secuencia de aminoácidos SEQ ID No. 1, que contiene la secuencia de aminoácidos SEQ ID No. 11 manteniendo la función;
R1 se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido, y R5-C(O)-; y
R2 se selecciona del grupo formado por -NR3R4, -OR3 y -SR3; donde R3 y R4 se seleccionan independientemente del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido y aralquilo sustituido o no sustituido; y
R5 se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido, heterociclilo sustituido o no sustituido y heteroarilalquilo sustituido o no sustituido,
para el tratamiento del dolor y/o inflamación.
24. Péptido según la reivindicación 23, donde R1 es H, grupo alifático de C2 a C24 no cíclico sustituido o no sustituido, grupo aliciclilo de C2 a C24 sustituido o no sustituido o R5-C(O)-, donde R5 es grupo alifático no cíclico de C1 a C24 sustituido o no sustituido o aliciclilo de C1 a C24 sustituido o no sustituido.
25. Péptido según la reivindicación 24, donde R1 se selecciona del grupo formado por H, acetilo, terc-butanoilo, hexanoilo, 2-metilhexanoilo, ciclohexancarboxilo, octanoilo, decanoilo, lauroilo, miristoilo, palmitoilo, estearoilo, oleoilo y linoleoilo.
26. Péptido según la reivindicación 23, donde R1 es un polímero de polietilenglicol.
27. Péptido según la reivindicación 26, donde dicho polímero de polietilenglicol es
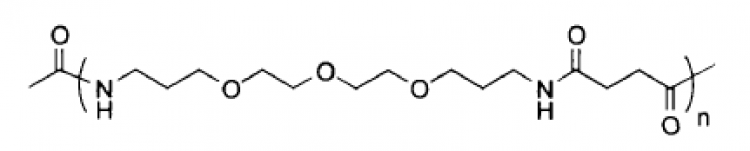
donde n puede variar entre 1 y 100.
28. Péptido según la reivindicación 27, donde n varía entre 1 y 5.
29. Péptido según la reivindicación 23, donde R2 es -NR3R4 o -OR3, donde R3 y R4 se seleccionan independientemente del grupo formado por H, grupo alifático no cíclico de C1 a C24 sustituido o no sustituido y grupo aliciclilo de C1 a C24 sustituido o no sustituido.
30. Péptido según la reivindicación 29, donde R3 y R4 se seleccionan del grupo formado por H, metilo, etilo, hexilo, dodecilo y hexadecilo.
31. Péptido según la reivindicación 23, donde AA es una secuencia de aminoácidos adyacentes contenida en una secuencia seleccionada del grupo formado por SEQ ID No.4, SEQ ID No.8, SEQ ID No.11, SEQ ID No.12, SEQ ID No.14, SEQ ID No.15, SEQ ID No.16, SEQ ID No.17, SEQ ID No.18, SEQ ID No.19, SEQ ID No.20, SEQ ID No.21, SEQ ID No.22, SEQ ID No.23, SEQ ID No.24, SEQ ID No.25 y SEQ ID No.26.
32. Péptido según cualquiera de las reivindicaciones 23 a 31, donde el péptido de fórmula general (I), sus estereoisómeros, mezclas de los mismos, o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado a un vehículo o a un sistema de liberación sostenida seleccionado del grupo formado por liposomas, milicápsulas, microcápsulas, nanocápsulas, esponjas, vesículas, micelas, miliesferas, microesferas, nanoesferas, lipoesferas, microemulsiones, nanoemulsiones, milipartículas, micropartículas y nanopartículas.
33. Péptido según cualquiera de las reivindicaciones 23 a 32, que se encuentra adsorbido sobre un polímero orgánico o soporte sólido mineral seleccionado del grupo formado por talco, bentonita, sílice, almidón o maltodextrina.
34. Péptido según cualquiera de las reivindicaciones 23 a 33, que está contenido en una formulación seleccionada del grupo formado por cremas, emulsiones múltiples, composiciones anhidras, dispersiones acuosas, aceites, leches, bálsamos, espumas, lociones, geles, soluciones hidroalcólicas, linimentos, sueros, jabones, champús, ungüentos, mousses, pomadas, polvos, barras, lápices, vaporizadores y aerosoles.
35. Péptido según cualquiera de las reivindicaciones 23 a 34, que se encuentra incorporado en productos de línea de maquillaje.
36. Péptido según cualquiera de las reivindicaciones 23 a 35, que se encuentra incorporado en un tejido, un tejido-no-tejido o un producto sanitario.
37. Péptido según la reivindicación 36, donde el tejido, tejido-no-tejido o producto sanitario se selecciona del grupo formado por vendas, gasas, camisetas, medias, calcetines, ropa interior, fajas, guantes, pañales, compresas, apósitos, cubrecamas, toallitas, hidrogeles, parches adhesivos, parches no adhesivos, parches microeléctricos y mascarillas faciales.
38. Péptido según cualquiera de las reivindicaciones 23 a 37, que está contenido en una composición en una concentración entre el 0.00000001% y el 20% en peso.
39. Péptido según la reivindicación 38, donde la concentración en la composición está entre el 0.0001% y el 5% en peso.
40. Péptido según cualquiera de las reivindicaciones 23 a 39, que está contenido en una composición que comprende una cantidad eficaz de al menos un principio activo seleccionado del grupo formado por un agente antioxidante, un inhibidor de la NO-sintasa, un agente dermorelajante, un agente antiinflamatorio, un agente analgésico, un agente antimicrobiano, un agente antifúngico, o mezclas de ellos.
41. Péptido según cualquiera de las reivindicaciones 23 a 40, que se administra por vía tópica, enteral o parenteral.
42. Péptido según la reivindicación 41, que se administra por vía tópica, transdérmica, oral, nasal, o inhalacional, o mediante inyección intramuscular, intravenosa, intraperitoneal o subcutánea.
43. Péptido según la reivindicación 42, donde la administración tópica o transdérmica se realiza mediante iontoforesis, sonoforesis, electroporación, presión mecánica, gradiente de presión osmótica, cura oclusiva, microinyecciones, inyecciones sin agujas mediante presión, parches microeléctricos o cualquier combinación de ellas.
44. Péptido según la reivindicación 23, donde el dolor y/o inflamación se seleccionan del grupo formado por dolor neuropático, dolor inflamatorio, dolor visceral, dolor abdominal, dolor del sistema digestivo, dolor del sistema respiratorio, dolor del sistema urogenital, dolor del sistema endocrino, dolor de corazón, dolor pancreático, dolor intestinal, dolor de estómago, dolor del bazo, dolor de los vasos sanguíneos, síndrome del colon irritable, dolor de cabeza tensional, dolor de cabeza asociado a sinusitis, migraña, dolor ocular, síndrome del ojo seco, dolor post-operativo, dolor post-operativo debido a las incisiones quirúrgicas, dolor post-operativo debido a la inserción de implantes en los huesos, dolor post-operativo debido a la sustitución de huesos, dolor post-operativo debido a las infecciones, dolor debido a cáncer, el dolor debido a cáncer de huesos, dolor asociado a tumores óseos benignos, dolor asociado a osteomas osteoides, dolor asociado a osteoblastomas, dolor debido al tratamiento del cáncer, dolor músculoesquelético, dolor muscular espástico, fibromialgia, dolor neurálgico, dolor de cuello asociado a distonias cervicales, dolor de espalda, lumbalgias, ciáticas, inflamación neurogénica, irritación cutánea, pieles sensibles, dermatitis atópica, dermatitis de contacto, dermatitis del pañal, eccema, artitis, artritis reumatoide, osteoartritis, neuralgia post-herpética, neuropatías periféricas, dolor fantasma, alodinia, dolor debido al síndrome del túnel carpiano, dolor quemante, parestesias, dolor facial, neuralgia del trigémino, dolor neuropático debido a diabetes, dolor asociado de procesos de tatuaje o a eliminación de tatuajes, dolor debido a juanetes, dolor testicular, dolor miofascial, dolor de la vejiga urinaria, dolor del tracto urinario, dolor vulvar, dolor vaginal, dolor escrotal, dolor perineal, dolor pélvico, dolor o irritación cutánea tras una intervención quirúrgica, tras un tratamiento con terapia de luz pulsada (IPL, Intense Pulse Light), tras un tratamiento con terapia de luz pulsada monocromática (láser), tras un tratamiento con agentes descamantes químicos o tras una sobreexposición a agentes externos agresivos.
Patentes similares o relacionadas:
ENTRENAMIENTO COGNITIVO AUMENTADO, del 6 de Febrero de 2012, de COLD SPRING HARBOR LABORATORY: Un agente de aumento de CREB para su uso en un procedimiento para tratar pérdida de función cognitiva del procedimiento dependiente de traumatismo, […]
MÉTODOS Y COMPUESTOS PARA TRATAR LA DIABETES, del 9 de Diciembre de 2011, de BIOCRINE AB: Uso de una cantidad eficaz del tetrámero de transtiretina para la fabricación de un medicamento para tratar la diabetes de tipo I o para prevenir la […]
USO DE LA PROTEÍNA RGS-14 PARA POTENCIAR LA MEMORIA, del 15 de Septiembre de 2011, de UNIVERSIDAD DE MALAGA: Uso de la proteína RGS-14 para potenciar la memoria.La administración de la proteína RGS-14, también conocida como regulador de la proteína-G señalizadora 14, en cerebro provoca […]
USO DE UN GEN ASOCIADO A LA DIFERENCIACIÓN DEL MELANOMA (MDA-7) PARA INVERTIR UN FENOTIPO CANCEROSO, del 5 de Septiembre de 2011, de THE TRUSTEES OF COLUMBIA UNIVERSITY IN THE CITY OF NEW YORK: Uso de un ácido nucleico que comprende un gen asociado a la diferenciación del melanoma (mda-7) para la preparación de una composición farmacéutica para […]
DETERMINANTES MOLECULARES DE LA OSTEOPATÍA POR MIELOMA Y USO DE LOS MISMOS, del 11 de Julio de 2011, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ARKANSAS: Método ex vivo para determinar el potencial de desarrollar una osteopatía lítica en un paciente con mieloma múltiple, comprendiendo el método la etapa […]
TRATAMIENTO DE LA INSUFICIENCIA RENAL AGUDA CON TROMBOMODULINA SOLUBLE, del 7 de Junio de 2011, de ELI LILLY AND COMPANY INDIANA UNIVERSITY RESEARCH AND TECHNOLOGY CORPORATION: Trombomodulina soluble para usar en el tratamiento de un sujeto humano que tiene insuficiencia renal aguda, en el que dicha trombomodulina soluble […]
COMPLEJOS DE CASEÍNA, del 10 de Mayo de 2011, de DSM IP ASSETS B.V.: Un complejo que comprende (i) un compuesto abarcado por la fórmula general en donde A significa un enlace sencillo o doble de carbono-carbono, pudiendo estar este […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]