VARIANTES DE RIBONUCLEASA CITOTÓXICA.
Una ribonucleasa diseñada por ingeniería de la superfamilia RNasa A que tiene al menos dos cambios de aminoácidos de la secuencia de aminoácidos nativa de la ribonucleasa,
siendo el primer cambio una sustitución de aminoácido en la región correspondiente a los restos de aminoácidos 85 a 94 de RNasa A pancreática bovina, y siendo el segundo cambio una alteración, sustitución o intercambio de aminoácido en un lugar seleccionado entre el grupo constituido por aminoácidos que corresponden a los restos 38, 39 y 67 de RNasa A pancreática bovina, teniendo la ribonucleasa diseñada por ingeniería una actividad citotóxica intensificada en comparación con una correspondiente ribonucleasa diseñada por ingeniería que tiene una modificación sólo en la región que corresponde a restos de los aminoácidos 85 a 94
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/023298.
Solicitante: WISCONSIN ALUMNI RESEARCH FOUNDATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 614 WALNUT STREET, P.O. BOX 7365 MADISON, WI 53707-7365 ESTADOS UNIDOS DE AMERICA.
Inventor/es: RAINES,RONALD,T, MITCHELL,JULIE,C, RUTKOSKI,THOMAS,J.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Junio de 2006.
Clasificación Internacional de Patentes:
- C12N9/22 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Ribonucleasas.
Clasificación PCT:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- C12N15/55 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Hidrolasas (3).
- C12N9/22 C12N 9/00 […] › Ribonucleasas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
REFERENCIA CRUZADA A SOLICITUDES RELACIONADAS
Esta solicitud reivindica la prioridad de la solicitud de patente provisional nº. de serie 60/690.970 presentada el 16 de junio de 2005. 5
DECLARACIÓN EN CUANTO A INVESTIGACIÓN O DESARROLLO PATROCINADO FEDERALMENTE
Esta invención se hizo con apoyo económico del gobierno de los Estados Unidos concedida por la siguiente agencia: NIH CA073808. Estados Unidos tiene ciertos 10 derechos en esta invención.
.
ANTECEDENTES DE LA INVENCIÓN
Las ribonucleasas son enzimas que catalizan la degradación de ARN. Una ribonucleasa bien estudiada es la ribonucleasa A bovina (RNasa A), cuya función biológica 15 putativa es descomponer la gran cantidad de ARN que se acumula en el intestino del rumiante. La superfamilia de RNasa A es un grupo de enzimas ribonucleasa clasificadas como homólogos a RNasa A. Algunos miembros de la superfamilia poseen varias propiedades biológicas de 20 interés que incluyen actividades antiproliferativas, citotóxicas, embriotóxicas, espermatogénicas y anti-tumorales. Un miembro de esta familia es un homólogo de RNasa A aislada originalmente de oocitos y embriones precoces de la rana leopardo Rana pipiens, que ahora se 25 conoce como Onconase (ONC), un nombre usado para la molécula que exhibe propiedades antitumorales in vitro e in vivo. Actualmente, la ONC se está evaluando como un agente terapéutico del cáncer en ensayos clínicos.
Una limitación significativa sobre la aptitud de la 30 ONC como agente quimioterapéutico es la toxicidad renal limitativa de la dosis. La ONC es retenida en el riñón a una concentración mucho mayor que la de los miembros
mamíferos de la superfamilia RNasa. Puede haber también manifestaciones alergénicas con la ONC, puesto que los ratones producen anticuerpos contra ONC pero no contra RNasa A, con la que ONC comparte aproximadamente 30% de sus aminoácidos. Esto sugiere que otros miembros de la familia 5 de RNasa pueden ser también candidatos para evaluación como agentes terapéuticos clínicos si se les pueden impartir las propiedades citotóxicas similares a las de ONC.
En el cuerpo, los niveles de actividad de RNasa son controlados por un inhibidor de la ribonucleasa (RI), que 10 es una proteína de 50-kDA encontrada en el citosol de todas las células mamíferas. RI es un miembro de una familia de proteínas rica en leucina y está compuesto por 15 repeticiones alternantes dispuestas simétricamente en una molécula con forma de herradura de caballo. RI tiene un 15 gran número de restos de cisteína (32 en IR humano), lo que significa que puede mantener su forma y función sólo en un medio reductor como el citosol. El IR actúa uniéndose a la superfamilia de RNasa, un IR a una molécula de RNasa, y, cuando está así unido, el IR inhibe completamente la 20 actividad catalítica de la ribonucleasa por bloqueo estérico del sitio activo de la enzima. La unión de IR a la RNasa es muy íntima, teniendo una afinidad de unión muy alta.
Algunos miembros de la familia RNasa, notoriamente 25 ONC y la ribonucleasa seminal bovina, poseen la capacidad nativa de evadir IR. El hecho de la evasión de IR es principalmente responsable de la citotoxicidad de ONC y la ribonucleasa seminal bovina. También se ha encontrado que miembros de la superfamilia de RNasa que no son nativamente 30 citotóxicos pueden hacerse citotóxicos por modificación de sus constituyentes aminoácidos de manera que inhiban la unión a IR y, en particular, haciendo sustituciones de
aminoácidos pequeños por grandes en uno de los puntos de más estrecha interacción entre IR y RNasa. Este procedimiento se describe en la patente U.S. nº. 5.840.296, que describe una variante citotóxica, G88R RNasa A, que tiene una afinidad aminorada para IR en comparación con la 5 RNasa A, pero que todavía, es 10 veces menos citotóxica que la ONC. La nomenclatura G88R significa que la molécula de RNasa A se alteró sustituyendo el resto de glicina (G) en la posición del aminoácido 88 por un resto de arginina (R).
Los procedimientos y las herramientas para modelar la 10 estructura tridimensional de las proteínas continúan evolucionando. Al analizar la interacción entre dos moléculas, por ejemplo entre RNasa A e IR, sólo está siendo ahora susceptible de solución el problema de definir los sitios de interacción entre las dos moléculas. A medida que 15 se están desarrollando las herramientas de modelación, puede aumentar la sofisticación del análisis de esa interacción.
BREVE SUMARIO DE LA INVENCIÓN
La presente invención proporciona una ribonucleasa 20 diseñada por ingeniería de la familia de la RNasa A que tiene al menos dos cambios de aminoácidos de la secuencia nativa de aminoácidos de la ribonucleasa, siendo el primer cambio una sustitución de aminoácido en la región correspondiente a los restos 85 a 94 de la RNasa A 25 pancreática bovina y siendo el segundo cambio una alteración, sustitución o un cambio de aminoácidos en un sitio seleccionado entre el grupo constituido por aminoácidos que corresponden a los restos 38, 39 y 67 de la RNasa AS pancreárica bovina, una ribonucleasa diseñada por 30 ingeniería que tiene una actividad citotóxica intensificada en comparación con una ribonucleasa correspondiente diseñada por ingeniería que tiene una modificación sólo en
la región correspondiente a los restos de aminoácido 85 a 94.
En particular, la invención proporciona las ribonucleasas bovinas diseñadas por ingeniería ribonucleasa A D38R/R39D/G88R y ribonucleasa A D38R/R39D/N67R/G88R. 5
La invención proporciona también una construcción de ADN que codifica la ribonucleasa diseñada por ingeniería de la invención y un alojante de células tal como un ADN.
La invención proporciona además:
un método in vitro para impartir actividad citotóxica 10 a células, que comprende la etapa de suministrar a las células in vitro una ribonucleasa diseñada por ingeniería de la invención;
una ribonucleasa de la invención diseñada por ingeniería para uso en un método de terapia en un cuerpo 15 humano o animal, en particular para uso en la impartición de actividad citotóxica a células.
Es un objetivo de la presente invención definir una ribonucleasa A diseñada por ingeniería que tenga propiedades citotóxicas mejoradas en comparación con 20 anteriores ribonucleasas diseñadas por ingeniería.
Otros objetivos, ventajas y características de la presente invención serán evidentes considerando la memoria siguiente junto con los dibujos que se acompañan.
25
BREVE DESCRIPCIÓN DE LAS DIFERENTES VISTAS DE LOS DIBUJOS
La Fig. 1 es una representación de la estructura tridimensional de la ribonucleasa A y del inhibidor de ribonucleasa.
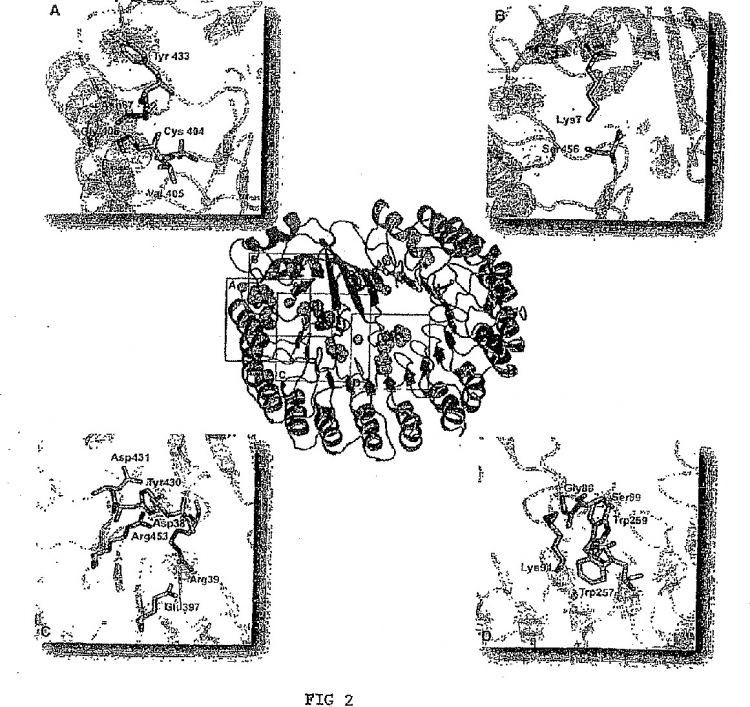
La Fig. 2 es una representación de la interacción 30 entre la estructura tridimensional de la ribonucleasa A y el inhibidor de ribonucleasa, que muestra los sitios
seleccionados como diana para modificaciones de la ribonucleasa A.
La Fig. 3 representa datos gráficos de los ejemplos siguientes que muestran el efecto de las ribonucleasas sobre la proliferación de células K-532. Los puntos de los 5 datos son la media de al menos tres experimentos, realizado cada uno por triplicado. Cada una de las curvas está marcada con la correspondiente variante de RNasa A.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN 10
La presente invención está dirigida a ribonucleasas alteradas de la superfamilia de RNasa A que han sido diseñadas por ingeniería para tener un nuevo nivel de citotoxicidad. Esto se consiguió usando una nueva herramienta de modelado de interacción molecular, el 15 algoritmo de Evaluación Rápida de la Densidad Atómica (FADE). Este algoritmo se usó para modelar las posiciones de contacto molecular entre la RNasa A y el inhibidor de ribonucleasa. Sobre la base de este modelo se diseñaron variantes de la secuencia de aminoácidos de RNasa A con el 20 fin de crear nuevas variantes de RNasa A que, mediante impedimento estérico, son capaces de evadir el IR. Se identifican aquí variantes que son más citotóxicas que las variantes de RNasa A antes conocidas.
El análisis empezó con un estudio de la interacción 25 entre la RNasa A y la moléculas de IR. Hay muchas propiedades de una interfaz de proteína-proteína...
Reivindicaciones:
1. Una ribonucleasa diseñada por ingeniería de la superfamilia RNasa A que tiene al menos dos cambios de aminoácidos de la secuencia de aminoácidos nativa de la ribonucleasa, siendo el primer cambio una sustitución de 5 aminoácido en la región correspondiente a los restos de aminoácidos 85 a 94 de RNasa A pancreática bovina, y siendo el segundo cambio una alteración, sustitución o intercambio de aminoácido en un lugar seleccionado entre el grupo constituido por aminoácidos que corresponden a los restos 10 38, 39 y 67 de RNasa A pancreática bovina, teniendo la ribonucleasa diseñada por ingeniería una actividad citotóxica intensificada en comparación con una correspondiente ribonucleasa diseñada por ingeniería que tiene una modificación sólo en la región que corresponde a 15 restos de los aminoácidos 85 a 94.
2. Una ribonucleasa diseñada por ingeniería según la reivindicación 1, en la que el segundo cambio es un intercambio de arginina en el resto 39 con un ácido aspártico en el resto 38. 20
3. Una ribonucleasa diseñada por ingeniería según la reivindicación 1, en la que el segundo cambio es una sustitución de una asparagina en el resto 67 por una arginina.
4. Una ribonucleasa diseñada por ingeniería según la 25 reivindicación 1, en la que el primer cambio es la sustitución de una glicina en el resto 88 por arginina.
5. La ribonucleasa A pancreática bovina D38R/R39D/G88R diseñada por ingeniería.
6. La ribonucleasa A pancreática bovina D38R/R39D/N67R/ 30 G88R diseñada por ingeniería.
7. Una construcción de ADN que codifica la ribonucleasa de una cualquiera de las reivindicaciones 1 a 6.
8. Una células que aloja la construcción de ADN de la reivindicación 7.
9. Un procedimiento in vitro para impartir actividad citotóxica en células, que comprende la etapa de suministrar a las células in vitro una ribonucleasa 5 diseñada por ingeniería según una cualquiera de las reivindicaciones 1 a 6.
10. Una ribonucleasa diseñada por ingeniería según una cualquiera de las reivindicaciones 1 a 6 para uso en un procedimiento de terapia en un cuerpo humano o animal. 10
11. Una ribonucleasa diseñada por ingeniería según la reivindicación 10 para uso en la impartición de actividad citotóxica a células.
Patentes similares o relacionadas:
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Métodos y composiciones para ingeniería genómica, del 3 de Junio de 2020, de Sangamo Therapeutics, Inc: Una pareja de nucleasas de dedo de zinc (ZFN) que comprende una ZFN izquierda y una ZFN derecha, comprendiendo cada ZFN un dominio de escisión […]
Métodos y composiciones para el tratamiento de enfermedades por almacenamiento lisosomal, del 27 de Mayo de 2020, de Sangamo Therapeutics, Inc: Uno o más transgenes y una o más nucleasas con dedos de zinc (ZFN) para su uso en un método de tratamiento de una enfermedad por almacenamiento lisosomal, el método […]
Métodos y composiciones para escisión dirigida y recombinación, del 20 de Mayo de 2020, de Sangamo Therapeutics, Inc: Un método in vitro para la escisión selectiva de un gen HLA clase I, un gen HLA que codifica una proteína de clase 1 del Complejo de Histocompatibilidad Mayor (MHC) […]
Métodos y composiciones para modular PD1, del 13 de Mayo de 2020, de Sangamo Therapeutics, Inc: Célula aislada que comprende una inserción o una deleción en un gen de PD1 endógeno dentro de, o entre, las secuencias mostradas en SEQ ID NO: 56 y SEQ ID NO: 60 del gen de PD1 […]
Cepas bacterianas que expresan genes de metilasa y sus usos, del 22 de Abril de 2020, de LOMA LINDA UNIVERSITY: Una bacteria aislada para usar en la producción de ADN plasmídico metilado, en donde la bacteria comprende un polinucleótido exógeno que codifica una CpG metilasa […]
Método y composiciones para reducir productos de amplificación no específicos, del 25 de Marzo de 2020, de Paragon Genomics, Inc: Un método para reducir productos de amplificación no específicos de una reacción de extensión de cebadores dependiente de plantilla, comprendiendo el método: […]
Proteínas que tienen actividad nucleasa, proteínas de fusión y usos de estas, del 18 de Marzo de 2020, de HELMHOLTZ ZENTRUM MUNCHEN DEUTSCHES FORSCHUNGSZENTRUM FUR GESUNDHEIT UND UMWELT (GMBH): Una molécula de ácido nucleico que codifica (I) un polipéptido que tiene la actividad de una endonucleasa, que es (a) una molécula de ácido nucleico que […]