USO TERAPÉUTICO DE LPI, UN INHIBIDOR DE LA VÍA DE LAS LECTINAS DE ORIGEN ESTAFILOCÓCICO, EN ENFERMEDADES INFLAMATORIAS.
Péptido o polipéptido codificado por una secuencia de nucleótidos que corresponde a una secuencia seleccionada entre el grupo que consiste en:
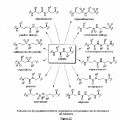
a) una secuencia de nucleótidos que comprende una parte de una de las secuencias representadas en la Figura 2a y 2b e identificada como SEQ ID NO: 2, SEQ ID NO:4, SEQ ID NO:6; b) secuencias de nucleótidos que codifican un péptido o polipéptido que posee la secuencia de aminoácidos representada en la Figura 3 e identificada como SEQ ID NO:3, SEQ ID NO:5 o SEQ ID NO: 7; c) secuencias de nucleótidos que codifican un péptido o polipéptido que posee una parte de la secuencia de aminoácidos representada en la Figura 3 identificada como SEQ ID NO:.3, SEQ ID NO:5 o SEQ ID NO: 7; d) secuencias de nucleótidos que son, al menos, 40% idénticas a una cualquiera de las secuencias de nucleótidos a), b) o c); e) secuencias nucleótidos que se hibridan en condiciones restrictivas con una cualquiera de las secuencias de nucleótidos a), b), c) o d), y f) secuencias complementarios de cualquiera de las secuencias de nucleótidos a), b), c), d) o e), en que dicho péptido o polipéptido posee actividad de LPI (Inhibidor de la Vía de las Lectinas), que evita la activación de la vía de las lectinas de activación del complemento evitando específicamente la escisión de C2 a C2a y C2b dependiente de MASP-2 (Proteasa-2 de Serina Asociada a Lectina que Une Manosa), y dicho péptido o polipéptido es para usar en la profilaxis o el tratamiento de reacciones inflamatorias agudas y crónicas, y dicho péptido es, homólogo, al menos 40%, con la proteína del LPI
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/007606.
Solicitante: UMC UTRECHT HOLDING B.V..
Nacionalidad solicitante: Países Bajos.
Dirección: YALELAAN 40 3584 CM UTRECHT PAISES BAJOS.
Inventor/es: VAN STRIJP, JOHANNES, ANTONIUS, GERARDUS, VAN KESSEL, CORNELIS, PETRUS, MARIA, VAN WAMEL,Willem,Jan,Bastiaan, ROOIJAKKERS,Suzan,Huberdina,Maria.
Fecha de Publicación: .
Fecha Solicitud PCT: 8 de Julio de 2004.
Clasificación Internacional de Patentes:
- C07K14/31 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Staphylococcus (G).
Clasificación PCT:
- A61K38/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- A61K39/085 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Staphylococcus.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- A61P37/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 37/00 Medicamentos para el tratamiento de problemas inmunológicos o alérgicos. › Inmunosupresores, p. ej. medicamentos para el tratamiento del rechazo en injertos.
Clasificación antigua:
- A61K39/085 A61K 39/00 […] › Staphylococcus.
- A61K39/40 A61K 39/00 […] › bacterianos.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- C07K14/31 C07K 14/00 […] › de Staphylococcus (G).
- C12N15/31 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas microbianas, p. ej. enterotoxinas.
- C12N15/63 C12N 15/00 […] › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12N7/01 C12N […] › C12N 7/00 Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00). › Virus, p. ej. Bacteriófagos, modificados por la introducción de material genético externo (vectores C12N 15/00).
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre.
PDF original: ES-2360399_T3.pdf


Fragmento de la descripción:
La presente invención se refiere a un (poli)péptido que posee actividad de Inhibidor de la Vía de las Lectinas (Lectin Pathway Inhibitor) (LPI), para usar en la profilaxis y el tratamiento de reacciones inflamatorias,
El complemento es la serie compleja de más de 20 proteínas séricas que forman parte de nuestro sistema inmunitario innato. El complemento actúa por sí mismo (a través de la lisis de microbios) o en asociación con otros componentes del sistema inmunitario innato (por ejemplo, fagocitosis). Nuestro sistema inmunitario innato está implicado principalmente en la protección del cuerpo contra invasores extraños (por ejemplo, bacterias, virus, hongos, y también células cancerosas).
Las células más importantes del sistema inmunitario innato son las células dendríticas, monocitos/macrófagos y neutrófilos. Junto a esto, nuestro sistema inmunitario innato contiene una gran variedad de factores solubles tales como proteínas de fase aguda, péptidos antimicrobianos, peptidasas, partes de la cascada de la coagulación, y el sistema del complemento. La muerte y eliminación de invasores se realiza principalmente mediante los monocitos y los neutrófilos, por reconocimiento directo de los invasores o con ayuda de anticuerpos específicos y/o del sistema del complemento (opsonización).
Las células del sistema inmunitario innato reaccionan de un modo relativamente agresivo. Dado que ellas constituyen parte de la primera línea de defensa del cuerpo, su tarea más importante es matar y retirar el agente invasor tan rápidamente como sea posible. Esto se lleva a efecto por medio de sustancias muy agresivas (por ejemplo, radicales libres y enzimas) que no solamente son letales para el invasor, sino que también causan daño a las células huésped de los alrededores. Las sustancias procedentes de esta células dañadas y de las células activadas localmente que proceden del propio sistema innato atraen cantidades crecientes de neutrófilos y monocitos, lo que ocasiona inflamaciones locales adicionales.
En la mayor parte de los casos, es innecesaria una reacción inflamatoria agresiva y dañina tal, ocasionada por neutrófilos sobreactivados. En algunos casos esta respuesta inflamatoria es responsable de lesiones graves, a veces letales, e incluye afecciones tales como el Síndrome de Insuficiencia Respiratoria del Adulto (ARDS), daño tisular grave que sigue a acontecimientos trombóticos tales como ataques cardiacos y apoplejía, enfermedades intestinales inflamatorias y artritis reumatoide.
La inflamación disminuirá una vez que todos los invasores hayan sido muertos y retirados, junto con las diversas células que hayan muerto durante el proceso. Después puede comenzar la curación de la herida causada por la respuesta inflamatoria. Aun cuando existe algún solapamiento de función, la tarea principal de los neutrófilos es atacar a los invasores y la tarea principal de los monocitos es retirar los desechos que resultan de este ataque. Además, los neutrófilos tienen otra tarea pacífica, la de ayudar al proceso de curación de las heridas.
Cuando el cuerpo ha sido invadido por bacterias, sustancias de origen microbiano activan el sistema del complemento directamente o por medio de anticuerpos preexistentes. La primera molécula implicada en la activación del complemento mediada por anticuerpos, es la Clq seguida de la activación de Clr y Cls. Una vía paralela no necesita anticuerpos específicos, debido a que reconoce directamente estructuras de la superficie microbiana. La H-ficolina, la Lficolina o la Lectina que une Manosa (MBL), reconocen microbios y mediante la activación de unas enzimas específicas , Proteasas de Serina Asociadas a MBL, (MASP-2), es activado el resto del sistema del complemento.
En ambos casos, la activación prosigue a través de C4 y C2 y es activada la molécula central C3 del sistema del complemento. Esto lleva a más deposición de C3 mediante la vía alternativa (factores B, D, H, I, P). Una vez convertida C3 en C3b, C3bi o, incluso, en C3d, es la opsonina más importante y media en la absorción de microbios por los fagocitos, y, importantemente, activa también estos fagocitos en el proceso. A continuación de esta acción dirigida por los fagocitos, el sistema del complemento puede continuar desde C3 por medio de C5, C6, C7 C8 y C9 hasta la lisis de la célula tumoral, la célula infectada por virus, bacterias gram-negativas o durante acaecimientos inflamatorios no deseados, una de las células saludables de nuestro cuerpo.
Normalmente nuestras células están protegidas del ataque indeseado del complemento por una diversidad de mecanismos (C1INH, C4bp, CR1, MCP, DAF, H, I, P, CD59) pero en casos de alteración o de activación local sumamente alta, puede ocurrir todavía daño directo mediado por el complemento. Además, en el proceso de activación del complemento, la formación de opsoninas y el ataque a la membrana, corren en paralelo con la formación de moléculas pequeñas inflamatorias muy fuertes (C5a, C3a). Estas sustancias activan directamente fagocitos y otras células (por medio de receptores de C5a y C3a) de un modo muy eficaz, dando por resultado daño para los microbios o células sanas. La interacción con diferentes tipos de células da lugar también a la producción de otras quimioquinas (tales como la interleuquina-8, IL-8): sustancias que pueden activar y atraer células desde los vasos sanguíneos (el proceso de migración). Los neutrófilos interaccionan con estas sustancias, debido a que poseen receptores para estas sustancias en el exterior de sus membranas celulares. Una visión de conjunto de los componentes del sistema del complemento se proporciona en la Tabla 1.
**(Ver fórmula)**
Tabla 1
PROTEINAS IMPLICADAS EN LA CASCADA DEL COMPLEMENTO
Unión a complejos Ag:Ab: Clq Reconocimiento directo de estructuras de la superficie microbiana: MBL, H-Ficolina, L-Ficolina, M-Ficolina Activación de enzimas: C1r, C1s, C2b, B, D, MASPI,2,3, Opsoninas de unión a membranas: C4b, C3b Mediadores de inflamación: C5a, C3a, C4a Ataque a la membrana: C5b, C6, C7, C8, C9 Receptores del complemento: CR1, CR2, CR3, CR4, C1qr, M-Ficolina Proteínas reguladoras del complemento: C1INH, C4bp, CR1, MCP, H, I, P, CD59* Adaptado de Janeway and Travers Immunobiology, 1996; Current Biology
Ltd/Garland Publishing Inc.
Los neutrófilos activados pueden emigrar fácilmente desde los vasos sanguíneos. Este hecho es debido a que las quimioquinas y los productos microbianos pueden haber aumentado la permeabilidad de los vasos y estimulado las células endoteliales de las paredes de los vasos para expresar ciertas moléculas de adhesión. Los neutrófilos expresan selectinas e integrinas (por ejemplo, CD11b/CD18) que se unen a estas moléculas de adhesión. Este proceso se denomina cebado (priming). Una vez que el neutrófilo se ha adherido a las células endoteliales, es capaz de emigrar a través de las células, bajo la guía de quimioquinas, hacia el lugar de la infección, donde la concentración de esas sustancias está en su máximo.
Estas sustancias activan también los neutrófilos produciendo una gama de otras moléculas, algunas de las cuales atraen más neutrófilos (y seguidamente monocitos), pero, principalmente, son responsables de la destrucción de las bacterias invasoras. Algunas de estas sustancias, (por ejemplo, radicales libres, enzimas que escinden proteínas (proteasas) y membranas celulares (lipasas), son tan reactivas e inespecíficas que destruyen células procedentes del tejido circundante (y de los propios neutrófilos), ocasionando daño a los tejidos. Este daño es exacerbado por la presencia de fluidos derivados de la sangre, que han traspasado la pared del vaso dañado y que es responsable del hinchamiento que siempre acompaña a la inflamación (denominado edema). La presión acumulada causada por estos fluidos en exceso da como resultado daño y muerte celular adicionales.
El comienzo de la reacción inflamatoria no tiene que tener, per se, origen microbiano. El daño tisular originado, en general, por falta de oxígeno, cambios de pH, desequilibrio salino o lesión físico, puede iniciar las reacciones inflamatorias. En muchos casos el acaecimiento clave es la activación del sistema del complemento. En enfermedades autoinmunitarias, la presencia de auto-anticuerpos da lugar a la activación de la vía clásica de complemento. En casi todos otros casos la activación de complemento ocurre por medio de la vía de las lectinas (véase, Jordan et al., Circulation, 2001, 104(12):1413-8; Collard et al.,... [Seguir leyendo]
Reivindicaciones:
1. Péptido o polipéptido codificado por una secuencia de nucleótidos que corresponde a una secuencia seleccionada entre el grupo que consiste en:
a) una secuencia de nucleótidos que comprende una parte de una de las secuencias representadas en la Figura 2a y 2b e identificada como SEQ ID NO: 2, SEQ ID NO:4, SEQ ID NO:6;
b) secuencias de nucleótidos que codifican un péptido o polipéptido que posee la secuencia de aminoácidos representada en la Figura 3 e identificada como SEQ ID NO:3, SEQ ID NO:5 o SEQ ID NO: 7;
c) secuencias de nucleótidos que codifican un péptido o polipéptido que posee una parte de la secuencia de aminoácidos representada en la Figura 3 identificada como SEQ ID NO:.3, SEQ ID NO:5 o SEQ ID NO: 7;
d) secuencias de nucleótidos que son, al menos, 40% idénticas a una cualquiera de las secuencias de nucleótidos a), b) o c);
e) secuencias nucleótidos que se hibridan en condiciones restrictivas con una cualquiera de las secuencias de nucleótidos a), b), c) o d), y
f) secuencias complementarios de cualquiera de las secuencias de nucleótidos a), b), c), d) o e),
en que dicho péptido o polipéptido posee actividad de LPI (Inhibidor de la Vía de las Lectinas), que evita la activación de la vía de las lectinas de activación del complemento evitando específicamente la escisión de C2 a C2a y C2b dependiente de MASP-2 (Proteasa-2 de Serina Asociada a Lectina que Une Manosa), y dicho péptido o polipéptido es para usar en la profilaxis o el tratamiento de reacciones inflamatorias agudas y crónicas, y dicho péptido es, homólogo, al menos 40%, con la proteína del LPI.
2. Péptido o polipéptido según la reivindicación 1, en que la parte de la secuencia de nucleótidos definida en la reivindicación 1, apartado a), corresponde a los nucleótidos 1 a 490 de la Figura 2a (SEQ ID NO: 2).
3. Péptido o polipéptido según la reivindicación 1, en que la parte de la secuencia de nucleótidos definida en la reivindicación 1 apartado a), corresponde a los nucleótidos 41 a 490 de la Figura 2a (SEQ ID NO: 2).
4. Péptido o polipéptido según la reivindicación 1, en que la parte de la secuencia de nucleótidos definida en la reivindicación 1, apartado a), corresponde a los nucleótidos 125 a 490 de la Figura 2a (SEQ ID NO: 2).
5. Péptido o polipéptido según la reivindicación 1, en que la parte de la secuencia de nucleótidos definida en la reivindicación 1, apartado a), corresponde a los nucleótidos 1 a 490 de lpi-B (SEQ ID NO:4) olpi-C (SEQ ID NO: 6) de la Figura 2b.
6. Péptido o polipéptido según la reivindicación 1, en que la parte de la secuencia de nucleótidos definida en la reivindicación 1, apartado a), corresponde a los nucleótidos 41 a 490 de lpi-B (SEQ ID NO:4) o lpi-C (SEQ ID NO: 6) de la Figura 2b.
7. Péptido o polipéptido según la reivindicación 1, en que la parte de la secuencia de nucleótidos definida en la reivindicación 1, apartado a), corresponde a los nucleótidos 125 a 490 de lpi-B (SEQ ID NO:4) olpi-C (SEQ ID NO: 6) de la Figura 2b.
8. Péptido o polipéptido según las reivindicaciones 1-7, en que la secuencia de nucleótidos definida en la reivindicación 1, apartado d), posee una identidad que es, al menos 50%, idéntica a una cualquiera de las secuencias de nucleótidos a, b o c.
9. Péptido o polipéptido según las reivindicaciones 1-7, en que la secuencia de nucleótidos definida en la reivindicación 1, apartado d), posee una identidad que es, al menos 60%, idéntica a una cualquiera de las secuencias de nucleótidos a, b o c.
10. Péptido o polipéptido según las reivindicaciones 1-7, en que la secuencia de nucleótidos definida en la reivindicación 1, apartado d), posee una identidad que es, al menos 70%, idéntica a una cualquiera de las secuencias de nucleótidos a, b o c.
11. Péptido o polipéptido según las reivindicaciones 1-7, en que la secuencia de nucleótidos definida en la reivindicación 1, apartado d), posee una identidad que es, al menos 75%, idéntica a una cualquiera de las secuencias de nucleótidos a, b o c.
12. Péptido o polipéptido según las reivindicaciones 1-7, en que la secuencia de nucleótidos definida en la reivindicación 1, apartado d), posee una identidad que es, al menos 80%, idéntica a una cualquiera de las secuencias de nucleótidos a, b o c.
**(Ver fórmula)**
13. Péptido o polipéptido según las reivindicaciones 1-7, en que la secuencia de nucleótidos definida en la reivindicación 1, apartado d), posee una identidad que es, al menos 90%, idéntica a una cualquiera de las secuencias de nucleótidos a, b o c.
14. Péptido o polipéptido según las reivindicaciones 1-13, en que las condiciones restrictivas están 5 constituidas por hibridación durante la noche a 42ºC en SSC 5x y lavado a 65ºC en SSC 0,1x..
15. Péptido o polipéptido según las reivindicaciones 1-14, en que una parte de la secuencia de aminoácidos según la reivindicación 1, apartado c), constituye sola o con otras partes de la secuencia de aminoácidos, la región o regiones del péptido o polipéptido que posee actividad de LPI.
16. Uso del péptido o polipéptido según las reivindicaciones 1-15, para fabricar una preparación terapéutica 10 para la profilaxis o el tratamiento de reacciones inflamatorias agudas y crónicas.
17. Una composición terapéutica que comprende un excipiente adecuado y el péptido o polipéptido según las reivindicaciones 1-15, para la profilaxis o el tratamiento de reacciones inflamatorias agudas y crónicas
18. Microorganismo que aloja una molécula de ácido nucleico según las reivindicaciones 1-15, para usar como medicamento para el tratamiento de reacciones inflamatorias agudas y crónicas.
Patentes similares o relacionadas:
Antígenos de coagulasa estafilocócica y métodos para su uso, del 13 de Mayo de 2020, de UNIVERSITY OF CHICAGO: Una composición inmunógena que comprende al menos dos dominios 1-2 de coagulasa estafilocócica diferentes, en donde cada uno de los al menos dos dominios […]
Proteína mutante, del 19 de Febrero de 2020, de Cytiva BioProcess R&D AB: Una proteína de unión a inmunoglobulina que se une a regiones de una molécula de inmunoglobulina distintas de las regiones determinantes de […]
Composiciones y métodos relacionados con variantes de la proteína A (SPA), del 12 de Febrero de 2020, de THE UNIVERSITY OF CHICAGO: Una variante inmunogénica de la proteína A (SpA) que comprende: (a) sustituciones de aminoácidos en un subdominio de unión a VH3 del dominio E, D, A, B o C de la SpA que […]
Variantes de hemolisina alfa con características alteradas, del 1 de Enero de 2020, de Genia Technologies, Inc: Una variante de hemolisina α (α-HL) que comprende una sustitución en una posición correspondiente a la posición 12 o 17 de SEQ ID NO:3, en la que la sustitución […]
Antígenos estafilocócicos mutantes, del 11 de Diciembre de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Un antígeno SpA mutante que comprende una secuencia de aminoácidos que comprende o que consiste en la SEQ ID NO: 49, en que los dipéptidos XX […]
Polipéptidos de unión que tienen un andamio mutado, del 19 de Junio de 2019, de AFFIBODY AB: Polipéptido que comprende una secuencia de aminoácidos seleccionada entre: i) EX2X3X4AX6X7EIX10 X11LPNLX16X17X18QX20 X21AFIX25X26LX28X29X30 PX32QSX35X36LLX39E […]
Nuevos polipéptidos, del 19 de Junio de 2019, de AFFIBODY AB: Dímero de unión a FcRn, que comprende una primera unidad monomérica, una segunda unidad monomérica y un enlazador de aminoácidos, en donde dichas primera y segunda […]
Métodos para aumentar la pureza de proteínas utilizando la cromatografía basada en proteína A, del 1 de Mayo de 2019, de EMD Millipore Corporation: Un método para reducir el nivel de agregados de proteínas en una mezcla de elución que contiene una proteína que contiene Fc, y el método […]