USO DE PÉPTIDOS MIMÉTICOS DEL ÁCIDO POLI-ALFA 2,8-SIÁLICO PARA MODULAR FUNCIONES DE NCAM.
Un péptido para uso como un medicamento para modular crecimiento,
regeneración y plasticidad de células de vertebrados que expresan NCAM, en el que dicho péptido es un mimótopo del ácido poli-(2,8 siálico unido a NCAM que se selecciona entre el grupo que consiste en: los péptidos lineales de hasta 30 aminoácidos que comprenden al menos una de las secuencias SEC ID Nº: 1 a 12, 14 y 15 y los péptidos cíclicos de hasta 30 aminoácidos que comprenden al menos una de las secuencias SEC ID Nº: 16 a 26
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2003/005108.
Solicitante: CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE
Université de la Méditerranée - Aix-Marseille II
Schafer-N
Universitätsklinikum Hamburg-Eppendorf.
Nacionalidad solicitante: Francia.
Dirección: 3, RUE MICHEL-ANGE 75794 PARIS CEDEX 16 FRANCIA.
Inventor/es: ROUGON,Geneviève, TORREGROSSA,Pascal, SCHACHNER,Melitta, SCHAFER NIELSEN,Claus.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Octubre de 2003.
Clasificación Internacional de Patentes:
- C07K1/04C
- C07K7/06A
- C07K7/08A
Clasificación PCT:
- A61K38/10 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 12 a 20 aminoácidos.
- C07K1/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › sobre soportes.
- C07K7/00 C07K […] › Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados.
- C07K7/08 C07K […] › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 12 a 20 aminoácidos.
- C07K7/64 C07K 7/00 […] › Péptidos cíclicos que contienen solamente enlaces peptídicos normales.
- C12N15/09 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Clasificación antigua:
- A61K38/10 A61K 38/00 […] › Péptidos que tienen de 12 a 20 aminoácidos.
- C07K1/04 C07K 1/00 […] › sobre soportes.
- C07K7/00 C07K […] › Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados.
- C07K7/08 C07K 7/00 […] › con 12 a 20 aminoácidos.
- C07K7/64 C07K 7/00 […] › Péptidos cíclicos que contienen solamente enlaces peptídicos normales.
- C12N15/09 C12N 15/00 […] › Tecnología del ADN recombinante.
- C12N5/10 C12N 5/00 […] › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2359810_T3.pdf


Fragmento de la descripción:
La invención se refiere al uso de péptidos miméticos del ácido poli-2,8 siálico (PSA) para modular funciones de NCAM dependientes específicamente de PSA in vitro e in vivo y a su aplicación para el tratamiento de enfermedades neurodegenerativas, lesiones del cerebro y de la médula espinal, problemas de aprendizaje y memoria relacionados con la edad y cáncer.
La capacidad de las células de modificar sus interacciones en la superficie celular con otras células, incluyendo neuronas y células gliales, es un componente crítico del desarrollo, remodelación y reparación del tejido nervioso, así como de la formación tumoral y metástasis. Entre muchas moléculas candidatas que están implicadas potencialmente en un proceso de esto tipo, las isoformas de la molécula de adhesión celular neuronal (NCAM), un miembro de la
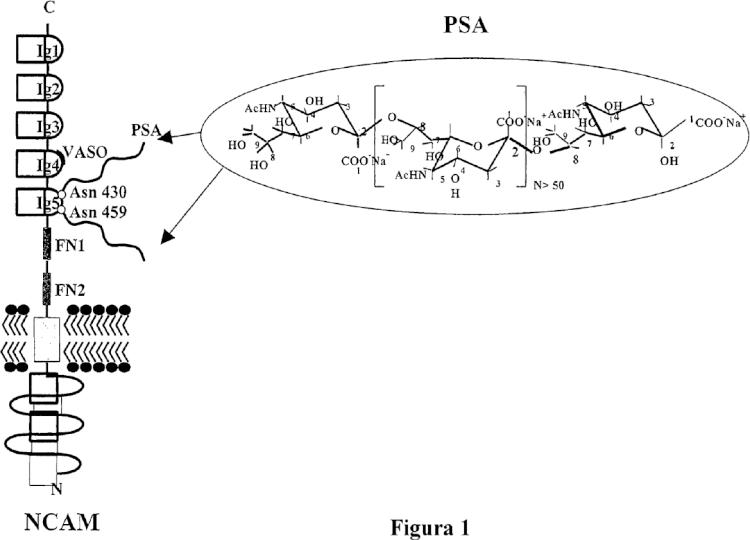
superfamilia de IgG, que portan un polímero de carbohidrato no convencional, ácido poli-2,8-siálico (PSA), son de interés particular.
El PSA es un polímero de restos de ácido N-acetilneuramínico cargados negativamente (ácido siálico) en un enlace alfa 2,8. La cadena de PSA única transportada por NCAM, consiste generalmente en al menos 30 unidades de repetición con la longitud de la cadena variando considerablemente en NCAM aislada a partir de diversas fuentes (von Der Ohe et al, Glicobiology, 2002, 12, 47-63; Rougon et al, Eur. J. Cell. Biol., 1993a, 61, 197-207). Por comparación, el ácido poli
2,8-siálico que se encuentra en la cápsula de bacterias tales como Neisseria meningitidis de Grupo B y E. coli K1 forma polímeros más largos de aproximadamente 200 unidades de repetición.
Los estudios que usan microscopía de NMR indican que PSA tiene una estructura helicoidal en solución que consiste en ocho o más unidades de ácido siálico contiguas (Rougon et al, 1993a, mencionado anteriormente; Yamasaki et al 1991). PSA tiene un volumen hidratado grande y una densidad de carga negativa elevada y, por lo tanto, está en condiciones de atenuar las fuerzas de adhesión y de regular negativamente las interacciones globales de la superficie celular (Rutishauser et al., Science, 1988, 240, 53-57). Todas las isoformas de corte y empalme alternativo conocidas de NCAM se pueden polisializar en el quinto dominio similar a Ig (Rougon et al, 1993a, mencionado anteriormente) y NCAM es la única transportadora identificada claramente de ácido polisiálico en el sistema nervioso (Rougon et al, J. Cell. Biol.,
1986, 103, 2429-2437). Aunque existe un informe que describe la asociación de PSA con la cadena del canal de Na (Zuber et al, J. Biol. Chem., 1992, 267, 9965-9971), la ausencia de inmunorreactividad de PSA en ratones knock-out de NCAM (Cremer et al, Nature, 1994367, 455-457) sugiere que NCAM es la transportadora principal si no la única de PSA en el cerebro de vertebrados.
La unión de PSA a NCAM es un proceso regulado embriológicamente; NCAM con alto contenido en PSA está asociada con los cambios morfogenéticos durante el desarrollo tales como migración celular, sinaptogénesis y crecimiento y ramificación axonal, mientras que en el cerebro adulto dominan las formas poco sialiladas de NCAM (Rougon et al, Polysialic Acid, 1993b, Roth J.R. Rutishauser U. y Troy F.A. (eds.), Birkhauser-Verlag: Basel, 323-333 ; Rutishauser et al., 1998, mencionado anteriormente; Edelman et al, Annu. Rev. Cell. Biol., 1986, 2, 81-116). Sin embargo, PSA-NCAM persiste en las estructuras del cerebro adulto que presentan un alto grado de plasticidad (Rougon et al, 1993a, mencionado anteriormente). Por ejemplo, PSA-NCAM es necesario para dos formas esenciales de plasticidad sináptica inducida por actividad, potenciación a largo plazo (LTP) y depresión a largo plazo (LTD), que se cree que son centrales para el aprendizaje y la memoria así como la formación de patrón dependiente de actividad durante el desarrollo. (Muller et al, Neuron, 1996, 17, 413-422). De hecho, el tejido del hipocampo preparado a partir de ratones mutantes de NCAM mostró una capacidad marcadamente reducida de LTP así de LTD y este defecto se podría mimetizar mediante la destrucción enzimática del resto PSA de NCAM. Estas observaciones indican que PSA en lugar de la proteína NCAM es necesario para la plasticidad. La plasticidad morfológica que ocurre en el sistema hipotálamo-neurohipofisario (Theodosis et al., J. Neurosci., 1999, 19, 10228-10236) también depende de la presencia de PSA ya que la inyección in vivo de endoneuraminidasa la evita.
PSA-NCAM se re-expresa en varias situaciones patológicas tales como regeneración muscular, regeneración axonal y tumores cerebrales (Figarella-Branger et al, Cancer res, 1990, 50, 6364-6370; Dubois et al, Neuromuscul. Disord., 1994, 4, 171-182; Aubert et al, Comp. Neurol. 1998, 399, 1-19; Muller et al, Neuroscience, 1994, 61, 441-445) o enfermedades neurodegenerativas cerebrales (Le Gal La Salle et al., J. Neurosci., 1992, 12, 872-882). Basándose en estas observaciones, PSA-NCAM surgió como un factor permisivo importante para los cambios dinámicos en las interacciones de la superficie celular necesarias para la morfogénesis y la remodelación de tejido (Rougon et al, 1993b, mencionado anteriormente; Figarella-Branger, 1993; Rutishauser, Development, 1992, 99-104).
Muchos tumores con características neurales y endocrinas expresaban PSA-NCAM. Por ejemplo, PSA-NCAM se ha detectado en neuroblastomas y méduloblastomas (Figarella-Branger et al., mencionado anteriormente), carcinoma de células pequeñas del pulmón (Patel et al, Int. J. Cancer, 1989, 44, 573-578) y rabdomiosarcomas y posiblemente está relacionado con el potencial invasivo y metastático de estos tumores (Rougon et al.1993b, mencionado anteriormente).
Recientemente, la inyección de neuraminidasa en un modelo de ratón desnudo para metástasis mostró que la eliminación de PSA en el tumor primario retardaba la metástasis. (Daniel et al., Oncogene, 2001, 20, 997-1004). Por tanto, la molécula de PSA-NCAM y más precisamente el PSA de carbohidrato representa una de las dianas potenciales de enfoques terapéuticos futuros para promover la plasticidad y recuperación funcional después de daño cerebral o para evitar la formación de metástasis.
Por lo tanto, se han desarrollado varias estrategias para modular las funciones de PSA:
manipulaciones genéticas: ratones knock-out para NCAM o polilsialiltransferasa (Cremer et al, mencionado anteriormente): esta estrategia no abre perspectiva para terapia,
digestión enzimática: endoneuraminidasa (Theodosis et al, mencionado anteriormente; Daniel et al, mencionado anteriormente): su potencial terapéutico es más bien limitado debido a su gran tamaño y a la difusión limitada in vivo y a la posibilidad de inducir una respuesta inmune,
anticuerpos monoclonales anti-PSA (Monnier et al, Developmental Biology, 2001, 229, 1-14); su potencial terapéutico es más bien limitado debido a su naturaleza de anticuerpo,
Ácido colomínico, un análogo de PSA aislado a partir de cápsula bacteriana; su potencial terapéutico está más bien limitado debido a su inestabilidad a pH ácido y a la imposibilidad de controlar su composición exacta en función de la pureza y homogeneidad (calibración de la longitud de la cadena de ácido siálico, de un lote a otro),
N-butanoilmanosamina (ManBut), una molécula pequeña capaz de inhibir la biosíntesis de PSA in vitro (Mahal et al, Science, 2001, 294, 380-382); su actividad no se ha demostrado in vivo.
Sin embargo, hasta la fecha estas estrategias que se han usado para descubrir mecanismos de acción o funciones de PSA, no han conducido al descubrimiento de nuevos fármacos capaces de modular las funciones de PSA in vivo. Por lo tanto, existe una necesidad de moléculas nuevas capaces de modular específicamente las funciones de NCAM dependientes de PSA in vivo, que se puedan usar como composiciones farmacéuticas para promover la plasticidad y la recuperación funcional después de daño cerebral o de la médula espinal o para evitar metástasis.
Los péptidos que representan miméticos moleculares de epítopos de carbohidrato a partir de microorganismos incluyendo epítopos específicos de PSA de Neisseria meningitidis de Grupo B se han descrito con miras a desarrollar candidatos de vacuna seguros y eficaces frente a estos microorganismos (Shin et al, Infection and Immunity, 2001, 69, 3335-3342); los péptidos específicos de PSA de Neisseria meningitidis de Grupo B descritos en Shin et al, representan... [Seguir leyendo]
Reivindicaciones:
1. Un péptido para uso como un medicamento para modular crecimiento, regeneración y plasticidad de células de vertebrados que expresan NCAM, en el que dicho péptido es un mimótopo del ácido poli-2,8 siálico unido a NCAM que se selecciona entre el grupo que consiste en: los péptidos lineales de hasta 30 aminoácidos que comprenden al menos
una de las secuencias SEC ID Nº: 1 a 12, 14 y 15 y los péptidos cíclicos de hasta 30 aminoácidos que comprenden al menos una de las secuencias SEC ID Nº: 16 a 26.
2. El péptido cíclico de acuerdo con la reivindicación 1 para uso como un medicamento, en la que la cadena lateral del resto de cisteína en la posición 1 de una de las secuencias SEC ID Nº: 16 a 26 está unido covalentemente al resto de la cadena lateral de la cisteína en la posición 10 u 11 de dicha secuencia.
3. El péptido de acuerdo con la reivindicación 1 o la reivindicación 2 para uso como un medicamento, que está incluido en un complejo que comprende varios péptidos idénticos o diferentes como se define en la reivindicación 1 o en la reivindicación 2, unidos por enlaces covalentes o no covalentes.
4. El péptido de acuerdo con una cualquiera de las reivindicaciones 1 a 3, para uso como un medicamento, que está asociado con una molécula que posibilita que dicho péptido atraviese la barrera hematoencefálica.
5. El péptido de acuerdo con una cualquiera de las reivindicaciones 1 a 4, que es para uso como un medicamento para activar el crecimiento, regeneración y plasticidad de células de vertebrado que expresan NCAM, para la prevención o el tratamiento de una afección patológica seleccionada entre el grupo que consiste en: enfermedades neurodegenerativas, lesiones cerebrales y de médula espinal, problemas de aprendizaje o memoria relacionados con la edad.
6. El péptido de acuerdo con una cualquiera de las reivindicaciones 1 a 4, que es para uso como un medicamento para inhibir el crecimiento, regeneración y plasticidad de células de vertebrado que expresan NCAM, para la prevención o el tratamiento de cáncer.
7. El péptido de acuerdo con la reivindicación 5 para uso como un medicamento, que es un péptido cíclico que comprende SEC ID Nº: 18 o SEC ID Nº: 22.
8. El péptido de acuerdo con la reivindicación 6 para uso como un medicamento, que es un péptido lineal que comprende SEC ID Nº: 1.
Patentes similares o relacionadas:
OLIGOPÉPTIDOS NO PROTEOLIZABLES INHIBIDORES DE LA GLICOPROTEINA GP41 DEL VIH, del 21 de Octubre de 2011, de UNIVERSIDAD DEL PAIS VASCO UNIVERSIDAD DE VALENCIA: Oligopéptidos no proteolizables inhibidores de la glicoproteína 41 del virus del SIDA. La presente invención se refiere a la identificación de oligopéptidos, […]
PÉPTIDOS ESPECÍFICOS PARA LAS METÁSTASIS Y SUS APLICACIONES EN DIAGNÓSTICO Y TERAPÉUTICAS, del 19 de Julio de 2011, de UNIVERSITA' DEGLI STUDI DI TORINO: Un péptido capaz de fijarse selectivamente a células metastásicas, preferiblemente células de metástasis hepáticas humanas, que tiene el motivo de secuencia LRS, una longitud […]
CITOQUINA QUE INDUCE APOPTOSIS, del 29 de Junio de 2011, de IMMUNEX CORPORATION: Un polipéptido TRAIL soluble purificado que contiene una secuencia de aminoácidos que es al menos 80% idéntica a una secuencia seleccionada del grupo […]
ANTICUERPOS ESPECIFICOS DE TGF BETA 1, del 15 de Junio de 2011, de ELI LILLY AND COMPANY: Un anticuerpo o un fragmento de unión antigénica del mismo que neutraliza la proteína TGF-ß1 humana y tiene una K d de menos de 40pM para la TGF-ß1 […]
COMPOSICIÓN COSMÉTICA O FARMACÉUTICA QUE CONTIENE PÉPTIDOS CON LA SECUENCIA ARG-GLY-SER, del 3 de Junio de 2011, de SOCIETE D'EXTRACTION DES PRINCIPES ACTIFS ( VINCIENCE SA): Composición cosmética y/o dermatológica y/o farmacéutica caracterizada porque contiene en un medio aceptable, como principio activo, por lo menos un péptido de fórmula […]
LIGACIÓN QUÍMICA "SEUDO"- NATURAL, del 1 de Junio de 2011, de AMYLIN PHARMACEUTICALS, INC.: Procedimiento para sintetizar un polipéptido deseado de fórmula: aaNH2-Q-aax-aay-W-aaCOOH en la que Q y W indican cada uno la presencia opcional de uno o más restos […]
 POLIPÉPTIDOS Y POLIMÉRICOS PARA LOS RECEPTORES Fc, del 19 de Mayo de 2011, de SUPPREMOL GMBH: Proteína o polipéptido polimérica/o soluble que puede inhibir la interacción de los receptores de leucocitos Fcγ (FcγR) y de inmunoglobulina G (IgG), comprendiendo […]
POLIPÉPTIDOS Y POLIMÉRICOS PARA LOS RECEPTORES Fc, del 19 de Mayo de 2011, de SUPPREMOL GMBH: Proteína o polipéptido polimérica/o soluble que puede inhibir la interacción de los receptores de leucocitos Fcγ (FcγR) y de inmunoglobulina G (IgG), comprendiendo […]
 COMBINACIONES DE PÉPTIDOS PARA VACUNAS CONTRA LA ALERGIA A LOS GATOS, del 1 de Marzo de 2011, de CIRCASSIA LIMITED: Una composición para uso en la prevención o tratamiento de alergia a los gatos en un individuo por tolerización que comprende los polipéptidos: CPAVKRDVDLFLT (SEC […]
COMBINACIONES DE PÉPTIDOS PARA VACUNAS CONTRA LA ALERGIA A LOS GATOS, del 1 de Marzo de 2011, de CIRCASSIA LIMITED: Una composición para uso en la prevención o tratamiento de alergia a los gatos en un individuo por tolerización que comprende los polipéptidos: CPAVKRDVDLFLT (SEC […]