PRODUCTOS INTERMEDIOS DE DIBENZO (B,F) AZEPINA.
Un procedimiento para la preparación de un compuesto de fórmula V **(Ver fórmula)**en la que R2 es alquilo (C1-4) o fenilo,
que comprende el cierre de anillo de un compuesto de fórmula VI **(Ver fórmula)**en la que R2 es como se define anteriormente
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09153375.
Solicitante: NOVARTIS AG.
Nacionalidad solicitante: Suiza.
Dirección: LICHTSTRASSE 35 4056 BASEL SUIZA.
Inventor/es: ZAUGG, WERNER, FUNFSCHILLING, PETER, KAUFMANN,DANIEL, LOHSE,OLIVIER, BEUTLER,ULRICH.
Fecha de Publicación: .
Fecha Solicitud PCT: 7 de Febrero de 2001.
Clasificación Internacional de Patentes:
- C07D223/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 223/00 Compuestos heterocíclicos que contienen ciclos de siete miembros que tienen un átomo nitrógeno como único heteroátomo del ciclo. › Dibenz [b, f] acepinas; Dibenz [b, f] acepinas hidrogenadas.
Clasificación PCT:
- C07C237/30 C07 […] › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 237/00 Amidas de ácidos carboxílicos, estando sustituida la estructura carbonada de la parte ácida por grupos amino. › con el átomo de nitrógeno del grupo carboxamido unido a átomos de hidrógeno o a átomos de carbono acíclicos.
- C07C271/28 C07C […] › C07C 271/00 Derivados del ácido carbámico, es decir, compuestos que contienen uno de los grupos en que el átomo de nitrógeno no forma parte de grupos nitro o nitroso. › a un átomo de carbono de un ciclo aromático de seis miembros no condensado.
- C07D223/22 C07D 223/00 […] › Dibenz [b, f] acepinas; Dibenz [b, f] acepinas hidrogenadas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre.
PDF original: ES-2363490_T3.pdf
Fragmento de la descripción:
La presente invención se refiere a nuevos derivados de dibenzo[b,f]azepina y su preparación. Los compuestos de la invención son útiles como productos intermedios para la preparación de productos farmacéuticos. Más particularmente, la invención proporciona los compuestos de fórmula I
**(Ver fórmula)**
en la que R1 es alquilo (C1-4) y R2 es alquilo (C1-4) o fenilo.
Los compuestos de fórmula I son materiales de partida útiles para el producto farmacéutico oxcarbazepina (Trileptal®) de fórmula IV (véase posteriormente), útil como anticonvulsivo, p. ej. en el tratamiento de la epilepsia. La oxcarbazepina puede prepararse a partir de los compuestos de fórmula I, por ejemplo de acuerdo con el siguiente esquema de reacción:
**(Ver fórmula)**
Las reacciones a, b y c pueden llevarse a cabo de acuerdo con procedimientos conocidos, por ejemplo como los descritos en el Ejemplo, etapas f a h. En un aspecto adicional, la invención proporciona un procedimiento para la producción de los compuestos de fórmula I, por el que un compuesto de fórmula V
**(Ver fórmula)**
La reacción puede efectuarse de modo conocido, p. ej. como se describe en el Ejemplo, etapas d, d' y d".
Los compuestos de fórmula V nunca se han descrito en la bibliografía y también son parte de la presente invención, así como un procedimiento para su producción.
De acuerdo con la invención, los compuestos de fórmula V pueden prepararse mediante el cierre de anillo de un compuesto de fórmula VI
**(Ver fórmula)**
en la que R2 es como se definió anteriormente. El cierre de anillo del compuesto de fórmula VI se lleva a cabo adecuadamente bajo condiciones ácidas, p. ej. como se describe en el Ejemplo, etapa c2. Si el compuesto de fórmula V resultante se prepara para la preparación de un compuesto de fórmula I, preferiblemente no se aísla sino que se hace reaccionar in situ hasta un compuesto de fórmula I, p. ej. como se describe en el Ejemplo, etapa e.
Se ha encontrado sorprendentemente que esta ciclación conduce a compuestos de fórmula V y no a la lactama de 5 15 miembros de fórmula VIII
**(Ver fórmula)**
con segmentación del -COOR2, como sería de esperar de J.W. Schulenberg et ál., J. Amer. Chem. Soc. 82, 2035 (1960) a la vista del carácter atrayente de electrones del grupo -COOR2.
Los compuestos de fórmula VI también son nuevos y parte de la presente invención, así como los procedimientos 20 para su producción.
De acuerdo con la invención, los compuestos de fórmula VI pueden prepararse mediante la reacción del compuesto de fórmula VIII bajo condiciones básicas fuertes con un compuesto de fórmula X-COOR2, siendo R2 como se define anteriormente y siendo X cloro o metoxi. La reacción puede efectuarse de manera convencional, p. ej. como se describe en el Ejemplo, etapa a2. El material de partida de fórmula VIII es conocido.
Además, se divulga un procedimiento mejorado para la producción de los compuestos de fórmula III mediante la carbamoilación de un compuesto de fórmula II. La carbamoilación del compuesto de fórmula II en la que R es metilo se describe en WO 96/21649. De acuerdo con esta divulgación, se usan cianatos metálicos en presencia de ácidos minerales o ácidos carboxílicos relativamente fuertes y un disolvente. Sorprendentemente, se ha encontrado ahora que esta carbamoilación también puede conseguirse bajo condiciones suaves, usando ácido acético. No se requiere la presencia de un ácido fuerte y un disolvente adicional. En vista de la Así, se divulga un procedimiento para la producción de un compuesto de fórmula III mediante la carbamoilación de un compuesto de fórmula II con un cianato metálico, por el que la reacción se efectúa usando ácido acético, en presencia de un exceso sustancial de cianato metálico y en ausencia de un disolvente adicional.
El cianato metálico es preferiblemente cianato sódico o potásico. “Exceso sustancial” de cianato significa al menos 0,2 equivalentes, preferiblemente de 0,2 a 0,5 equivalentes. Tal exceso es una condición esencial para que la reacción tenga lugar con el rendimiento mejorado en comparación con el procedimiento de carbamoilación conocido. La reacción puede efectuarse, por ejemplo, según se describe en el Ejemplo, etapa g.
El siguiente ejemplo ilustra la invención.
Ejemplo
a2) Ácido [2-(metoxicarbonil-fenil-amino)-fenil]-acético
Una mezcla de 1-fenil-1,3-dihidro-indol-2-ona (80 g, 382 mmol), hidróxido sódico (16,06 g, 402 mmol) y tetrahidrofurano (113 ml) se calienta hasta reflujo (67°C) a lo largo de 5 horas. La solución se diluye con otra porción de tetrahidrofurano (169 ml) y se enfría hasta -10°C. Se añade a esta temperatura una solución al 20% de butil-litio en ciclohexano (122,3 g, 382 mmol), seguido por carbonato de dimetilo (51,7 g, 573 mmol). Posteriormente, la solución se agita a -10°C a lo largo de 2 horas. Se añaden ácido clorhídrico concentrado (38 ml) y agua (125 ml) y los disolventes orgánicos se separan por destilación a presión reducida. Después de la adición de tolueno (345 ml) a la suspensión, el pH de la fase acuosa se ajusta hasta 1,5 usando ácido clorhídrico (34 ml). Después de la separación de fases a 75°C, la fase orgánica se lava con otra porción de agua (120 ml), se concentra a presión reducida y se deja cristalizar a 0°C para dar 81,2 g de compuesto del epígrafe puro (75%).
d) Éster metílico de ácido 10-metoxi-dibenzo[b,f]azepin-5-carboxílico
Éster metílico de ácido 10-oxo-10,11-dihidro-dibenzo[b,f]azepin-5-carboxílico en bruto (22,3 g, 0,083 mol, 1 eq.) se disuelve en metanol (112 ml) a 50°C. Se añade una cantidad catalítica de ácido p-toluenosulfónico (0,445 mg), seguido por ortoformiato de trimetilo (11,5 ml, 1,25 eq.). La mezcla se deja reaccionar a lo largo de 5 horas antes de que el metanol se deje separar por destilación. Se añade continuamente metanol reciente para reemplazar el destilado. Cuando se han destilado 100 ml de metanol, la mezcla se deja enfriar hasta 25°C en 1 hora. La suspensión se enfría adicionalmente hasta 3°C en 20 minutos, se agita a esta temperatura a lo largo de 1 hora y se filtra. El sólido se lava con metanol frío y se seca a vacío a lo largo de 15 horas (50°C, 50 mbar). Se obtiene el compuesto del epígrafe puro como un polvo amarillo claro (188,02 g, 80,8% de rendimiento).
c2) Éster metílico de ácido 10-oxo-10,11-dihidro-dibenzo[b,f]azepin-5-carboxílico
Una mezcla de ácido [2-(metoxicarbonil-fenil-amino)-fenil]-acético (16 g, 55,5 mmol) y ácido polifosfórico (29 g, 167 mmol en términos de P2O5) se calienta hasta 100°C durante 4 horas. Se añade agua (41 ml) gota a gota a la mezcla de reacción a 85-100°C con agitación y enfriamiento. A 65°C, se añade tolueno (41 ml) y la mezcla se agita a lo largo de 30 min. Las dos fases se separan y se lavan. Las fases orgánicas se concentran y se dejan cristalizar a 0°C para dar 12 g de compuesto del epígrafe puro (80%).
d') Éster metílico de ácido 10-metoxi-dibenzo[b,f]azepin-5-carboxílico
Una suspensión de éster metílico de ácido 10-oxo-10,11-dihidro-dibenzo[b,f]azepin-5-carboxílico (15 g, 56 mmol) en metanol (75 ml) se calienta hasta 60°C y se añade una cantidad catalítica de ácido p-toluenosulfónico (0,213 g, 1,1 mmol). Después de la adición de ortoformiato de trimetilo (6,25 g, 58,9 mmol), la solución se agita a 60-70°C a lo largo de 4 horas. Durante esta reacción, el producto precipita como cristales blancos. La mezcla se enfría hasta temperatura ambiente, se filtra y se seca para dar 15,5 g de compuesto del epígrafe puro (98%).
d") Éster metílico de ácido 10-etoxi-dibenzo[b,f]azepin-5-carboxílico
Una suspensión de éster metílico de ácido 10-oxo-10,11-dihidro-dibenzo[b,f]azepin-5-carboxílico (15 g, 56 mmol) en etanol (75 ml) se calienta hasta 60°C y se añade una cantidad catalítica de ácido p-toluenosulfónico (0,213 g, 1,1 mmol). Después de la adición de ortoformiato de trietilo (8,73 g, 58,9 mmol), la solución se agita a 60-70°C a lo largo de 4 horas. Durante esta reacción, el producto precipita como cristales blancos. La mezcla se enfría hasta temperatura ambiente, se filtra y se seca para dar 16,0 g de compuesto del epígrafe puro (97%).
Una mezcla de ácido [2-(metoxicarbonil-fenil-amino)-fenil]-acético (16 g, 55,5 mmol) y ácido polifosfórico (29... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para la preparación de un compuesto de fórmula V
**(Ver fórmula)**
en la que R2 es alquilo (C1-4) o fenilo, que comprende el cierre de anillo de un compuesto de fórmula VI
**(Ver fórmula)**
en la que R2 es como se define anteriormente.
2. Un compuesto de fórmula V, como se define en la reivindicación 1.
3. Un compuesto de fórmula I
**(Ver fórmula)**
10 en la que R1 es alquilo (C1-4) y R2 es como se define en la reivindicación 1.
4. Un procedimiento para la preparación de un compuesto de fórmula I como se define en la reivindicación 3, que comprende hacer reaccionar un compuesto de fórmula V como se define en la reivindicación 1 con un compuesto de fórmula R1OH o (R1O)3CH, en la que R1 es alquilo (C1-4).
5. Un compuesto de fórmula VI
en la que R2 es como se define en la reivindicación 1.
6. Un procedimiento para la preparación de un compuesto de fórmula VI como se define en la reivindicación 5, que comprende hacer reaccionar el compuesto de fórmula VIII
**(Ver fórmula)**
**(Ver fórmula)**
bajo condiciones básicas fuertes con un compuesto de fórmula X-COOR2, en la que R2 es como se define en la reivindicación 1 y X es cloro o metoxi.
7. Un procedimiento de acuerdo con la reivindicación 4, que comprende además preparar el compuesto de fórmula IV posterior de acuerdo con el siguiente esquema de reacción:
**(Ver fórmula)**
Patentes similares o relacionadas:
Dihidrodibenzo(b,f)azepinas, substituidas, método para su preparación, su utilización en el tratamiento de diversos trastornos del sistema nervioso central y composiciones farmacéuticas que las contienen, del 28 de Enero de 2019, de BIAL - PORTELA & CA., S.A: SE DESCRIBEN NUEVOS COMPUESTOS DE FORMULA GENERAL I, QUE INCLUYEN TODOS LOS POSIBLES ESTEREOISOMEROS DONDE: R ES HIDROGENO, ALQUILO, AMINOALQUILO, HALOGENALQUILO, […]
Procedimiento para la preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenzo[b,f]azepina-5-carboxamida y ésteres de la misma mediante reducción enantioselectiva de 10,11-dihidro-10-oxo-5H-dibenzo[b,f]azepina-5-carboxamida, del 26 de Octubre de 2018, de Jubilant Life Sciences Limited: Un procedimiento para la preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenzo[b,f]azepina-5- carboxamida (V) o ésteres de la misma en […]
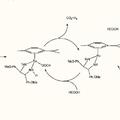 Reducción catalítica asimétrica de oxcarbazepina, del 8 de Marzo de 2016, de BIAL - PORTELA & CA., S.A: Un procedimiento de preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida o (R)- -10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida, […]
Reducción catalítica asimétrica de oxcarbazepina, del 8 de Marzo de 2016, de BIAL - PORTELA & CA., S.A: Un procedimiento de preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida o (R)- -10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida, […]
Método para la preparación de 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida, del 9 de Octubre de 2013, de BIAL - PORTELA & CA., S.A: Un proceso para la preparación de 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida medianteapertura de anillo de 1a,10b-dihidro-6H-dibenz/b,f/oxireno[d]azepin-6-carboxamida […]
REDUCCIÓN CATALÍTICA ASIMÉTRICA DE OXCARBAZEPINA, del 5 de Enero de 2012, de BIAL - PORTELA & CA., S.A: Un procedimiento para preparar (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida o (R)- - 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida […]
UN PROCEDIMIENTO PARA LA PREPARACIÓN DE 10,11-DIHIDRO-10-OXO-5H-DIBENZ[B,F]AZEPINA-5-CARBOXAMIDA, del 11 de Julio de 2011, de BIAL - PORTELA & CA., S.A: Un procedimiento para la preparación de 10,11-dihidro-10-oxo-5H-dibenz[b,f]azepina-5-carboxamida a partir de 10,11-dihidro-10-hidroxi-5H-dibenz[b,f]azepina-5-carboxamida […]
PROCEDIMIENTO DE PREPARACIÓN DE OXCARBAZEPINA, del 7 de Marzo de 2011, de ARCHIMICA S.R.L.: Procedimiento de preparación de oxcarbazepina de fórmula que incluye: a) la reacción de clorocarbonilación del compuesto de fórmula con trifosgeno en […]
PREPARACIÓN DE ESLICARBAZEPINA Y COMPUESTOS RELACIONADOS POR HIDROGENACIÓN ASIMÉTRICA, del 18 de Enero de 2011, de BIAL - PORTELA & CA., S.A: Un procedimiento para preparar un compuesto de formula IA o IB:**Fórmula** en la que R es un grupo alquilo, aminoalquilo, haloalquilo, aralquilo, […]