PROCEDIMIENTO DE PREPARACIÓN DE OXCARBAZEPINA.
Procedimiento de preparación de oxcarbazepina de fórmula que incluye:
a) la reacción de clorocarbonilación del compuesto de fórmula con trifosgeno en presencia de una base, para proporcionar el compuesto de fórmula
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2005/000452.
Solicitante: ARCHIMICA S.R.L.
Nacionalidad solicitante: Italia.
Dirección: VIA VITTOR PISANI 16 20124 MILANO ITALIA.
Inventor/es: DI LERNIA, GIANLUCA, BANFI, ALDO, SERRA, MAURIZIO, BOLLINI,DEBORAH.
Fecha de Publicación: .
Fecha Solicitud PCT: 21 de Febrero de 2005.
Fecha Concesión Europea: 29 de Septiembre de 2010.
Clasificación Internacional de Patentes:
- C07D223/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 223/00 Compuestos heterocíclicos que contienen ciclos de siete miembros que tienen un átomo nitrógeno como único heteroátomo del ciclo. › Dibenz [b, f] acepinas; Dibenz [b, f] acepinas hidrogenadas.
- C07D223/28 C07D 223/00 […] › que tienen un enlace simple entre las posiciones 10 y 11.
Clasificación PCT:
- C07D223/02 C07D 223/00 […] › no condensados con otros ciclos.
- C07D223/28 C07D 223/00 […] › que tienen un enlace simple entre las posiciones 10 y 11.
Clasificación antigua:
- C07D223/02 C07D 223/00 […] › no condensados con otros ciclos.
- C07D223/28 C07D 223/00 […] › que tienen un enlace simple entre las posiciones 10 y 11.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania.
Fragmento de la descripción:
PROCEDIMIENTO DE PREPARACIÓN DE OXCARBAZEPINA
La presente invención se refiere a un procedimiento novedoso de preparación de oxcarbazepina, que es particularmente ventajoso desde un punto de vista industrial, caracterizado por el uso de trifosgeno como agente de clorocarbonilación. 5
TÉCNICA ANTERIOR
La oxcarbazepina (Índice Merck, 1996, nº 7063) de fórmula
es un agente anticonvulsionante conocido, que se describió por primera vez en la patente alemana DE2011087 (Ciba-Geigy). 10
Se han publicado diversos procedimientos en la bibliografía para preparar oxcarbazepina, implicando estos procedimientos básicamente la introducción del grupo funcional carboxamida en el nitrógeno en posición 5 por medio de carbamoilación con cianatos, por ejemplo, en los documentos WO01/56992, EP1302464, IT1318371 y WO96/21649, o, según se ilustra en el Esquema 1 posterior y en los documentos US3642775 y HU63389, mediante clorocarbonilación (a) seguida de amonolisis (b) e hidrólisis final (c): 15
ESQUEMA 1
En concreto, el documento US3642775 describe una reacción de clorocarbonilación (a) realizada con fosgeno, en tolueno a 95°C, con un rendimiento del 77% de compuesto II tras cristalización con etanol, y posterior amonolisis (b) con amoniaco gaseoso en etanol, con un rendimiento del 73% de compuesto IV, 20 también calculado tras cristalización con etanol (rendimiento global del 56% para las dos etapas a y b).
La desprotección del compuesto IV para proporcionar oxcarbazepina (c) se realiza mediante reflujo con ácido clorhídrico 2N, con un rendimiento del 80%, tras cristalización con etanol. El rendimiento global de este procedimiento (II → III → IV → I) es igual a aproximadamente el 45%.
Sin embargo, el uso de fosgeno como agente de clorocarbonilación en esta vía de síntesis representa 25 un importante inconveniente debido a su elevada toxicidad y corrosividad.
Según el resumen del Chemical Abstracts de la patente húngara HU63389, se realiza la misma
secuencia que en el Esquema 1, pero con difosgeno en tolueno a reflujo (a), posterior amonolisis del producto intermedio III, que no se aísla, con amoniaco gaseoso (b) (rendimiento de las etapas a) y b) igual al 58,9%) y, finalmente, hidrólisis del producto intermedio IV con HCl 2M, con un rendimiento igual al 73,5%. En este caso, el rendimiento global del procedimiento, calculado en base a los valores parciales indicados en el resumen, es igual al 43,3%. 5
Ahora, los inventores han descubierto, sorprendentemente, un procedimiento industrialmente aceptable para preparar oxcarbazepina que, sin usar reactivos corrosivos como fosgeno, hace posible obtener el producto deseado aumentando significativamente los rendimientos globales al mismo tiempo.
DESCRIPCIÓN DE LA INVENCIÓN
Un objeto de la presente invención es, por tanto, un procedimiento para preparar oxcarbazepina de 10 fórmula
que incluye:
a) la reacción de clorocarbonilación del compuesto de fórmula
15
con trifosgeno en presencia de una base, para proporcionar el compuesto de fórmula
b) amonolisis del compuesto de fórmula III para proporcionar el compuesto de fórmula
y 20
c) hidrólisis ácida del compuesto de fórmula IV para proporcionar oxcarbazepina I.
Este procedimiento se puede realizar mediante aislamiento y opcional purificación de los productos intermedios individuales de fórmulas II y III o, preferiblemente, minimizando este procedimiento, es decir,
trabajando directamente con el producto de reacción crudo de la etapa anterior parcialmente tratada, como se ilustra en la sección experimental.
El compuesto de partida de fórmula II del procedimiento que es el objeto de la presente invención está disponible comercialmente.
La etapa de clorocarbonilación a) se realiza con trifosgeno en una proporción molar, respecto al 5 compuesto de fórmula II, preferiblemente de entre 0,46:1 y 0,54:1 y, más preferiblemente, de aproximadamente 0,5:1, en presencia de una base, preferiblemente una base orgánica y, más preferiblemente, trietilamina, en una proporción molar respecto al compuesto de fórmula II de entre 1,4:1 y 1,6:1 y, preferiblemente, de aproximadamente 1,5:1.
El disolvente de la reacción generalmente se elige de hidrocarburos aromáticos, preferiblemente 10 tolueno, y la temperatura de reacción es habitualmente de entre 90 y 110°C; preferiblemente, la temperatura al comienzo de la adición gota a gota del trifosgeno es superior a 90°C, para alcanzar posteriormente la temperatura de reflujo del tolueno durante la adición gota a gota.
Preferiblemente, cuando se ha completado la etapa a), el medio de reacción se somete a una mejora mínima y el producto residual crudo, obtenido mediante evaporación, se usa directamente en la etapa posterior 15 b).
Esta etapa de amonolisis generalmente se realiza con amoniaco, preferiblemente amoniaco acuoso, en un disolvente adecuado, preferiblemente un alcohol y, más preferiblemente, metanol.
La posterior etapa de desprotección c) preferiblemente se realiza sobre el concentrado obtenido directamente de la etapa anterior, en condiciones ácidas, preferiblemente con ácido clorhídrico, en medio 20 acuoso a un pH de entre 0 y 2, preferiblemente aproximadamente a un pH de 1, y a una temperatura superior a 50°C, preferiblemente entre 90 y 95°C.
El producto final se purifica preferiblemente mediante cristalización, más preferiblemente mediante cristalización con dimetilacetamida/metanol.
El rendimiento global del presente procedimiento es generalmente de aproximadamente el 80%, es 25 decir, considerablemente mayor que los rendimientos de los procedimientos similares descritos en la técnica.
Los siguientes ejemplos se proporcionan ahora con el fin de ilustrar mejor la presente invención sin, no obstante, limitar la misma.
SECCIÓN EXPERIMENTAL
EJEMPLO 1 30
Preparación de 10-metoxi-5H-dibenzo[b,f]azepina-5-carboxamida (IV)
Se introducen 100 g (0,4479 mol) de 10-metoxi-5H-dibenz[b,f]azepina (II) en un matraz de fondo redondo, se suspenden mediante la adición de 500 ml de tolueno, se añaden 67,2 g (0,6641 mol) de trietilamina y la mezcla se calienta hasta 90°C. Se añade entonces gota a gota una disolución constituida por 66 g de trifosgeno (0,2224 mol) en 150 ml de tolueno durante 40 minutos, mientras se deja que la temperatura 35 aumente hasta 110°C.
Cuando se ha completado la adición gota a gota, la monitorización por HPLC indica que la reacción se ha completado. La mezcla de reacción se enfría hasta 80°C y entonces se añaden 300 ml de agua gota a gota. Tras la adición gota a gota, le temperatura interna de la mezcla es de 60-65°C. Las fases se separan a una temperatura superior a 30-35°C y se elimina la fase acuosa. 40
La fase orgánica se evapora hasta sequedad al vacío a aproximadamente 40°C y, a continuación, se recupera en 125 ml de metanol. Esta disolución se evapora al vacío a 40°C y el residuo se recupera de nuevo en 500 ml de metanol.
La disolución se calienta hasta 50°C, se añaden gota a gota 300 ml de amoniaco acuoso al 28% (2,11 mol) a la disolución homogénea y la mezcla se agita a 50°C durante 1 hora. La monitorización por HPLC 45 después de 1 hora indica que la reacción se ha completado y el disolvente se destila parcialmente a 40°C al vacío, hasta un volumen residual de aproximadamente 400 ml. La disolución a 25°C se vuelve turbia debido a la precipitación de 10-metoxi-5H-dibenzo[b,f]azepina-5-carboxamida (IV) y la suspensión así formada se usa sin purificación adicional en la etapa posterior.
EJEMPLO 2 50
Preparación de oxcarbazepina (I)
Se añaden 600 ml de agua al matraz de fondo redondo que contiene la suspensión de 10-metoxi-5H-dibenzo[b,f]azepina-5-carboxamida (IV) del Ejemplo 1 y se añaden gota a gota aproximadamente 12 g de HCl al 37% hasta pH=1. La suspensión se agita a aproximadamente 95°C durante 4 horas.
La mezcla se enfría hasta 25°C y se añaden gota a gota aproximadamente 14 g de NaOH al 30% 55...
Reivindicaciones:
1. Procedimiento de preparación de oxcarbazepina de fórmula
que incluye:
a) la reacción de clorocarbonilación del compuesto de fórmula 5
con trifosgeno en presencia de una base, para proporcionar el compuesto de fórmula
2. Procedimiento según la Reivindicación 1, que incluye posteriormente: 10
b) amonolisis del compuesto de fórmula III para proporcionar el compuesto de fórmula
y
c) hidrólisis ácida del compuesto de fórmula IV para proporcionar oxcarbazepina I.
3. Procedimiento según la Reivindicación 1 ó 2, en el que dicha reacción de clorocarbonilación a) se 15 realiza con trifosgeno en una proporción molar, respecto al compuesto de fórmula II, de entre 0,46:1 y 0,54:1 y, más preferiblemente, de aproximadamente 0,5:1.
4. Procedimiento según las Reivindicaciones 1 a 3, en el que dicha reacción de clorocarbonilación a) se realiza usando trietilamina como base, en una proporción molar respecto al compuesto de fórmula II de entre 1,4:1 y 1,6:1 y, preferiblemente, de aproximadamente 1,5:1. 20
5. Procedimiento según las Reivindicaciones 1 a 4, en el que dicha reacción de clorocarbonilación a) se
realiza en tolueno y a una temperatura de entre 90 y 110°C.
6. Procedimiento según las Reivindicaciones 2 a 5, en el que la amonolisis b) se realiza con amoniaco acuoso en metanol.
7. Procedimiento según las Reivindicaciones 2 a 6, en el que la desprotección c) se realiza con ácido clorhídrico en medio acuoso a un pH de aproximadamente 1 y a una temperatura de entre 90 y 95°C. 5
Patentes similares o relacionadas:
Dihidrodibenzo(b,f)azepinas, substituidas, método para su preparación, su utilización en el tratamiento de diversos trastornos del sistema nervioso central y composiciones farmacéuticas que las contienen, del 28 de Enero de 2019, de BIAL - PORTELA & CA., S.A: SE DESCRIBEN NUEVOS COMPUESTOS DE FORMULA GENERAL I, QUE INCLUYEN TODOS LOS POSIBLES ESTEREOISOMEROS DONDE: R ES HIDROGENO, ALQUILO, AMINOALQUILO, HALOGENALQUILO, […]
Anticuerpos de unión de manera genérica con múltiples aplicaciones, del 21 de Diciembre de 2015, de RANDOX LABORATORIES LTD.: Inmunógeno de estructura**Fórmula** en la que el accm es un material portador que confiere antigenicidad.
PROCEDIMIENTO PARA LA PREPARACION DE (S)-(+)-10,11-DIHIDRO-10-HIDROXI-5H-DIBENZO(B,F)AZEPIN-5-CARBOXAMIDA, del 29 de Diciembre de 2009, de FARCHEMIA S.R.L.: Procedimiento para la preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenzo[b,f]azepin-5-carboxiamida de fórmula 2 **(Ver fórmula)** caracterizado porque el grupo nitrilo […]
METODO PARA LA RACEMIZACION DE (S)-(+)- Y (R)-(-)-10,11-DIHIDRO-10-HIDROXI-5H-DIBENZ/B ,F/AZEPINA-5-CARBOXAMIDA Y SUS MEZCLAS OPTICAMENTE ENRIQUECIDAS., del 1 de Abril de 2007, de PORTELA & CA., S.A.: 10-cloro-10, 11-dihidro-5H-dibenz/b , f/azepina-5-carboxamida (VII) (Ver fórmula)
5-CIANO-10-HIDROXI-10 ,11-DIHIDRO-5H-DIBENZ(B ,F)AZEPINA, PROCEDIMIENTOS PARA SU PREPARACION Y PARA SU CONVERSION EN 5-CARBAMOIL-10-OXO-10 ,11DIHIDRO-5H-DIBENZ(B ,F)AZEPINA O EN 5-CARBAMOIL-5H-DIBENZ(B ,F)AZEPINA., del 1 de Diciembre de 2004, de FARCHEMIA S.R.L.: El compuesto 5-ciano-10-hidroxi-10 , 11-dihidro-5H-dibenz[b , f]azepina (VI): HO. En una forma de realización preferente, el procedimiento de acuerdo con la presente invención […]
DERIVADOS DE 10,11-DIHIDRO-10-OXO-5H-DIBENZ/B ,F/AZEPIN-5-CARBOXAMIDA., del 16 de Junio de 2001, de PORTELA & CA., S.A.: SE DESCRIBEN COMPUESTOS DE LA FORMULA GENERAL I: ASI COMO UN PROCESO PARA SU PREPARACION QUE CONSISTE EN HACER REACCIONAR UN COMPUESTO DE FORMULA II: CON HIDROXILAMINA […]
REACTIVOS Y PROCEDIMIENTOS DE CUANTIFICACION DE LA IMIPRAMINA O DE LA DESIPRAMINA EN FLUIDOS BIOLOGICOS., del 1 de Enero de 2001, de ABBOTT LABORATORIES: SE PRESENTAN METODOS DE INMUNOENSAYOS Y REACTIVOS PARA LA CUANTIFICACION ESPECIFICA DE IMIPRAMINA O DESIPRAMINA EN UNA MUESTRA DE PRUEBA. LAS MEDICIONES DE […]
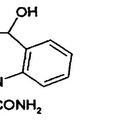 MONOHIDROXICARBAMEZEPINA PARA USO EN LA PREPARACION DE UN MEDICAMENTO PARA EL TRATAMIENTO DEL TRASTORNO AFECTIVO Y DE ATENCION Y DOLOR NEUROPATICO, del 16 de Marzo de 2009, de NOVARTIS AG NOVARTIS PHARMA GMBH: El uso de un compuesto de la Fórmula: (Ver fórmula) para la fabricación de un medicamento para el tratamiento de un trastorno, cuyo trastorno […]
MONOHIDROXICARBAMEZEPINA PARA USO EN LA PREPARACION DE UN MEDICAMENTO PARA EL TRATAMIENTO DEL TRASTORNO AFECTIVO Y DE ATENCION Y DOLOR NEUROPATICO, del 16 de Marzo de 2009, de NOVARTIS AG NOVARTIS PHARMA GMBH: El uso de un compuesto de la Fórmula: (Ver fórmula) para la fabricación de un medicamento para el tratamiento de un trastorno, cuyo trastorno […]