PREPARACIÓN DE ESLICARBAZEPINA Y COMPUESTOS RELACIONADOS POR HIDROGENACIÓN ASIMÉTRICA.
Un procedimiento para preparar un compuesto de formula IA o IB:
**Fórmula** en la que R es un grupo alquilo, aminoalquilo, haloalquilo, aralquilo, cicloalquilo, cicloalquilalquilo, alcoxi, fenilo o fenilo sustituido o piridilo; el termino alquilo significa una cadena de carbono, lineal o ramificada, que contiene de 1 a 18 atomos de carbono; el termino halogeno o halo representa fluor, cloro, bromo o yodo; el termino cicloalquilo representa un grupo aliciclico saturado con 3 a 6 atomos de carbono; el termino arilo representa un grupo fenilo no sustituido o fenilo sustituido con alcoxi, un grupo haloge- no o nitro, comprendiendo el procedimiento la hidrogenacion asimetrica de un compuesto de formula II: **Fórmula** en la que R tiene los mismos significados que antes, usando un catalizador quiral y una fuente de hidrogeno
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/PT2007/000017.
Solicitante: BIAL - PORTELA & CA., S.A.
Nacionalidad solicitante: Reino Unido.
Dirección: A.A. THORNTON & CO. 235 HIGH HOLBORN GB-LONDON WC1V 7LE PORTUGAL.
Inventor/es: YU, BING, LI,WENGE, LEARMONTH,DAVID.
Fecha de Publicación: .
Fecha Solicitud PCT: 11 de Abril de 2007.
Fecha Concesión Europea: 25 de Agosto de 2010.
Clasificación Internacional de Patentes:
- C07D223/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 223/00 Compuestos heterocíclicos que contienen ciclos de siete miembros que tienen un átomo nitrógeno como único heteroátomo del ciclo. › Dibenz [b, f] acepinas; Dibenz [b, f] acepinas hidrogenadas.
Clasificación PCT:
- C07D223/22 C07D 223/00 […] › Dibenz [b, f] acepinas; Dibenz [b, f] acepinas hidrogenadas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
Esta invención se refiere a la síntesis de derivados enantiómeros de dibenz/b,f/azepina. Más en particular, la presente invención se refiere a la hidrogenación asimétrica de sustratos enólicos en la síntesis de derivados enantiómeros de dibenz/b,f/azepina, en particular, a un procedimiento para la preparación de acetato de eslicarbazepina ((S)-(-)-10-acetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida) y acetato de R-(+)-licarbazepina ((R)-(+)-10acetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5-carboxamida) y sus derivados, por hidrogenación asimétrica del correspondiente acetato enólico o del correspondiente derivado éster enólico.
En los últimos años, ha habido un cambio significativo en la forma en la que se consideran los compuestos quirales dentro de la industria farmacéutica. En el pasado, muchas moléculas que tienen centros asimétricos fueron lanzadas al mercado de los fármacos en forma de mezclas racémicas. Los problemas subsiguientes en cuanto a la seguridad y/o la eficacia de tales fármacos racémicos han persuadido a la industria de la necesidad de investigar y desarrollar fármacos estereoisómeros únicos. Estos problemas estaban basados en el concepto de que podría considerarse que los fármacos racémicos son un 50% impuros, dado que un isómero de una mezcla racémica dada es frecuentemente farmacológicamente inactivo o es significativamente menos activo que el otro isómero; en realidad, un isómero puede ejercer una acción diferente o dar origen a efectos secundarios no deseados. Los compuestos isómeros pueden experimentar distintos procesos metabólicos que complican más las cuestiones farmacocinéticas. En consecuencia, los organismos reguladores de los fármacos se han ido haciendo cada vez más precavidos y con frecuencia piden una información concisa acerca de las propiedades y el comportamiento de isómeros individuales.
Un ejemplo particularmente interesante en relación con esto es el caso de la oxcarbazepina (OXC), el análogo 10ceto de la carbamazepina (CBZ).
**(Ver fórmula)**
Estos dos compuestos son estructuralmente muy similares y actualmente se usan en el tratamiento de la epilepsia. La oxcarbazepina fue diseñada para evitar la transformación metabólica oxidativa de la CBZ y se reivindica como fármaco mejor tolerado (Grant, S. M. et al., Drugs, 43, 873 -888 (1992)). Sin embargo, la oxcarbazepina experimenta un metabolismo rápido y completo in vivo para dar el derivado racémico 10-hidroxi de la oxcarbazepina, llamado "MHD" (véase (±)-MHD, Schutz, H. et al., Xenobiotica, 16(8), 769 -778 (1986)) y por consiguiente representa un fármaco aparentemente quiral que experimenta una transformación metabólica para dar una mezcla de dos enantiómeros farmacológicamente activos.
La síntesis y las propiedades anticonvulsivas mejora-das de la (S)-(-)-10-acetoxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida (acetato de eslicarbazepina), y la (R)-(+)-10-acetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida (acetato de R-(+)-licarbazepina), ambos fármacos de isómero único específicamente diseñados para evitar tal formación de mezclas racémicas de metabolitos activos, han sido ya descritas (Benes, J. et al., patente de EE.UU. nº 5.753.646 y Benes, J. et al., J. Med. Chem., 42, 2582 2587 (1999)). La etapa clave de la síntesis de los compuestos acetato de eslicarbazepina y acetato de R-(+)licarbazepina implica la resolución de racémicos 10,11dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida ((+)-MHD) en sus estereoisómeros separados, ópticamente puros, (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida ((S)-(+)-MHD), y (R)-(-)-10,11-dihidro-10hidroxi-5H-dibenz/b,f/azepina-5-carboxamida ((R)-(-)-MHD), que son los principales productos intermedios.
Ambos estereoisómeros de MHD son compuestos conocidos y se usan comúnmente como patrones en estudios del metabolismo de la oxcarbazepina. Además, la MHD es un bloqueante del canal del sodio, y tiene una potencial eficacia en el tratamiento de episodios maníacos agudos de los trastornos bipolares I
La resolución del alcohol racémico, (+)-MHD, ha sido descrita con anterioridad en la literatura química (Benes,
J. et al., J. Med. Chem., 42, 2582 -2587 (1999) y Volosov,
A. et al., Epilepsia, 41(9), 1107 -1111 (2000)). Estos métodos implican la formación de derivados diaestereoisómeros de éster mentoxiacetato de (±)-MHD; aprovechando las diferentes solubilidades de estos ésteres diaestereoisómeros, es posible la separación por cristalización fraccionada y la subsiguiente hidrólisis proporciona los estereoisómeros individualmente puros, (S)-(+)-MHD y (R)-(-)-MHD. Sin embargo, este método fue utilizado para la preparación de tan solo cantidades más bien pequeñas de cada estereoisómero y lleva ciertos inconvenientes inherentes que impiden su uso para la preparación de cantidades a escala piloto, y a continuación para la producción industrial. Los agentes de resolución ópticamente puros necesarios, ácido (+) y (-)mentoxiacético, son extraordinariamente caros y no son fácilmente disponibles en cantidades suficientemente grandes a partir de fuentes comerciales. Podría considerarse su preparación a partir de (+) o (-)-mentol ópticamente puro, más barato y fácilmente disponible, pero esta preparación es engorrosa, lenta y potencialmente peligrosa. Además, estos ácidos mentoxiacéticos requieren “activación” con el fin de que reaccionen con (±)-MHD y formen el producto intermedio clave de ésteres mentoxiacetato diaestereoisómeros. Esta activación se consigue normalmente a través de la conversión de los ácidos libres en los cloruros de ácido (estos cloruros de ácido son de nuevo productos muy caros a partir de fuentes comerciales), una etapa de síntesis extra que requiere el uso de reactivos de halogenación desagradables tales como, por ejemplo, cloruro de tionilo o cloruro
de oxalilo. Alternativamente, esta reacción puede realizarse usando un reactivo de acoplamiento tal como, por ejemplo, diciclohexilcarbodiimida. Este reactivo es también caro; adicionalmente, es difícil de manipular debido a su bajo punto de fusión y está señalado como un poderoso irritante de la piel, con el riesgo que supone para los operarios. Con frecuencia se encuentran dificultades para eliminar completamente el subproducto diciclohexilurea del producto deseado. Otra limitación más, y muy seria, de este método es el relativamente bajo rendimiento que se obtiene del éster mentoxiacetato ópticamente puro que se aísla después de la cristalización, en rendimientos que habitualmente no son más que ligeramente mejores que el 20% (siendo el máximo rendimiento el 50% para cada isómero).
El documento WO02/092572 describe un procedimiento para la separación de los estereoisómeros de (S)-(+)-MHD y (R)-(-)-MHD de la mezcla racémica por medio de un procedimiento que implica el uso de un anhídrido de ácido tartárico apropiado, para resolver los estereoisómeros. En particular, puede usarse el anhídrido de ácido tartárico (2R,3R)-di-O,O'-sustituido, para precipitar el precursor diaestereoisómero de (S)-(+)-MHD, y puede usarse el anhídrido de ácido tartárico (2S,3S)-di-O,O'-sustituido para precipitar el precursor diaestereoisómero de (R)-(-)-MHD. El acetato de eslicarbazepina y el acetato de R-(+)licarbazepina pueden obtenerse a partir de las (S)-(+)-MHD y (R)-(-)-MHD resueltas mediante acilación.
Los derivados dibenz/b,f/azepina de interés particular en la presente invención son los compuestos que tienen la fórmula química siguiente:
**(Ver fórmula)**
en la que R es un grupo alquilo, aminoalquilo, haloalquilo, aralquilo, cicloalquilo, cicloalquilalquilo, alcoxi, fenilo
o fenilo sustituido o piridilo; el término alquilo significa una cadena de carbono, lineal o ramificada, que contiene 5 de 1 a 18 átomos de carbono; el término halógeno o halo representa flúor, cloro, bromo o yodo; el término cicloalquilo representa un grupo alicíclico saturado con 3 a 6 átomos de carbono; el término arilo representa un grupo fenilo no sustituido o fenilo sustituido con alcoxi, un grupo halógeno o nitro. Los compuestos de fórmula IA y IB se describen en la patente de EE.UU. nº 5.753.646.
Es un objeto de la presente invención proporcionar un procedimiento mejorado para la preparación de acetato de eslicarbazepina y acetato de R-(+)-licarbazepina, y procedimientos mejorados para la preparación de derivados di-benz/b,f/azepina de fórmula IA y IB, en general.
De acuerdo con un primer aspecto de la presente...
Reivindicaciones:
1ª. Un procedimiento para preparar un compuesto de fórmula IA o IB:
**(Ver fórmula)**
en la que R es un grupo alquilo, aminoalquilo, haloalquilo, aralquilo, cicloalquilo, cicloalquilalquilo, alcoxi, fenilo
o fenilo sustituido o piridilo; el término alquilo significa una cadena de carbono, lineal o ramificada, que contiene 10 de 1 a 18 átomos de carbono; el término halógeno o halo representa flúor, cloro, bromo o yodo; el término cicloalquilo representa un grupo alicíclico saturado con 3 a 6 átomos de carbono; el término arilo representa un grupo fenilo no sustituido o fenilo sustituido con alcoxi, un grupo halógeno o nitro, comprendiendo el procedimiento la hidrogenación asimétrica de un compuesto de fórmula II:
**(Ver fórmula)**
en la que R tiene los mismos significados que antes, usando un catalizador quiral y una fuente de hidrógeno. 20 2ª. Un procedimiento según la reivindicación 1ª, en el que R es alquilo C1 a C3.
3ª. Un procedimiento según la reivindicación 2ª, en 25 el que R es metilo.
4ª. Un procedimiento según la reivindicación 1ª, en el que el compuesto de fórmula IA o IB es el enantiómero S ó R, respectivamente, de:
(1) 10-acetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5-carboxamida
(2) 10-benzoiloxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(3) 10-(4-metoxibenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(4) 10-(3-metoxibenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(5) 10-(2-metoxibenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(6) 10-(4-nitrobenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(7) 10-(3-nitrobenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(8) 10-(2-nitrobenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(9) 10-(4-clorobenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(10) 10-(3-clorobenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(11) 10-(2-acetoxibenzoiloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(12) 10-propioniloxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(13) 10-butiriloxi-10,1-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(14) 10-pivaloiloxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(15) 10-[(2-propil)pentanoiloxi]-10,11-dihidro-5H-dibenz /b,f/azepina-5-carboxamida
(16) 10-[(2-etil)hexanoiloxi]-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(17) 10-esteariloxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(18) 10-ciclopentanoiloxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(19) 10-ciclohexanoiloxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(20) 10-fenilacetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(21) 10-(4-metoxifenil)acetoxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(22) 10-(3-metoxifenil)acetoxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(23) 10-(4-nitrofenil)acetoxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(24) 10-(3-nitrofenil)acetoxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(25) 10-nicotinoiloxi-10,11-dihidro-5H-dibenz/b,f/azepina5-carboxamida
(26) 10-isonicotinoiloxi-10,11-dihidro-5H-dibenz/b,f/azepina-5-carboxamida
(27) 10-cloroacetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(28) 10-bromoacetoxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(29) 10-formiloxi-10,11-dihidro-5H-dibenz/b,f/azepina-5carboxamida
(30) 10-etoxicarboniloxi-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida
(31) 10-(2-cloropropioniloxi)-10,11-dihidro-5H-dibenz/b,f/ azepina-5-carboxamida.
5ª. Un procedimiento según cualquiera de las reivindicaciones precedentes, en el que el catalizador quiral es un complejo de rodio.
6ª. Un procedimiento según la reivindicación 5ª, en el que el catalizador quiral se elige entre complejos de
Rh(I) que tienen ligandos quirales con las estructuras siguientes:
**(Ver fórmula)**
y sus estereoisómeros, en donde R se elige entre alquilo, 5 arilo, alquilo sustituido, arilo sustituido, hetereoarilo, ferrocenilo, alcoxi y ariloxi.
7ª. Un procedimiento según la reivindicación 6ª, en el que R se elige entre CH3, Et, i-Pr, t-Bu, 1-adamantilo, 10 Et3C, ciclo-C5H9, ciclo-C6H11, fenilo, p-tolilo, 3,5-dimetil
fenilo, 3,5-di-t-butilfenilo, orto-anisilo y naftilo.
8ª. Un procedimiento según la reivindicación 7ª, en el que R es t-Bu. 15
9ª. Un procedimiento según cualquiera de las reivindicaciones precedentes, en el que el catalizador quiral se elige entre un estereoisómero de [Rh(NBD)(DuanPhos)]BF4, [Rh(COD)(DuanPhos)]BF4, [Rh(NBD)(TangPhos)]BF4 y [Rh(COD)(TangPhos)]BF4, en donde COD es º-1,5-ciclooctadieno, NBD es norbornadieno, y los estereoisómeros ScRp-DuanPhos y RRSS-TangPhos tienen la estructura química siguiente:
Patentes similares o relacionadas:
Dihidrodibenzo(b,f)azepinas, substituidas, método para su preparación, su utilización en el tratamiento de diversos trastornos del sistema nervioso central y composiciones farmacéuticas que las contienen, del 28 de Enero de 2019, de BIAL - PORTELA & CA., S.A: SE DESCRIBEN NUEVOS COMPUESTOS DE FORMULA GENERAL I, QUE INCLUYEN TODOS LOS POSIBLES ESTEREOISOMEROS DONDE: R ES HIDROGENO, ALQUILO, AMINOALQUILO, HALOGENALQUILO, […]
Procedimiento para la preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenzo[b,f]azepina-5-carboxamida y ésteres de la misma mediante reducción enantioselectiva de 10,11-dihidro-10-oxo-5H-dibenzo[b,f]azepina-5-carboxamida, del 26 de Octubre de 2018, de Jubilant Life Sciences Limited: Un procedimiento para la preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenzo[b,f]azepina-5- carboxamida (V) o ésteres de la misma en […]
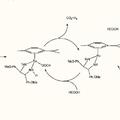 Reducción catalítica asimétrica de oxcarbazepina, del 8 de Marzo de 2016, de BIAL - PORTELA & CA., S.A: Un procedimiento de preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida o (R)- -10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida, […]
Reducción catalítica asimétrica de oxcarbazepina, del 8 de Marzo de 2016, de BIAL - PORTELA & CA., S.A: Un procedimiento de preparación de (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida o (R)- -10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida, […]
Método para la preparación de 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida, del 9 de Octubre de 2013, de BIAL - PORTELA & CA., S.A: Un proceso para la preparación de 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepin-5-carboxamida medianteapertura de anillo de 1a,10b-dihidro-6H-dibenz/b,f/oxireno[d]azepin-6-carboxamida […]
REDUCCIÓN CATALÍTICA ASIMÉTRICA DE OXCARBAZEPINA, del 5 de Enero de 2012, de BIAL - PORTELA & CA., S.A: Un procedimiento para preparar (S)-(+)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida o (R)- - 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida […]
PRODUCTOS INTERMEDIOS DE DIBENZO (B,F) AZEPINA, del 5 de Agosto de 2011, de NOVARTIS AG: Un procedimiento para la preparación de un compuesto de fórmula V **(Ver fórmula)**en la que R2 es alquilo (C1-4) o fenilo, que comprende el cierre de anillo de […]
UN PROCEDIMIENTO PARA LA PREPARACIÓN DE 10,11-DIHIDRO-10-OXO-5H-DIBENZ[B,F]AZEPINA-5-CARBOXAMIDA, del 11 de Julio de 2011, de BIAL - PORTELA & CA., S.A: Un procedimiento para la preparación de 10,11-dihidro-10-oxo-5H-dibenz[b,f]azepina-5-carboxamida a partir de 10,11-dihidro-10-hidroxi-5H-dibenz[b,f]azepina-5-carboxamida […]
PROCEDIMIENTO DE PREPARACIÓN DE OXCARBAZEPINA, del 7 de Marzo de 2011, de ARCHIMICA S.R.L.: Procedimiento de preparación de oxcarbazepina de fórmula que incluye: a) la reacción de clorocarbonilación del compuesto de fórmula con trifosgeno en […]