GLICOSILACIÓN DE TIPO MAMÍFERO EN PLANTAS.
Una planta que comprende una proteína funcional que proporciona la biosíntesis de N-glucanos,
en donde la proteína es una &946;-1,4-galactosiltransferasa de mamífero; y una segunda proteína de mamífero en donde dicha segunda proteína comprende un glucano galactosilado unido por N; y en donde la planta comprende adicionalmente: 5 (a) una sialil-transferasa; o (b) una glucuronil-transferasa
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E06077065.
Solicitante: STICHTING DIENST LANDBOUWKUNDIG ONDERZOEK.
Nacionalidad solicitante: Países Bajos.
Dirección: COSTERWEG 50 6701 BH WAGENINGEN PAISES BAJOS.
Inventor/es: BOSCH, HENDRIK, JAN, BAKKER,HENDRIKUS,ANTONIUS,CORNELIS.
Fecha de Publicación: .
Fecha Solicitud PCT: 26 de Octubre de 2000.
Fecha Concesión Europea: 18 de Agosto de 2010.
Clasificación Internacional de Patentes:
- C12N15/82C4D
- C12N9/10D1A
Clasificación PCT:
- A01H5/00 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01H NOVEDADES VEGETALES O PROCEDIMIENTOS PARA SU OBTENCION; REPRODUCCION DE PLANTAS POR TECNICAS DE CULTIVO DE TEJIDOS. › Angiospermas,es decir, plantas con flores, caracterizadas por sus partes vegetales; Angiospermas caracterizadas de forma distinta que por su taxonomía botánica.
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
- C12N15/82 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para células vegetales.
- C12N9/10 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Transferasas (2.) (ribonucleasas C12N 9/22).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
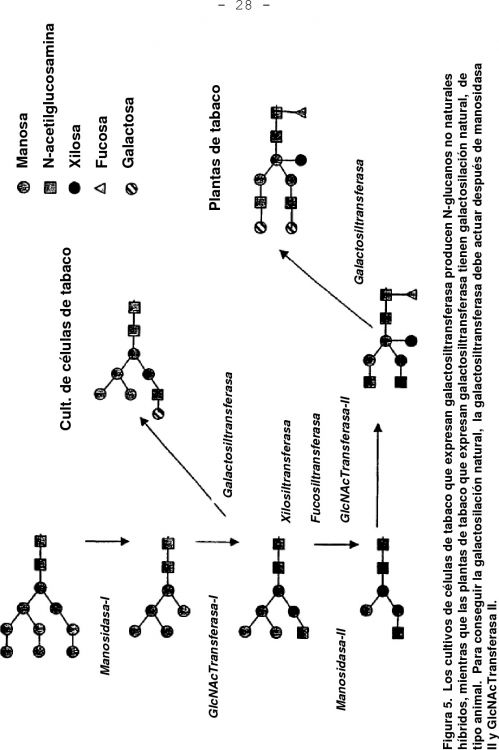
Fragmento de la descripción:
La invención se refiere al campo del procesamiento de glicoproteínas en plantas transgénicas utilizadas como factorías eficientes en costes y exentas de contaminación para 5 la producción de sustancias proteínicas útiles tales como proteínas biofarmacéuticas re-combinantes o composiciones (farmacéuticas) que comprenden éstas.
La creación de proteínas recombinantes como v.g. medicamentos o composiciones farmacéuticas por agricultura fármaco-molecular constituye uno de los atractivos principales de las plantas transgénicas; es también el dominio en el que su utilización está mejor acep-10 tada por la opinión pública. Además del rendimiento y el coste favorable que pueden espe-rarse de la producción en campo de proteínas recombinantes, las plantas transgénicas presentan ciertas ventajas sobre otros sistemas de producción, tales como bacterias, leva-duras, y células animales. De hecho, las mismas están desprovistas de virus que podrían ser peligrosos para los humanos, y pueden acumular las proteínas de interés en sus "órga-15 nos de almacenamiento" tales como semillas o tubérculos. Esto facilita su manipulación, su transporte y su almacenamiento a la temperatura ambiente, al tiempo que proporciona la posibilidad de extracción subsiguiente de acuerdo con las necesidades. Además, la planta transgénica, o algunas de sus partes, pueden utilizarse como vector de medicamentos o de vacunas. En 1996, el equipo de Charles Arntzen (Boyce Thompson Institute for Plant Rese-20 arch, Cornell University, Nueva York) demostró la producción de una vacuna recombinante contra la enterotoxina termolábil de Escherichia coli por la patata. Su eficacia ha sido de-mostrada en ratones y por pruebas clínicas realizadas en individuos voluntarios que han consumido 50 a 100 gramos de patatas transgénicas crudas durante un periodo de 6 me-ses. Otro equipo, en Loma Linda, de California, ha testado con éxito en ratones una vacuna 25 contra el cólera formada en la patata.
La vacunación tradicional contra los gérmenes responsables de enteropatías está considerada como "demasiado costosa" para ser implementada generalmente en los países en desarrollo. Sin embargo, la producción de vacunas orales por ejemplo no ya en la patata sino en el plátano podría, con un coste muy bajo, hacer posible la implementación general 30 de la vacunación contra las diarreas de origen bacteriano, que causan la muerte de 3 millo-nes de niños cada año. En los países desarrollados, puede imaginarse que los niños prefie-ren ciertamente una vacuna de banana o de fresa a la aguja del doctor. Más generalmente, la agricultura molecular podría lograr que los países en desarrollo produjeran, con un coste bajo, cantidades sustanciales de proteínas terapéuticas utilizando las capacidades de su 35 agricultura, sin que sea necesario invertir en factorías farmacéuticas.
Aunque las ventajas de las plantas con factorías de sustancias proteínicas se expli-can en su mayoría a la luz de los productos biofarmacéuticos, las plantas son útiles también
para producción de otras proteínas, v.g. enzimas industriales y análogas, debido a su capa-cidad glicosilación, que conduce v.g. a una mayor estabilidad. Hoy en día, la utilización de plantas para la producción de proteínas o glicoproteínas para uso terapéutico ha avanzado mucho más allá del dominio de la ciencia-ficción dado que soja, tabaco, patata, arroz o col-za son objeto de investigaciones para la producción de vacunas, proteínas o péptidos de 5 mamíferos tales como: anticuerpos monoclonales, antígenos de vacuna, enzimas tales co-mo la lipasa gástrica canina, citoquinas tales como el factor de crecimiento epidérmico, in-terleuquinas 2 y 4, eritropoyetina, encefalinas, interferón y albúmina sérica, en su mayor parte de origen humano Algunas de estas proteínas han demostrado ya su eficacia en indi-viduos humanos voluntarios; sin embargo, su inmunogenicidad potencial y su posible carác-10 ter alergénico restringen todavía su desarrollo.
Varias proteínas heterólogas han sido producidas con éxito en plantas. Entre estas proteínas se encuentran anticuerpos monoclonales, hormonas, antígenos de vacunas, en-zimas y proteínas de la sangre (Dieryck et al., 1997; Florack et al., 1995; Ma et al., 1995; Matsumoto et al., 1163; Saito et al., 1991; Thanavala et al. 1995). Una limitación importante 15 de las plantas, compartida con otros sistemas de expresión heteróloga como bacterias, le-vaduras y células de insecto, es su diferente perfil de glicosilación comparado con el de los mamíferos. En contraste con las bacterias, que carecen de glucanos unidos por N, y la le-vadura, que tiene solamente glucanos ricos en manosa, las plantas son capaces de producir proteínas con glucanos complejos unidos por N. Las glicoproteínas de plantas tienen gluca-20 nos complejos unidos por N que contienen una fucosa de núcleo enlazada en α1,3 y resi-duos xilosa enlazados en β1,2 que no se encuentran en los mamíferos (Lerouge et al., 1998) (Figura 1). El núcleo de los N-glucanos de las plantas puede, como en el caso de los mamíferos, estar sustituido por 2 residuos GlcNAc1, que son transferidos por las N-acetilglucosaminiltransferasas I y II (Schachter, 1991) aunque su aspecto varía (Rayon et 25 al., 1999). Los N-glucanos de algunas glicoproteínas de plantas contienen adicionalmente un epítope LewisA (Fucα1,4(Galβ1,3)GlcNAc) (Fitchette Laine et al., 1997); Melo et al., 1997). Sin embargo, las glicoproteínas de plantas carecen de los N-glucanos complejos que contienen galactosa (NeuAcα2,6Galβ1,4) característicos encontrados en los mamíferos, no encontrándose nunca tampoco una fucosa de núcleo enlazada en α1,6 (Figura 1); (Schach-30 ter, 1991). Un anticuerpo monoclonal de ratón producido en plantas de tabaco (Ma et al., 1995) tiene una N-glicosilación típica de planta. 40% de glucanos ricos en manosa y 60% de glucanos complejos que contienen xilosa, fucosa y 0, 1 ó 2 residuos terminales GlcNAc (Cabanes Macheteau et al., 1999).
En resumen, los análisis de glicoproteínas de las plantas han indicado que varios 35 pasos en los caminos de glicosilación de plantas y mamíferos son muy similares, si no idén-ticos. Existen también, sin embargo, diferencias claras, particularmente en la síntesis de glucanos complejos. Los glucanos complejos de plantas son generalmente mucho más pe-
queños y contienen residuos β-1,2-xilosa o α-1,3-fucosa unidos al núcleo Man3 (GlcNAc) 2. Se sabe que tales residuos en la glicoproteína son altamente inmunógenos. Esto causará problemas para ciertas aplicaciones de proteínas recombinantes que contienen estos azú-cares.
Adicionalmente, aunque es común y a menudo esencial en las glicoproteínas de 5 mamífero, no se ha encontrado nunca ácido siálico en los glucanos de plantas. Esto es par-ticularmente importante dado que experimentos realizados han demostrado que la ausencia de ácido siálico terminal en las cadenas laterales glucosídicas puede reducir espectacular-mente la actividad biológica in vivo. Muy probablemente, los receptores de asialo-glicoproteínas en el hígado pueden fijar la asialo-glicoproteína, y causar por ello un aclara-10 miento de la glicoproteína de la circulación, que se refleja en una semivida metabólica redu-cida y baja bioactividad in vivo.
La invención proporciona una planta que comprende una enzima funcional de mamí-fero que proporciona la biosíntesis de N-glucanos que no está presente normalmente en las plantas. Es especialmente el carácter de "planta" de los glucanos lo que hace que las glico-15 proteínas producidas en las plantas sean menos adecuadas para uso farmacéutico. Este carácter de "planta" imparte características antigénicas e inmunógenas indeseables a la glicoproteína en cuestión, lo que requeriría una estrategia destinada a prevenir la inmuno-genicidad de las glicoproteínas producidas por las plantas transgénicas. La finalidad de la estrategia es modificar el genoma de las células vegetales de tal manera que las mismas 20 maduren sus proteínas como lo harían las células humanas. Numerosos genes de glicosil-transferasas de mamíferos han sido ya clonados, lo que no es el caso de las plantas. Te-miendo en cuenta la facilidad de transformación de los sistemas vegetales, es acuciante la tentación de "complementar" el aparato de Golgi de las plantas por glicosiltransferasas de mamíferos a fin de "humanizar" o "mamiferita" los glucanos de las glicoproteínas que produ-25 cen. El éxito de una estrategia de este tipo no es evidente, sin embargo. En particular,...
Reivindicaciones:
Reivindicaciones
1. Una planta que comprende una proteína funcional que proporciona la biosíntesis de N-glucanos, en donde la proteína es una β-1,4-galactosiltransferasa de mamífero; y una segunda proteína de mamífero en donde dicha segunda proteína comprende un glucano galactosilado unido por N; y en donde la planta comprende adicionalmente: 5
(a) una sialil-transferasa; o
(b) una glucuronil-transferasa.
2. La planta de la reivindicación 1, en donde los genes responsables de la adición de xilosa y/o fucosa están bloqueados.
Patentes similares o relacionadas:
PROCEDIMIENTO PARA LA PRODUCCIÓN DE PLANTAS TRANSGÉNICAS QUE PRESENTAN ALTO CONTENIDO Y RENDIMIENTO EN ALMIDÓN Y BIOMASA, del 26 de Enero de 2012, de IDEN BIOTECHNOLOGY: Procedimiento para la producción de plantas transgénicas que presentan alto contenido y rendimiento en almidón y biomasa. Las SSs en plantas (incluida la […]
PRODUCCIÓN DE OLIGOSACÁRIDOS EN PLANTAS TRANSGÉNICAS, del 16 de Enero de 2012, de STICHTING SCHEIKUNDIG ONDERZOEK IN NEDERLAND (SON): LA INVENCION SE REFIERE A UN METODO PARA PRODUCIR OLIGOSACARIDOS, QUE CONSTA DE LA SELECCION DE UN GEN QUE CODIFICA UNA ENZIMA QUE ES CAPAZ DE CONVERTIR SACAROSA EN […]
PREPARACIÓN Y UTILIZACIONES DE LAS SECUENCIAS GÉNICAS CODIFICANTES DE LAS GLUCOSILTRANSFERASAS QUIMÉRICAS CON ACTIVIDAD DE GLUCOSILACIÓN OPTIMIZADA, del 15 de Noviembre de 2011, de UNIVERSITE DE PROVENCE (AIX-MARSEILLE 1) CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Procedimiento para la producción de secuencias génicas codificantes de glucosiltransferasas membranales quiméricas que presentan una actividad de glucosilación optimizada […]
BIOCATALIZADOR INMOVILIZADO BASADO EN ALGINATO PARA LA BIOTRANSFORMACION DE CARBOHIDRATOS, del 10 de Octubre de 2011, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC) (85%) UNIVERSIDAD AUTONOMA DE MADRID (UAM)(15%): Biocatalizador inmovilizado basado en alginato para la biotransformación de carbohidratos.Procedimiento de obtención de un biocatalizador, que comprende: inmovilizar una enzima […]
NUEVAS COMPOSICIONES VACUNALES ANTIPALÚDICAS Y SUS APLICACIONES, del 19 de Agosto de 2011, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS) UNIVERSITE DES SCIENCES ET TECHNOLOGIES DE LILLE: Polipéptido del que: la secuencia N-terminal comprende la secuencia polipeptídica de la GBSSI (Granule Bound Starch Synthase I), una secuencia polipeptídica […]
MÉTODOS PARA PRODUCIR HIALURONANO EN UNA CÉLULA HUÉSPED RECOMBINANTE, del 4 de Julio de 2011, de NOVOZYMES BIOPHARMA DK A/S: Método para la producción de un ácido hialurónico, que comprende: (I) cultivo de una célula huésped de Bacillus bajo condiciones adecuadas para […]
MÉTODO PARA FABRICACIÓN DE GLICOPROTEÍNAS QUE TIENEN GLICOSILACIÓN DE TIPO HUMANO, del 17 de Enero de 2011, de PHYTON HOLDINGS, LLC: Un método de expresar una glicosiltransferasa y una glicoproteína exógena que tienen una cadena de azúcar de tipo humano en una célula de planta transformada, […]
MÉTODO DE EXPRESIÓN DE PÉPTIDOS PEQUEÑOS USANDO PROTEÍNAS DE CEREAL QUE NO SON PROTEÍNAS DE ALMACENAMIENTO COMO PORTADOR DE FUSIÓN EN EL ENDOSPERMO Y USO DE LOS MISMOS, del 13 de Enero de 2012, de HEALTHGEN BIOTECHNOLOGY INC. IN WUHAN: Método de uso de una proteína de cereal que no es una proteína de almacenamiento como portador de fusión para expresar altamente un péptido pequeño en células de endospermo del […]