USO DE UN COMPUESTO PROTEICO DERIVADO DE LA GLICOPROTEINA (GG) DE HSV PARA LA ELABORACION DE UNA COMPOSICION FARMACEUTICA UTIL PARA LA INDUCCION DE MIGRACION CELULAR MEDIADA POR QUIMIOQUINAS.
Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV para la elaboración de una composición farmacéutica útil para la inducción de migración celular mediada por quimioquinas.
La invención describe el uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV (HSV-1 y HSV-2) inductor de la migración celular mediada por quimioquina para la elaboración de un medicamento o composición farmacéutica para el tratamiento de una enfermedad o desorden causada por un déficit de la migración celular, preferentemente del sistema inmune. Además, forman parte de la invención composiciones terapéuticas que comprenden dichos compuestos y sus aplicaciones terapéuticas
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200601934.
Solicitante: CONSEJO SUPERIOR INVESTIG. CIENTIFICAS.
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: ALCAMI PERTEJO,ANTONIO, VIEJO BORBOLLA,ABEL.
Fecha de Solicitud: 20 de Julio de 2006.
Fecha de Publicación: .
Fecha de Concesión: 28 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K38/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C07K14/035 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Virus herpes simple I o II.
Clasificación PCT:
- A61K38/16 A61K 38/00 […] › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C07K14/035 C07K 14/00 […] › Virus herpes simple I o II.
- C12N15/38 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Herpetoviridae, p. ej. virus del herpes simple, Herpesvirus varicellae, virus Epstein-Barr, citomegalovirus, virus de la pseudorrabia.
Fragmento de la descripción:
Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV para la elaboración de una composición farmacéutica útil para la inducción de migración celular mediada por quimioquinas.
Sector de la técnica
Biomedicina y biotecnología. Desarrollo de principios terapéuticos activos. Desarrollo de composiciones farmacéuticas para el tratamiento de enfermedades humanas que cursan con alteraciones de la migración de células del sistema inmune.
Estado de la técnica
Durante la evolución, los virus han desarrollado numerosas estrategias para modular el sistema inmune. Entre ellas se encuentra la de inhibir la función de las quimioquinas. Las quimioquinas son una familia de citoquinas básicas de 8-10 kDa que inducen la migración de leucocitos y la infiltración de tejidos infectados o dañados (Baggiolini, M. (1998) Chemokines and leukocyte traffic. Nature, 392: 565-568) jugando un papel fundamental en la defensa contra patógenos y en las enfermedades inflamatorias. Las quimioquinas se localizan en la superficie celular mediante su interacción con glicosaminoglicanos (GAGs), interacción necesaria para la presentación correcta de las quimioquinas a los leucocitos y su función in vivo (Cinamon, G., Shinder, V. and Alon, R. (2001) Shear forces promote lymphocyte migration across vascular endothelium bearing apical chemokines. Nat. Immunol. 2: 515-522; Proudfoot, A.E., Handel, T.M., Johnson, Z., Lau, E.K., LiWang, P., Clark-Lewis, I., Borlat, F., Wells, T.N., and Kosco-Vilbois, M.H. (2003) Glycosaminoglycan binding and oligomerization are essential for the in vivo activity of certain chemokines. Proc. Natl. Acad. Sci. U.S.A. 100: 1885-1890; Rot, A. (1992) Endothelial cell binding of NAP-1/IL-8: role in neutrophil emigration. Immunol. Today, 13: 291-294). El sistema de las quimioquinas es complejo, con más de 50 quimioquinas humanas identificadas clasificadas en cuatro clases (C, CC, CXC y CX3C) y alrededor de 20 receptores. El papel crítico de las quimioquinas en la defensa anti-viral y en la respuesta inmune en general se refleja en el descubrimiento de muchos mecanismos virales para modular la actividad de las quimioquinas (Alcami A. (2003). Viral mimicry of cytokines, chemokines and their receptors. Nat. Rev. Immunol., 3: 36-50; Alcami, A., Symons, J.A., Collins, P.D., Williams, T.J. and Smith, G.L. (1998) Blockade of chemokine activity by a soluble chemokine binding protein from vaccinia virus. J. Immunol., 160: 624-633; Lalani, A.S., Barrett, J.W. and McFadden, G. (2000) Modulating chemokines: more lessons from viruses. Immunol. Today, 21: 100-106; Lalani, A.S., Graham, K., Mossman, K., Rajarathnam, K., Clark-Lewis, I., Kelvin, D. and McFadden, G. (1997) The purified myxoma virus gamma interferon receptor homolog M-T7 interacts with the heparin-binding domains of chemokines. J. Virol. 71: 4356-4363; Murphy, P.M. (2001) Viral exploitation and subversion of the immune system through chemokine mimicry. Nat. Immunol., 2: 116-122; van Berkel, V., Barrett, J., Tiffany, H.L., Fremont, D.H., Murphy, P.M., McFadden, G., Speck, S.H. and Virgin, H.I. (2000) Identification of a gammaherpesvirus selective chemokine binding protein that inhibits chemokine action. J. Virol., 74: 6741-6747). Tanto poxviruses como herpesviruses codifican para proteínas secretadas con capacidad de unión e inhibición de las quimioquinas (viral chemokine-binding protein, vCKBP). Las vCKBPs no poseen homología de secuencia con los receptores celulares de quimioquinas o entre sí, por lo que cada una representa una nueva estructura capaz de unir quimioquinas (Lalani, A.S., Barrett, J.W. and McFadden, G. (2000) Modulating chemokines: more lessons from viruses. Immunol. Today, 21: 100-106; Murphy, P.M. (2001) Viral exploitation and subversion of the immune system through chemokine mimicry. Nat. Immunol., 2: 116-122).
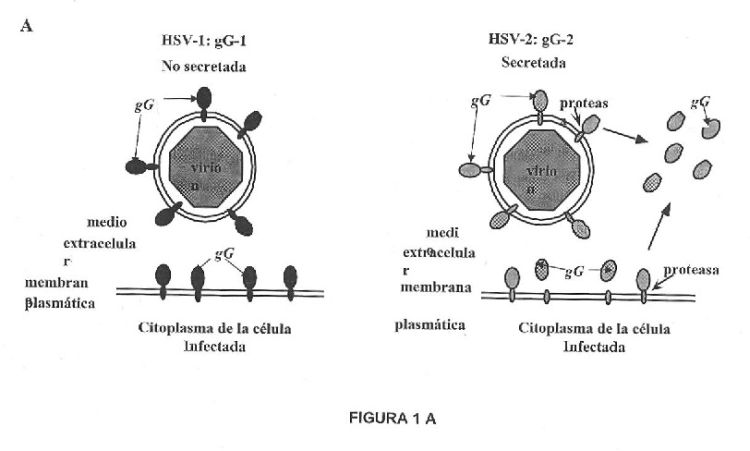
La glicoproteína G (gG) presente en algunos herpesvirus alfa tiene esa capacidad (Bryant, N.A., Davis-Poynter, N., Vanderplasschen, A., and Alcami, A. (2003) Glycoprotein G isoforms from some alphaherpesviruses function as broad-spectrum chemokine binding proteins. EMBO J., 22: 833-846; Costes B, Ruiz-Arguello MB, Bryant NA, Alcami A, Vanderplasschen A. (2005) Both soluble and membrane-anchored forms of Felid herpesvirus 1 glycoprotein G function as a broad-spectrum chemokine-binding protein. J. Gen. Virol. 86: 3209-3214). Los miembros de la subfamilia herpesvirus alpha tienen un rango de hospedador variable y la capacidad de establecer infecciones latentes de forma primaria pero no exclusiva en ganglios sensoriales (Roizman, B. and Pellet, P.E. (2001) The family herpesviridae: and introduction. In Knipe, D.M. and Howley, P.M. (eds.), Fields Virology. Lippincott Williams and Wilkins, Philadelphia, Vol. 2, pp. 2381-2397). Esta subfamilia incluye patógenos animales como los herpesvirus equino 1 y 3 (EHV-1 y EHV-3) y los herpesvirus bovino 1 y 5 (BHV-1 y BHV-5) y patógenos humanos como HSV-1 y HSV-2, que replican en mucosa oral y genital y el virus varicela zoster (VZV). Algunas de las glicoproteínas de los herpesvirus alfa presentes en la partícula viral juegan un papel fundamental en la morfogénesis viral, unión a la célula y tropismo celular. La función de la glicoproteína G (gG), sin embargo, se desconocía hasta que se descubrió que la gG codificada por los herpesvirus alfa constituye una nueva familia de proteínas virales con capacidad de unión a quimioquinas (Bryant, N.A., Davis-Poynter, N., Vanderplasschen, A., and Alcami, A. (2003) Glycoprotein G isoforms from some alphaherpesviruses function as broad-spectrum chemokine binding proteins. EMBO J., 22: 833-846). La gG de EHV-1, EHV-3, BHV-1 y BHV-5 tiene actividad de unión a un amplio abanico de quimioquinas con alta afinidad, inhibe la interacción de quimioquinas con los receptores celulares y su actividad de inducir migración celular, a pesar de carecer de similitud de secuencia con los receptores de quimioquinas celulares. Debido a que las quimioquinas juegan un papel crítico en la activación de la respuesta inflamatoria, induciendo la migración de las células inmunes a los tejidos infectados o dañados, la capacidad de gG de inhibir quimioquinas postuló el papel antiinflamatorio de la gG. Sin embargo, no se observó tal actividad en la gG de HSV-1 y HSV-2 -que tiene muy baja similitud de secuencia con las gG de los virus equinos y bovinos- con las quimioquinas usadas en esta invención (CCL1, CCL2, CCL11, CCL17, CCL20, CXCL1, CXCL10, CXCL21, CX3CL1 (ver más adelante en la presente invención; Bryant et al., 2003). En este sentido, recientemente se ha demostrado que la gG del herpesvirus felino es capaz de unir quimimoquinas (B. Costes, M. B. Ruiz-Argüello, N. A. Bryant, A. Alcami and A. Vanderplasschen. 2005. Both soluble and membrane-anchored forms of feline herpesvirus 1 glycoprotein G function as a broad spectrum chemokine binding protein. J. Gen. Virol. 86, 3209-3214).
Tanto HSV-1 como HSV-2 son importantes patógenos humanos. HSV-1 infecta y replica, por lo general, en la mucosa oro-labial y ocular. HSV-2 replica en la mucosa genital. Los virus herpes simplex 1 y 2 (HSV-1 y HSV-2) son patógenos humanos con una alta prevalencia en la población, de tal forma que HSV-1 en adultos se encuentra entre el 60 y el 90% dependiendo de la zona geográfica del mundo. La reactivación de ambos virus ocasiona la producción de partículas virales con la aparición de lesiones que tienen un gran impacto clínico. HSV-1 es el causante de queratitis en la córnea que puede ocasionar ceguera, meningitis y es la principal causa viral de encefalitis debido a su carácter neurotrópico. Tanto HSV-1 como HSV-2 pueden causar encefalitis si la infección tiene lugar en sistema nervioso central. La encefalitis herpética es un proceso encefálico focal localizado en las zonas frontotemporal y parietal del cerebro. La encefalitis subaguda asociada con HSV ha sido identificada en el 2% de los casos estudiados en pacientes con síndrome de la inmunodeficiencia adquirida (SIDA). HSV supone un riesgo para los neonatos ya que la infección durante el tercer trimestre de gestación y/o el parto puede dar lugar a enfermedad diseminada, fallo de múltiples órganos, incluyendo el sistema nervioso central, y muerte del feto o neonato. En ausencia de una terapia antiviral específica la mortalidad supera el 80% en la enfermedad diseminada y el 50% en aquellos pacientes que presentan síntomas únicamente en el CNS. La mayoría de los recién nacidos infectados desarrolla trastornos neurológicos. Un nuevo aspecto de la patología de HSV que ha adquirido especial relevancia en los últimos años es la asociación de infecciones de HSV con enfermedades neurodegenerativas...
Reivindicaciones:
1. Uso de un compuesto proteico derivado de la glicoproteína (gG) de HSV perteneciente al siguiente grupo: la proteína gG-1s del HSV-1 (secuencia de aminoácidos SEQ ID NO2) y la proteína gG-2s del HSV-2 (secuencia de aminoácidos SEQ ID NO4), para la elaboración de un medicamento o composición farmacéutica útil para la inducción de migración celular mediada por quimioquinas.
2. Secuencia de nucleótidos útil para la expresión de un péptido caracterizada porque es codificante de un fragmento extracelular de la proteína gG de HSV-1 constituido por la SEQ ID NO1, que codifica para la forma gG-1s del HSV-1 (SEQ ID NO2).
3. Secuencia de nucleótidos útil para la expresión de un péptido caracterizada porque es codificante de un fragmento extracelular de la proteína gG de HSV-2 constituido por la SEQ ID NO3, que codifica para la forma gG-2s del HSV-2 (SEQ ID NO4).
4. Vector de expresión recombinante útil para la expresión de un péptido caracterizado porque comprende una secuencia de nucleótidos según las reivindicaciones 2 y 3.
5. Célula transformada o transfectada útil para la producción de un péptido caracterizada porque comprende una secuencia de nucleótidos según las reivindicaciones 2 y 3 ó un vector según la reivindicación 4.
6. Proteína derivada o fragmento de las gG de HSV, ya sean del tipo HSV-1 o HSV-2, útil como inductora de la migración celular mediada por quimioquinas caracterizada porque pertenece al siguiente grupo: SEQ ID NO2, forma proteica gG-1s del HSV-1, y SEQ ID NO4, forma proteica gG-2s del HSV-2.
7. Composición farmacéutica o medicamento útil para la inducción de migración celular mediada por quimioquinas caracterizada porque comprende una secuencia de aminoácidos perteneciente al siguiente grupo: secuencia de aminoácidos constituida por la SEQ ID NO2, que codifica para la forma gG-1s del HSV-1 y secuencia de aminoácidos constituida por la SEQ ID NO4, que codifica para la forma gG-2s del HSV-2, en cantidad terapéuticamente efectiva junto con, opcionalmente, uno o más adyuvantes y/o vehículos farmacéuticamente aceptables.
8. Uso de la composición farmacéutica según la reivindicación 7 en un método de tratamiento o profilaxis de un mamífero, preferentemente un ser humano, afectado por una enfermedad, desorden o patología que cursa con alteraciones en la migración celular mediada por quimioquinas consistente en la administración de dicha composición terapéutica en dosis adecuada que permita la recuperación de la capacidad de migración celular, preferentemente de células del sistema inmune.
9. Uso de la composición farmacéutica según la reivindicación 8 caracterizado porque la enfermedad con alteraciones en la migración celular pertenece al siguiente grupo: cardiomiopatía isquémica, terapia post-infarto con células de la médula espinal, síndromes coronarios agudos, carcinoma, carcinoma espontáneo bronquio-alveolar o fiebre crónica Q.
10. Procedimiento de identificación de compuestos útiles para el tratamiento de infecciones provocadas por HSV caracterizado porque se utiliza una proteína perteneciente al siguiente grupo: proteína gG-1s de HSV-1 (SEQ ID NO2) y proteína gG-2s de HSV-2 (SEQ ID NO4).
Patentes similares o relacionadas:
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Polipéptidos de unión específica novedosos y usos de los mismos, del 15 de Julio de 2020, de Pieris Pharmaceuticals GmbH: Muteína de lipocalina lagrimal humana que tiene especificidad de unión para IL-17A, en la que la muteína se une a IL-17A con una KD de aproximadamente 1 nM o menos, en la que […]
Métodos de tratamiento y prevención de infecciones por staphylococcus aureus y afecciones asociadas, del 15 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición para uso en un método de inmunización de un sujeto contra la infección por S. aureus, comprendiendo dicha composición: (i) un fragmento de polipéptido […]
Administración de agentes terapéuticos mediante una proteína de unión a colágeno, del 15 de Julio de 2020, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ARKANSAS: Una composición que comprende un segmento polipeptídico de unión a colágeno de origen bacteriano unido a un agente terapéutico, para su uso en el tratamiento […]
Composiciones farmacéuticas para el tratamiento de superinfecciones bacterianas post-influenza, del 24 de Junio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un polipéptido de flagelina en combinación con al menos un antibiótico para su uso en el tratamiento de una superinfección bacteriana post-influenza […]
Reactivos SIRP-alfa de alta afinidad, del 24 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un polipéptido SIRPα de alta afinidad que comprende al menos una y no más de 15 modificaciones de aminoácidos dentro del dominio d1 de una secuencia SIRPα de tipo […]
Péptidos de unión beta amiloide y sus usos para el tratamiento y el diagnóstico de la demencia de Alzheimer, del 17 de Junio de 2020, de Priavoid GmbH: Péptido que contiene al menos una secuencia de aminoácidos que se une a especies beta amiloides y en el que la carga negativa del grupo carboxilo presente […]