SILENCIAMIENTO PORTRANSCRIPCIONAL DE LA EXPRESION DEL FACTOR TISULAR MEDIANTE ARN DE INTERFERENCIA CORTOS.
Molécula de ARN corto de interferencia (ARNsi), caracterizada porque comprende por lo menos 19 nucleótidos dirigida hacia un factor tisular (FT) que codifica la secuencia de ácido nucleico o fragmentos de la misma,
y en la que la molécula de ARNsi comprende una secuencia nucleotídica seleccionada de entre el grupo constituido por
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/NO03/00045.
Solicitante: SIRNASENSE AS.
Nacionalidad solicitante: Noruega.
Dirección: GAUSTADALLEE 21,0349 OSLO.
Inventor/es: PRYDZ,HANS PETER B, HOLEN,TORGEIR, AMARZGUIOUI,MOHAMMED, WIIGER,MERETE, BABAIE,ESHRAT.
Fecha de Publicación: .
Fecha Concesión Europea: 25 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- C07H21/00C4
Clasificación PCT:
- A61K31/7088 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
Clasificación antigua:
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- C12N15/11 C12N 15/00 […] › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
Fragmento de la descripción:
Silenciamiento postranscripcional de la expresión del factor tisular mediante ARN de interferencia cortos.
La presente invención se refiere a los ARN sintetizados, más específicamente a los ARN cortos de interferencia (ARNsi) que pueden modular la expresión del Factor Tisular (FT), así como a la preparación farmacéutica que comprende los ARNsi sintetizados y a su utilización.
Antecedentes de la invención
Los mecanismos que silencian la expresión génica innecesaria son críticos para la función celular normal, y el silenciamiento del ARN es un nuevo campo de investigación que ha reunido durante la última década estudios independientes en varios organismos. Se ha sabido durante un largo periodo que las interacciones entre las secuencias homólogas del ADN y/o del ARN pueden silenciar genes y provocar la metilación del ADN (1). El descubrimiento de la interferencia del ARN (ARNi) en C. elegans en 1998 centró la atención en el ARN bicatenario (ARNds) como un productor de silenciamiento génico, y muchos efectos de silenciamiento génico en las plantas son conocidos por estar mediados por el ARNds (1).
El ARNi se describe normalmente como un fenómeno de silenciamiento génico tras las transcripción (PTGS) en que el ARNds activa la degradación del ARNm homólogo en el citoplasma (1). Sin embargo, el potencial del ARNds nuclear para introducir una serie de reacciones que conducen a modificaciones epigenéticas de secuencias de ADN homólogas y silenciar en el nivel de transcripción no debería pasarse por alto. Además, aun cuando los aspectos nucleares del silenciamiento del ARN han sido estudiados especialmente en plantas, existen indicaciones de que el ADN dirigido por ARN similar o las modificaciones de cromatina pueden producirse también en otros organismos.
El ARNi en animales, y los fenómenos relacionados de PTGS en plantas, proceden del mismo mecanismo muy conservado, indicando un origen antiguo (1). EL procedimiento básico implica un ARNds que es procesado en unidades más cortas (denominadas ARN corto de interferencia; ARNsi) que guían el reconocimiento y la escisión conocida del ARN mensajero (ARNm) homólogo. Los ARNds que (después del tratamiento) activan ARNi/PTGS pueden prepararse en el núcleo o citoplasma de numerosas maneras.
El tratamiento del ARNds en los ARNsi, que a su vez degradan el ARNm es un procedimiento de degradación del ARN en dos etapas. La primera etapa implica una actividad de ARNds endonucleasa (ribonucleasa de tipo III; ARNasa de tipo III) que procesa el ARNds en los ARN transcrito y complementario que presentan 21 a 25 nucleótidos (nt) de longitud, es decir ARNsi. En Drosophila esta proteína ARNasa de tipo III se denomina Dicer. En la segunda etapa los ARNsi complementarios producidos se combinan con un complejo de ribonucleasa denominado complejo de silenciamiento producido por ARN (RISC), y actúan como guías del mismo, que escinde los ARNm monocatenarios homólogos. El RISC corta el ARNm aproximadamente en la mitad de la zona emparejada con el ARNsi complementario, después de lo cual el ARNm se degrada más. Los ARNds de diferentes procedencias pueden introducir la serie de reacciones de tratamiento lo que conduce a ARNi/PTGS. Además, recientes trabajos también sugieren que puede haber más de una serie de reacciones para la incisión del ARNds, produciendo distintas clases de ARNsi que pueden no ser funcionalmente equivalentes.
El silenciamiento del ARN, (que es activo a diferentes niveles de expresión génica en el citoplasma y en el núcleo) parece que ha evolucionado para contrarrestar la proliferación de secuencias extrañas tales como los elementos transponibles y los virus (muchos de los cuales producen ARNds durante la replicación). Sin embargo ya que el ARNi/PTGS produce una señal móvil que provoca el silenciamiento en puntos distantes, debería considerarse la posibilidad de inyectar directamente los ARNsi corta la síntesis de proteínas y/o funciona como una herramienta terapéutica en células de mamífero.
Hasta ahora, se sabe poco acerca de los efectos generales de las mutaciones o modificaciones químicas en una secuencia de ARNsi. Boutla et al. (14) publicaron que un ARNsi mutado con un solo apareamiento incorrecto situado en el centro con respecto a la secuencia diana del ARNm conservaba sustancialmente actividad en Drosophila. En cambio, Elbashir et al. (15) observaron que un solo apareamiento incorrecto era perjudicial para la actividad en un ensayo in vitro de lisado de embrión de Drosophila. En el contexto de la presente solicitud se ha tratado de reconciliar estos dos resultados conflictivos describiendo el proceso del ARNi in vivo como un proceso dinámico donde influyen varios factores en el resultado final, entre ellos la posición diana del ARNsi, la concentración de ARNsi, la concentración de ARNm, la producción de ARNm, y la actividad de la división inherente a los ARNsi, actividad que puede ser reducida gradualmente por mutaciones de apareamiento incorrecto.
Se han descrito también otros resultados. Por ejemplo, Jacque et al. (16) observan que un solo apareamiento incorrecto en un ARNsi que dirige la LTR de los VIH perdía solamente alguna actividad, mientras que otro ARNsi que dirige el VIF de los VIH no pierde casi ninguna actividad. Cuatro mutaciones, sin embargo, suprimieron la actividad completamente. Otros ejemplos de supresión completa de actividad son observados por Gitlin et al. (17), Klahre et al. (18) y Garrus et al. (19), utilizando 5, 6 y 7 mutaciones respectivamente. Unas mutaciones dobles, centrales, utilizadas por Boutla y el grupo propio de los autores (14, 15), condujo a una grave pérdida de actividad también para Yu et al. (20) y Wilda et al. (21), este último utilizando un ARNsi con solo 17 pares de bases. Es interesante, en vista de los ARNsi muy activos, metilados en el extremo de los inventores, que en el informe de Tuschl el ARNsi metilado en 2'-OH completamente es inactivo.
Además, existen dos artículos publicados de supresión de la actividad por una sola mutación. Uno de ellos, sin embargo, el trabajo de Brummelkamp et al. (22), está utilizando un ARN corto en horquilla (ARNsh) que se supone que produce ARNsi por acción de Dicer (23). Este montaje de ARNsh fue inactivado por una sola mutación en el supuesto segundo nucleótido del ARNsh, o por un solo apareamiento incorrecto en el supuesto noveno nucleótido. Gitlin et al. (17), por otra parte, discutió el caso para la inactivación de una sola mutación más intensamente aislando cepas de poliovirus resistentes al ARNsi que contienen una sola mutación en la secuencia diana en el ARN genómico, o bien en el sexto nucleótido del ARNsi o en el noveno nucleótido, ambos contrarrestados en el extremo 5' de la cadena transcrita. En equilibrio, el ARNsi diferente parece estar activado a diferentes grados.
Tradicionalmente, la modificación química de los ácidos nucleicos ha sido utilizada entre otras cosas para proteger las secuencias de ácido nucleico monocatenario contra la degradación por la nucleasa y obtener de este modo secuencias con una vida media más larga. Por ejemplo, el documento WO 91/15499 da a conocer los 2'O-alquilo oligonucleótidos útiles como sondas complementarias. Además, se ha utilizado la 2-O-metilación para estabilizar los ribozimas de cabeza de martillo (4). Sin embargo, se sabe poco acerca de los efectos de las modificaciones químicas de los ARNsi. Además, la presencia de sustituyentes largos en el 2'-hidroxilo del nucleótido con terminal 5' puede interferir con la propia fosforilación del ARNsi que se ha derepresentado que es necesaria para la actividad del ARNsi (24).
De este modo, una actividad diferencial inherente en varios ARNsi en una población significaría que diferentes ARNsi serán afectados por las modificaciones del ARNsi, químicas o mutacionales, de diferentes maneras.
El Factor Tisular (FT) es el activador más potente de la coagulación sanguínea (2) e instrumental originando la trombosis arterial en el momento de la ruptura de las placas ateroscleróticas. Existen además muchas pruebas de que el alto contenido de FT en las células cancerosas se correlaciona con la angiogénesis dirigida por el cáncer y con tendencia a la metástasis. Además, FT es de importancia patógena central en caso de la coagulación intravascular séptica diseminada (por ejemplo, sepsia meningocócica). De este modo, los procedimientos para modular o silenciar el FT serían de gran valor.
La solicitud de patente WO 01/75164 (A2) da a conocer un sistema de...
Reivindicaciones:
1. Molécula de ARN corto de interferencia (ARNsi), caracterizada porque comprende por lo menos 19 nucleótidos dirigida hacia un factor tisular (FT) que codifica la secuencia de ácido nucleico o fragmentos de la misma, y en la que la molécula de ARNsi comprende una secuencia nucleotídica seleccionada de entre el grupo constituido por
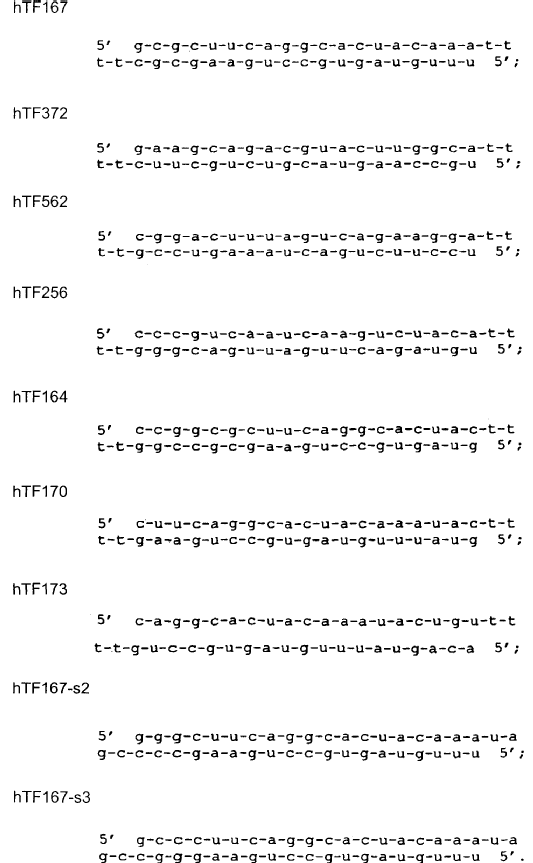
2. Molécula de ARN (ARNsi) según la reivindicación 1, caracterizada porque dicha molécula es bicatenaria.
3. Molécula de ARN (ARNsi) según las reivindicaciones 1 a 2, caracterizada porque dicha molécula es de 21 a 25 nucleótidos de longitud, preferentemente de 21 nucleótidos de longitud.
4. Molécula de ARN (ARNsi) según las reivindicaciones 1 a 3, caracterizada porque dicha molécula está constituida por una de las secuencias seleccionadas de entre el grupo constituido por


5. Molécula de ARN (ARNsi) según cualquiera de las reivindicaciones 1 a 3, caracterizada porque se introducen una o más mutaciones en relación con la secuencia natural en la que dicha molécula está constituida por la secuencia
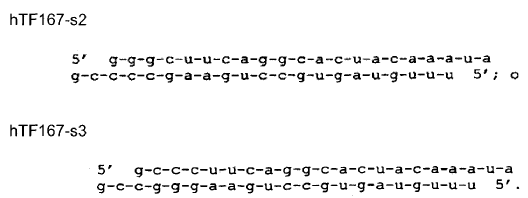
6. Molécula de ARN (ARNsi) según la reivindicación 1, caracterizada porque dicha molécula de ARNsi se modifica sustituyendo el enlace fosfodiéster con un enlace tiofosfodiéster.
7. Molécula de ARN (ARNsi) según la reivindicación 6, caracterizada porque dicha molécula de ARNsi se selecciona de entre el grupo constituido por
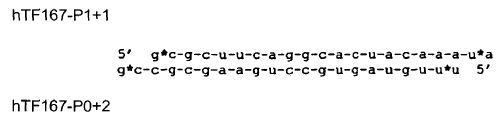
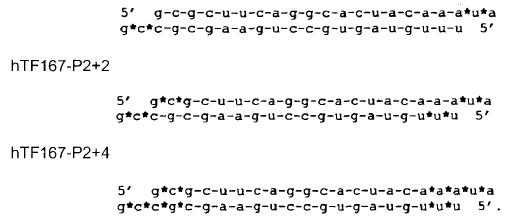
en las que el asterisco indica los nucleótidos unidos por enlaces fosforotioato.
8. Molécula de ARN (ARNsi) según la reivindicación 7, caracterizada porque dicha molécula es
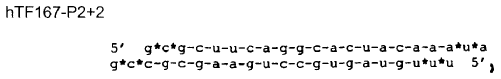
en la que el asterisco indica los nucleótidos unidos por enlaces fosforotioato.
9. Molécula de ARN (ARNsi) según cualquiera de las reivindicaciones 1 a 3, caracterizada porque dicha molécula está modificada por la introducción de un grupo alquilo C1-C3, alquenilo C1-C3 o alquililo C1-C3 en uno o más de entre los grupos hidroxilo 2' OH en la secuencia.
10. Molécula de ARN (ARNsi) según la reivindicación 9, caracterizada porque dicha molécula se selecciona de entre el grupo constituido por


en la que una letra mayúscula en negrita indica que el nucleótido está metilado en 2-O y en la que una letra mayúscula en negrita subrayada indica que el nucleótido está alilado en 2-O.
11. Molécula de ARN (ARNsi) según la reivindicación 10, caracterizada porque dicha molécula está constituida por la secuencia
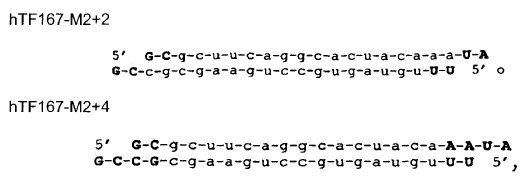
en la que una letra mayúscula en negrita indica que el nucleótido está metilado en 2-O.
12. Molécula de ARN (ARNsi) según la reivindicación 10, caracterizada porque dicha molécula está constituida por la secuencia

en la que una letra mayúscula en negrita indica que el nucleótido está metilado en 2-O.
13. Molécula de ARN (ARNsi) según cualquiera de las reivindicaciones 1 a 11, caracterizada porque el FT o fragmento del mismo es de origen vertebrado, preferentemente de origen mamífero, más preferentemente de origen humano.
14. Preparación farmacéutica, caracterizada porque comprende una o más de las moléculas de ARN corto de interferencia (ARNsi) según cualquiera de las reivindicaciones 1 a 13.
15. Preparación farmacéutica según la reivindicación 14, caracterizada porque comprende la secuencia
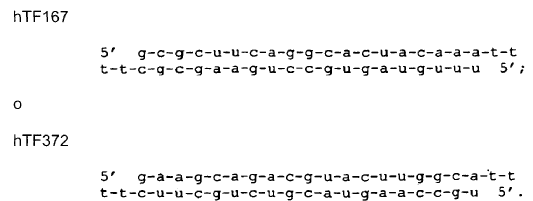
16. Preparación farmacéutica según la reivindicación 14, caracterizada porque comprende la secuencia
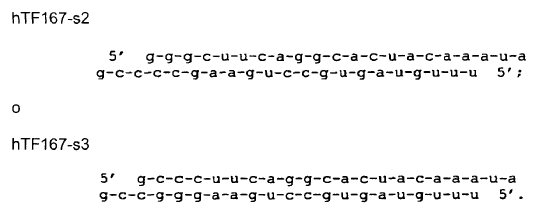
17. Preparación farmacéutica según la reivindicación 14, caracterizada porque dichas moléculas se seleccionan de entre el grupo constituido por:

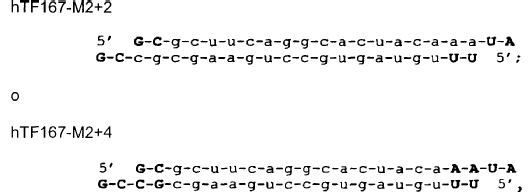
en la que el asterisco indica los nucleótidos unidos por enlaces fosforotioato y en la que una letra mayúscula en negrita indica que el nucleótido está metilado en 2-O.
18. Preparación farmacéutica según la reivindicación 17, en la que la molécula de ARN es una molécula de ARN aislada que comprende la secuencia

en la que una letra mayúscula en negrita indica que el nucleótido está metilado en 2-O.
19. Preparación farmacéutica según cualquiera de las reivindicaciones 14 a 18, caracterizada porque comprende además diluyentes, lubricantes, aglutinantes, portadores, medios de disgregación, medios de absorción, colorantes, edulcorantes y/o saborizantes.
20. Preparación farmacéutica según cualquiera de las reivindicaciones 14 a 19, caracterizada porque comprende adyuvantes.
21. Preparación farmacéutica según cualquiera de las reivindicaciones 14 a 20, adecuada para ser administrada por vía parenteral, preferentemente por inyección o infusión subcutánea, intravenosa, intramuscular o intraperitoneal, por vía oral, nasal, bucal, rectal, vaginal y/o por inhalación o insuflado.
22. Preparación farmacéutica según cualquiera de las reivindicaciones 14 a 21, caracterizado porque se formula como suspensiones o soluciones de infusión, un aerosol, cápsulas, comprimidos, píldoras, atomizadores, supositorios, en formulaciones de dosificación que contienen portadores, adyuvantes y/o vehículos farmacéuticamente aceptables no tóxicos convencionales.
23. Utilización de una o más de las moléculas de ARN (ARNsi) según cualquiera de las reivindicaciones 1 a 13 para preparar una preparación farmacéutica adecuada para el tratamiento, la prevención y/o la inhibición de la coagulación de la sangre indeseada.
24. Utilización según la reivindicación 23, en la que dicha preparación se formula para administración parenteral, preferentemente por inyección o infusión subcutánea, intravenosa, intramuscular o intraperitoneal, por vía oral, nasal, bucal, rectal, vaginal y/o por inhalación o insuflado.
Patentes similares o relacionadas:
ACIDO L-NUCLEICO MODIFICADO, del 19 de Octubre de 2010, de NOXXON PHARMA AG: Un ácido L-nucleico modificado, que comprende un resto de ácido L-nucleico y un resto diferente de ácido L-nucleico, en el que el resto de ácido L-nucleico está […]
OLIGOMEROS NO AGREGANTES Y SIN BLOQUEO DE LA FLUORESCENCIA QUE COMPRENDEN ANALOGOS DE NUCLEOTIDOS; METODOS DE SINTESIS Y USO DE LOS MISMOS, del 25 de Agosto de 2010, de EPOCH BIOSCIENCES, INC: Un conjugado que comprende: (a) un polímero que comprende una serie de unidades de monómero; y (b) un fluoróforo unido covalentemente a ellos, en el que uno o más de […]
MODULACION ANTISENTIDO DE LA EXPRESION DE SURVIVINA, del 1 de Febrero de 2010, de ISIS PHARMACEUTICALS, INC.: Un oligonucleótido antisentido con una longitud de hasta 30 nucleótidos dirigido a una molécula de ácido nucleico que codifica la survivina humana, que comprende una secuencia […]
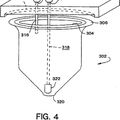 APARATO PARA LA SINTESIS DE OLIGOMEROS, ESPECIALMENTE PEPTOIDES, CON RECICLADO DE REACTIVOS, del 2 de Diciembre de 2009, de NOVARTIS VACCINES AND DIAGNOSTICS, INC.: Un equipo para sintetizar oligómeros inmovilizados sobre partículas en fase sólida en una suspensión de partículas, comprendiendo dicho equipo:
(a) un […]
APARATO PARA LA SINTESIS DE OLIGOMEROS, ESPECIALMENTE PEPTOIDES, CON RECICLADO DE REACTIVOS, del 2 de Diciembre de 2009, de NOVARTIS VACCINES AND DIAGNOSTICS, INC.: Un equipo para sintetizar oligómeros inmovilizados sobre partículas en fase sólida en una suspensión de partículas, comprendiendo dicho equipo:
(a) un […]
Proteínas del factor VIII que tienen secuencias ancestrales, vectores de expresión, y usos relacionados con ellos, del 15 de Julio de 2020, de EMORY UNIVERSITY: Una proteína FVIII recombinante o quimérica que comprende una o más mutaciones ancestrales y una eliminación del dominio B, y en donde la secuencia […]
Método para romper un ácido nucleico y añadir un adaptador por medio de transposasa y reactivo, del 1 de Julio de 2020, de MGI Tech Co., Ltd: Un metodo para romper un acido nucleico y anadir un adaptador por medio de una transposasa, que comprende las siguientes etapas: interrumpir […]
Vacuna subunitaria contra Mycoplasma spp., del 1 de Julio de 2020, de Agricultural Technology Research Institute: Una composición para prevenir una infección por Mycoplasma spp., que comprende: un principio activo, que comprende una proteína de PdhA; y un adyuvante […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]