PRODUCTO GRANULAR GASTRORRESISTENTE BASADO EN NIACINA O DERIVADOS DE LA MISMA Y PROCESO PARA LA PRODUCCION DE DICHO PRODUCTO.
Producto granular gastrorresistente basado en niacina o derivados de la misma,
que comprende una parte interna en la que está/están sustancialmente concentrada/concentrados dicha niacina o derivados de la misma y un recubrimiento externo que cubre y protege dicha parte interna, estando constituido dicho recubrimiento externo por una matriz que tiene una fracción en peso total de ácidos grasos saturados C16-C22 de cadena larga de entre el 40% y el 95% con respecto a la matriz, caracterizado porque dicha matriz comprende además un agente mineral, dispersado en la misma, en una fracción en peso de entre el 2% y el 20% con respecto a la matriz
Tipo: Resumen de patente/invención. Número de Solicitud: W06011271EP.
Solicitante: SILA S.R.L.
Nacionalidad solicitante: Italia.
Dirección: VIA TEMPESTA, 91/C,30030 NOALE (VE).
Inventor/es: LORENZON,MAURIZIO.
Fecha de Publicación: .
Fecha Concesión Europea: 19 de Agosto de 2009.
Clasificación Internacional de Patentes:
- A61K9/00M18
- A61K9/16H4
- A61K9/16P
- A61K9/50H4
- A61K9/50P
Clasificación PCT:
- A61K9/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/16 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aglomerados; Granulados; Microbolitas.
- A61K9/50 A61K 9/00 […] › Microcápsulas (A61K 9/52 tiene prioridad).
Fragmento de la descripción:
Producto granular gastrorresistente basado en niacina o derivados de la misma y proceso para la producción de dicho producto.
Campo técnico
La presente invención se refiere a un producto granular gastrorresistente basado en niacina o derivados de la misma según las características expuestas en la cláusula precaracterizante de la reivindicación principal 1. Trata también sobre un proceso para la producción de dicho producto, que presenta las características mencionadas en la cláusula precaracterizante de la reivindicación independiente 11.
Antecedentes de la técnica
La niacina, a la que se conoce también como vitamina B3 ó vitamina PP, es una sustancia que tiene funciones metabólicas muy importantes en humanos y animales, siendo un precursor de las coenzimas NAD y NADP que, a su vez, están involucradas en las reacciones de oxidación-reducción (por ejemplo, en el ciclo de Krebs) a partir de las cuales un organismo obtiene la energía que requiere para sus actividades.
Estrictamente hablando, la niacina se corresponde con el ácido nicotínico, cuya fórmula estructural se muestra en (I), aunque el término se usa frecuentemente, por analogía, también para indicar la amida de ácido nicotínico, nicotinamida, cuya fórmula estructural se muestra en (II).
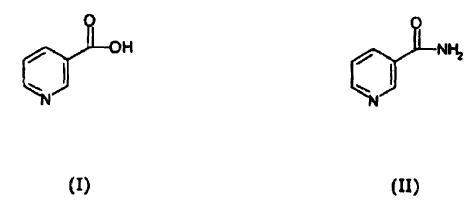
Una deficiencia de niacina en el organismo da como resultado una ralentización global del metabolismo que se manifiesta, en los casos más serios, en el trastorno conocido como pelagra. La niacina presenta además propiedades vasodilatadoras, razón por la cual se puede usar para el tratamiento terapéutico de la hipertensión arterial, y se sabe además que es eficaz en el control de niveles altos de colesterol en la sangre (hipercolesterolemia). En particular, la niacina se usa para reducir la concentración de colesterol de baja densidad (LDL-C), conocido como "colesterol malo", debido a su implicación directa en cardiopatías.
La niacina requerida para el funcionamiento correcto del organismo se obtiene en gran medida de fuera del cuerpo, ya en forma de NAD ó NADP, en particular mediante la ingestión de alimentos de origen animal, aunque, si es necesario, también se puede ingerir como tal, o bien en forma de ácido nicotínico o bien en forma de nicotinamida.
No obstante, se sabe que la ingestión de cantidades relativamente grandes de niacina puede producir la aparición de un enrojecimiento cutáneo severo y no deseado similar a la quemadura solar (un fenómeno conocido como "rubor") que viene acompañado frecuentemente por prurito, trastornos gástricos y una reducción de la presión arterial. Habitualmente, esta serie de contraindicaciones tiene un impacto muy severo sobre los individuos, de tal manera que, según estudios clínicos recientes, una proporción muy alta de pacientes, estimada entre el 10% y el 50%, dejaría el tratamiento precisamente debido a estas desventajas.
Para limitar las contraindicaciones asociadas a la administración de niacina, en particular, el fenómeno del rubor, se han desarrollado varias soluciones que pretenden ralentizar la liberación de niacina en el organismo, en particular, su liberación en el estómago. Un primer ejemplo de dichas soluciones conlleva la dispersión de una cantidad apropiada de niacina en una matriz de sustancias excipientes, mientras que una segunda solución conocida, descrita, por ejemplo, en la patente de Estados Unidos 4.868.180, propone la encapsulación de la niacina en un recubrimiento basado en sustancias celulósicas.
Las patentes US. n.º 3080293 y n.º 3037911 dan a conocer ambas un proceso para incorporar niacina en una matriz de ácidos grasos saturados, en particular, en una matriz de ácido esteárico, para mejorar el sabor desagradable de la niacina como tal.
No obstante, estas soluciones no superan satisfactoriamente los inconvenientes encontrados, razón por la cual perdura una necesidad, en este campo técnico, de proporcionar un producto basado en niacina que presente efectos secundarios reducidos, en particular, que reduzca significativamente el fenómeno del rubor.
Exposición de la invención
El problema que subyace tras la presente invención es el de proporcionar un producto granular gastrorresistente basado en niacina o derivados de la misma y proporcionar un proceso para la producción de dicho producto, estando diseñados estructural y funcionalmente los mismos para superar los inconvenientes previamente mencionados de la técnica antes citada.
En el contexto de este problema, un primer objetivo de la invención es además proporcionar un producto granular basado en ácido nicotínico en una forma utilizable en las aplicaciones más variadas en el campo de la nutrición humana.
Un segundo objetivo es proporcionar un producto granular con un contenido elevado de ácido nicotínico.
Dicho problema se resuelve y dichos objetivos se logran a través de la presente invención por medio de un producto granular y un proceso para la producción de dicho producto de acuerdo con las siguientes reivindicaciones.
Las características y ventajas de la invención se pondrán más claramente de manifiesto a partir de la siguiente descripción detallada conjuntamente con una realización preferida de la misma.
El producto de la presente invención se produce a partir de niacina o derivados de la misma en forma granular, que, en una primera fase del proceso, se mezcla uniformemente con una matriz de composición apropiada definida de forma más detallada posteriormente.
La operación de mezcla se lleva a cabo a una temperatura tal para conseguir que una proporción elevada de los componentes de la matriz se funda, aunque, al mismo tiempo, tal como para no provocar una degradación o deterioro térmico de las sustancias presentes en la mezcla. Esta temperatura es menor que 120ºC y, preferentemente, está entre 60ºC y 75ºC, y, todavía más preferentemente, es aproximadamente 70ºC.
La mezcla se lleva a cabo con un nivel de agitación y durante un periodo de tiempo que sean suficientes para conseguir que la mezcla resulte lo más uniforme y homogénea posible.
Los gránulos de ácido nicotínico, preferentemente en forma pura, tienen un tamaño de entre 0,1 y 1,5 mm, el cual se selecciona también en función del tamaño medio deseado y la distribución de tamaños para el producto acabado. Los gránulos de ácido nicotínico tienen un tamaño preferentemente de entre 0,1 y 0,5 mm.
Según un primer aspecto de la presente invención, la matriz usada en la mezcla tiene un contenido total de ácidos grasos saturados C16-C22 de cadena larga de entre el 40% y el 95%, con respecto a la matriz. En particular, comprende una fracción en peso de C18 saturado (ácido esteárico) de entre el 40 y el 95%, preferentemente el 60% y el 80%.
En este contexto, el contenido total de ácidos grasos se calcula teniendo en cuenta tanto la presencia de ácidos grasos como tales como la presencia de los mismos en forma de ésteres o sales. En particular, la matriz comprende un componente basado en glicéridos, que incluye los ácidos grasos C16-C22 antes mencionados, y puede comprender no solamente monoglicéridos, sino también diglicéridos y triglicéridos. Preferentemente, el componente de ácidos grasos asociado a glicéridos se origina a partir de triglicéridos derivados de aceites vegetales (tales como, por ejemplo, aceite de palma y aceite de girasol) o de grasas animales (tales como, por ejemplo, manteca de cerdo o cebo) con un contenido elevado de ácidos grasos de cadena larga. Los triglicéridos derivados de estas fuentes son apropiadamente hidrogenados para eliminar cualquier enlace doble presente opcionalmente en la cadena, con el fin de dar origen a ácidos grasos saturados en los porcentajes antes mencionados.
La matriz también puede comprender opcionalmente triglicéridos que tengan ácidos grasos de cadena media a corta C12-C14, tales como, por ejemplo, los derivados de aceite de coco y/o de aceite de soja, o, por el contrario, sustancias alifáticas más complejas, de cadena más larga, tales como, por ejemplo, ceras.
De acuerdo con un segundo aspecto de la invención, la matriz también contiene agentes minerales, tales como, por ejemplo, carbonato de calcio CaCO3 ó, preferentemente, sulfato de calcio dihidratado CaSO4*2(H2O).
El agente mineral está presente en la matriz en una fracción...
Reivindicaciones:
1. Producto granular gastrorresistente basado en niacina o derivados de la misma, que comprende una parte interna en la que está/están sustancialmente concentrada/concentrados dicha niacina o derivados de la misma y un recubrimiento externo que cubre y protege dicha parte interna, estando constituido dicho recubrimiento externo por una matriz que tiene una fracción en peso total de ácidos grasos saturados C16-C22 de cadena larga de entre el 40% y el 95% con respecto a la matriz, caracterizado porque dicha matriz comprende además un agente mineral, dispersado en la misma, en una fracción en peso de entre el 2% y el 20% con respecto a la matriz.
2. Producto según la reivindicación 1, en el que dicho producto granular tiene un tamaño de entre 0,15 y 2 milímetros.
3. Producto según la reivindicación 2, en el que dicho producto granular tiene un tamaño de entre 0,25 y 0,8 milímetros.
4. Producto según la reivindicación 1, 2 ó 3, en el que dicha matriz comprende una fracción en peso de ácido graso saturado C18 de entre el 40% y el 95% con respecto a la matriz.
5. Producto según la reivindicación 4, en el que dicha fracción en peso de ácido graso saturado C18 está entre el 60% y el 80% con respecto a la matriz.
6. Producto según cualquiera de las reivindicaciones anteriores, en el que dicho agente mineral es sulfato de calcio dihidratado.
7. Producto según cualquiera de las reivindicaciones anteriores, en el que dicha matriz comprende una cantidad eficaz de agente emulsionante.
8. Producto según la reivindicación 7, en el que dicho agente emulsionante está basado en diestearato de propilenglicol.
9. Producto según cualquiera de las reivindicaciones anteriores, en el que dicha niacina está presente en una fracción en peso de entre el 40% y el 70%.
10. Producto granular gastrorresistente basado en niacina o derivados de la misma según cualquiera de las reivindicaciones anteriores, para ser usado en el tratamiento de la hipertensión arterial o la hipercolesterolemia.
11. Proceso para la producción de productos granulares gastrorresistentes basados en niacina o derivados de la misma, que comprende las fases de:
- - mezclar material granular basado en niacina o derivados de la misma con una matriz que tiene un contenido total de ácidos grasos saturados C16-C22 de cadena larga de entre el 40% y el 95% con respecto a la matriz, ajustar dicha mezcla a una temperatura tal para fundir dichos ácidos grasos saturados, y
- - pulverizar dicha mezcla en una cámara con una temperatura por debajo de la temperatura de fusión de la matriz, de tal manera que dicha matriz se solidifique alrededor de dicho material granular, formando así un producto que tiene una parte interna en la que está/están sustancialmente concentrada/concentrados dicha niacina o derivados de la misma y un recubrimiento externo constituido por dicha matriz,
caracterizado por que dicha matriz comprende además un agente mineral en una fracción en peso de entre el 2% y el 20% con respecto a la matriz.
12. Proceso según la reivindicación 11, en el que dicho material granular basado en niacina tiene un tamaño de entre 0,1 y 1,5 milímetros.
13. Proceso según la reivindicación 12, en el que dicho material granular basado en niacina tiene un tamaño de entre 0,1 y 0,5 milímetros.
14. Proceso según la reivindicación 11, 12 ó 13, en el que dicha matriz comprende una fracción en peso de ácido graso saturado C18 de entre el 40% y el 95% con respecto a la matriz.
15. Proceso según la reivindicación 14, en el que dicha fracción en peso de ácido graso saturado C18 está entre el 60% y el 80% con respecto a la matriz.
16. Proceso según cualquiera de las reivindicaciones 11 a 15, en el que dicho agente mineral es sulfato de calcio dihidratado.
17. Proceso según cualquiera de las reivindicaciones 11 a 16, en el que en dicha matriz se proporciona una cantidad eficaz de agente emulsionante.
18. Proceso según la reivindicación 17, en el que dicho agente emulsionante está basado en diestearato de propilenglicol.
19. Proceso según cualquiera de las reivindicaciones 11 a 18, en el que dicha niacina se mezcla con dicha matriz en una fracción en peso de entre el 40% y el 70% con respecto a la mezcla completa.
20. Proceso según cualquiera de las reivindicaciones 11 a 19, en el que dicha fase de mezcla se lleva a cabo a una temperatura de entre 60ºC y 75ºC.
21. Proceso según cualquiera de las reivindicaciones 11 a 20, en el que dicha mezcla se pulveriza en una cámara que tiene una temperatura por debajo de -5ºC.
22. Proceso según la reivindicación 21, en el que dicha mezcla se pulveriza en una cámara que tiene una temperatura de entre -20ºC y -25ºC.
23. Uso de un producto granular según se define en cualquiera de las reivindicaciones 1 a 10 en la producción de un medicamento para el tratamiento de la hipertensión arterial o la hipercolesterolemia.
24. Uso de un producto granular según se define en cualquiera de las reivindicaciones 1 a 10 como complemento alimenticio para seres humanos.
Patentes similares o relacionadas:
PREPARADO FARMACÉUTICO QUE COMPRENDE UN INGREDIENTE ACTIVO DISPERSADO SOBRE UNA MATRIZ, del 27 de Diciembre de 2011, de NYCOMED GMBH: Un preparado, en el que un ingrediente activo seleccionado del grupo de N-(3,5-dicloropirid-4-il)-3ciclopropilmetoxi-4-difluorometoxibenzamida (INN: roflumilast), el […]
COMPOSICIONES FARMACÉUTICAS ESTABILIZADAS QUE COMPRENDEN FESOTERODINA, del 23 de Diciembre de 2011, de UCB PHARMA GMBH: Una composición farmacéutica que comprende fesoterodina o una sal o solvato farmacéuticamente aceptable de la misma y un estabilizante farmacéuticamente […]
GRANULADO QUE CONTIENE UNA SUSTANCIA FARMACÉUTICAMENTE ACTIVA Y UN EMULSIONANTE Y MÉTODO PARA SU PRODUCCIÓN, del 12 de Diciembre de 2011, de ECHO PHARMACEUTICALS B.V: Un granulado con un diámetro medio ponderado en volumen de 1-200 µm y que contiene: - al menos 0,1 % en peso de una sustancia farmacéuticamente activa; - al menos 10 […]
ADMINISTRACIÓN PULMONAR DE AMINOGLUCÓSIDOS, del 8 de Septiembre de 2011, de NOVARTIS AG: Una composición de polvo seco dispersable para la administración localizada a los pulmones, para utilizar en el tratamiento o prevención de infecciones respiratorias, […]
NUEVA FORMA DE SUPOSITORIO QUE COMPRENDE UN COMPUESTO ACTIVO ÁCIDO-LÁBIL, del 5 de Julio de 2011, de NYCOMED GMBH: Un supositorio para compuestos activos ácido-lábiles, en donde el compuesto ácido-lábil es un inhibidor de la bomba de protones ácido-lábil, una sal […]
FORMULACIÓN FARMACEÚTICA QUE COMPRENDE ATORVASTANINA CÁLCICA, del 20 de Junio de 2011, de LEK PHARMACEUTICALS D.D.: Una formulación farmacéutica que comprende atorvastatina cálcica como ingrediente activo y una sustancia de ajuste del pH, caracterizada porque […]
 PROCEDIMIENTO PARA LA PREPARACIÓN DE MICROPARTÍCULAS, del 7 de Junio de 2011, de EVONIK ROHM GMBH: Procedimiento para la preparación de micropartículas, que comprende las etapas a) preparar una masa fundida de polímero que comprende al menos un polímero de soporte y […]
PROCEDIMIENTO PARA LA PREPARACIÓN DE MICROPARTÍCULAS, del 7 de Junio de 2011, de EVONIK ROHM GMBH: Procedimiento para la preparación de micropartículas, que comprende las etapas a) preparar una masa fundida de polímero que comprende al menos un polímero de soporte y […]
COMPOSICIÓN FARMACÉUTICA QUE COMPRENDE LOS DERIVADOS DE 2,3-DIHIDRO-6-NITROIMIDAZO[2,1-B]OXAZOL, del 28 de Marzo de 2011, de OTSUKA PHARMACEUTICAL CO., LTD.: Composición farmacéutica que comprende: (I) por lo menos un compuesto oxazol seleccionado de entre el grupo constituido por compuestos de 2,3-dihidro-6-nitroimidazo[2,1-b]oxazol […]