ESFINGOLIPIDOS.
Un compuesto para uso en el tratamiento de cáncer, estando el compuesto seleccionado entre:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IL01/00909.
Solicitante: YISSUM RESEARCH DEVELOPMENT COMPANY OF THE HEBREW UNIVERSITY OF JERUSALEM.
Nacionalidad solicitante: Israel.
Dirección: HI TECH PARK, EDMOND J. SAFRA CAMPUS, THE HEBREW UNIVERSITY OF JERUSALEM,<,91390 JERUSALEM.
Inventor/es: DAGAN,ARIEH, GATT,SHIMON.
Fecha de Publicación: .
Fecha Concesión Europea: 30 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- C07C215/10 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 215/00 Compuestos que contienen grupos amino e hidroxi unidos a la misma estructura carbonada. › con un grupo amino y al menos dos grupos hidroxi unidos a la estructura carbonada.
- C07C215/24 C07C 215/00 […] › y acíclica.
- C07C215/36 C07C 215/00 […] › Ari-1 amino-2 propanodioles-1,3.
- C07C215/68 C07C 215/00 […] › con grupos amino unidos a átomos de carbono de ciclos aromáticos de seis miembros y grupos hidroxi unidos a átomos de carbono acíclicos o a átomos de carbono de ciclos, distintos de los ciclos aromáticos de seis miembros, de la misma estructura carbonada.
- C07C233/43 C07C […] › C07C 233/00 Amidas de ácidos carboxílicos. › con el átomo de carbono del grupo carboxamido unido a un átomo de hidrógeno o a un átomo de carbono de una estructura carbonada saturada.
- C07C271/16 C07C […] › C07C 271/00 Derivados del ácido carbámico, es decir, compuestos que contienen uno de los grupos en que el átomo de nitrógeno no forma parte de grupos nitro o nitroso. › a átomos de carbono de radicales hidrocarbonados sustituidos por átomos de oxígeno unidos por enlaces sencillos.
- C07C271/20 C07C 271/00 […] › a átomos de carbono de radicales hidrocarbonados sustituidos por átomos de nitrógeno que no forman parte de grupos nitro o nitroso.
- C07C271/22 C07C 271/00 […] › a átomos de carbono de radicales hidrocarbonados sustituidos por grupos carboxilo.
- C07C311/04 C07C […] › C07C 311/00 Amidas de ácidos sulfónicos, es decir, compuestos en los que átomos de oxígeno, unidos por enlaces sencillos, de grupos sulfónicos han sido sustituidos por átomos de nitrógeno que no forman parte de grupos nitro o nitroso. › a átomos de carbono acíclicos de radicales hidrocarbonados sustituidos por átomos de oxígeno unidos por enlaces sencillos.
- C07F9/10 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › C07F 9/00 Compuestos que contienen elementos de los grupos 5 o 15 del sistema periódico. › Fosfátidos, p. ej. lecitina.
- C07F9/113 C07F 9/00 […] › con alcoholes acíclicos insaturados.
Clasificación PCT:
- A61K31/135 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos aromáticos, p. ej. metadona.
- A61K31/165 A61K 31/00 […] › teniendo ciclos aromáticos, p. ej. colchicina, atenolol, progabide.
- A61K31/66 A61K 31/00 […] › Compuestos del fósforo.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- A61P43/00 A61P […] › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- C07C215/24 C07C 215/00 […] › y acíclica.
- C07C215/28 C07C 215/00 […] › y conteniendo ciclos aromáticos de seis miembros.
- C07C215/68 C07C 215/00 […] › con grupos amino unidos a átomos de carbono de ciclos aromáticos de seis miembros y grupos hidroxi unidos a átomos de carbono acíclicos o a átomos de carbono de ciclos, distintos de los ciclos aromáticos de seis miembros, de la misma estructura carbonada.
- C07C233/43 C07C 233/00 […] › con el átomo de carbono del grupo carboxamido unido a un átomo de hidrógeno o a un átomo de carbono de una estructura carbonada saturada.
- C07C311/04 C07C 311/00 […] › a átomos de carbono acíclicos de radicales hidrocarbonados sustituidos por átomos de oxígeno unidos por enlaces sencillos.
- C07F9/113 C07F 9/00 […] › con alcoholes acíclicos insaturados.
Clasificación antigua:
- A61K31/135 A61K 31/00 […] › que tienen ciclos aromáticos, p. ej. metadona.
- A61K31/165 A61K 31/00 […] › teniendo ciclos aromáticos, p. ej. colchicina, atenolol, progabide.
- A61K31/66 A61K 31/00 […] › Compuestos del fósforo.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- A61P43/00 A61P […] › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- C07C215/24 C07C 215/00 […] › y acíclica.
- C07C215/28 C07C 215/00 […] › y conteniendo ciclos aromáticos de seis miembros.
- C07C215/68 C07C 215/00 […] › con grupos amino unidos a átomos de carbono de ciclos aromáticos de seis miembros y grupos hidroxi unidos a átomos de carbono acíclicos o a átomos de carbono de ciclos, distintos de los ciclos aromáticos de seis miembros, de la misma estructura carbonada.
- C07C233/43 C07C 233/00 […] › con el átomo de carbono del grupo carboxamido unido a un átomo de hidrógeno o a un átomo de carbono de una estructura carbonada saturada.
- C07C311/04 C07C 311/00 […] › a átomos de carbono acíclicos de radicales hidrocarbonados sustituidos por átomos de oxígeno unidos por enlaces sencillos.
- C07F9/113 C07F 9/00 […] › con alcoholes acíclicos insaturados.
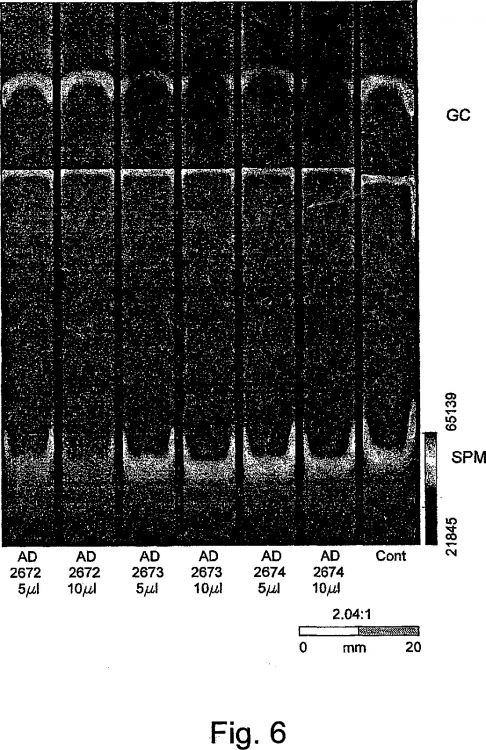
Fragmento de la descripción:
Esfingolípidos.
Antecedentes de la invención
Los esfingolípidos (SL) comprenden un grupo de lípidos que tienen ceramida, es decir, N-acilesfingosina, como el grupo básico. Existen dos tipos principales de SL, fosfoSL y glucoSL. En tanto que el primero tiene un componente principal es decir, esfingomielina (ceramida-fosforilcolina), los glucoesfingolípidos comprenden un amplio grupo. Abarcan desde mono-hexosilceramidas (ceramida ß-glucosa y ceramida ß-galactosa), pasando por oligohexosil ceramida (por ejemplo, di- y trihexosil ceramidas) hasta un gran número de gangliósidos compuestos de oligohexosil ceramidas a los cuales está también unido el ácido siálico. Los SLs están presentes prácticamente en cada tipo de célula y tejido y abundan particularmente en el sistema nervioso. La composición relativa del SL puede variar con la edad; de acuerdo con ello, se ha mostrado que la relación de esfingomielina a lecitina aumenta con la edad.
Los glucoesfingolípidos tienen un alto potencial de unión y actúan como receptores específicos para un cierto número de de agentes externos, por ejemplo, lectinas, toxinas, hormonas y virus. Ejemplo de ello son: la toxina vibrio cholerae se une al GM1-ganglósido y las verotoxinas Shigella dysenteriae a la globotriaosil ceramida.
Durante la pasada década, ha existido un enorme incremento de investigación sobre esfingolípidos debido a descubrimientos que implican a miembros de este grupo en procesos de transducción de señales [recientemente revisados por Levade y otros, en Biochem. Biophys. Acta, vol. 1438, págs. 1-17, (1999); Mathias y otros, Biochem. J., vol. 335, págs. 465-480, (1998); Perry y otros, Biochem. Biophys. Acta, vol. 1436, págs. 233-243, (1998); Riboni y otros, Prog. Lipid Res., vol. 36, págs. 153-195, (1997)]. El compuesto el más estudiado fue la ceramida, la cual se mostró que juega un papel en la regulación de procesos claves tales como inhibición, diferenciación y apoptosis del desarrollo [Hannun y otros, Biochem. Biophys. Acta, vol. 1154, págs. 223-236; Hannun y otros, Trends Cell Biol., vol. 10, págs. 73-80, (2001); Higgins y otros, Trends Biochem. Sci., vol. 17, págs. 18-21, (1982)]. El SPM se considera generalmente como la fuente metabólica primaria de ceramida cuya generación en una localización particular en la célula (por ejemplo, la membrana) la hace adecuada para la mediación en los procesos de señalización celular. Igualmente, se ha descrito una síntesis de novo incrementada de ceramida como una fuente potencial para la señalización [Bose y otros, Cell, vol. 82, págs. 405-414, (1995)], En consecuencia, se ha orientado un esfuerzo fundamental para modular la generación de ceramida intra-celular mediante esfingomielinasas, fundamentalmente la enzima unida a la membrana, neutra, aunque la enzima ácida ha sido también implicada. Sin embargo, debería hacerse hincapié que la modificación de los mecanismos de biosíntesis tales como la reducción de la conversión de ceramida a SPM o glucolípidos y, en paralelo, su hidrólisis mediante ceramidasas, incrementaría igualmente su concentración en la célula.
El papel de los esfingolípidos en la transducción de señal [revisada por Riboni y otros, en Progr. Lipid Res., vol. 36, págs. 153-195, (1997) y A Gomez-Munoz, Biochim. Biophys. Acta, vol. 1391, págs. 32-109, (1998)] ha sido ampliamente estudiada, y se propuso que operaba a través del "ciclo esfingomielina". De acuerdo con esta hipótesis, la unión de un ligando extracelular particular a su receptor activa una esfingomielinasa unida a la membrana del plasma, dando lugar a la ceramida, la cual actúa como un mediador de los efectos intracelulares del ligando. Numerosas publicaciones describen y enfatizan el papel de la ceramida en la muerte celular por apoptosis, así como su efecto sobre episodios celulares importantes tales como proliferación, diferenciación y reacción a condiciones de estrés. Son igualmente de particular interés los informes de que las ceramidas permeables a las células, de cadena corta (por ejemplo C2 o C6) evocan respuestas biológicas que conducen a la muerte de células. Otros estudios, que usan el precursor de ceramida, es decir, esfingosina, han mostrado sus efectos sobre el desarrollo y viabilidad de células. Además, se ha mostrado que la esfingosina inhibe la proteína quinasa C e incrementa la concentración intracelular de iones calcio. La forma fosforilada de la esfingosina, es decir, esfingosina-1-fosfato, se ha mostrado que es un potente activador de fosfolipasa D. Y la esfingosina di- o tri-metilada ha mostrado que inhibe el desarrollo de células de cáncer [Endo y otros, Cancer Research, vol. 51, págs. 1613-1618, (1981)].
Se ha estudiado la implicación del metabolismo de la ceramida y del esfingolípido en el cáncer. Se ha demostrado que la apoptosis inducida mediante la administración de una diversidad de agentes quimioterapéuticos está mediada por ceramida [Strum y otros, J. Biol. Chem., vol. 269, págs. 15493-15497, (1994); Maurer y otros, J. Natl. Cancer Inst., vol. 91, págs.1138-1146, (1999); Suzuki y otros, Exp. Cell Res., vol. 233, págs. 41-47, (1997)]. Se ha mostrado que las antraciclinas (por ejemplo, daunorubicina) inducen la acumulación de ceramida, lo cual posteriormente conduce a la muerte de células de cáncer [Bose y otros, Cell, vol. 82, págs. 405-414, (1995)]. La segunda línea de estudio mostró que las células de cáncer resistentes a fármacos difieren en su metabolismo esfingolípido de las sensibles a fármacos. A este respecto, es de especial interés los estudios de Cabot y otros [Lavie y otros, J. Biol. Chem., vol. 271, págs. 19530-19536, (1996)], los cuales han demostrado que la guclosilceramida, un producto metabólico directo de la ceramida, se elevó en diversas células resistentes a fármacos que sobre-expresan la bomba P-glucoproteína (Pgp). La sobre-expresión de la enzima que sintetiza este glucolípido, es decir, glucosilceramida sintetasa (GCS), mediante un sistema de expresión retrovírico, dio como resultado la conversión de células sensibles a la doxorubicina en unas resistentes [Liu y otros, J. Biol. Chem., vol. 274, págs. 1140-1146, (1999)]. Inversamente, la inhibición de la expresión de GCS, mediante tecnología antisentido, dio como resultado una sensibilidad incrementada a la doxorubicina. Cabot y otros, han propuesto igualmente que moduladores de resistencia a fármacos tales como tamoxifeno, verapamil y el análogo de ciclosporina, PSC 833, ejercen su efecto mediante la inhibición de GCS [Cabot y otros, FEBS Letters, vol. 394, págs. 129-131, (1996), FEBS Letters, vol. 431, págs.. 185-199, (1998); Lavie y otros, J. Biol. Chem., vol. 272, págs. 1682-1687, (1999); Lucci y otros, Cancer, vol. 86, págs. 300-311, (1999)], dando como resultado un incremento de ceramida celular. Nicholson y otros (British J. Cancer, vol. 81, págs. 423-430, (1989)], han mostrado que un inhibidor de GCS, 1-fenil-2-decanoil-amino-3-morfolino-1-propanol, mató de manera preferencial células resistentes a multifármacos, en comparación con sus contrapartes sensibles a fármacos. Tomados en su conjunto, los estudios anteriores sugieren un mecanismo metabólico que en células MDR disminuye su contenido en ceramida mediante su conversión a glucosilceramida, haciéndola resistente a una serie de fármacos quimioterapéuticos.
De especial interés es el mecanismo propuesto por el fármaco anti-cáncer hexadecilfosfocolina [HePC, Wieder y otros, J. Biol. Chem., vol. 273, págs.. 11025-11031, (1998)]. Este es un fármaco antiproliferativo, el cual se usa actualmente para el tratamiento de metástasis extrañas de carcinoma mamario y del que se ha mostrado que induce apoptosis a una concentración de 25 µM. La publicación anterior proporciona la prueba de que la HePC, la cual inhibe la biosíntesis de fosfatidilcolina, ejerce un efecto secundario al disminuir la biosíntesis de esfingomielina y, en consecuencia, incrementar los niveles de ceramida y probablemente esta última sea la responsable de las propiedades pro-apóptoticas de la HePC. Y, por tanto, los autores mostraron que la apoptosis inducida por PC fue bloqueada por Fumonisin B1, un inhibidor de la síntesis de ceramida. Y, que las ceramidas permeables a la membrana, de cadena corta, incrementaron de manera aditiva el efecto apoptótico de la HePC.
Otro aspecto principal del metabolismo de los esfingolípidos es su acumulación en los órganos de pacientes afligidos con las enfermedades genéticas de almacenamiento de lípidos, tal como la enfermedad...
Reivindicaciones:
1. Un compuesto para uso en el tratamiento de cáncer, estando el compuesto seleccionado entre:

2. Una composición farmacéutica para uso en el tratamiento de cáncer, que comprende como ingrediente activo un compuesto de acuerdo con la reivindicación 1, y opcionalmente comprende además un vehículo, adyuvante o diluyente aceptable farmacéuticamente.
3. Un compuesto de acuerdo con la reivindicación 1, en el que el tratamiento de cáncer comprende la muerte de células de cáncer de tipo salvaje y resistentes a fármacos.
4. Un compuesto de acuerdo con la reivindicación 3, en el que dicha muerte es la muerte selectiva de células de cáncer resistentes a fármacos.
5. Un compuesto seleccionado entre AD-2646, AD-2672, y AD-2754:
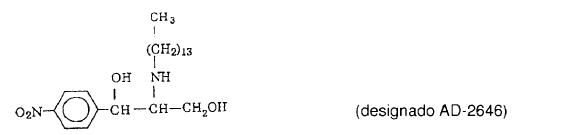

6. Uso de un compuesto de acuerdo con la reivindicación 1 en la preparación de un medicamento para el tratamiento de cáncer.
Patentes similares o relacionadas:
Enlazadores sensibles al pH para suministrar un agente terapéutico, del 8 de Abril de 2020, de GNT Biotech & Medicals Corporation: Un enlazador sensible al pH que tiene la siguiente fórmula (I), **(Ver fórmula)** en donde X es **(Ver fórmula)** -SH, -NH2, Boc-NH-, Fmoc-NH-, -COOH; n […]
Proceso de preparación de N-boc bifenil alaninol, del 26 de Febrero de 2020, de Chiral Quest (suzhou) Co., Ltd: Un proceso para preparar compuesto 4, que comprende en uno de los disolventes alcohólicos, hidrogenación asimétrica de 5 en presencia de [Rh(Duanphos)(X)]Y e hidrógeno […]
Fabricación de 4,5,6,7-tetrahidroisozaxolo[5,4-c]piridin-3-ol, del 26 de Febrero de 2020, de H. LUNDBECK A/S: Un procedimiento para la fabricación del compuesto de fórmula VI a continuación, **(Ver fórmula)** en donde tanto R1 como R2 son o metilo o etilo, comprendiendo […]
Procesos para la preparación de compuestos de pirimidinilciclopentano, del 23 de Octubre de 2019, de F. HOFFMANN-LA ROCHE AG: Un proceso para la preparación de un compuesto de fórmula (I) **(Ver fórmula)** o sales del mismo, que comprende la reacción de acoplamiento […]
Compuesto capaz de unirse al receptor de S1P y uso farmacéutico del mismo, del 25 de Septiembre de 2019, de ONO PHARMACEUTICAL CO., LTD.: Un compuesto representado por la formula (I-S-7a):**Fórmula** en el que el anillo A representa un grupo carbociclico C3-15; X representa un enlace o un grupo […]
Modificaciones de proteínas quimioenzimáticas específicas para lisina utilizando transglutaminasa microbiana, del 21 de Agosto de 2019, de NOVARTIS AG: Un método para modificar una proteína, que comprende: proporcionar una proteína diana que tiene al menos un residuo de lisina; poner […]
N-Fenil-1-sulfonil-2-pirrolidinacarboxamidas para la identificación de actividad biológica y farmacológica, del 16 de Agosto de 2019, de INSTITUT UNIV. DE CIENCIA I TECNOLOGÍA, S.A: Un compuesto de fórmula (I) **(Ver fórmula)** y las sales y estereoisómeros del mismo, donde R1 es hidrógeno, halo, hidroxilo, nitro, ciano, […]
Procedimientos para la preparación de derivados ácidos de GalNAc, del 3 de Julio de 2019, de F. HOFFMANN-LA ROCHE AG: Procedimiento para la preparación de derivados ácidos de GalNAc de fórmula I **Fórmula** en la que n es un número entero entre 0 y 10, y sus sales, sus enantiómeros correspondientes […]