DERIVADOS DE PIRIMIDINA LIGADOS A HETEROALQUILO.
Compuesto de la fórmula (I):
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/SG2006/000353.
Solicitante: S*BIO PTE LTD.
Nacionalidad solicitante: Singapur.
Dirección: 1 SCIENCE PARK ROAD, 05-09 THE CAPRICORN,SINGAPORE SCIENCE PARK II, SIN.
Inventor/es: SUN, ERIC T., BLANCHARD, STEPHANIE, ETHIRAJULU,KANTHARAJ, LEE,CHENG HSIA,ANGELINE, NAGARAJ,HARISH,KUMAR,MYSORE, POULSEN,ANDERS, TAN,YEE LING,EVELYN, TEO,EE LING, WILLIAM,ANTHONY,DEODAUNIA.
Fecha de Publicación: .
Fecha Concesión Europea: 26 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07D498/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 498/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tienen átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo (4-oxa-1-azabiciclo [3.2.0] heptanos, p. ej. oxapenicilinas C07D 503/00; 5-oxa-1-azabiciclo [4.2.0] octanos, p. ej. oxacefalosporinas C07D 505/00; aquéllos de sus análogos que tienen el átomo de oxígeno del ciclo en otra posición C07D 507/00). › Sistemas peri-condensados.
- C07D498/16 C07D 498/00 […] › Sistemas peri-condensados.
- C07D515/16 C07D […] › C07D 515/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tiene átomos de nitrógeno, oxígeno y azufre como únicos heteroátomos del ciclo, no previstos en los grupos C07D 463/00, C07D 477/00 ó C07D 499/00 - C07D 507/00. › Sistemas peri-condensados.
Clasificación PCT:
- A61K31/505 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Pirimidinas; Pirimidinas hidrogenadas, p. ej. trimetoprima.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- A61P35/02 A61P […] › A61P 35/00 Agentes antineoplásicos. › específicos para la leucemia.
- C07D495/12 C07D […] › C07D 495/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tiene átomos de azufre como únicos heteroátomos del ciclo. › en los que el sistema condensado contiene tres heterociclos.
- C07D498/02 C07D 498/00 […] › en los que el sistema condensado contiene dos heterociclos.
- C07D498/12 C07D 498/00 […] › en los que el sistema condensado contiene tres heterociclos.
Fragmento de la descripción:
Derivados de pirimidina ligados a heteroalquilo.
Campo de la invención
La presente invención se refiere a compuestos de pirimidina que pueden ser útiles como agentes antiproliferativos. Más en particular, la presente invención se refiere a compuestos de pirimidina ligados a y sustituidos por heteroalquilo, a métodos para su preparación, a composiciones farmacéuticas que contienen a dichos compuestos. Estos compuestos pueden ser útiles como medicamentos para el tratamiento de un número de trastornos proliferativos incluyendo tumores y cánceres así como otras afecciones o trastornos asociados con cinasas.
Antecedentes de la invención
Los trastornos proliferativos tales como cáncer se caracterizan por el crecimiento incontrolado de células dentro del cuerpo. Los trastornos proliferativos como tal implican generalmente una anormalidad en el control del crecimiento y/o división celular que conduce a la formación del tumor y finalmente a la muerte. Sin desear estar limitados por la teoría se cree que esto es causado por la alteración de las rutas que regulan el crecimiento y división celular en las células del cáncer. La alteración es tal que los efectos de estos mecanismos reguladores normales para controlar el crecimiento y división celular fallan o se evitan.
El crecimiento y/o división celular incontrolados finalmente resultan fatales para el paciente debido a que rondas sucesivas de mutaciones por parte de la célula típicamente conducen entonces a que las células de cáncer tengan una ventaja selectiva sobre las células sanas normales en el cuerpo del paciente, lo que lleva a que las células de cáncer predominen en la masa celular del paciente. Las células de cáncer típicamente experimentan después metástasis para colonizar otros tejidos o partes del cuerpo diferentes a la parte de origen de la célula de cáncer lo que conduce a tumores secundarios que eventualmente conducen al fallo de órganos y a la muerte del paciente. Es la dificultad para controlar el rápido crecimiento y división celular que son característicos de las células de cáncer lo que hace difícil obtener estrategias quimioterapéuticas efectivas.
Un número de tratamientos tradicionales para trastornos proliferativos tales como el cáncer buscan tomar ventaja de su capacidad proliferativa más alta y por lo tanto mayor sensibilidad al daño al ADN. Los tratamientos que se han utilizado incluyen radiación ionizante (rayos ?, rayos X y similares) así como agentes citotóxicos tales como bleomicina, cis-platina, vinblastina, ciclofosfamida, 5'-fluorouracilo y metotrexato. Todos estos tratamientos se basan en ocasionar daño al ADN y en la desestabilización de la estructura cromosómica lo que eventualmente conduce a la muerte de las células de cáncer.
El problema con muchas de estas estrategias es que éstas son no selectivas para células de cáncer y las células sanas pueden, y con frecuencia son afectadas de manera adversa por el tratamiento. Esto es difícilmente sorprendente dado que los mecanismos celulares elegidos como blanco por estas estrategias tienen lugar tanto en células sanas así como en células de cáncer (aunque típicamente a velocidades más lentas) y únicamente sirve para resaltar la dificultad para lograr el tratamiento exitoso del cáncer en el paciente sin ocasionar daño irreparable a las células sanas. Con muchos de estos tratamientos como tal puede haber efectos secundarios devastadores los cuales pueden no sólo reducir en forma significativa la calidad de vida a corto plazo del paciente, sino que también pueden tener perjuicios a largo plazo sobre la salud del paciente en caso que estos sobrevivan al ataque de cáncer.
Aunque algunos de los problemas anteriores se han superado sustancialmente mediante el desarrollo de agentes anti-cáncer selectivos (tales como tamoxifeno) la efectividad de todos los agentes quimioterapéuticos está sujeta al desarrollo de resistencia a los fármacos por parte de las células de cáncer en el paciente. El desarrollo de resistencia a fármacos en las células de cáncer de un paciente tiende a ser específica de clase y, por lo tanto, si las células de cáncer de un paciente desarrollan resistencia a fármacos para una clase de fármacos anti-cáncer, entonces todos los compuestos dentro de dicha clase se vuelven típicamente inefectivos en el tratamiento adicional de dicho paciente. Por lo tanto, en la mejora de los resultados clínicos para los pacientes la identificación de agentes quimioterapéuticos alternativos es esencial para proporcionar al oncólogo de un arsenal de fármacos que se puedan utilizar en cualquier situación dada.
El desarrollo de diferentes clases de agentes terapéuticos es por lo tanto importante debido a que esto puede ayudar a evitar el desarrollo de resistencia a fármacos y también se puede utilizar en terapias de combinación. Dichas terapias de combinación típicamente implican el uso de fármacos anti-cáncer con diferentes propiedades y objetivos celulares lo que a su vez tiende a incrementar la efectividad general de cualquier régimen de quimioterapia elegido y limita la posibilidad de que se desarrolle resistencia a fármacos en el paciente.
Uno de los mayores avances en la investigación del cáncer ha sido la validación clínica de fármacos dirigidos molecularmente que inhiben la actividad de proteína cinasas. Los inhibidores de cinasa de molécula pequeña que actualmente están aprobados para indicaciones en oncología incluyen imatinib, gefitinib, erlotinib, sorafenib, sunitinib y dasatinib [Baselga J., Science, 2006, 312, 1175-1178]. Un número de cinasas tales como JAK2, FLT3 y CDK2 son objetivos de cinasa prometedores para intervención farmacológica en tumores sólidos, enfermedades hematológicas malignas, trastornos mielo-proliferativos y trastornos proliferativos no malignos como los queloides. Las cinasas Janus (JAK) son una familia de tirosina cinasas citoplasmáticas que consisten en JAK1, JAK2, JAK3 y Tyk2. Estas juegan un papel fundamental en las rutas de señalización de numerosas citocinas, hormonas y factores de crecimiento [Rawlings JS et al, J. Cell Sci., 2004, 117, 1281-1283]. Sus substratos intracelulares incluyen la familia de proteínas llamadas Transductor de Señal y Activador de Transcripción (STAT por sus siglas en inglés). Las rutas de JAK-STAT, a través de las acciones apropiadas de los ligandos, regulan procesos fisiológicos importantes tales como la respuesta inmune a los virus, eritropoyesis, lactación, homeostasis de lípidos, etc. Sin embargo, la señalización disfuncional ocasionada por una multitud de factores da como resultado afecciones fisiopatológicas tales como alergias, asma, artritis reumatoide, deficiencia inmune combinada severa, enfermedades hematológicas malignas, etc. En particular, las mutaciones en JAK2 se han asociado con trastornos mielo-proliferativos (incluyendo policitemia vera, trombocitemia esencial y mielofibrosis idiopática) y una gama amplia de leucemias y linfomas [Percy MJ et al, Hematol. Oncol., 2005, 23, 91-93). Como un aspecto importante, los trastornos mielo-proliferativos pertenecen a un área de necesidad médica no satisfecha en la cual algunas realizaciones de tratamiento no se han actualizado a lo largo de las últimas décadas [Schafer AI, Blood, 2006, 107, 4214-4222].
Los trastornos mielo-proliferativos (MPD por sus siglas en inglés) pertenecen a un grupo de enfermedades hematológicas malignas que surgen de la expansión de clones de células madre progenitoras mutadas en la médula ósea. La asociación de un MPD, leucemia mieloide crónica, con el cromosoma Filadelfia se ha documentado bien. Los MPDs Filadelfia-negativos incluyen Trombocitopenia Esencial (ET), Policitemia Vera (PV) y Mielofibrosis Idiopática Crónica (MF). Actualmente no se dispone de ningún tratamiento efectivo. El descubrimiento reciente de que una sola mutación somática adquirida en JAK2 parece ser la responsable de muchas de las características de estos MPDs promete impactar la diagnosis y tratamiento de pacientes con estos trastornos e impulsar la investigación adicional en los orígenes del crecimiento y funcionamiento celular des-regulados. Hasta hace poco, se consideraba que la mayoría de los MPDs eran enfermedades raras o huérfanas pero los estudios que se están efectuando sugieren una predominancia mucho más alta.
La Trombocitopenia Esencial es un MPD crónico caracterizado por un número incrementado de plaquetas en circulación, hiperplasia megacariocítica de médula profunda, esplenomegalia y un curso clínico acentuado por episodios hemorrágicos o trombóticos o ambos. Las opciones de tratamiento actuales incluyen...
Reivindicaciones:
1. Compuesto de la fórmula (I):
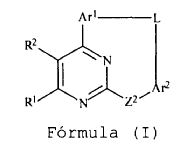
en la cual:
R1 y R2 se seleccionan cada uno de manera independiente a partir del grupo que consiste en: H, halógeno, alquilo, alquenilo, alquinilo, halogenoalquilo, halogenoalquenilo, heteroalquilo, cicloalquilo, cicloalquenilo, heterocicloalquilo, heterocicloalquenilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo, arilalquenilo, cicloalquilheteroalquilo, heterocicloalquilheteroalquilo, heteroarilheteroalquilo, arilheteroalquilo, hidroxi, hidroxialquilo, alcoxi, alcoxialquilo, alcoxiarilo, alqueniloxi, alquiniloxi, cicloalquiloxi, heterocicloalquiloxi, ariloxi, arilalquiloxi, fenoxi, benciloxi, heteroariloxi, amino, alquilamino, aminoalquilo, acilamino, arilamino, sulfonilamino, sulfinilamino, -COOH, -COR3, -COOR3, -CONHR3, -NHCOR3, -NHCOOR3, -NHCONHR3, alcoxicarbonilo, alquilaminocarbonilo, sulfonilo, alquilsulfonilo, alquilsulfinilo, arilsulfonilo, arilsulfinilo, aminosulfonilo, -SR3, R4S(O)R6-, R4S(O)2R6-, R4C(O)N(R5)R6-, R4SO2N(R5)R6-, R4N(R5)C(O)R6-, R4N(R5)SO2R6-, R4N(R5)C(O)N(R5)R6- y acilo, cada uno de los cuales puede estar opcionalmente sustituido;
cada R3, R4, y R5 se selecciona de manera independiente a partir del grupo que consiste en H, alquilo, alquenilo, alquinilo, halogenoalquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo y acilo, cada uno de los cuales puede estar opcionalmente sustituido;
cada R6 se selecciona de manera independiente a partir del grupo que consiste en un enlace, alquilo, alquenilo, alquinilo, halogenoalquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo y acilo, cada uno de los cuales puede estar opcionalmente sustituido;
Z2 se selecciona a partir del grupo que consiste en un enlace, O, S, -N(R7)-, -N(R7)-alquil(C1-2)-, y -alquil(C1-2)-N(R7)-;
cada R7 se selecciona de manera independiente a partir del grupo que consiste en H, alquilo, alquenilo, alquinilo, halogenoalquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo y acilo, cada uno de los cuales puede estar opcionalmente sustituido;
Ar1 y Ar2 se seleccionan de manera independiente a partir del grupo que consiste en arilo y heteroarilo, cada uno de los cuales puede estar opcionalmente sustituido;
L es un grupo de la fórmula:
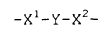
en la cual X1 está unido a Ar1 y X2 está unido a Ar2, y en la cual X1, X2 e Y se seleccionan de manera tal que el grupo L tenga entre 5 y 15 átomos en la cadena normal,
X1 y X2 son cada uno de manera independiente un grupo heteroalquilo opcionalmente sustituido de modo tal que X1 y X2 no sean ambos grupos heteroalquilo que contengan por lo menos un átomo de oxígeno en la cadena normal,
Y es un grupo de la fórmula -CRa=CRb- o un grupo cicloalquilo opcionalmente sustituido,
caracterizado porque Ra y Rb se seleccionan cada uno de manera independiente a partir del grupo que consiste en H, alquilo, alquenilo, alquinilo, halogenoalquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo y acilo, cada uno de los cuales puede estar opcionalmente sustituido, o
Ra y Rb se pueden unir de modo tal que cuando se toman junto con los átomos de carbono a los cuales éstos están unidos éstos forman un grupo cicloalquenilo o cicloheteroalquenilo;
o una sal o N-óxido de los mismos farmacéuticamente aceptable.
2. Compuesto de conformidad con la reivindicación 1, caracterizado porque Z2 es -N(H)-.
3. Compuesto de conformidad con la reivindicación 1 o 2, caracterizado porque Ar1 se selecciona a partir del grupo que consiste en:
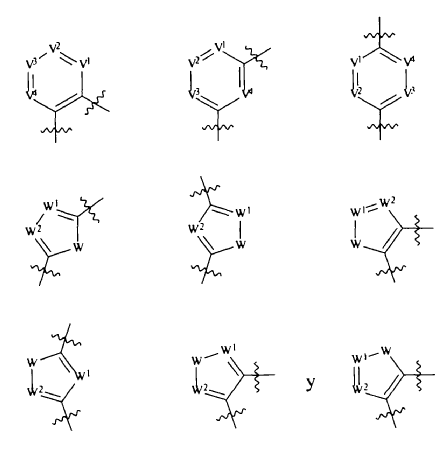
en los cuales V1, V2, V3 y V4 se seleccionan cada uno de manera independiente a partir del grupo que consiste en N, y C(R10);
W se selecciona a partir del grupo que consiste en O, S y N(R10);
W1 y W2 se seleccionan cada uno de manera independiente a partir del grupo que consiste en N y C(R10);
en los cuales cada R10 se selecciona de manera independiente a partir del grupo que consiste en: H, halógeno, alquilo, alquenilo, alquinilo, halogenoalquilo, halogenoalquenilo, heteroalquilo, cicloalquilo, cicloalquenilo, heterocicloalquilo, heterocicloalquenilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo, arilalquenilo, cicloalquilheteroalquilo, heterocicloalquilheteroalquilo, heteroarilheteroalquilo, arilheteroalquilo, hidroxi, hidroxialquilo, alcoxi, alcoxialquilo, alcoxiarilo, alqueniloxi, alquiniloxi, cicloalquiloxi, heterocicloalquiloxi, ariloxi, arilalquiloxi, fenoxi, benciloxi, heteroariloxi, amino, alquilamino, aminoalquilo, acilamino, arilamino, sulfonilamino, sulfinilamino, -COOH, -COR3, -COOR3, -CONHR3, -NHCOR3, -NHCOOR3, -NHCONHR3, alcoxicarbonilo, alquilaminocarbonilo, sulfonilo, alquilsulfonilo, alquilsulfinilo, arilsulfonilo, arilsulfinilo, aminosulfonilo, -SR3, R4S(O)R6-, R4S(O)2R6-, R4C(O)N(R5)R6-, R4SO2N(R5)R6-, R4N(R5)C(O)R6-, R4N(R5)SO2R6-, R4N(R5)C(O)N(R5)R6- y acilo, cada uno de los cuales puede estar opcionalmente sustituido,
en los cuales R3, R4, R5 y R6 son como se definieron en la reivindicación 1.
4. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 3, caracterizado porque Ar1 se selecciona a partir del grupo que consiste en:

en los cuales
R10 es como se definió en la reivindicación 3,
k es un número entero que se selecciona a partir del grupo que consiste en 0, 1, 2, 3, y 4;
n es un número entero que se selecciona a partir del grupo que consiste en 0, 1, 2, y 3; y
q es un número entero que se selecciona a partir del grupo que consiste en 0, 1, y 2.
5. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 4, caracterizado porque Ar2 es un grupo que se selecciona a partir del grupo que consiste en:
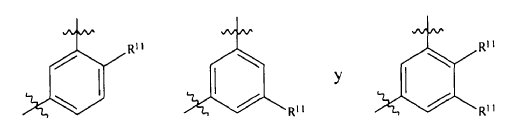
en los cuales cada R11 se selecciona de manera independiente a partir del grupo que consiste en: H, halógeno, alquilo, alquenilo, alquinilo, halogenoalquilo, halogenoalquenilo, heteroalquilo, cicloalquilo, cicloalquenilo, heterocicloalquilo, heterocicloalquenilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo, arilalquenilo, cicloalquilheteroalquilo, heterocicloalquilheteroalquilo, heteroarilheteroalquilo, arilheteroalquilo, hidroxi, hidroxialquilo, alcoxi, alcoxialquilo, alcoxiarilo, alqueniloxi, alquiniloxi, cicloalquiloxi, heterocicloalquiloxi, ariloxi, arilalquiloxi, fenoxi, benciloxi, heteroariloxi, amino, alquilamino, aminoalquilo, acilamino, arilamino, sulfonilamino, sulfinilamino, -COOH, -COR3, -COOR3, -CONHR3, -NHCOR3, -NHCOOR3, -NHCONHR3, alcoxicarbonilo, alquilaminocarbonilo, sulfonilo, alquilsulfonilo, alquilsulfinilo, arilsulfonilo, arilsulfinilo, aminosulfonilo, -SR3, R4S(O)R6-, R4S(O)2R6-, R4C(O)N(R5)R6-, R4SO2N(R5)R6-, R4N(R5)C(O)R6-, R4N(R5)SO2R6-, R4N(R5)C(O)N(R5)R6- y acilo, cada uno de los cuales puede estar opcionalmente sustituido.
6. Compuesto de conformidad con cualquiera de las reivindicaciones precedentes, caracterizado porque el compuesto es de la fórmula:
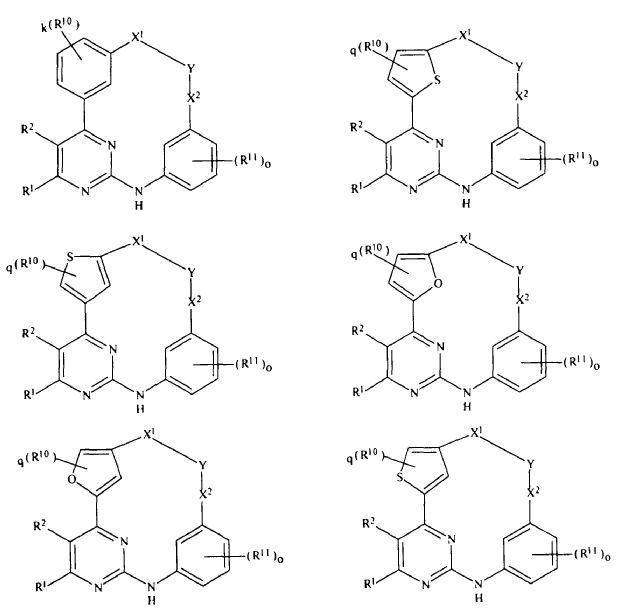
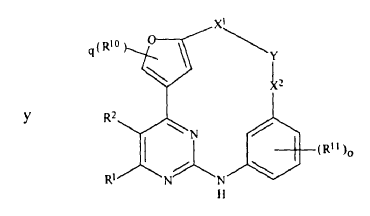
en las cuales
R1, R2, R10, R11, k, X1, X2, Y, q y "o" son como se definieron anteriormente,
o una sal farmacéuticamente aceptable de los mismos.
7. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 6, caracterizado porque X1 se selecciona a partir del grupo que consiste en:
8. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 7, caracterizado porque X1 se selecciona a partir del grupo que consiste en:
9. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 8, caracterizado porque X1 es -OCH2CH2-.
10. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 9, caracterizado porque X2 se selecciona a partir del grupo que consiste en:
en los cuales R8b se selecciona a partir del grupo que consiste en: H, halógeno, alquilo, alquenilo, alquinilo, halogenoalquilo, halogenoalquenilo, heteroalquilo, cicloalquilo, cicloalquenilo, heterocicloalquilo, heterocicloalquenilo, arilo, heteroarilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo, arilalquenilo, cicloalquilheteroalquilo, heterocicloalquilheteroalquilo, heteroarilheteroalquilo, arilheteroalquilo, hidroxi, hidroxialquilo, alcoxi, alcoxialquilo, alcoxiarilo, alqueniloxi, alquiniloxi, cicloalquiloxi, heterocicloalquiloxi, ariloxi, arilalquiloxi, fenoxi, benciloxi, heteroariloxi, amino, alquilamino, aminoalquilo, acilamino, arilamino, sulfonilamino, sulfinilamino, -COOH, -COR3, -COOR3, -CONHR3, -NHCOR3, -NHCOOR3, -NHCONHR3, alcoxicarbonilo, alquilaminocarbonilo, sulfonilo, alquilsulfonilo, alquilsulfinilo, arilsulfonilo, arilsulfinilo, aminosulfonilo, SR3, R4S(O)R5-, R4S(O)2R5-, R4C(O)N(R5)R6-, R4SO2N(R5)R6-, R4N(R5)C(O)R6-, R4N(R5)SO2R6-, R4N(R5)C(O)N(R5)R6- y acilo, cada uno de los cuales puede estar opcionalmente sustituido.
11. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 10, caracterizado porque X2 se selecciona a partir del grupo que consiste en:
en los cuales R8b es como se define en la reivindicación 10.
12. Compuesto de conformidad con la reivindicación 1, que se selecciona a partir del grupo que consiste en:
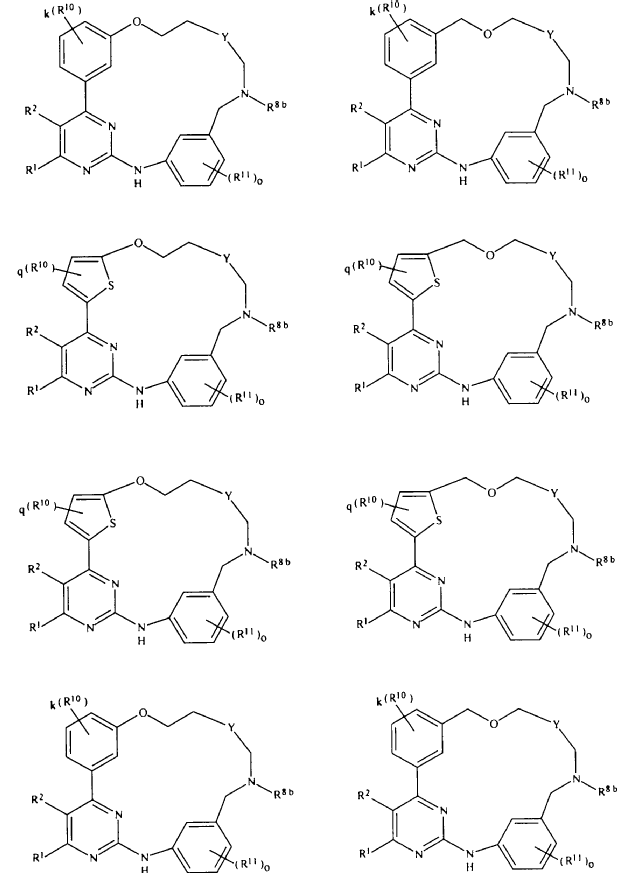
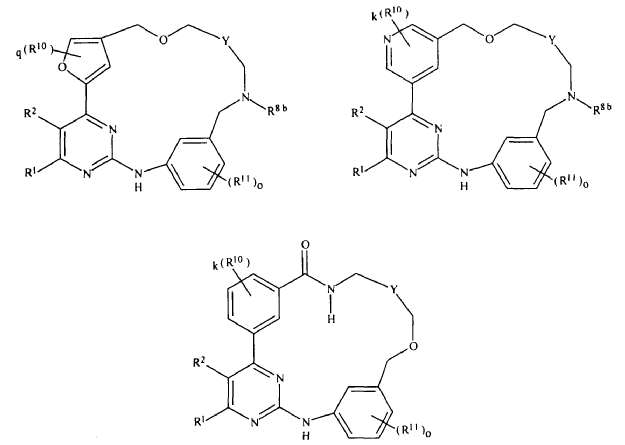
en las cuales
R1, R2, R10, R11, k, Y, q y "o" son como se definieron anteriormente,
o una sal farmacéuticamente aceptable de los mismos.
13. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 12, caracterizado porque R1 y R2 son H.
14. Compuesto de conformidad con cualquiera de las reivindicaciones 3, 4, 6 o 12, caracterizado porque R10 se selecciona a partir del grupo que consiste en H, halógeno, amino, alquilo, halogenoalquilo, halogenoalquenilo, heterocicloalquilo, arilo, cicloalquilalquilo, heterocicloalquilalquilo, arilalquilo, heteroarilalquilo, cicloalquilheteroalquilo, heterocicloalquilheteroalquilo, heteroarilheteroalquilo, arilheteroalquilo, hidroxi, hidroxialquilo, alcoxi, y alcoxialquilo, cada uno de los cuales puede estar opcionalmente sustituido.
15. Compuesto de conformidad con cualquiera de las reivindicaciones 3, 4, 6, 12 o 14, caracterizado porque R10 se selecciona a partir del grupo que consiste en H, hidroxilo, metoxi, fluoro, metilo, etilo, propilo, butilo, pentilo, hexilo, fenilo, y 2-morfolino-etoxi, cada uno de los cuales puede estar opcionalmente sustituido.
16. Compuesto de conformidad con cualquiera de las reivindicaciones 3, 4, 6, 12, 14 o 15, caracterizado porque cada R11 se selecciona de manera independiente a partir del grupo que consiste en H, alcoxi, heteroalquilo, heterocicloalquilo, heterocicloalquilheteroalquilo, heteroarilheteroalquilo, y arilsulfoniloxi, cada uno de los cuales puede estar opcionalmente sustituido.
17. Compuesto de conformidad con cualquiera de las reivindicaciones 3, 4, 6, 12, 14, 15 o 16, caracterizado porque cada R11 se selecciona de manera independiente a partir del grupo que consiste en:
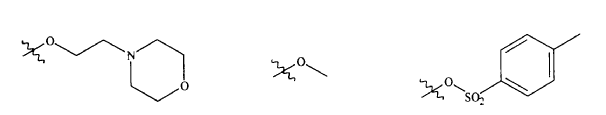
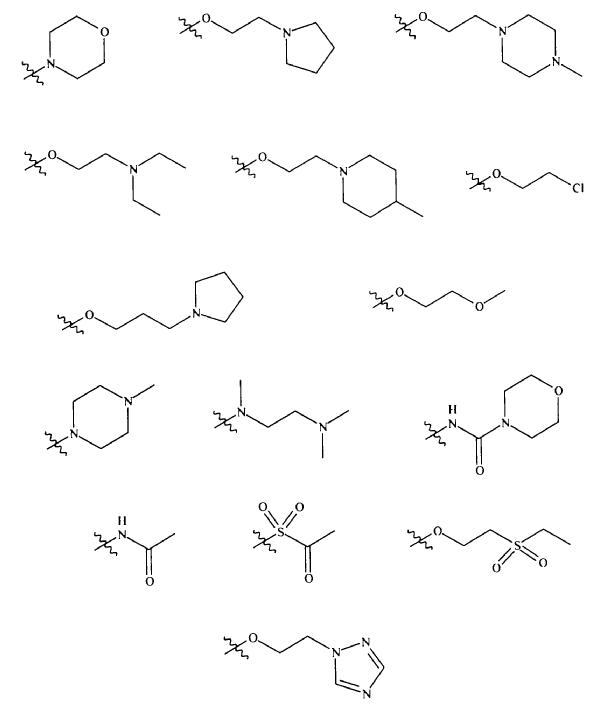
18. Compuesto de conformidad con cualquiera de las reivindicaciones 10, 11 o 12, caracterizado porque R8b se selecciona a partir del grupo que consiste en H, metilo, ciclopropilmetilo, 2-piridinil-metilo, ciclopropilo, 2-metilpropilo, 2,2-dimetil-propilo, trifluoroacetilo, -COCH2NHCH(CH3)2, y N-morfolino-carboxilo.
19. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 18, caracterizado porque el sustituyente opcional se selecciona a partir del grupo que consiste en: halógeno, =O, =S, -CN, -NO2, -CF3, -OCF3, alquilo, alquenilo, alquinilo, halogenoalquilo, halogenoalquenilo, halogenoalquinilo, heteroalquilo, cicloalquilo, cicloalquenilo, heterocicloalquilo, heterocicloalquenilo, arilo, heteroarilo, hidroxi, hidroxialquilo, alcoxi, alcoxialquilo, alcoxiarilo, alcoxiheteroarilo, alqueniloxi, alquiniloxi, cicloalquiloxi, cicloalqueniloxi, heterocicloalquiloxi, heterocicloalqueniloxi, ariloxi, heteroariloxi, arilalquilo, heteroarilalquilo, arilalquiloxi, -amino, alquilamino, acilamino, aminoalquilo, arilamino, sulfonilo, alquilsulfonilo, arilsulfonilo, aminosulfonilo, aminoalquilo, alcoxialquilo, -COOH, -COR5, -C(O)OR5, -SH, -SR5, -OR6 y acilo.
20. Compuesto de conformidad con la reivindicación 1, que se selecciona a partir del grupo que consiste en:
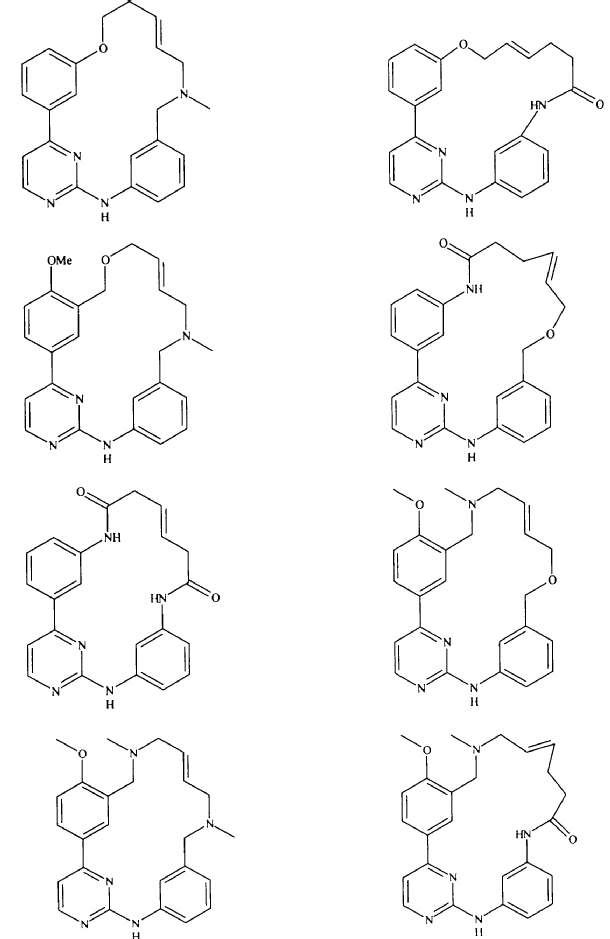
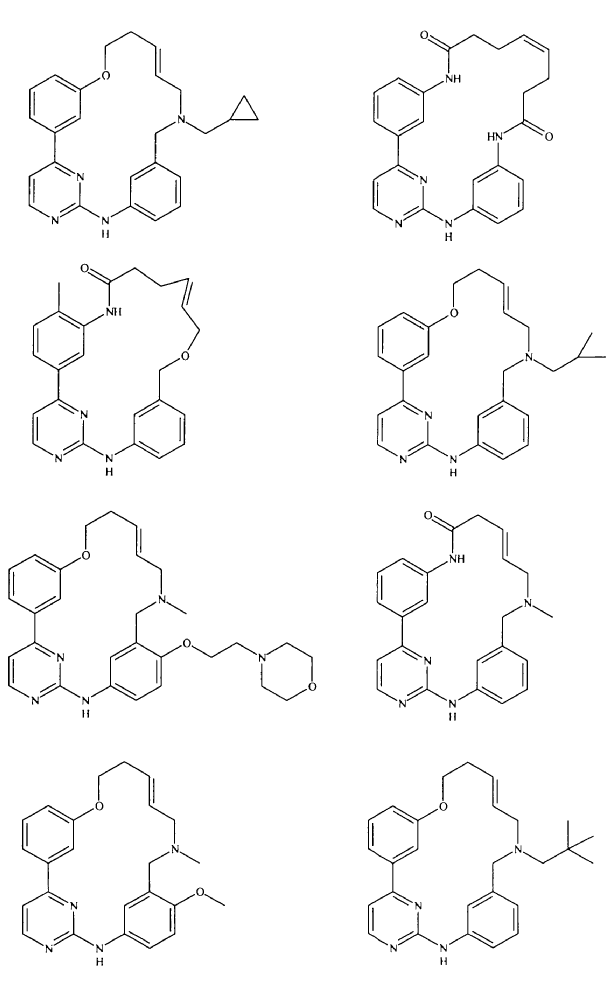
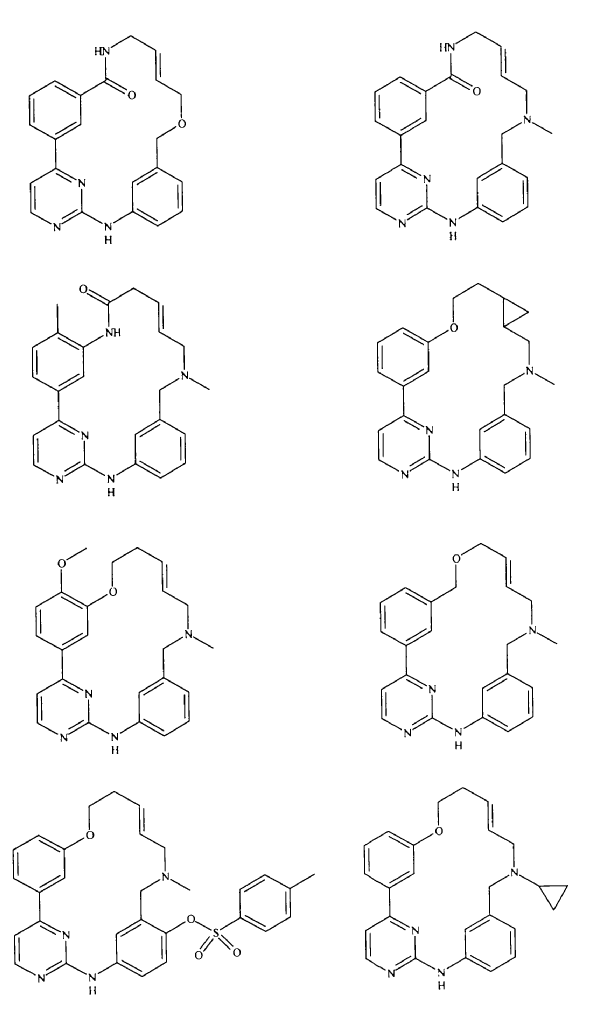
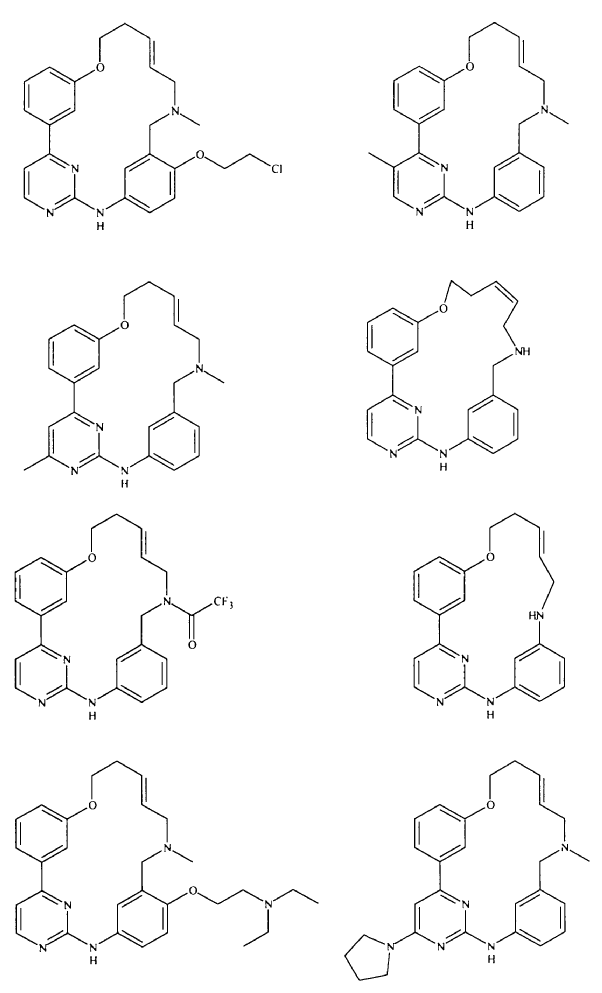
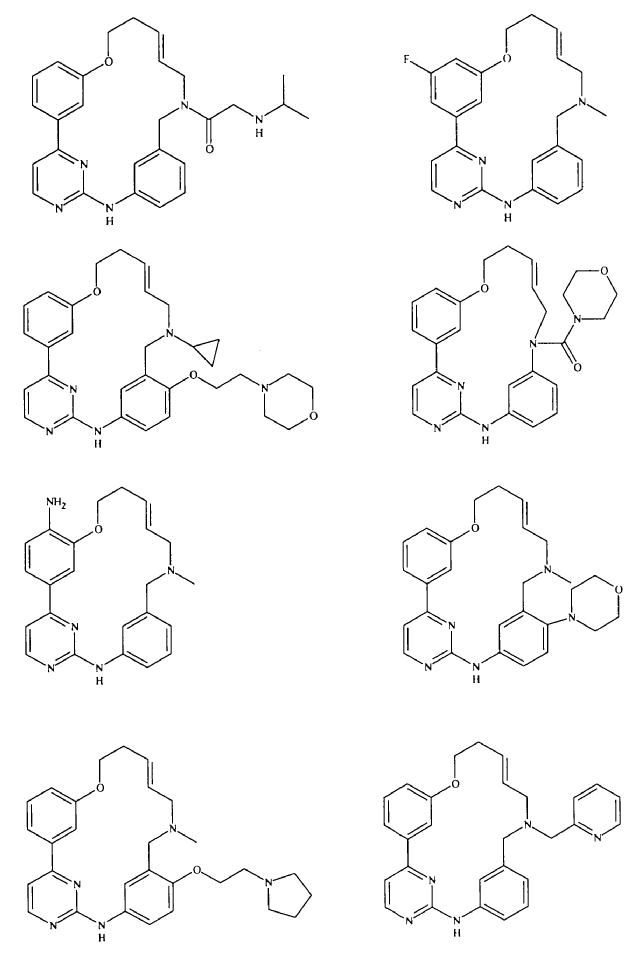
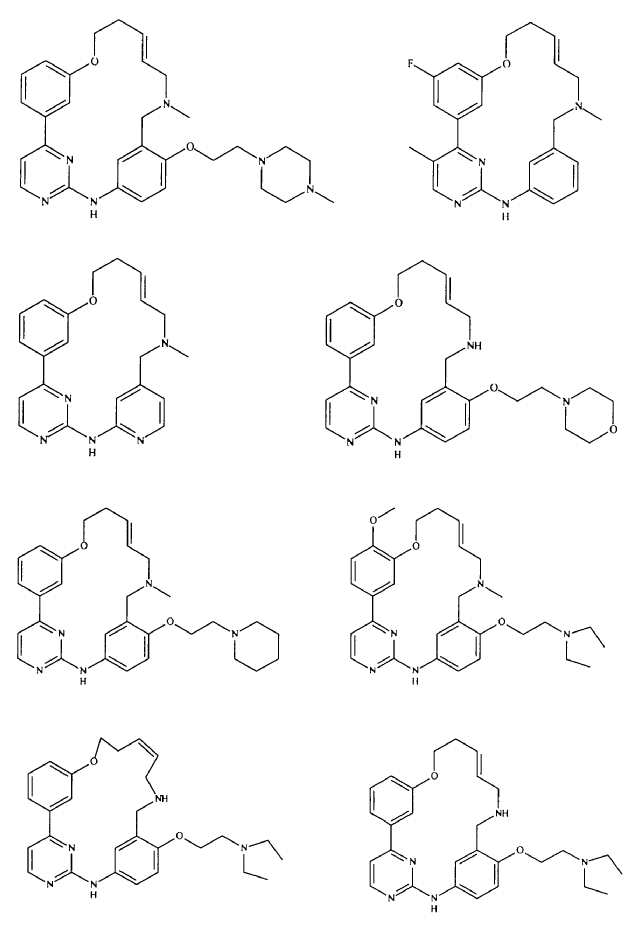
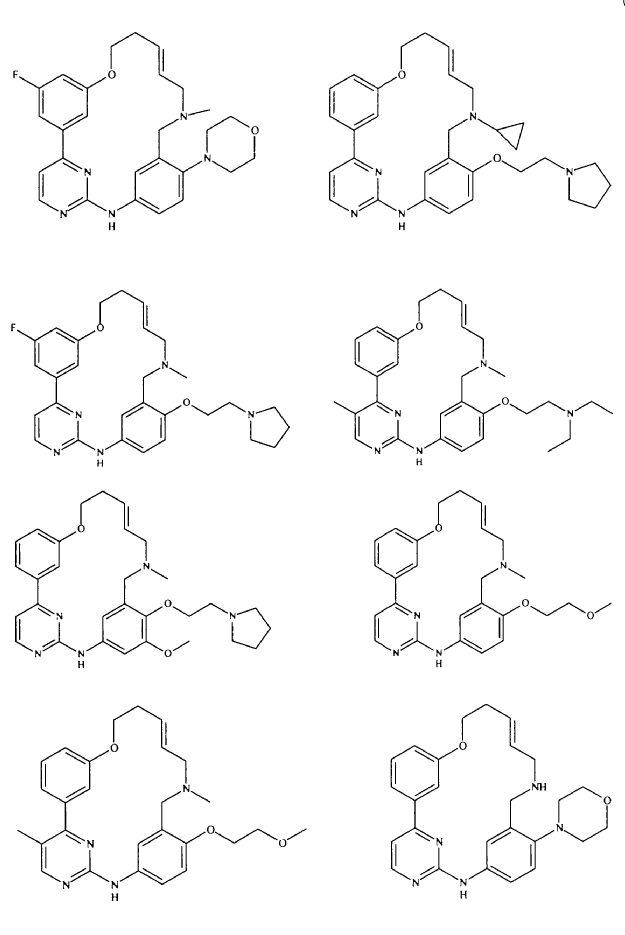
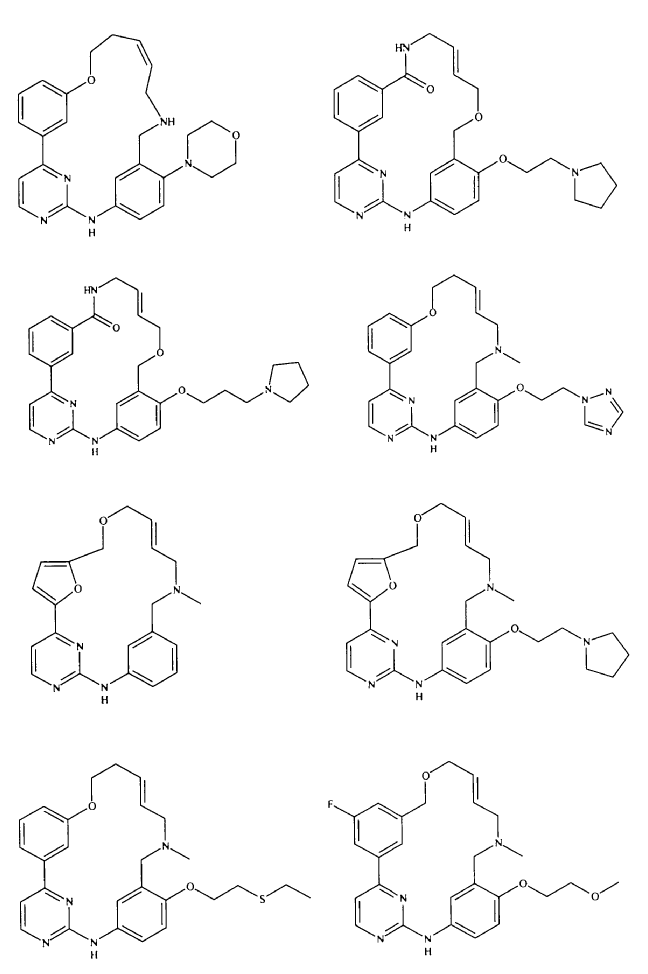
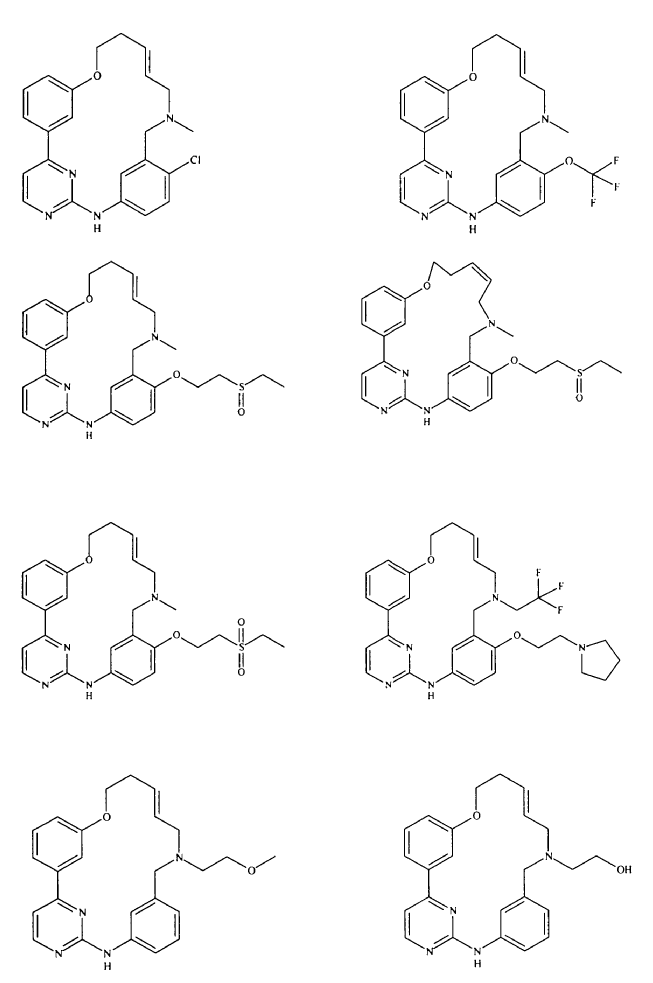
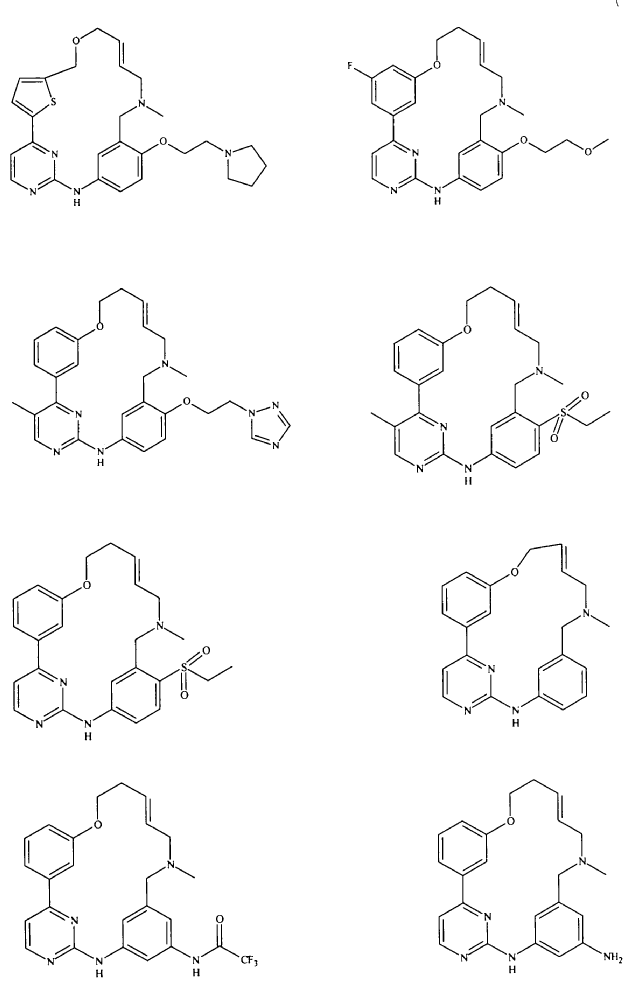
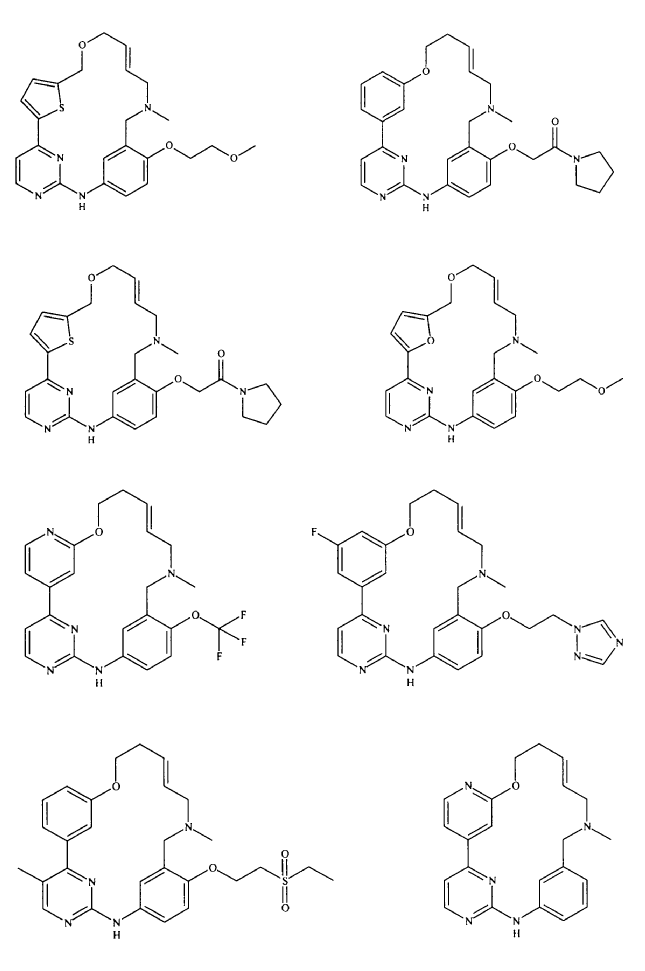
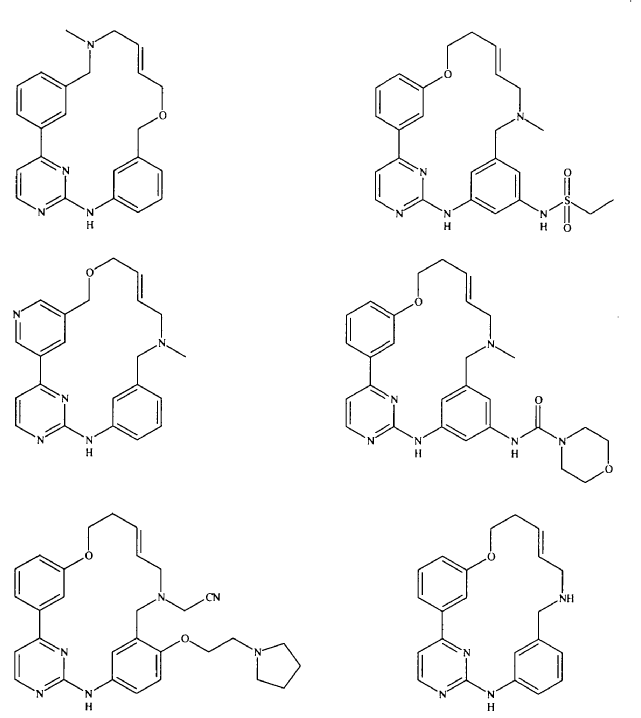
o una sal de los mismos farmacéuticamente aceptable.
21. Compuesto seleccionado del grupo que consiste en:
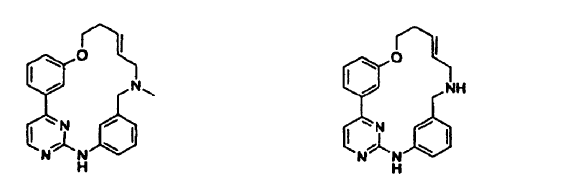
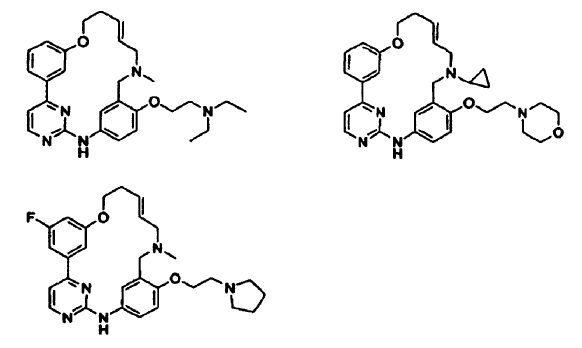
o una sal de los mismos farmacéuticamente aceptable.
22. Composición farmacéutica que incluye un compuesto de conformidad con cualquiera de las reivindicaciones 1 a 21 y un diluyente, excipiente o vehículo farmacéuticamente aceptable.
23. Uso de un compuesto de conformidad con cualquiera de las reivindicaciones 1 a 21 para inhibir una o más proteína cinasa(s) in vitro.
24. Uso de conformidad con la reivindicación 23, caracterizado porque dicha una o más proteína cinasa(s) es una proteína cinasa dependiente de ciclina o una proteína tirosina cinasa.
25. Uso de conformidad con la reivindicación 24, caracterizado porque la cinasa dependiente de ciclina es una CMCG cinasa de Grupo I que se selecciona a partir del grupo que consiste en CDC2Hs, CDK2, CDK3, CDK4, CDK5, CDK6, CDK9, PCTAIRE1, PCTAIRE2, PCTAIRE3, CAK/MO15, Dm2, Dm2c, Ddcdc2, DdPRK, LmmCRK1, PfC2R, EhC2R, CfCdc2R, cdc2+, CDC28, PHO85, KIN28, FpCdc2, MsCdc2B, y OsC2R o un equivalente funcional de las mismas.
26. Uso de conformidad con la reivindicación 25, caracterizado porque la CMCG cinasa de Grupo I es CDK2 o un equivalente funcional de la misma.
27. Uso de conformidad con la reivindicación 24, caracterizado porque la proteína tirosina cinasa es una proteína tirosina cinasa del grupo VII o una proteína tirosina cinasa del grupo XIV.
28. Uso de conformidad con la reivindicación 27, caracterizado porque la proteína tirosina cinasa del grupo VII se selecciona a partir del grupo que consiste en TYK2, JAK1, JAK2 y HOP o un equivalente funcional de las mismas.
29. Uso de conformidad con las reivindicaciones 27 o 28, caracterizado porque la proteína tirosina cinasa del grupo VII es JAK2 o un equivalente funcional de la misma.
30. Uso de conformidad con la reivindicación 29, caracterizado porque la JAK2 incluye una mutación de V a F en la posición 617.
31. Uso de conformidad con la reivindicación 27, caracterizado porque la proteína tirosina cinasa del Grupo XIV se selecciona a partir del grupo que consiste en PDGFR-b, PDGFR-a, CSF1R, c-kit, Flk2, FLT1, FLT2, FLT3 y FLT4 o un equivalente funcional de las mismas.
32. Uso de conformidad con la reivindicación 31, caracterizado porque la proteína tirosina cinasa del Grupo XIV es FLT3 o un equivalente funcional de la misma.
33. Uso de conformidad con la reivindicación 32, caracterizado porque la FLT3 incluye una duplicación interna en tándem de los aminoácidos VDFREYEYDH en la posición 592-601.
34. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 21, de uso en el tratamiento de una afección en un animal en el cual la inhibición de una o más proteína cinasa(s) puede prevenir, inhibir o mejorar la patología o sintomatología de la afección.
35. Compuesto de conformidad con la reivindicación 34, caracterizado porque dicha una o más proteína cinasa(s) es (son) una(s) proteína(s) cinasa(s) dependiente(s) de ciclina.
36. Compuesto de conformidad con la reivindicación 35, caracterizado porque la cinasa dependiente de ciclina es una CMCG cinasa de Grupo I que se selecciona a partir del grupo que consiste en CDC2Hs, CDK2, CDK3, CDK4, CDK5, CDK6, CDK9, PCTAIRE1, PCTAIRE2, PCTAIRE3, CAK/MO15, Dm2, Dm2c, Ddcdc2, DdPRK, LmmCRK1, PfC2R, EhC2R, CfCdc2R, cdc2+, CDC28, PHO85, KIN28, FpCdc2, MsCdc2B, y OsC2R o un equivalente funcional de las mismas.
37. Compuesto de conformidad con la reivindicación 36, caracterizado porque la CMCG cinasa de Grupo I es CDK2 o un equivalente funcional de la misma.
38. Compuesto de conformidad con cualquiera de las reivindicaciones 34 a 37, caracterizado porque la afección se selecciona a partir del grupo que consiste en cáncer de próstata, retinoblastoma, neoplasma maligno de tejido mamario, tumor maligno de colon, hiperplasia del endometrio, osteosarcoma, carcinoma de célula escamosa, cáncer pulmonar de célula no pequeña, melanoma, carcinoma de célula hepática, neoplasma maligno del páncreas, leucemia mieloide, carcinoma cervical, tumor fibroide, adenocarcinoma del colon, leucemia de célula T, glioma, glioblastoma, oligodendroglioma, linfoma, cáncer de ovario, restenosis, astrocitoma, neoplasmas de la vejiga, neoplasmas musculoesqueléticos y Enfermedad de Alzheimer.
39. Compuesto de conformidad con la reivindicación 35, caracterizado porque la proteína tirosina cinasa es una proteína tirosina cinasa del grupo VII o una proteína tirosina cinasa del grupo XIV.
40. Compuesto de conformidad con la reivindicación 39, caracterizado porque la proteína tirosina cinasa del grupo VII se selecciona a partir del grupo que consiste en TYK2, JAK1, JAK2 y HOP o un equivalente funcional de las mismas.
41. Compuesto de conformidad con la reivindicación 40, caracterizado porque la proteína tirosina cinasa del grupo VII es JAK2 o un equivalente funcional de la misma.
42. Compuesto de conformidad con la reivindicación 41, caracterizado porque la JAK2 incluye una mutación de V a F en la posición 617.
43. Compuesto de conformidad con cualquiera de las reivindicaciones 39 a 42, caracterizado porque la afección se selecciona a partir del grupo que consiste en trastornos mieloproliferativos (mielofibrosis idiopática crónica, policitemia vera, trombocitopenia esencial, leucemia mieloide crónica), metaplasia mieloide, leucemia mielomonocítica crónica, leucemia linfocítica aguda, leucemia aguda de eritroblasto, enfermedad de Hodgkin, linfoma de célula B, leucemia de célula T aguda, carcinoma de tejido mamario, cáncer de ovario, carcinoma de colon, cáncer de próstata, melanoma, síndromes mielodisplásicos, queloides, insuficiencia cardiaca congestiva, isquemia, trombosis, hipertrofia cardiaca, hipertensión pulmonar, y degeneración de la retina.
44. Compuesto de conformidad con la reivindicación 39, caracterizado porque la proteína tirosina cinasa del Grupo XIV se selecciona a partir del grupo que consiste en PDGFR-b, PDGFR-a, CSF1R, c-kit, Flk2, FLT1, FLT2, FLT3 y FLT4 o un equivalente funcional de las mismas.
45. Compuesto de conformidad con la reivindicación 44, caracterizado porque la proteína tirosina cinasa del Grupo XIV es FLT3 o un equivalente funcional de la misma.
46. Compuesto de conformidad con la reivindicación 45, caracterizado porque la FLT3 incluye una duplicación interna en tándem de los aminoácidos VDFREYEYDH en la posición 592-601.
47. Compuesto de conformidad con cualquiera de las reivindicaciones 44 a 46, caracterizado porque la afección se selecciona a partir del grupo que consiste en leucemia mieloide aguda, leucemia promielocítica aguda, leucemia linfocítica aguda, síndromes mielodisplásicos, leucocitosis, leucemia mielomonocítica juvenil, leucemia de célula B aguda, leucemia mieloide crónica, leucemia de célula T aguda, trastornos mielo-proliferativos, y leucemia mielomonocítica crónica.
48. Compuesto de conformidad con cualquiera de las reivindicaciones 1 a 21 de uso en el tratamiento o prevención de un trastorno relacionado con cinasa.
49. Compuesto de conformidad con la reivindicación 48, caracterizado porque el trastorno relacionado con cinasa es un trastorno proliferativo.
50. Compuesto de conformidad con la reivindicación 49, caracterizado porque el trastorno proliferativo se selecciona a partir del grupo que consiste en trastornos mielo-proliferativos (mielofibrosis idiopática crónica, policitemia vera, trombocitopenia esencial, leucemia mieloide crónica), metaplasia mieloide, leucemia mielomonocítica crónica, leucemia mieloide aguda, leucemia mielomonocítica juvenil, leucemia promielocítica aguda, leucemia linfocítica aguda, leucemia aguda de eritroblasto, leucemia de célula B aguda, leucocitosis, enfermedad de Hodgkin, linfoma de célula B, leucemia de célula T aguda, carcinoma de tejido mamario, cáncer de ovario, carcinoma de colon, cáncer de próstata, melanoma, síndromes mielodisplásicos, queloides, retinoblastoma, neoplasma maligno de tejido mamario, tumor maligno de colon, hiperplasia del endometrio, osteosarcoma, carcinoma de célula escamosa, cáncer pulmonar de célula no pequeña, melanoma, carcinoma de célula hepática, neoplasma maligno del páncreas, leucemia mieloide, carcinoma cervical, tumor fibroide, adenocarcinoma del colon, glioma, glioblastoma, oligodendroglioma, linfoma, cáncer de ovario, restenosis, astrocitoma, neoplasmas de la vejiga, y neoplasmas musculoesqueléticos.
51. Compuesto de conformidad con la reivindicación 49, caracterizado porque el trastorno proliferativo es cáncer.
52. Compuesto de conformidad con la reivindicación 51, caracterizado porque el cáncer es un tumor sólido o cáncer hematológico.
53. Compuesto de conformidad con la reivindicación 52, caracterizado porque el tumor sólido es un tumor presente en o metastatizado a partir de un órgano o tejido que se selecciona a partir del grupo que consiste en mama, ovario, colon, próstata, endometrio, hueso, piel, pulmón, hígado, páncreas, cuello uterino, cerebro, tejido neural, tejido linfático, vaso sanguíneo, vejiga y músculo.
54. Compuesto de conformidad con la reivindicación 52, caracterizado porque el cáncer hematológico se selecciona a partir del grupo que consiste en leucemia mieloide aguda, leucemia promielocítica aguda, leucemia linfocítica aguda, síndrome mielodisplásico, leucocitosis, leucemia mielomonocítica juvenil, leucemia de célula B aguda, leucemia mieloide crónica, leucemia de célula T aguda, leucemia mielomonocítica crónica, metaplasia mieloide, leucemia mielomonocítica crónica, leucemia aguda de eritroblasto, enfermedad de Hodgkin, y linfoma de célula B.
55. Método para sintetizar un compuesto de la fórmula I como se define en la reivindicación 1, el método incluye los pasos de:
(a) proporcionar un compuesto de la fórmula
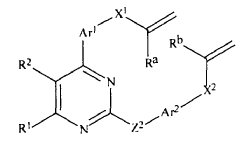
en la cual
R1, R2, Ra, Rb, Z2, Ar1, Ar2, X1 y X2 son como se definieron en la reivindicación 1;
(b) someter el compuesto a metátesis de cierre de anillo;
(c) opcionalmente hacer reaccionar el doble enlace formado de esta manera para formar un grupo cicloalquilo.
56. Método de conformidad con la reivindicación 55, caracterizado porque el paso (b) implica tratar la sal de ácido trifluoroacético (TFA) o de ácido clorhídrico (HCl) del compuesto con 5-10% molar de catalizador de segunda generación de Grubbs en diclorometano a 40ºC.
57. Método de conformidad con las reivindicaciones 55 o 56, caracterizado porque el paso (c) incluye tratar el producto de metátesis con una solución etérea recién preparada de diazometano (CH2N2) en diclorometano/dioxano a 0ºC.
Patentes similares o relacionadas:
Heterciclos tricíclicos como inhibidores de proteína BET, del 21 de Agosto de 2019, de Incyte Holdings Corporation: Un compuesto de Fórmula (I):**Fórmula** o una de sus sales farmacéuticamente aceptables, en donde: --- representa un enlace sencillo o un doble […]
Tetrazolonas como bioisósteros de ácido carboxílico, del 3 de Julio de 2019, de RIGEL PHARMACEUTICALS, INC.: Un compuesto seleccionado de:**Fórmula**
Intermediarios para la síntesis de ligadores P1 cíclicos como inhibidores del factor XIA, del 10 de Abril de 2019, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de la Fórmula 14i:**Fórmula** en el que: el anillo A se selecciona del grupo que consiste en un arilo de 6 miembros y […]
Derivado de N-acilo O-aminofenol CBI cíclico, del 27 de Febrero de 2019, de THE SCRIPPS RESEARCH INSTITUTE: Un derivado cíclico de N-acilo O-aminofenol CBI representado por la Fórmula I:**Fórmula** en donde: 20 R es hidrido o un hidrocarbilo C1-C6; y R3 se selecciona […]
Macrociclos como inhibidores del factor XIa, del 2 de Mayo de 2018, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Formula (I):**Fórmula** o un estereoisomero, un tautomero, una sal farmaceuticamente aceptable, un solvato del mismo, en donde: […]
Macrociclos novedosos como inhibidores del factor XIa, del 7 de Junio de 2017, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Fórmula (I): **(Ver fórmula)** o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable, un solvato del mismo, […]
Heterociclos tricíclicos como inhibidores de la proteína NET, del 18 de Mayo de 2016, de Incyte Holdings Corporation: Un compuesto de fórmula (I):**Fórmula** o una sal farmacéuticamente aceptable del mismo; en la que: ----___ representa un enlace sencillo o un doble enlace; L […]
Naftiridonas y quinolonas 7-amino alquilidenil-heterocíclicas, del 1 de Marzo de 2016, de JANSSEN PHARMACEUTICA NV: Un compuesto seleccionado de**Tablas** o un isómero óptico, diastereómero, o enantiómero del mismo; una sal farmacéuticamente aceptable o hidrato del mismo.