COMPOSICION EN MICROPILDORAS CON LIBERACION CONTROLADA DE SUSTANCIAS FISIOLOGICAMENTE ACTIVAS, METODO PARA SU PREPARACION Y USO EN EL SECTOR ZOOTECNICO.
Composición resistente al rumen en píldoras con liberación controlada de substancias fisiológicamente activas en la zona posruminal de rumiantes,
que comprende:
i) un núcleo que comprende:
- una o varias sustancias fisiológicamente activas seleccionadas a partir del grupo que se compone de: aminoácidos, vitaminas, enzimas, proteínas, carbohidratos, microorganismos probióticos, alimentos prebióticos, sales minerales, colina y sus derivados y ácidos orgánicos; y
- una matriz que comprende una cera de carnauba y/o una cera microcristalina,
ii) una primera capa de revestimiento del núcleo que comprende una primera sustancia hidrófoba seleccionada a partir del grupo que se compone de: grasas, ácidos grasos, aceites hidrogenados, mono y bi-glicéridos de ácidos grasos, esteres de ácidos grasos, alcoholes grasos, con cadenas de 12 a 22 átomos de carbono y un punto de fusión comprendido entre 40 y 74ºC;
iii) una segunda capa de revestimiento de dicha primera capa que comprende una segunda sustancia hidrófoba seleccionada a partir del grupo que se compone de: ceras microcristalinas, ceras de parafina, ceras vegetales y ceras sintéticas con un punto de fusión comprendido entre 80 y 100ºC
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2005/002144.
Solicitante: VALENTINI S.R.L.
Nacionalidad solicitante: Italia.
Dirección: VIA CADUTI DI VIA FANI 830,47032 BERTINORO (FC).
Inventor/es: CAVASSINI,PAOLO, CICOGNANI,PAOLO.
Fecha de Publicación: .
Fecha Concesión Europea: 19 de Mayo de 2010.
Clasificación Internacional de Patentes:
- A23K1/00B2
- A23K1/00B3
- A23K1/00B3B
- A23K1/16I
- A61K9/16H2
- A61K9/16H4
- A61K9/50K
Clasificación PCT:
- A23K1/00
- A61K9/50 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Microcápsulas (A61K 9/52 tiene prioridad).
Fragmento de la descripción:
Composición en micropíldoras con liberación controlada de sustancias fisiológicamente activas, método para su preparación y uso en el sector zootécnico.
Campo técnico de la invención
La presente invención se refiere a una composición con liberación controlada para uso zootécnico. En particular, el objeto de la presente invención es una composición que comprende micropíldoras en condiciones de liberar de manera controlada las substancias fisiológicamente activas que contienen. Además, la presente invención se refiere a un método para preparar dicha composición así como al uso de dicha composición en el sector zootécnico.
Técnica existente
Es conocida la utilización de substancias fisiológicamente activas (de aquí en adelante sustancias activas) para suplementar o agregar aditivos a la dieta alimenticia de animales de granja de modo de mejorar sus condiciones de salud y sus prestaciones productivas.
Las sustancias activas de interés incluyen aminoácidos, vitaminas, enzimas, nutrientes tales como proteínas y carbohidratos, microorganismos probióticos, alimentos prebióticos, sales minerales, colina y sus derivados.
Algunas de las sustancias mencionadas con anterioridad normalmente ya están presentes en los piensos que se utilizan para alimentar los animales. Sin embargo, a veces el agregado de dichas sustancias activas, presentes en la dieta alimenticia, puede ser insuficiente o inadecuado para enfrentar estados de deficiencia o situaciones de alta productividad.
Tales sustancias activas, con propiedades nutricionales, vienen administradas a los animales por vía oral a través de la preparación de productos de fórmula (premezclas o piensos complementarios) en los cuales dichas sustancias activas vienen "diluidas" mediante mezclado mecánico con un determinado medio; el producto consiguiente está listo para ser agregado al alimento final (pienso).
Las sustancias activas y el pienso que contiene dichas sustancias activas sufren una degradación química-enzimática, antes de llegar al intestino, en el primer tramo del tracto digestivo del animal. En el caso de rumiantes (que tienen cuatro compartimientos digestivos) la degradación puede ser sumamente intensa debido a dos factores concomitantes principales: un tiempo de tránsito muy prolongado del alimento en los preestómagos (especialmente en el rumen) y la presencia de flora microbiana que efectúa una acción de degradación sobre la mayor parte de las moléculas que pasan a través del rumen.
La acción microbiana de los microorganismos ruminales altera químicamente algunas sustancias activas, tales como, por ejemplo, colina, transformándolas en sustancias con un menor valor de nutrición o con una actividad biológica significativamente menor que en el compuesto inicial.
Además, los productos de fórmula que contienen dichas sustancias activas, sufren degradación durante su preparación, especialmente en las etapas de mezclado, empaquetado y almacenamiento, así como en sus tratamientos tecnológicos tales como, por ejemplo, aglomeración (corte en cubitos o granulación) por aplicación de calor y/o presión de vapor.
Para reducir dichos inconvenientes, ha sido propuesto encapsular o revestir algunas sustancias activas biológicamente para uso zootécnico con una película de material sensible al pH resistente al ambiente gástrico empleando polímeros tales como: polivinilpirrolidone, poliamidas y celulosas químicamente modificadas.
Esta solución presenta la desventaja de un alto costo de producción, junto con el hecho de que el uso de polímeros sintéticos introduce sustancias no fisiológicas en la dieta alimenticia del animal.
Otra solución propuesta fue la de proteger las sustancias biológicamente activas para uso zootécnico con liberación controlada en el intestino de los animales con algunas sustancias de origen vegetal.
Esta solución no garantiza una protección satisfactoria de las sustancias biológicamente activas contra los ataques por parte de la flora microbiana o enzimas digestivas antes de llegar al intestino.
Es conocida la presencia en el mercado de algunas formulaciones que contienen las sustancias biológicamente activas con forma ruminalmente protegida (es decir, protegidas contra el degrado que produce el ecosistema ruminal).
Una formulación ruminalmente protegida tiene la capacidad de pasar a través del rumen, sin ser substancialmente descompuesta, y transportar la sustancia protegida, hasta un punto después del rumen, con la posibilidad de poder liberar la sustancia activa.
Por consiguiente, para una contribución eficaz de las sustancias biológicamente activas a rumiantes, una formulación ruminalmente protegida o de by-pass ruminal debe estar en condiciones de permitir el atravesamiento del rumen y la liberación de la sustancia activa protegida en el abomaso y/o en el tracto digestivo que está después del mismo.
El documento EP 940.088 A da a conocer una composición aditiva para piensos de rumiantes que contiene: (A) fosfato de magnesio y lisina, (B) óxido de magnesio, (C) un aglutinante que es un aglutinante soluble en agua, y (D) agua. Esta mezcla viene extrudida y luego revestida con un aceite o una mezcla de aceites, tales como aceite de soja y aceite de palma.
La composición revelada es un paliativo resistente al rumen que se disuelve rápidamente en el abomaso.
El documento JP 06.237.702 A (resumen) describe un aditivo para piensos para aumentar el nivel de aminoácidos de rumiantes que contiene un núcleo de metionina y/o lisina revestido con un agente de revestimiento que contiene lecitina, substancias inorgánicas tales como carbonato de magnesio estable en un medio neutro y soluble en ácido, ácido monocarboxílico 14C-22C, aceite de vegetal endurecido, cera, etc.
Sin embargo, sigue siendo necesaria la posibilidad de tener una composición para uso zootécnico que pueda liberar de manera controlada las sustancias que fisiológicamente contiene y que no presente los inconvenientes de las composiciones disponibles en el mercado.
Asimismo, sigue existiendo la necesidad de tener una composición con liberación controlada de sustancias fisiológicamente activas que presenten especiales características mecánicas-estructurales tales como resistencia al mezclado incluso con medios minerales y resistencia a esfuerzos térmicos (granulación o corte en cubitos).
Sumario de la invención
Un primer cometido es el de proporcionar una composición para uso zootécnico que libere de manera controlada las sustancias fisiológicamente activas que contiene para reducir la degradación provocada por la flora bacteriana y por la producción de enzimas endógenas.
Otro cometido es el de proporcionar una composición para uso zootécnico con liberación controlada que tenga propiedades químicas y físicas tales de permitir la preparación de productos de fórmula resistentes a la degradación mecánica-estructural.
Tales cometidos y aún otros que serán aclarados mediante la siguiente descripción detallada han sido obtenidos por parte del solicitante que ha perfeccionado un método para preparar micropíldoras capaces de liberar de manera controlada las sustancias activas que contienen, compuestas por un núcleo y un revestimiento externo de dos capas.
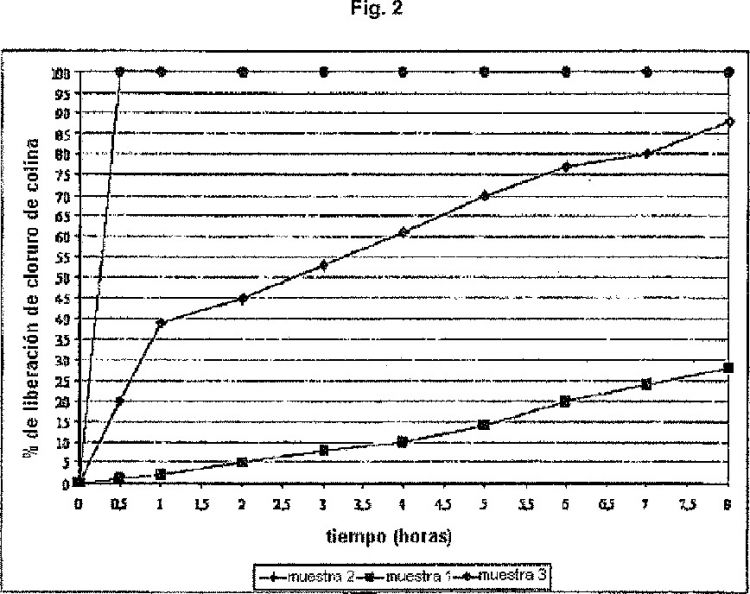
Las micropíldoras, en el caso de rumiantes, permite la liberación localizada y controlada de las sustancias activas principalmente transportadas dentro de la zona posruminal, desde el abomaso al intestino chico, y su posterior absorción en forma no degradada.
El primer objeto de la presente invención es una composición para uso zootécnico con liberación controlada que tenga las características señaladas en la anexa reivindicación independiente.
Otro objeto de la presente invención es un método para preparar una composición para uso zootécnico con liberación controlada que tenga las características señaladas en la anexa reivindicación independiente.
Aún otro objeto de la presente invención es el uso de una composición para uso zootécnico con liberación controlada que tenga las características señaladas en la anexa reivindicación independiente.
La invención viene ilustrada con mayores detalles en la descripción que sigue con la ayuda de algunas formas de ejecución, dadas a título puramente ejemplificador y, por ende, no restrictivo.
Breve descripción de los dibujos
La figura 1 (Fig. 1) muestra...
Reivindicaciones:
1. Composición resistente al rumen en píldoras con liberación controlada de substancias fisiológicamente activas en la zona posruminal de rumiantes, que comprende:
2. Composición según la reivindicación 1, donde la sustancia fisiológicamente activa viene seleccionada a partir de: metionina, colina, cloruro de colina, lisina, vitamina C, acetato de vitamina C, vitamina E, vitamina B2, vitamina PP y una mixtura de ácidos que comprende ácido láctico, ácido fumárico, ácido cítrico y ácido málico.
3. Composición según la reivindicación 1, donde la matriz contiene cera de carnauba y cera microcristalina con una relación de peso en el intervalo comprendido entre 1:3 y 3:1; preferentemente con una relación de 1:1.
4. Composición según una cualquiera de las precedentes reivindicaciones 1 o 2, donde la matriz contiene solamente cera microcristalina.
5. Composición según la reivindicación 1, donde la sustancia hidrófoba de la primera capa que viene seleccionada tiene un punto de fusión en el intervalo comprendido entre 60 y 64ºC.
6. Composición según la reivindicación 1, donde la sustancia hidrófoba de la primera capa viene seleccionada a partir del grupo que se compone de: ácido láurico, ácido esteárico, ácido palmítico, estearina, aceite hidrogenado de soja, aceite hidrogenado de algodón, aceite hidrogenado de palma, aceite hidrogenado de linaza, mono, bi, tri-estearato de sodio y glicerilo, estearato de calcio, estearato de magnesio, alcohol de estearilo, alcohol de cetilo y estearilo.
7. Composición según la reivindicación 6, donde la sustancia hidrófoba de la primera capa viene seleccionada entre aceite hidrogenado de palma y/o aceite hidrogenado de soja.
8. Composición según la reivindicación 1, donde la sustancia hidrófoba de la segunda capa viene seleccionada entre una cera de carnauba y/o una cera microcristalina.
9. Composición según la reivindicación 1, donde la matriz, además, comprende silicatos hidrófobos seleccionados a partir de: sílice coloidal, sílice amorfo sintético, sílice precipitada, silicatos de sodio y aluminio, silicato de calcio, talco, caolín, zeolitas hidrófobas sintéticas, estearato de magnesio y BHT.
10. Composición según una cualquiera de las precedentes reivindicaciones, donde las micropíldoras tienen una forma substancialmente cilíndrica con un diámetro comprendido en el intervalo de 0,5 a 5 mm, preferentemente de 0,8 a 1,2 mm, y una longitud en el intervalo de 0,5 a 5 mm, preferentemente de 0,8 a 2,0 mm.
11. Método para la preparación de una composición resistente al rumen en micropíldoras de conformidad con una o varias de las reivindicaciones de 1 a 10 que comprende las siguientes etapas:
12. Premezcla para alimentación de animales que contiene la composición resistente al rumen de conformidad con una o varias de las reivindicaciones de 1 a 10.
13. Pienso para alimentación de animales que comprende una premezcla según la reivindicación 12.
14. Uso de una composición resistente al rumen de conformidad con una o varias de las reivindicaciones de 1 a 10 en el sector de alimentación de animales.
Patentes similares o relacionadas:
COMPOSICIONES Y MÉTODOS PARA REDUCCIÓN DEL OXALATO, del 14 de Julio de 2011, de OXTHERA, INC: Una composición que comprende partículas que contienen una o más enzimas degradantes del oxalato incrustadas en un primer material polímero, en donde la enzima incrustada […]
 PRODUCTO PARA SUMINISTRO DE FÁRMACO Y MÉTODOS, del 1 de Abril de 2011, de UNIVERSITY OF MASSACHUSETTS: Sistema de suministro de partícula, caracterizado porque comprende una pared celular de levadura extraída que comprende menos del 90 por ciento en peso de beta-glucano […]
PRODUCTO PARA SUMINISTRO DE FÁRMACO Y MÉTODOS, del 1 de Abril de 2011, de UNIVERSITY OF MASSACHUSETTS: Sistema de suministro de partícula, caracterizado porque comprende una pared celular de levadura extraída que comprende menos del 90 por ciento en peso de beta-glucano […]
 RECUBRIMIENTOS TISULARES POLIMÉRICOS MULTIFUNCIONALES, del 7 de Marzo de 2011, de CALIFORNIA INSTITUTE OF TECHNOLOGY: Un implante o dispositivo médico que comprende una superficie no biológica destinada a ser colocada en contacto con un ambiente biológico, que comprende un recubrimiento superficial […]
RECUBRIMIENTOS TISULARES POLIMÉRICOS MULTIFUNCIONALES, del 7 de Marzo de 2011, de CALIFORNIA INSTITUTE OF TECHNOLOGY: Un implante o dispositivo médico que comprende una superficie no biológica destinada a ser colocada en contacto con un ambiente biológico, que comprende un recubrimiento superficial […]
 COMPOSICIONES FARMACÉUTICAS FÁCILES DE TRAGAR, QUE NO PROVOCAN UNA SENSACIÓN DESAGRADABLE EN LA BOCA Y QUE COMPRENDEN PARTÍCULAS CON UN INGREDIENTE ACTIVO, del 31 de Enero de 2011, de LOSAN PHARMA GMBH: Una composición farmacéutica para la administración oral, que comprende al menos una partícula que contiene un ingrediente activo, comprendiendo dicha […]
COMPOSICIONES FARMACÉUTICAS FÁCILES DE TRAGAR, QUE NO PROVOCAN UNA SENSACIÓN DESAGRADABLE EN LA BOCA Y QUE COMPRENDEN PARTÍCULAS CON UN INGREDIENTE ACTIVO, del 31 de Enero de 2011, de LOSAN PHARMA GMBH: Una composición farmacéutica para la administración oral, que comprende al menos una partícula que contiene un ingrediente activo, comprendiendo dicha […]
PREPARACIONES GRANULARES PARA ADMINISTRACIÓN ORAL, del 20 de Enero de 2011, de MITSUBISHI TANABE PHARMA CORPORATION: Una preparación en forma de gránulos para administración oral que comprende un agente hinchable en la boca como componente activo, en la que la preparación tiene una capa de […]
 MICROCAPSULAS QUE TIENEN MULTIPLES CORTEZAS, Y METODO PARA SU PREPARACION, del 25 de Octubre de 2010, de OCEAN NUTRITION CANADA LIMITED: Una microcápsula de múltiples núcleos que comprende:
(a) una aglomeración de microcápsulas primarias, comprendiendo cada microcápsula primaria un núcleo y una primera […]
MICROCAPSULAS QUE TIENEN MULTIPLES CORTEZAS, Y METODO PARA SU PREPARACION, del 25 de Octubre de 2010, de OCEAN NUTRITION CANADA LIMITED: Una microcápsula de múltiples núcleos que comprende:
(a) una aglomeración de microcápsulas primarias, comprendiendo cada microcápsula primaria un núcleo y una primera […]
 FORMA DE DOSIFICACION ORAL QUE COMPRENDE UN AGENTE TERAPEUTICO Y UN AGENTE DE EFECTO ADVERSO, del 28 de Abril de 2010, de EURO-CELTIQUE S.A.: Forma de dosificación oral que comprende una primera composición y una segunda composición, en la que la primera composición comprende una cantidad eficaz de un agente […]
FORMA DE DOSIFICACION ORAL QUE COMPRENDE UN AGENTE TERAPEUTICO Y UN AGENTE DE EFECTO ADVERSO, del 28 de Abril de 2010, de EURO-CELTIQUE S.A.: Forma de dosificación oral que comprende una primera composición y una segunda composición, en la que la primera composición comprende una cantidad eficaz de un agente […]
PROCEDIMIENTO PARA OBTENER SALES DE ÁCIDO RECUBIERTAS, del 12 de Enero de 2012, de AVICOLA DE TARAGONA, S.A: Se describe un procedimiento para obtener una sal de ácido recubierta ya se parcial o totalmente que comprende realizar una reacción exotérmica entre […]