Cadena ligera común de ratón.
Un ratón que comprende:
(a) una sustitución en el locus endógeno del ratón de la región variable de cadena ligera κ
de inmunoglobulina de los segmentos genéticos endógenos del ratón de la región variable de cadena ligera κ de inmunoglobulina con un único segmento genético Vκ 1-39/Jκ humano reordenado o un único segmento genético Vκ 3-20/Jκ humano reordenado, donde el segmento genético humano está unido operativamente a un gen constante κ endógeno del ratón y donde el ratón carece de un locus de la región variable de cadena ligera κ de inmunoglobulina de ratón que sea capaz de reordenar y formar un gen que codifique una región variable κ ; y,
(b) una sustitución de 90-100% del locus del gen endógeno del ratón de la región variable de cadena pesada con una pluralidad de segmentos genéticos humanos de la región variable de la cadena pesada, donde los segmentos genéticos humanos de la región variable de cadena pesada están unidos operativamente a un gen endógeno del ratón constante de cadena pesada, y los segmentos genéticos humanos de la región variable de cadena pesada son capaces de reordenar y formar un gen quimérico humano/ratón de cadena pesada reordenado.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2011/023971.
Solicitante: REGENERON PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 777 OLD SAW MILL RIVER ROAD TARRYTOWN, NY 10591 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DAVIS, SAMUEL, MURPHY, ANDREW, J., MCWHIRTER,JOHN, STEVENS,Sean, MACDONALD,LYNN, BUCKLER,DAVID R.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- C07K16/46 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C12N15/85 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para células animales.
PDF original: ES-2547142_T3.pdf
Fragmento de la descripción:
Cadena ligera común de ratón Campo de la invención
Se proporciona un ratón modificado genéticamente que expresa anticuerpos que tienen una cadena ligera variable de ser humano/constante de ratón común asociada con cadenas pesadas variables de ser humano/constantes de ratón distintas. Se proporciona un método para producir un anticuerpo biespecífico humano a partir de las secuencias genéticas de la región variable humana de células B del ratón.
Antecedentes
Los anticuerpos comprenden típicamente un componente de cadena pesada homodimérica, donde cada monómero de cadena pesada se asocia con una cadena ligera idéntica. Los anticuerpos que tienen un componente de cadena pesada heterodimérica (por ejemplo, los anticuerpos biespecíficos) son deseables como anticuerpos terapéuticos. Pero producir anticuerpos que tengan un componente de cadena ligera adecuado que se pueda unir satisfactoriamente con cada una de las cadenas pesadas de un anticuerpo biespecífico resulta problemático.
En una estrategia, se puede seleccionar una cadena ligera supervisando las estadísticas de utilización de todos los dominios variables de cadena ligera, identificando la cadena ligera que más se utiliza en anticuerpos humanos, y emparejando esa cadena ligera in vitro con las dos cadenas pesadas de especificidad diferente.
En otra estrategia, se puede seleccionar una cadena ligera observando las secuencias de cadena ligera de una biblioteca de fagos de presentación (por ejemplo, una biblioteca de fagos de presentación que comprenden las secuencias de la región variable de cadena ligera humana, por ejemplo, una biblioteca de ScFV humanos) y seleccionando la región variable de cadena ligera más usada comúnmente de la biblioteca. Entonces, la cadena ligera se puede ensayar en las dos cadenas ligeras diferentes de interés.
En otra estrategia, se puede seleccionar una cadena ligera ensayando una biblioteca de fagos de presentación de secuencias variables de cadena ligera utilizando las secuencias variables de cadena pesada de ambas cadenas pesadas de interés como sondas. Se puede seleccionar na cadena ligera que se asocia con ambas secuencias variables de cadena pesada como cadena ligera para las cadenas pesadas.
En otra estrategia, una cadena ligera candidata se puede alinear con las cadenas ligeras equivalentes de las cadenas pesadas, y se hacen modificaciones en la cadena ligera para que coincida estrechamente en las características de secuencia comunes con las cadenas ligeras equivalentes de ambas cadenas pesadas. Si se necesita minimizar las probabilidades de ¡nmunogenicidad, las modificaciones preferiblemente darán como resultado secuencias que están presentes en cadenas ligeras humanas conocidas, de forma que sea improbable que el proceso proteolítico genere un epítopo para células T en base a los parámetros y métodos conocidos en la técnica para evaluar la probabilidad de ¡nmunogenicidad (es decir, en sílice así como en ensayos húmedos).
Todas las estrategias anteriores se basan en métodos in vitro que incluye una serie de limitaciones a priori, por ejemplo, la identidad de secuencia, la capacidad para asociarse con cadenas pesadas específicas preseleccionadas, etc. Existe la necesidad en la técnica de composiciones y métodos que no se basen en la manipulación de las condiciones in vitro, sino que en su lugar emplee estrategias biológicamente más sensibles para producir proteínas de unión a epítopos humanos que incluyan una cadena ligera común.
Breve descripción de las figuras
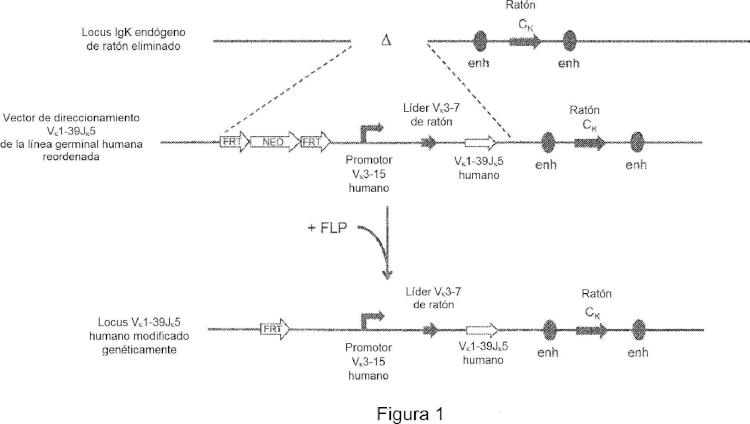
La FIG. 1 ¡lustra una estrategia de dirección para remplazar segmentos genéticos de la región variable de cadena ligera de ¡nmunoglobulina endógena de ratón con un gen de la región Vk1-39Jk5 humano.
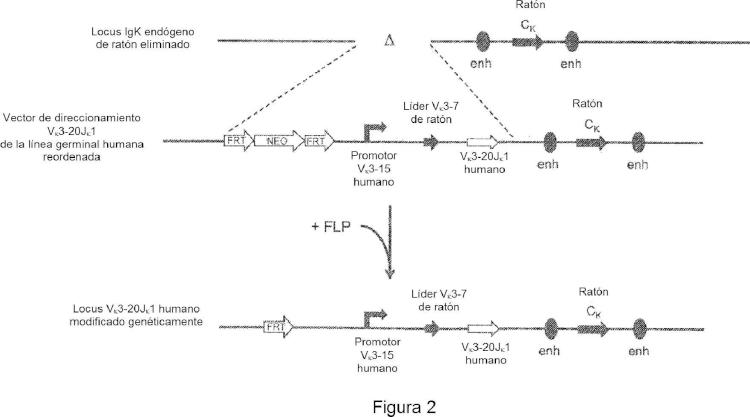
La FIG. 2 ilustra una estrategia de dirección para remplazar segmentos genéticos de la región variable de cadena ligera de ¡nmunoglobulina endógena de ratón con un gen de la región Vk3-20Jk1 humano.
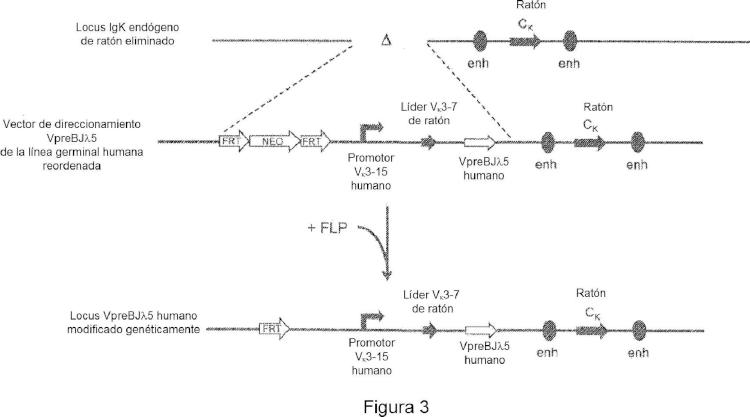
La FIG. 3 ilustra una estrategia de dirección para remplazar segmentos genéticos de la región variable de cadena ligera de ¡nmunoglobulina endógena de ratón con un gen de la región VpreB/J>.5 humano.
Sumario
Se proporcionan ratones modificados genéticamente que expresan dominios variables de cadena pesada y ligera de ¡nmunoglobulina humanos, donde los ratones tienen un repertorio variable de cadena ligera limitado. En particular, se proporciona un ratón donde el ratón comprende:
(a) una sustitución en el locus endógeno del ratón de la región variable de cadena ligera k de ¡nmunoglobulina de los segmentos genéticos endógenos del ratón de la región variable de cadena ligera k de ¡nmunoglobulina con
un único segmento genético Vk1-39/Jk5 humano reordenado o un único segmento genético Vk3-20/Jk humano reordenado, donde el segmento genético humano está unido operativamente a un gen constante k endógeno del ratón y donde el ratón carece de un locus de la región variable de cadena ligera k de inmunoglobulina de ratón que sea capaz de reordenar y formar un gen que codifique una región variable k; y,
(b) una sustitución de 90-100% del locus del gen endógeno del ratón de la región variable de cadena pesada con una pluralidad de segmentos genéticos humanos de la región variable de la cadena pesada, donde los segmentos genéticos humanos de la región variable de cadena pesada están unidos operativamente a un gen endógeno del ratón constante de cadena pesada, y los segmentos genéticos humanos de la región variable de cadena pesada son capaces de reordenar y formar un gen quimérico humano/ratón de cadena pesada reordenado.
También se proporciona una célula aislada a partir de un ratón modificado genéticamente de acuerdo con una cualquiera de las reivindicaciones precedentes, donde la célula comprende:
(a) una sustitución en el locus endógeno del ratón de la región variable de cadena ligera k de inmunoglobulina de los segmentos genéticos endógenos del ratón de la región variable de cadena ligera k de inmunoglobulina con un único segmento genético Vk1-39/Jk5 humano reordenado o un único segmento genético Vk3-20/Jk humano reordenado, donde el segmento genético humano está unido operativamente a un gen constante k endógeno del ratón y donde el ratón carece de un locus de la región variable de cadena ligera k de inmunoglobulina de ratón que sea capaz de reordenar y formar un gen que codifique una región variable k; y,
(b) una sustitución de 90-100% del locus del gen endógeno del ratón de la región variable de cadena pesada con una pluralidad de segmentos genéticos humanos de la región variable de la cadena pesada, donde los segmentos genéticos humanos de la región variable de cadena pesada están unidos operativamente a un gen endógeno del ratón constante de cadena pesada, y los segmentos genéticos humanos de la región variable de cadena pesada son capaces de reordenar y formar un gen quimérico humano/ratón de cadena pesada reordenado.
Además se proporciona un método para producir un anticuerpo que se une a un antigeno de interés que comprende la inmunización de dicho ratón con un antígeno de interés, obtención de una secuencia genética de la región variable de inmunoglobulina del ratón y el empleo de la secuencia genética de la región variable de inmunoglobulina para producir un anticuerpo que se une el antígeno.
Adicionalmente se proporciona un método para producir un anticuerpo humano biespecífico, donde el método comprende la inmunización de dicho ratón y la producción del anticuerpo biespecífico utilizando secuencias genéticas de la región variable humanas de células B a partir del ratón.
También se proporciona el uso de dicho ratón para seleccionar un dominio variable de cadena pesada de inmunoglobulina o segmento genético humanos.
También se hace referencia a un sistema biológico para genera un dominio variable de cadena ligera que se asocia y expresa con un repertorio diverso de dominios variables de cadena pesada humanos maduros de afinidad.
También se hace referencia a métodos para producir proteínas de unión que comprenden dominios variables de inmunoglobulina, que comprenden la inmunización de ratones que tienen un repertorio de cadena ligera de inmunoglobulina limitado con un antígeno de interés, y el empleo de una secuencia genética de la región variable de inmunoglobulina del ratón en una proteína de unión que se une específicamente al antígeno de interés. Los métodos incluyen métodos para producir dominios variables de cadena pesada de inmunoglobulina humanos adecuados para su uso en la producción de proteínas de unión al antígeno multiespecífico.
Los ratones modificados genéticamente... [Seguir leyendo]
Reivindicaciones:
1. Un ratón que comprende:
(a) una sustitución en el locus endógeno del ratón de la región variable de cadena ligera k de inmunoglobulina de los segmentos genéticos endógenos del ratón de la región variable de cadena ligera k de inmunoglobulina con un único segmento genético Vk1-39/Jk5 humano reordenado o un único segmento genético Vk3-20/Jk humano reordenado, donde el segmento genético humano está unido operativamente a un gen constante k endógeno del ratón y donde el ratón carece de un locus de la región variable de cadena ligera k de inmunoglobulina de ratón que sea capaz de reordenar y formar un gen que codifique una región variable k; y,
(b) una sustitución de 90-100% del locus del gen endógeno del ratón de la región variable de cadena pesada con una pluralidad de segmentos genéticos humanos de la región variable de la cadena pesada, donde los segmentos genéticos humanos de la región variable de cadena pesada están unidos operativamente a un gen endógeno del ratón constante de cadena pesada, y los segmentos genéticos humanos de la región variable de cadena pesada son capaces de reordenar y formar un gen quimérico humano/ratón de cadena pesada reordenado.
2. El ratón de la reivindicación 1, donde:
(a) el ratón comprende además un amplificador intrónico k de ratón 5 respecto a la región constante de cadena ligera del ratón; o
(b) el ratón comprende además un amplificador k de ratón 3
3. El ratón de la reivindicación 2, donde:
(a) la pluralidad de segmentos genéticos humanos de la región variable de cadena pesada comprende un segmento que se selecciona de entre el grupo que consiste en los segmentos genéticos humanos de la región variable de inmunoglobulina 1-2, 1-8, 1-24, 2-5, 3-7, 3-9, 3-11, 3-13, 3-15, 3-20, 3-23, 3-30, 3-33, 3-48, 4-31, 4- 39, 4-59, 5-51, y 6-1, y una combinación de los mismos;
(b) la pluralidad de segmentos genéticos humanos de la región variable de cadena pesada comprende un segmento que se selecciona de entre el grupo que consisten en los segmentos genéticos D1-7, D1-26, D3-3, D3- 10, D3-16, D3-22, D5-5, D5-12, D6-6, D6-13, y D7-27, y una combinación de los mismos;
(c) el ratón comprende una célula B que comprende una secuencia genética de la región variable de cadena pesada de inmunoglobulina reordenada que comprende un gen humano de la región variable de cadena pesada derivado de un segmento genético VH que se selecciona de entre el grupo que consiste en VH2-5, VH3-23, VH3- 30, VH4-39, VH4-59, y VH5-51, y se derivan de un segmento genético D que se selecciona de entre el grupo que consiste en D1-7, D1-26, D3-3, D3-16, D3-10, D3-22, D5-5, D5-12, D6-6, D6-13, y D7-27; o
(d) el ratón comprende una célula B que comprende una secuencia genética de la región variable de cadena pesada de inmunoglobulina reordenada que comprende un segmento genético VH, JH y DH que se selecciona de entre el grupo que consiste en VH 2-5 + JH 1 + D6-6, VH3-23 + JH4 + D3, VH3-23 + JH4 + D3-10, VH3-30 + JH 1 + D6-6, VH3-30 +JH3 + D6-6, VH3-30 + JH4 + D1 -7, VH3-30 + JH4 + D5-12, VH3-30 + JH4 + D6-13, VH3- 30 + JH4 + D6-6, VH3-30 + JH4 + D7-27, VH3-30 + JH5 + D3-22, VH3-30 + JH5 + D6-6, VH3-30 + JH5 + D7-27, VH4-39 + JH3 + D1 -26, VH4- 59 + JH3 + D3-16, VH4-59 + JH3 + D3-22, VH4-59 + JH4 + D3-16, VH5-51 + JH3 + D5-5, VH5-51 + JH5 + D6-13, y VH5-51 + JH6 + D3-16.
4. El ratón de la reivindicación 1, donde:
(a) el segmento genético Vk1-39 está presente en un reordenamiento con un segmento genético Jk5; o
(b) el segmento genético Vk3-20 está presente en un reordenamiento con un segmento genético Jk1.
5. Una célula aislada de un ratón modificado genéticamente de acuerdo con una cualquiera de las reivindicaciones precedentes, donde la célula comprende:
(a) una sustitución en el locus endógeno del ratón de la región variable de cadena ligera k de inmunoglobulina de los segmentos genéticos endógenos del ratón de la región variable de cadena ligera k de inmunoglobulina con un único segmento genético Vk1-39/Jk5 humano reordenado o un único segmento genético Vk3-20/Jk humano reordenado, donde el segmento genético humano está unido operativamente a un gen constante k endógeno del ratón y donde el ratón carece de un locus de la región variable de cadena ligera k de inmunoglobulina de ratón que sea capaz de reordenar y formar un gen que codifique una región variable k; y,
(b) una sustitución de 90-100% del locus del gen endógeno del ratón de la región variable de cadena pesada con una pluralidad de segmentos genéticos humanos de la región variable de la cadena pesada, donde los segmentos genéticos humanos de la región variable de cadena pesada están unidos operativamente a un gen endógeno del ratón constante de cadena pesada, y los segmentos genéticos humanos de la región variable de cadena pesada son capaces de reordenar y formar un gen quimérico humano/ratón de cadena pesada reordenado.
6. Un método no terapéutico para producir un anticuerpo que se une a un antígeno de interés que comprende inmunizar un ratón de acuerdo con una cualquiera de las reivindicaciones 1 a 4 con un antígeno de interés, obtener una secuencia genética de la región variable de inmunoglobulina del ratón y emplear la secuencia genética de la región variable de inmunoglobulina para producir un anticuerpo que se une al antígeno.
7. El método de la reivindicación 6 que comprende además:
- expresar en una sola célula: (a) una primera secuencia genética de la región variable de cadena pesada (Vh) de acuerdo de una cualquiera de las reivindicaciones 1 a 4 del ratón que se ha inmunizado, donde la secuencia genética Vh se fusiona con una secuencia genética humana región constante de cadena pesada (Ch); y (b) una secuencia genética de la región variable de cadena ligera (Vl) del ratón de acuerdo con una cualquiera de las reivindicaciones 1 a 4 que se ha inmunizado, donde la secuencia genética Vl se fusiona con una secuencia genética humana de la reglón constante de la cadena ligera (CL);
- mantener la célula bajo condiciones suficientes para expresar un anticuerpo completamente humano; y
- aislar el anticuerpo.
8. El método de acuerdo con la reivindicación 7, donde la célula comprende una segunda secuencia genética Vh de un ratón de acuerdo con una cualquiera de las reivindicaciones 1 a 4 que se ha inmunizado, donde la secuencia Vh se fusiona con una secuencia genética Ch humana, donde la primera secuencia genética Vh codifica un dominio Vh que reconoce un primer epítopo, y la segunda secuencia genética Vh codifica un dominio Vh que reconoce un segundo epítopo, donde el primer epítopo y el segundo epítopo no son idénticos.
9. Un método no terapéutico para producir un anticuerpo biespecífico humano, donde el método comprende inmunizar un ratón de acuerdo con una cualquiera de las reivindicaciones 1 a 4 y produciendo el anticuerpo específico utilizando secuencias genéticas de la región variable humana de células B del ratón.
10. El método de acuerdo con la reivindicación 9, donde el método comprende:
(a) identificar un linfocito seleccionado por clonación del ratón de acuerdo con una cualquiera de las reivindicaciones 1 a 4, donde el ratón se ha inmunizado y se la ha permitido desarrollar una respuesta inmunitaria a un antígeno de interés, donde el linfocito expresa un anticuerpos que se une específicamente al antígeno de interés;
(b) obtener del linfocito o el anticuerpo una secuencia de nucleótidos que codifica la región variable de la cadena pesada humana del anticuerpo que se une específicamente al antígeno de interés; y,
(c) emplear la secuencia de nucleótidos de (b) para producir un anticuerpo biespecífico.
11. El método de la reivindicación 10, donde las etapas (a) a (c ) se llevan a cabo una primera vez para un primer antígeno de interés para generar una primera secuencia de región variable de cadena pesada humana, y las etapas (a) a (c) se llevan a cabo una segunda vez para un segundo antígeno para generar una segunda secuencia de la región variable de cadena pesada humana, y donde la primera secuencia de región variable de cadena pesada humana se expresa fusionada con una primera región constante de cadena pesada humana para formar una primera cadena pesada humana, la segunda secuencia de región variable de cadena pesada humana se expresa fusionada con una segunda región constante de cadena pesada humana para formar una segunda cadena pesada humana, donde la primera y segunda cadenas pesadas humanas se expresan en presencia de una única cadena ligera humana que se expresa a partir de un segmento genético Vk1-39 o Vk3-20.
12. El método de acuerdo con la reivindicación 10, donde el método comprende:
(a) clonar las secuencias de la región variable de la cadena pesada de células B de:
- el ratón de acuerdo con una cualquiera de las realizaciones 1 a 4 que se han inmunizado con un primer
antígeno de interés; y
- el mismo ratón, o un ratón diferente que es genéticamente el mismo, que se ha inmunizado con un segundo
antígeno de interés
(b) expresar en una célula las secuencias de la región variable de cadena pesada humana de (a) con la misma región constante de cadena pesada y la misma cadena ligera para producir un anticuerpo biespecífico.
13. El método de la reivindicación 11 o la reivindicación 12, donde la primera cadena pesada humana comprende una modificación que elimina o reduce sustancialmente la afinidad de la primera cadena pesada humana a la proteína A, y una segunda cadena pesada humana que mantiene la capacidad de unirse a la proteína A, donde la modificación que elimina o reduce sustancialmente la afinidad de la primera cadena pesada humana a la proteína A se selecciona de entre una 95R (EU 435R), una 96F (EU 436F), y una combinación de las mismas.
14. El uso de un ratón de acuerdo con una cualquiera de las reivindicaciones 1 a 4 para seleccionar un dominio o segmento genético variable de cadena pesada de inmunoglobulina humana.
Patentes similares o relacionadas:
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
 Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Ratones con un sistema inmunitario humanizado con células dendríticas reforzadas, del 22 de Julio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un ratón Rag-/-, γc-/-, Flk2-/- deficiente para el gen activador de recombinación 2 (Rag2) y/o el gen activador de recombinación 1 (Rag1), cadena gamma […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Expresión de proteína biotecnológica mejorada que usa un activador CHEF1 híbrido, del 17 de Junio de 2020, de AGC Biologics, Inc: Un vector de expresión que comprende ADN regulador de la transcripción del factor 1α de elongación de hámster chino (CHEF1) 5' y un activador de citomegalovirus (CMV) que […]
Estructuras artificiales de poliepítopos para uso en inmunoterapia, del 17 de Junio de 2020, de Invectys: Un vector de expresión de ADN o una mezcla de vectores de expresión de ADN que codifica al menos dos epítopos de CD4 de la transcriptasa inversa de la telomerasa […]
Roedores con alelos mutantes de Acvr1 condicionales, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una construcción de ácido nucleico que comprende: (i) un exón 5 de Acvr1 que codifica una secuencia de tipo silvestre a nivel de proteína, […]