Proceso para la producción de anticuerpos de la glicoforma G1.
Método para producir una inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con glicoestructura G1 que comprende las siguientes etapas:
- incubar un eluato de columna de cromatografía de afinidad que contiene la inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una galactosiltransferasa,
- incubar el producto de reacción de galactosiltransferasa con una sialiltransferasa,
- incubar el producto de reacción de sialiltransferasa con una beta-1,4-galactosidasa,
- eliminar o inactivar la beta-1,4-galactosidasa, e
- incubar el producto de reacción de beta-1,4-galactosidasa, en el que la beta-1,4-galactosidasa se ha eliminado o inactivado, con una sialidasa y así producir una inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con glicoestructura G1.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2012/069394.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Inventor/es: REUSCH,DIETMAR, HUELLER,MARTINA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C07K16/28 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C07K16/32 C07K 16/00 […] › contra productos de traducción de oncogenes.
PDF original: ES-2548215_T3.pdf
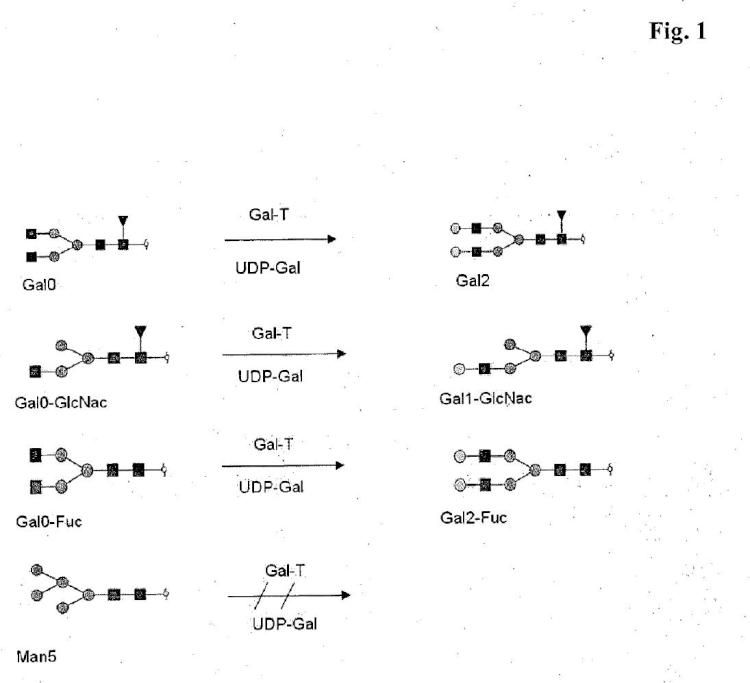
Fragmento de la descripción:
Proceso para la producción de anticuerpos de la glicoforma G1
La presente invención se refiere a un método para el procesamiento enzimático aguas abajo de inmunoglobulinas recombinantemente producidas. En más detalle, la presente invención se refiere a un método para producir una inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura después de una etapa de cromatografía de afinidad por un tratamiento enzimático.
Antecedentes de la invención
Los polipéptidos obtenidos a partir de células eucariotas se producen como polipéptidos glicosilados. Las glicoestructuras están unidas al esqueleto del aminoácido como modificación enzimática postraduccional.
Las glicosiltransferasas son reconocidas como una familia funcional de aproximadamente 250-300 enzimas unidas a membrana intracelulares diferentes que participan en la biosíntesis coordinada de las glicoestructuras de polipéptidos, que incluyen glicoproteínas, proteoglicanos y glicolípidos. Las glicosiltransferasas se clasifican en grupos basándose en su especificidad por donante de monosacárido de nucleótido. Por ejemplo, las galactosiltransferasas son el subconjunto de glicosiltransferasas que usan UDP-galactosa como donante de monosacárido activado, mientras que las sialiltransferasas usan CMP-ácido siálico y las fucosiltransferasas usan GDP-fucosa (Formar, N.L., et al., J. Mamm. Gland Biol. Neopl. 3 (1998) 315-324).
Un método para el examen clínico basado en las estructuras de oligosacáridos ligados a inmunoglobulina G se informa en el documento EP 0 698 793. En el documento EP 1 878 747 se informan anticuerpos glicomanipulados. El marcado selectivo de glicanos de inmunoglobulina se informa en el documento WO 2007/071347. En el documento WO 1997/016064 se informan métodos y composiciones para la reducción del rechazo de xenotrasplante. Preparaciones de anticuerpos con glicoestructuras sustancialmente homogéneas y no sialiladas, tales como G0 y G2, que se preparan por tratamiento enzimático, expresión bajo ciertas condiciones, uso de células huésped particulares y contacto con suero, se informan en el documento WO 2007/024743.
En el documento WO 2008/057634 se informan polipéptidos con propiedades antiinflamatorias mejoradas y citotóxicas reducidas y métodos relacionados. Las preparaciones de anticuerpos resistentes a la proteólisis se informan en el documento WO 2007/024743.
Sumario de la invención
Se ha encontrado que con la secuencia de etapas enzimáticas que se informa en el presente documento puede obtenerse una inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura, es decir, con una pureza del 90 % o más, con una pureza del 95 % o más, o con una pureza del 98 % o más.
Por tanto, en el presente documento se informa un método para producir una inmunoglobulina o fragmento de inmunoglobulina o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura a partir de una inmunoglobulina glicosilada o un fragmento de inmunoglobulina glicosilada o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada que es una mezcla de glicoestructuras G0, G1 y G2.
Por tanto, en el presente documento se informa un método para producir una inmunoglobulina o fragmento de inmunoglobulina o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura a partir de una inmunoglobulina glicosilada o un fragmento de inmunoglobulina glicosilada o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada que tiene una glicoestructura G0.
Por tanto, en el presente documento se informa un método para producir una inmunoglobulina o fragmento de inmunoglobulina o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura a partir de una inmunoglobulina glicosilada o un fragmento de inmunoglobulina glicosilada o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada que tiene una glicoestructura G2.
Así, en el presente documento se informa un método para producir una inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura o un fragmento de inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura que comprende las siguientes etapas en el siguiente orden:
proporcionar un eluato de columna de cromatografía de afinidad que contiene una inmunoglobulina o un fragmento de inmunoglobulina o un polipéptido de fusión, que es una mezcla de una glicoestructura G0, G1 y G2, incubar la inmunoglobulina o fragmento de inmunoglobulina con una galactosiltransferasa,
incubar la inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una sialiltransferasa, incubar la inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una beta-1,4- galactosidasa o lactasa,
eliminar o inactivar la beta-1,4-galactosidasa o lactasa, e
incubar la inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una sialidasa y así producir una inmunoglobulina con una glicoestructura G1 o un fragmento de inmunoglobulina con una glicoestructura G1 o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura.
Asi, en el presente documento se informa un método para producir una inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura o un fragmento de inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura que comprende las siguientes etapas en el siguiente orden:
proporcionar un eluato de columna de cromatografía de afinidad que contiene una inmunoglobulina, que tiene una glicoestructura G0, o un fragmento de inmunoglobulina, que tiene una glicoestructura G0, o un polipéptido de fusión, que tiene una glicoestructura G0,
incubar la inmunoglobulina o el fragmento de inmunoglobulina o el polipéptido de fusión con una galactosiltransferasa,
incubar la inmunoglobulina o fragmento de inmunoglobulina o el polipéptido de fusión con una sialiltransferasa, incubar la inmunoglobulina o fragmento de inmunoglobulina o el polipéptido de fusión con una beta-1,4- galactosidasa o lactasa,
eliminar o inactivar la beta-1,4-galactosidasa o lactasa, e
incubar la inmunoglobulina o fragmento de inmunoglobulina o el polipéptido de fusión con una sialidasa y así producir una inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una glicoestructura G1 en forma sustancialmente pura.
Así, en el presente documento se informa un método para producir una inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura o un fragmento de inmunoglobulina con una glicoestructura G1 en forma sustancialmente pura o un polipéptido de fusión que comprende un fragmento de inmunoglobulina glicosilada con una glicoestructura G1 en forma sustancialmente pura que comprende las siguientes etapas en el siguiente orden:
proporcionar un eluato de columna de cromatografía de afinidad que contiene una inmunoglobulina, que tiene una glicoestructura G2, o un fragmento de inmunoglobulina, que tiene una glicoestructura G2, o un polipéptido de fusión, que tiene una glicoestructura G2,
incubar la inmunoglobulina o fragmento de inmunoglobulina o un polipéptido de fusión con una sialiltransferasa, incubar la inmunoglobulina o fragmento de inmunoglobulina o un polipéptido de fusión con una beta-1,4- galactosidasa o lactasa,
eliminar o inactivar la beta-1,4-galactosidasa o lactasa, e
incubar la inmunoglobulina o fragmento de inmunoglobulina o un polipéptido de fusión con una sialidasa y así producir una inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una glicoestructura G1 en forma sustancialmente pura.
En una realización, la galactosiltransferasa se añade en una a diez alícuotas. En una realización, la galactosiltransferasa se añade en dos a siete alícuotas. En una realización, la galactosiltransferasa se añade en tres a seis alícuotas. En una realización, la galactosiltransferasa se añade en cuatro o seis alícuotas.
En una realización, la incubación con la galactosiltransferasa es durante aproximadamente 30 horas a aproximadamente 60 horas.
En una realización, la primera... [Seguir leyendo]
Reivindicaciones:
1. Método para producir una inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con glicoestructura G1 que comprende las siguientes etapas:
- incubar un eluato de columna de cromatografía de afinidad que contiene la inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con una galactosiltransferasa,
- incubar el producto de reacción de galactosiltransferasa con una sialiltransferasa,
- incubar el producto de reacción de sialiltransferasa con una beta-1,4-galactosidasa,
- eliminar o inactivar la beta-1,4-galactosidasa, e
- incubar el producto de reacción de beta-1,4-galactosidasa, en el que la beta-1,4-galactosidasa se ha eliminado o ¡nactlvado, con una sialidasa y así producir una inmunoglobulina o fragmento de inmunoglobulina o polipéptido de fusión con glicoestructura G1.
2. Método según la reivindicación 1, caracterizado porque la galactosiltransferasa se añade durante la incubación en dos o más alícuotas.
3. Método según una cualquiera de las reivindicaciones 1 o 2, caracterizado porque la galactosiltransferasa se añade durante la incubación en tres a seis alícuotas.
4. Método según una cualquiera de las reivindicaciones precedentes, caracterizado porque la primera alícuota de la galactosiltransferasa se añade después de cero a dos horas de tiempo de incubación.
5. Método según una cualquiera de las reivindicaciones precedentes, caracterizado porque una alícuota de la galactosiltransferasa se añade cada una después de seis a doce horas de tiempo de incubación.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Métodos y composiciones para tratar y prevenir enfermedades asociadas con la integrina AVB8, del 29 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un anticuerpo aislado que se une específicamente a la integrina β8 humana e inhibe la adhesión del péptido asociado a latencia (LAP) a ανβ8, en donde el […]
Proteínas de unión al antígeno ST2, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo aislado que se une a un antígeno ST2 que tiene la secuencia de aminoácidos 19-556 del SEQ ID NO: 1, comprendiendo dicho anticuerpo una secuencia de […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Bloqueo de CD73, del 22 de Julio de 2020, de Innate Pharma: Un anticuerpo aislado que específicamente se une a un polipéptido CD73 humano en la superficie de una célula y que tiene capacidad de neutralizar […]
Composición de anticuerpos monoclonales dirigidos contra BDCA-2, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Composición de anticuerpos monoclonales dirigidos contra la proteína BDCA-2, presentando dichos anticuerpos un porcentaje de fucosilación inferior al 60% […]