Polipéptidos dependientes de la vitamina K modificados.
Un polipéptido del Factor VII o Factor VIIa que comprende un dominio de GLA modificado que mejora la afinidad de unión a membranas de dicho polipéptido con relación a un polipéptido del Factor VII o Factor VIIa natural correspondiente,
comprendiendo dicho dominio de GLA modificado un residuo de glutamina en la posición 11 y un residuo de ácido glutámico en la posición 33, en donde dichos residuos están numerados de acuerdo con el Factor IX.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05026205.
Solicitante: REGENTS OF THE UNIVERSITY OF MINNESOTA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1000 WESTGATE DRIVE, SUITE 160 SAINT PAUL, MN 55114 ESTADOS UNIDOS DE AMERICA.
Inventor/es: NELSESTUEN,GARY L.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K38/43 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Enzimas; Proenzimas; Sus derivados.
- A61K38/48 A61K 38/00 […] › que actúan sobre enlaces peptídicos (3.4).
- A61P7/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Agentes antitrombóticos; Anticoagulantes; Inhibidores de la agregación plaquetaria.
- A61P7/04 A61P 7/00 […] › Antihemorrágicos; Procoagulantes; Hemostáticos; Antifibrinolíticos.
- C12N15/09 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/55 C12N 15/00 […] › Hidrolasas (3).
- C12N15/57 C12N 15/00 […] › que actúan sobre los enlaces peptídicos (3.4).
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- C12N9/64 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › que provienen de tejido animal, p. ej. renina.
PDF original: ES-2496104_T3.pdf




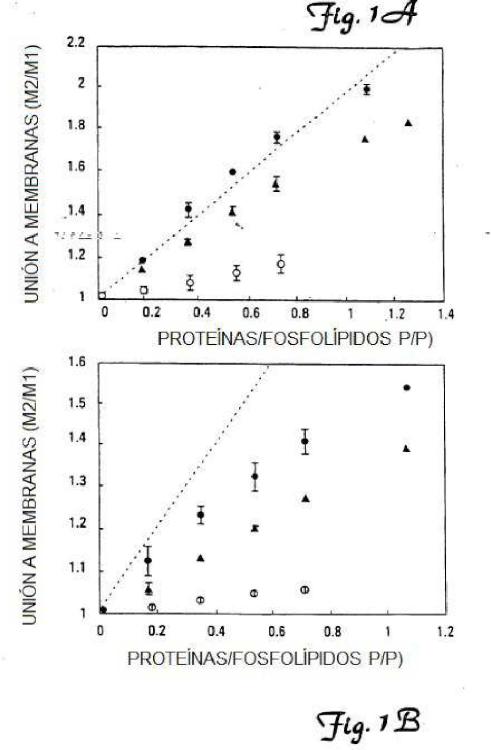
Fragmento de la descripción:
Polipéptidos dependientes de la vitamina K modificados Antecedentes de la invención
Las proteínas dependientes de la vitamina K contienen de 9 a 13 residuos de ácido gamma-carboxiglutámico (Gla) en sus 45 residuos amino-terminales. Los residuos Gla son producidos por enzimas del hígado que emplean la vitamina K para carboxilar las cadenas laterales de los residuos de ácido glutámico, en los precursores proteínicos. Las proteínas dependientes de la vitamina K están implicadas en varios procesos biológicos, entre los cuales el mejor descrito es la coagulación de la sangre (revisados por Furie, B. and Furie, B.C., 1988, Cell, 53:505-518). Las proteínas dependientes de la vitamina K incluyen la proteína Z, la proteína S, la protrombina, el Factor X, el Factor IX, la proteína C, el Factor Vil y Gas6. La última proteína actúa en la regulación del crecimiento celular. Matsubara et al., 1996, Dev. Biol., 180:499-510. Los residuos Gla son necesarios para la unión adecuada del calcio y para la interacción con membranas por estas proteínas. Se cree que el sitio de contacto con membranas del Factor X se encuentra en los residuos de aminoácidos 1-37. Evans and Nelsestuen, 1996, Protein Science 5: suppl. 1, 163 Abs. Aunque las regiones de las proteínas plasmáticas que contienen Gla muestran un alto grado de homología en las secuencias, tienen al menos 1000 veces más afinidad hacia membranas. McDonald, J.F., et al., 1997, Biochemistry, 36:5120-5137.
El Factor Vil actúa en la etapa inicial de la coagulación de la sangre y puede ser un elemento clave para la formación de coágulos de sangre. El precursor inactivo o zimógeno, tiene baja actividad enzimática que se incrementa considerablemente por digestión proteolítica para formar el Factor Vlla. Esta activación puede estar catalizada por el Factor Xa, así como por el Factor tisular Vlla, una proteína integral de la membrana encontrada en varios tipos celulares. Fiore, M.M., et al., 1994, J. Biol. Chem., 269:143-149. La activación por el Factor tisular Vlla se denomina autoactivación. Está implicada tanto en la activación (formación del Factor Vlla a partir del Factor Vil) como en la actividad posterior del Factor Vlla. La vía más importante para la activación in vivo es desconocida. El Factor Vlla puede activar los Factores IX y X de la coagulación de la sangre.
El Factor tisular se expresa con altos niveles en la superficie de algunas células tumorales. Es posible que el Factor tisular y el Factor Vlla actúen en el desarrollo de tumores y en la invasión de tejidos. Vrana, J.A., et al., Cáncer Res., 56:5063-5070. La expresión celular y la acción del Factor tisular son también un Factor principal en la respuesta tóxica al choque endotóxico. Dackiw, A.A., et al., 1996, Arch. Surg., 131:1273-1278.
La proteína C es activada por trombina en presencia de trombomodulina, una proteína integral de la membrana de las células endoteliales. Esmon, N.L., et al., 1982, J. Biol. Chem., 257:859-864. La proteína C activada (APC) degrada los Factores Va y Villa junto con su cofactor, la proteína S. La resistencia a APC es la forma más común de la enfermedad trombosis hereditaria. Dahlback, B., 1995, Blood, 85:607-614. Los inhibidores de la vitamina K se administran generalmente como una profilaxis para la trombosis.
Las proteínas dependientes de la vitamina K se emplean para tratar ciertos tipos de hemofilia. La hemofilia A se caracteriza por la ausencia del Factor VIII activo, el Factor Villa o la presencia de inhibidores del Factor VIII. La hemofilia B se caracteriza por la ausencia del Factor IX activo, el Factor IXa. La carencia de Factor Vil, aunque es rara, responde bien a la administración del Factor Vil. Bauer, K.A., 1996, Haemostasis, 26:155-158, suppl. 1. La terapia de sustitución del Factor VIII está limitada en algunos pacientes debido al desarrollo de títulos elevados de anticuerpos inhibidores del Factor VIII. Alternativamente, el Factor Vlla se puede utilizar en el tratamiento de las hemofilias A y B. El Factor IXa y el Factor Villa activan el Factor X. El Factor Vlla elimina la necesidad de los Factores IX y VIII, activando directamente el Factor X y pueden superar los problemas de carencia de los Factores IX y VIII, con pocas consecuencias inmunológicas. Hedner et al., 1993, Transfus. Medí. Rev., 7:78-83; Nicolaisen, E.M., et al., 1996, Thromb. Haemost., 76:200-204. Los niveles eficaces de administración del Factor Vlla son frecuentemente altos (45 a 90 pg/kg de peso corporal) y la administración se puede tener que repetir cada pocas horas. Shulmav, S., et al., 1996, Thromb. Haemost., 75:432-436.
Se ha encontrado que una forma soluble del Factor tisular (Factor tisular soluble o sTF) que no contiene la región de contacto con las membranas, es eficaz en el tratamiento de la hemofilia cuando se administra junto con el Factor Vlla. Patente de EE.UU. N° 5.504.064. En perros, se observó que el sTF reduce la cantidad de Factor Vlla, necesario para tratar la hemofilia. La asociación a las membranas por sTF-Vlla, depende totalmente del sitio de contacto con la membrana del Factor Vil. Esto está en contraste con el complejo tejido normal-Factor Vlla que se une a las membranas tanto a través del Factor tisular como del VII(a).
Sumario de la invención
Se ha descubierto que modificaciones en el dominio del ácido y-carboxiglutámico (GLA) de los polipéptidos dependientes de la vitamina K, mejoran sus afinidades de unión a las membranas. Los polipéptidos dependientes de la vitamina K, modificados de esta manera, tienen una actividad mejorada y se pueden emplear como anti-coagulantes, pro-coagulantes o para otras funciones que emplean proteínas dependientes de la vitamina K. Por ejemplo, una molécula mejorada del Factor Vil puede proporcionar algunos beneficios disminuyendo la dosificación del Factor
Vlla necesaria, la frecuencia relativa de la administración y/o proporcionando cambios cualitativos que permiten un tratamiento más eficaz de los estados de deficiencia.
La invención se refiere a un polipéptido del Factor Vil o Factor Vlla que comprende un dominio de GLA modificado que mejora la afinidad de unión a las membranas de dicho polipéptido con relación a un polipéptido correspondiente al Factor Vil natural o al Factor Vlla, comprendiendo dicho dominio de GLA modificado un residuo de glutamina en la posición 11 y un residuo de ácido glutámico en la posición 33, en donde dichos residuos se numeran según el Factor IX. El dominio de GLA modificado comprende desde aproximadamente el aminoácido 1 hasta aproximadamente el aminoácido 45 e incluye al menos una sustitución de aminoácidos como se indica anteriormente. El aminoácido sustituido puede ser el aminoácido 11, 12, 29, 33 o 34 (numerándose los residuos de acuerdo con el Factor IX). El dominio de GLA modificado puede incluir una secuencia de aminoácidos que, en el estado saturado con calcio, forma una estructura terciaria que tiene un núcleo catiónico con un halo de carga electronegativa.
[0009] El polipéptido dependiente de la vitamina K de la invención es el Factor Vil o Factor Vlla. El dominio de GLA modificado del Factor Vil o Factor Vlla contiene un residuo de glutamina en el aminoácido 11 y un residuo de ácido glutámico en el aminoácido 33 (SEQ ID NO: 30).
[0010] La invención también se refiere a un ácido nucleico aislado que codifica un polipéptido dependiente de la vitamina K de acuerdo con la reivindicación 3. Como se usa en la presente memoria, el término aislado (purificado) se refiere a una secuencia que corresponde a todo o parte del gen que codifica un polipéptido dependiente de la vitamina K, pero libre de secuencias que normalmente flanquean uno o ambos lados del gen en un genoma de mamífero.
[0011] La invención también se refiere a una célula hospedante de mamífero que incluye un vector de ácido nucleico que codifica un polipéptido dependiente de la vitamina K, de acuerdo con la reivindicación 4.
[0012] La invención también se refiere a una composición farmacéutica que incluye un vehículo farmacéuticamente aceptable y una cantidad de un polipéptido dependiente de la vitamina K eficaz para aumentar la formación de coágulos en un mamífero, en el que dicho polipéptido es como se define en la reivindicación 1. La composición farmacéutica puede incluir también el Factor tisular soluble.
[0013] La invención también se refiere al uso de un polipéptido dependiente de la vitamina K en la fabricación de un medicamento para el tratamiento de un trastorno de la coagulación, de acuerdo con la reivindicación 7.
[0014] Aunque no es parte de la invención reivindicada, se describe también un método para disminuir la formación de coágulos en un mamífero. El método incluye... [Seguir leyendo]
Reivindicaciones:
1. Un polipéptido del Factor Vil o Factor VIla que comprende un dominio de GLA modificado que mejora la afinidad de unión a membranas de dicho polipéptido con relación a un polipéptido del Factor Vil o Factor VIla natural correspondiente, comprendiendo dicho dominio de GLA modificado un residuo de glutamina en la posición 11 y un residuo de ácido glutámico en la posición 33, en donde dichos residuos están numerados de acuerdo con el Factor IX.
2. El polipéptido de la reivindicación 1, en donde dicho polipéptido es el Factor VIIa.
3. Un ácido nucleico aislado que codifica un polipéptido del Factor Vil o Factor VIla, en donde dicho polipéptido comprende un dominio de GLA modificado que mejora la afinidad de unión a membranas de dicho polipéptido con relación a un polipéptido del Factor Vil o Factor VIIa natural correspondiente, comprendiendo dicho dominio de GLA modificado un residuo de glutamina en la posición 11 y un residuo de ácido glutámico en la posición 33, en donde dichos residuos están numerados según el Factor IX.
4. Una célula hospedante de mamífero que comprende un vector de ácido nucleico, codificando dicho vector un polipéptido del Factor Vil o Factor VIla, comprendiendo dicho polipéptido un dominio de GLA modificado que mejora la afinidad de unión a membranas de dicho polipéptido con relación a un polipéptido del Factor Vil o Factor VIla natural correspondiente, comprendiendo dicho dominio de GLA modificado un residuo de glutamina en la posición 11 y un residuo de ácido glutámico en la posición 33, en donde dichos residuos están numerados de acuerdo con el Factor IX.
5. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable y una cantidad de un polipéptido del Factor Vil o Factor VIla eficaz para aumentar la formación de coágulos en un mamífero, en donde dicho polipéptido es como se define en cualquiera de las reivindicaciones 1-2.
6. La composición farmacéutica de la reivindicación 5, en donde dicho polipéptido es el Factor Vlla.
7. Uso de un polipéptido del Factor Vil o Factor Vlla como se define en cualquiera de las reivindicaciones 1-2, para la fabricación de un medicamento para el tratamiento de un trastorno de la coagulación, aumentando la formación de coágulos.
8. Uso de acuerdo con la reivindicación 7, en donde el trastorno de la coagulación es la hemofilia A, la hemofilia B o una enfermedad hepática.
9. Uso de acuerdo con la reivindicación 7 u 8, en donde dicho polipéptido es el Factor Vlla.
10. Un polipéptido del Factor Vil o Factor Vlla como se define en cualquiera de las reivindicaciones 1-2, para uso en un método para el tratamiento de un trastorno de la coagulación aumentando la formación de coágulos en un mamífero.
11. El polipéptido para uso en el método para el tratamiento de un trastorno de la coagulación de acuerdo con la reivindicación 10, en donde dicho polipéptido es el Factor Vlla.
Patentes similares o relacionadas:
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
 Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Ratones con un sistema inmunitario humanizado con células dendríticas reforzadas, del 22 de Julio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un ratón Rag-/-, γc-/-, Flk2-/- deficiente para el gen activador de recombinación 2 (Rag2) y/o el gen activador de recombinación 1 (Rag1), cadena gamma […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Estructuras artificiales de poliepítopos para uso en inmunoterapia, del 17 de Junio de 2020, de Invectys: Un vector de expresión de ADN o una mezcla de vectores de expresión de ADN que codifica al menos dos epítopos de CD4 de la transcriptasa inversa de la telomerasa […]
Expresión de proteína biotecnológica mejorada que usa un activador CHEF1 híbrido, del 17 de Junio de 2020, de AGC Biologics, Inc: Un vector de expresión que comprende ADN regulador de la transcripción del factor 1α de elongación de hámster chino (CHEF1) 5' y un activador de citomegalovirus (CMV) que […]
Roedores con alelos mutantes de Acvr1 condicionales, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una construcción de ácido nucleico que comprende: (i) un exón 5 de Acvr1 que codifica una secuencia de tipo silvestre a nivel de proteína, […]