Procedimiento para sintetizar compuestos macrólidos.
Un procedimiento para sintetizar un compuesto macrólido que comprende:
(i) convertir un compuesto de Estructura 2 en un compuesto de Estructura 3;
(ii) reducir el compuesto de Estructura 3 en presencia de un disolvente polar aprótico y un agente reductor paraformar un compuesto de Estructura 7, en el que el compuesto de Estructura 3 se reduce con hidrógeno en presenciade un catalizador de platino o paladio; y
(iii) hacer reaccionar el compuesto de Estructura 7 con un aldehído de estructura R-C(O)H en presencia de unagente reductor para formar un compuesto de Estructura 8a; en el que R es hidrógeno, alquilo, alquenilo, alquinilo,arilo, heteroarilo, o aralquilo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/061797.
Solicitante: MERIAL LTD..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3239 SATELLITE BLVD. DULUTH, GA 30096 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HEGGIE, WILLIAM, MENDES,ZITA, HENRIQUES,ANTONIO CARLOS SILVA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/70 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Hidratos de carbono; Azúcares; Sus derivados (sorbitol A61K 31/047).
- C07H17/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 17/00 Compuestos que contienen radicales heterocíclicos unidos directamente a los heteroátomos de los radicales sacárido. › Heterociclos que contienen ocho o más miembros cíclicos, p. ej. eritromicinas.
PDF original: ES-2426124_T3.pdf
Fragmento de la descripción:
Procedimiento para sintetizar compuestos macrólidos
Campo de la invención [0001] La presente invención se refiere a un procedimiento para sintetizar un grupo de compuestos químicos que tienen actividad antibacteriana, que son útiles en el tratamiento de las infecciones bacterianas en mamíferos. De forma más específica, la invención se refiere a procedimientos para sintetizar los compuestos macrólidos, por
ejemplo, gamitromicina.
Incluso de forma más específica, la invención se refiere a un procedimiento para producir gamiromicina utilizando una novedosa configuración de catalizadores, estructuras químicas, y/o procedimientos.
La presente invención proporciona también un procedimiento novedoso para inhibir la degradación a la vez que se aísla una estructura de una composición farmacéutica.
Antecedentes de la invención [0004] Los macrólidos son un grupo de compuestos químicos, algunos de los cuales tienen actividad antibacteriana y son útiles en el tratamiento de infecciones bacterianas en mamíferos. Los antibióticos macrólidos incluyen los que tienen un anillo de lactona de muchos miembros a los cuales se unen una o más moléculas de desoxiazúcares. Estos antibióticos son generalmente bacteriostáticos, pero se ha demostrado también que son bactericidas para algunos organismos. Los antibióticos macrólidos son eficaces frente a cocos y bacilos gram
positivos, aunque algunos de ellos poseen alguna actividad frente a algunos organismos gram-negativos. Los antibióticos macrólidos ejercen su actividad bacteriostática inhibiendo la síntesis de proteínas bacterianas. ("Goodman & Gillman’s the Pharmacological Basis of Therapeutics, " 9ª ed., J.G. Hadman & L.E. Limbird, eds., ch. 47, pp. 1135-1140, McGraw-Hill, Nueva York (1996) ) .
Como clase, los macrólidos tienden a ser incoloros y usualmente cristalinos. Los compuestos son generalmente estables en disolución casi neutra, pero pueden ser menos estables en disoluciones ácidas o básicas. Los precursores de los compuestos macrólidos utilizados en el procedimiento de la invención (por ejemplo, (9E) -9desoxi-9-hidroxiiminoeritromicina A (a partir de ahora en el presente documento "Estructura 1") ; 9- (Z) -eritromicina oxima (a partir de ahora en el presente documento "Estructura 2") ; y 9-deoxo-12-desoxi-9, 12-epoxi-8a, 9-didehidro
8a-aza-8a homoeritromicina A (a partir de ahora en el presente documento "Estructura 3") se han descrito en las Patentes de los Estados Unidos Nos 5, 202.434 y US 5.985.844. Además Yang y col., Tetrahedron Letters, 1994, 35 (19) , 3025-3028 y Djokic y col., J. Chem. Soc. Perkin Trans. 1, 1986, 1881-1890 describen la síntesis de compuestos macrólidos que usan estos compuestos como intermedios. Sin embargo, la síntesis y aislamiento de compuestos macrólidos tales como gamitromicina requiere normalmente múltiples extracciones y separaciones de fase.
Por tanto, existe todavía una necesidad de simplificar la síntesis y el aislamiento de macrólidos así como de aumentar la estabilidad de los macrólidos y de sus intermedios.
La cita o la identificación de cualquier documento en esta solicitud no es una declaración de que dicho documento está disponible como la técnica anterior a la presente invención.
Resumen de la invención 50 [0008] La presente invención se refiere a un procedimiento novedoso para sintetizar compuestos macrólidos. Una realización de la presente invención puede incluir permitir que prosigan múltiples reacciones químicas sin el aislamiento de intermedios químicos. Por ejemplo, un compuesto químico puede reducirse y posteriormente alquilarse sin aislamiento de los intermedios químicos. De esta manera, se pueden producir múltiples reacciones en un recipiente de reacción lo que puede dar lugar a una considerable disminución en el tiempo de ciclo del
procedimiento. En una realización alternativa, se pueden aislar uno o más de los intermedios antes de la reacción.
En una realización (9E) -9-desoxi-9-hidroxiiminoerithromicina A (a partir de ahora en el presente documento "Estructura 1") puede isomerizarse para formar 9- (Z) -eritromicina oxima (a partir de ahora en el presente documento "Estructura 2") . En algunas realizaciones, se puede utilizar una reordenación para convertir la 9- (Z) eritromicina oxima en 9-deoxo-12-desoxi-9, 12-epoxi-8a, 9-didehidro-8a-aza-8a homoeritromicina A (a partir de ahora en el presente documento "Estructura 3") . La reducción y la alquilación se pueden utilizar para convertir la 9-deoxo12-desoxi-9, 12-epoxi-8a, 9-didehidro-8a-aza-8a homoeritromicina A en gamitromicina. En otra realización, se puede reducir la cantidad de subproductos resultantes de las destilaciones y lavados.
Estas y otras realizaciones se dan a conocer o son evidentes a partir de, y quedan abarcadas por, la siguiente Descripción Detallada.
Además, una realización de la invención puede incluir el aislamiento de un intermedio en condiciones 10 que están controladas para inhibir la degradación del intermedio.
Se resalta que, en esta divulgación, y particularmente en las reivindicaciones y/o los párrafos, términos tales como “comprende”, “comprendido”, “que comprende” y similares pueden tener el significado atribuido a estos en la Ley de Patentes de los Estados Unidos; por ejemplo, pueden significar “incluye”, “incluido”, “que incluye”, y
similares; y los términos tales como “que consta esencialmente de” y “que consiste esencialmente en” tienen el significado adscrito a los mismos en la Ley de Patentes de los Estados Unidos, por ejemplo permiten no enumerar los elementos de forma explícita, pero excluyen los elementos que se encuentran en la técnica anterior y que afectan a una característica básica o novedosa de la invención.
Breve descripción de los dibujos [0013] La siguiente descripción detallada, que se proporciona por medio de ejemplos, pero que no se pretende que limite la invención únicamente a las realizaciones específicas descritas, se puede comprender mejor junto con los dibujos que la acompañan, en que:
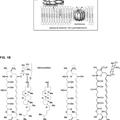
La FIG. 1 representa gráficamente las estructuras químicas implicadas en un procedimiento para sintetizar gamitromicina.
La FIG. 2 representa gráficamente las estructuras químicas de los productos de degradación de la Estructura 3 en 30 un procedimiento para sintetizar gamitromicina.
La FIG. 3 representa gráficamente una traza de HPLC de una muestra de la Estructura 3 aislada.
La FIG. 4 representa gráficamente una traza de HPLC de una muestra de la Estructura 7 aislada obtenida utilizando 35 hidrogenación en condiciones ácidas.
La FIG. 5 representa gráficamente una traza de HPLC de una muestra de la Estructura 7 aislada obtenida utilizando hidrogenación en condiciones menos ácidas.
La FIG. 6 representa gráficamente una traza de HPLC de una muestra de la Estructura 8 (Gamitromicina) .
La FIG. 7 representa gráficamente una traza de HPLC de una muestra de gamitromicina aislada.
La FIG. 8 representa gráficamente un revestimiento de una traza de HPLC de un procedimiento de síntesis 45 convencional y una traza de HPLC del procedimiento descrito en el presente documento
Descripción detallada [0014] Por claridad, la numeración de las lactonas macrocíclicas y las lactamas macrocíclicas descritas en el
presente documento utilizará la numeración del anillo utilizada en la Patente de los Estados Unidos 5.202.434, que se incorpora en el presente documento por referencia en su totalidad. La numeración del anillo del anillo de la eritromicina A lactona que se muestra a continuación se mantendrá a lo largo de este documento para los compuestos descritos con un anillo de 14 miembros. De manera similar, la numeración de la lactama descrita de 15 miembros que se muestra a continuación se utilizará para los compuestos descritos en el presente documento con 55 un anillo de 15 miembros Definiciones [0015] Los términos utilizados en el presente documento tienen su significado acostumbrado en la técnica a no ser que se especifique otra cosa. Los restos orgánicos mencionados en las definiciones de las variables de fórmula (I) o (II) son -similares al término halógeno –términos colectivos para listados individuales de los miembros individuales del grupo-. El prefijo Cn – Cm indica en cada caso el número posible de átomos de carbono en el grupo.
El término “alquilo” tal como se usa en el presente documento, se refiere a hidrocarburos primarios, secundarios o terciarios, saturados lineales, ramificados, cíclicos, que incluyen aquellos... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para sintetizar un compuesto macrólido que comprende:
(i) convertir un compuesto de Estructura 2 en un compuesto de Estructura 3;
(ii) reducir el compuesto de Estructura 3 en presencia de un disolvente polar aprótico y un agente reductor para formar un compuesto de Estructura 7, en el que el compuesto de Estructura 3 se reduce con hidrógeno en presencia de un catalizador de platino o paladio; y
(iii) hacer reaccionar el compuesto de Estructura 7 con un aldehído de estructura R-C (O) H en presencia de un agente reductor para formar un compuesto de Estructura 8a; en el que R es hidrógeno, alquilo, alquenilo, alquinilo, arilo, heteroarilo, o aralquilo;
2. El procedimiento de la reivindicación 1, en el que en la etapa (i) el compuesto de Estructura 2 se trata con un agente sulfonilante para convertir el compuesto de Estructura 2 en el compuesto de Estructura 3.
4. El procedimiento de la reivindicación 1, en el que el compuesto de Estructura 3 se aísla a una temperatura por debajo de aproximadamente 10º C.
6. El procedimiento de la reivindicación 1, en el que el agente reductor en la etapa (iii) es hidrógeno; y en el que la reacción se lleva a cabo en presencia de un catalizador de platino, rodio o paladio. 15
7. El procedimiento de la reivindicación 1, en el que el disolvente polar aprótico en la etapa (ii) es N, N’dimetiletilenurea, dimetilformamida, dimetilacetamida, dietilacetamida, N-metilpirrolidona, dimetilsulfóxido, hexametilfosforotriamida, o sus mezclas.
8. El procedimiento de la reivindicación 7, en el que el disolvente polar aprótico es dimetilformamida o dimetilacetamida.
9. El procedimiento de la reivindicación 1, en el que el compuesto de Estructura 3 en la etapa (ii) se aísla antes de la etapa (iii) . 25
10. El procedimiento de la reivindicación 1, en el que las etapas (ii) y (iii) se llevan a cabo sin aislar el compuesto de Estructura 7.
11. El procedimiento de la reivindicación 1 o la reivindicación 10, en el que en la etapa (iii) RC (O) H es 30 propanal y el compuesto de Estructura 8a es gamitromicina de Estructura 8.
12. Un procedimiento de acuerdo con la reivindicación para sintetizar gamitromicina, que comprende:
(i) convertir un compuesto de Estructura 2 en un compuesto de Estructura 3:
(ii) reducir el compuesto de Estructura 3 en presencia de un disolvente polar aprótico y un agente reductor para
formar un compuesto de Estructura 7; y 5
(iii) hacer reaccionar el compuesto de Estructura 7 con propanal en presencia de un agente reductor para formar 10 gamitromicina de Estructura 8;
en el que el compuesto de Estructura 7 procedente de la etapa (ii) no se aísla antes de la etapa (iii) ;
13. El procedimiento de la reivindicación 12, en el que el disolvente polar aprótico en la etapa (ii) es N, N’dimetiletilenurea, dimetilacetamida, dietilacetamida, N-metilpirrolidona, dimetilsulfóxido, dimetilformamida, hexametilfosforotriamida, o sus mezclas.
Patentes similares o relacionadas:
Polimorfos de 20,23-piperidinil-5-O-micaminosiltilonolida, del 20 de Mayo de 2020, de INTERVET INTERNATIONAL B.V: Una forma cristalina de 20,23-dipiperidinil-5-O-micaminosil-tilonolida que tiene al menos una de las siguientes características: un espectro FT-Raman que comprende […]
Derivados de azitromicina con propiedades de potenciación de la barrera epitelial, del 13 de Mayo de 2020, de EpiEndo Pharmaceuticals ehf: Un compuesto de acuerdo con la fórmula (I) **(Ver fórmula)** En donde R1 es OH; R2 es de acuerdo con la fórmula (III) **(Ver […]
Derivados de avermectina B1 que tienen un sustituyente alcoximetilo en la posición 4'''' o 4'', del 17 de Febrero de 2020, de Boehringer Ingelheim Animal Health USA Inc: Compuesto de fórmula**Fórmula** en la que n es 0 o 1; A-B es -CH=CH; R1 es sec-butilo o isopropilo; R2 es CH2CH3, p-ClC6H4, CH2(CH2)2N3 […]
Levoisovalerilespiramicina III y preparaciones, métodos de preparación y utilizaciones de la misma, del 1 de Enero de 2020, de Shenyang Fuyang Pharmaceutical Technology Co., Ltd: Compuesto cristalino de levoisovalerilespiramicina III, en el que, la fórmula estructural química de la levoisovalerilespiramicina III se representa como la fórmula […]
 Derivado de anfotericina b con toxicidad reducida, del 25 de Septiembre de 2019, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ILLINOIS: C2'epiAmB, representado por**Fórmula**
o una sal farmacéuticamente aceptable del mismo.
Derivado de anfotericina b con toxicidad reducida, del 25 de Septiembre de 2019, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ILLINOIS: C2'epiAmB, representado por**Fórmula**
o una sal farmacéuticamente aceptable del mismo.
Forma cristalina de levoisovalerilespiramicina II y preparaciones, procedimientos de preparación y utilizaciones de la misma, del 7 de Agosto de 2019, de Shenyang Fuyang Pharmaceutical Technology Co., Ltd: Compuesto de levoisovalerilespiramicina II, en el que, la fórmula estructural química de la levoisovalerilespiramicina II se representa como la fórmula (II), en condiciones […]
Derivados de la anfotericina B con índice terapéutico mejorado, del 20 de Septiembre de 2018, de The Board of Trustees of the University of Illionis: Un compuesto, o una sal farmacéuticamente aceptable del mismo, el compuesto que se selecciona de**Fórmula**
Procedimientos para tratar enfermedades gastrointestinales, del 11 de Abril de 2018, de Cempra Pharmaceuticals, Inc: Una cantidad terapéuticamente efectiva de un compuesto de fórmula **Fórmula** o una sal farmacéuticamente aceptable del mismo, donde: R10 es hidrógeno […]